Un cromosoma è costituito da una molecola di DNA associata a proteine
Definizione
Prima della divisione, una cellula eucariotica deve assicurare la duplicazione coordinata degli organuli circondati da membrana. Durante la crescita cellulare, tali organuli aumentano di volume grazie all’incorporazione di nuove componenti molecolari; successivamente, si suddividono e vengono ripartiti tra le due cellule figlie. L’espansione degli organuli richiede sia l’apporto di lipidi, per generare ulteriore superficie di membrana, sia la fornitura di proteine specifiche, destinate tanto al bilayer quanto al lume organellare. Anche in assenza di divisione, la cellula rinnova continuamente il proprio corredo proteico: le proteine neo-sintetizzate devono essere smistate verso la sede corretta, alcune per essere secrete, altre per rimpiazzare proteine consunte o degradate. La precisione nello smistamento è quindi essenziale per accrescimento, divisione e funzionalità cellulare.
Una parte degli organuli riceve proteine direttamente dal citosol: ciò vale per mitocondri, cloroplasti, perossisomi e per il nucleo (compreso il suo contenuto interno). Altri compartimenti, come apparato di Golgi, lisosomi, endosomi e membrane nucleari interne, ricevono proteine e lipidi prevalentemente in modo indiretto tramite il reticolo endoplasmatico (RE), che costituisce un polo primario di biosintesi di proteine e fosfolipidi. Le proteine entrano nell’RE a partire dal citosol; una quota vi rimane stabile, mentre la maggior parte viene inoltrata, mediante vescicole, al Golgi e quindi ad altri organuli o alla membrana plasmatica. I perossisomi acquisiscono una parte delle proteine di membrana dall’RE, ma la maggioranza dei loro enzimi è importata direttamente dal citosol.
Nel trasferimento diretto dal citosol agli organuli delimitati da membrana, lo smistamento è governato da informazioni codificate nella sequenza amminoacidica delle proteine. Tali “indirizzi” molecolari consentono l’inserimento nella membrana o l’ingresso nel lume dell’organulo di destinazione, assicurando che ogni proteina raggiunga il compartimento appropriato.
La sintesi proteica avviene, nella quasi totalità dei casi, su ribosomi citosolici; fanno eccezione poche proteine codificate e sintetizzate nei mitocondri e nei cloroplasti. Tuttavia, la maggioranza delle proteine destinate a questi organuli è codificata dal genoma nucleare, tradotta nel citosol e successivamente importata. Il destino di una proteina neoformata è determinato da specifiche sequenze amminoacidiche di smistamento: in assenza di tali segnali, le proteine restano nel citosol; in loro presenza, esse vengono riconosciute e indirizzate verso l’organulo corretto. Poiché le membrane sono barriere per le macromolecole idrofile, ogni organulo ha evoluto soluzioni specializzate per consentire il passaggio selettivo delle proteine attraverso uno o più doppi strati lipidici.
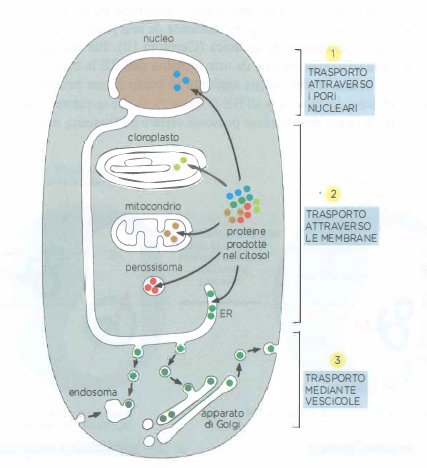
- Le proteine dirette al nucleo attraversano l’involucro nucleare mediante complessi di pori nucleari, che costituiscono varchi altamente selettivi: essi permettono la libera diffusione di piccole molecole e, al contempo, importano ed esportano attivamente macromolecole specifiche (meccanismo 1) (Figura 05.18-01). La selettività è mediata da domini ricchi in ripetizioni fenilalanina-glicina e dall’azione di recettori di trasporto regolati dal gradiente di Ran-GTP;
- Le proteine dirette all’RE, ai mitocondri o ai cloroplasti attraversano la membrana dell’organulo mediante traslocatori proteici intramembrana. A differenza del passaggio attraverso i pori nucleari, la catena polipeptidica è in genere traslocata in forma non ripiegata, assistita da chaperoni che ne prevengono l’aggregazione e ne guidano l’inserimento (meccanismo 2) (Figura 05.18-01). Nell’RE il complesso Sec61 media la traslocazione co- o post-traduzionale in risposta al riconoscimento, da parte della SRP, di un segnale idrofobico N-terminale; nei mitocondri, i complessi TOM e TIM coordinano l’attraversamento delle membrane esterna e interna; nei cloroplasti, i complessi TOC e TIC svolgono un ruolo analogo. Traslocatori correlati sono presenti anche nella membrana plasmatica dei batteri e trasferiscono proteine dal citosol all’ambiente esterno;
- Le proteine che procedono oltre l’RE e, più in generale, le componenti che si spostano tra compartimenti del sistema endomembranoso sono veicolate da vescicole di trasporto. Tali vescicole gemmano dalla membrana di un compartimento e si fondono con quella del compartimento ricevente, trasferendo sia proteine solubili (cargo) sia proteine e lipidi di membrana (meccanismo 3) (Figura 05.18-01). La formazione e la scelta delle vescicole coinvolgono rivestimenti (per esempio COPII, COPI, clatrina), recettori di cargo, piccole GTPasi della famiglia Rab e proteine SNARE che assicurano il riconoscimento e la fusione specifica.
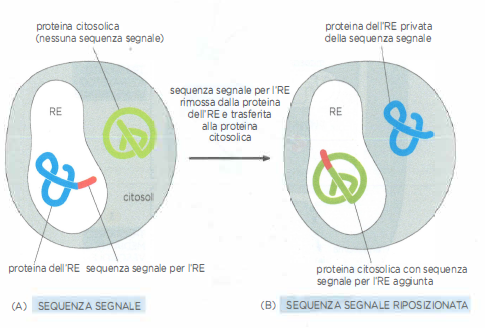
Un tipico segnale di smistamento consiste in un tratto continuo di 15–60 amminoacidi e, in molti casi, viene rimosso una volta raggiunta la destinazione. La (Tabella 05.18-01) riporta esempi rappresentativi di sequenze di indirizzamento per diverse mete intracellulari. Tali segnali sono necessari e sufficienti a determinare la localizzazione: esperimenti di biologia molecolare hanno dimostrato che l’eliminazione del segnale impedisce l’importazione, mentre il suo trasferimento a una proteina priva di indirizzo ne provoca il reindirizzamento verso la destinazione del segnale aggiunto (Figura 05.18-02).
Sequenze che specificano la medesima destinazione possono differire anche in modo marcato nella composizione primaria: spesso contano soprattutto proprietà fisico-chimiche, quali idrofobicità, distribuzione di cariche o capacità di formare eliche anfipatiche, più che l’identità puntuale dei residui. Le classi principali possono essere sintetizzate come segue:
- Segnale per il RE: tipicamente un peptide segnale N-terminale con nucleo idrofobico, riconosciuto dalla particella di riconoscimento del segnale (SRP); spesso viene scisso dalla signal peptidasi e, in combinazione con sequenze start/stop-transfer, determina l’orientamento delle proteine di membrana multipasso;
- Presequenza mitocondriale: sequenza N-terminale che tende a formare un’elica anfipatica, ricca di residui basici e povera di acidi; riconosciuta dai recettori TOM e traslocata attraverso TIM, con clivaggio da parte della peptidasi della matrice e possibile instradamento successivo a membrane interne o spazi intermembrana;
- Transit peptide cloroplastico: regione N-terminale ricca in Ser/Thr e povera in residui acidi, riconosciuta dai complessi TOC/TIC; ulteriori segnali possono indirizzare la proteina al tilacoide, dove operano vie Sec, Tat o SRP specifiche del cloroplasto;
- Segnali per perossisomi: motivi PTS1 (C-terminale, classico SKL o varianti affini) e PTS2 (N-terminale, nonapeptide conservato), riconosciuti dalle proteine Pex; peculiare è la capacità di importare proteine anche parzialmente ripiegate o oligomeriche;
- Segnali di localizzazione nucleare (NLS) e di esportazione nucleare (NES): brevi motivi ricchi in residui basici (per l’importazione) o leucina (per l’esportazione), non rimossi dopo il trasporto, riconosciuti da importine/esportine e modulati dal gradiente di Ran-GTP;
- Motivi di ritenzione o recupero nel sistema endomembranoso: sequenze come KDEL/KKXX che favoriscono il rientro di proteine residenti dell’RE dal Golgi tramite recettori specifici.
Un esempio sperimentale, distinto ma didatticamente equivalente, riguarda proteine fluorescenti reporter: una proteina citosolica priva di NLS rimane distribuita nel citosol; l’aggiunta di un NLS classico ne determina l’accumulo nel nucleo, mentre la mutazione dei residui basici critici impedisce l’importazione. Analogamente, il trasferimento di una presequenza mitocondriale a una proteina solubile può reindirizzarla alla matrice mitocondriale, dove il segnale viene rimosso. Questi risultati, in linea con quanto illustrato in (Figura 05.18-02), comprovano che le sequenze segnale sono moduli trasferibili capaci di determinare con precisione la destinazione cellulare.
In sintesi, la fedeltà dello smistamento dipende dall’integrazione tra le proprietà intrinseche dei segnali, i recettori di trasporto e i macchinari di traslocazione e fusione vescicolare. Tale coordinamento garantisce che la produzione di lipidi e proteine confluisca coerentemente nella biogenesi e nel mantenimento degli organuli.
| Funzione del segnale | Sequenza amminoacidica tipica |
|---|---|
| Importazione nel reticolo endoplasmatico | Met–Ser–Phe–Val–Ser–Leu–Leu–Val–Gly–Ile–Phe–Trp–Ala–Thr |
| Ritenzione nel lume del RE | Lys–Asp–Glu–Leu–COO⁻ |
| Importazione nei mitocondri | Met–Leu–Ser–Leu–Arg–Gln–Ser–Ile–Arg–Phe–Lys–Pro–Ala–Thr |
| Segnale per il nucleo (importazione) | Pro–Pro–Lys–Lys–Lys–Arg–Lys–Val |
| Segnale di esportazione dal nucleo | Met–Glu–Leu–Ser–Gln–Ala–Leu–Ala–Ser–Ser–Phe |
| Importazione nei perossisomi | Ser–Lys–Leu |
Sequenze segnale per il traffico intracellulare
Le proteine destinate a specifici compartimenti cellulari contengono brevi sequenze amminoacidiche che ne guidano il riconoscimento e il trasporto. Questi segnali molecolari permettono di indirizzare correttamente le proteine verso reticolo endoplasmatico, mitocondri, nucleo o perossisomi, garantendo la compartimentazione e la funzionalità dei processi cellulari.
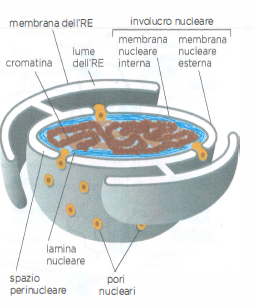
L’involucro nucleare, che separa il materiale genetico dal citoplasma, è costituito da due membrane concentriche che delimitano lo spazio perinucleare. La membrana interna ospita proteine in grado di ancorarsi ai cromosomi e alla lamina nucleare, una rete di filamenti di tipo lamina che fornisce sostegno meccanico e organizza l’architettura del nucleo. La membrana esterna, in continuità con il reticolo endoplasmatico (RE), condivide molte caratteristiche biochimiche con quest’ultimo e partecipa al medesimo sistema di membrane (Figura 05.18-03).
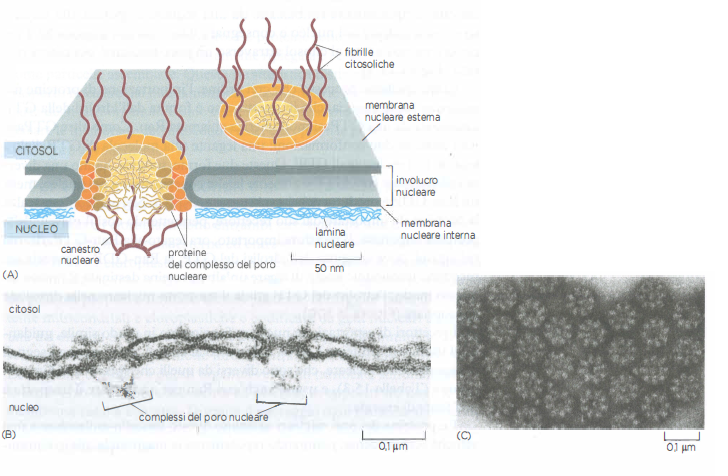
L’involucro è perforato da complessi del poro nucleare (NPC), vere e proprie porte regolabili che mediano il traffico bidirezionale tra nucleo e citosol. Ogni NPC è un’assemblata macromolecolare imponente, formata da circa 30 classi di nucleoporine organizzate con simmetria a otto raggi (Figura 05.18-04). Molte nucleoporine della via centrale possiedono regioni intrinsecamente disordinate, ricche di motivi fenilalanina-glicina (FG), che si comportano come una fase polimerica selettiva: un reticolo dinamico capace di ostacolare il passaggio di complessi voluminosi pur consentendo la diffusione rapida di soluti piccoli. In termini pratici, metaboliti e proteine di dimensioni ridotte attraversano passivamente il canale, mentre macromolecole e complessi superiori a una certa soglia dimensionale richiedono un trasporto mediato.
Le proteine dirette al nucleo portano in genere un segnale di localizzazione nucleare (NLS), spesso costituito da brevi sequenze ricche di lisina e arginina, presenti in forma mono- o bipartita, la cui diversità è riassunta nella (Tabella 05.18-01). A differenza di molti peptidi segnale per altri organuli, l’NLS non viene normalmente rimosso dopo l’ingresso e può essere riconosciuto reiteratamente.
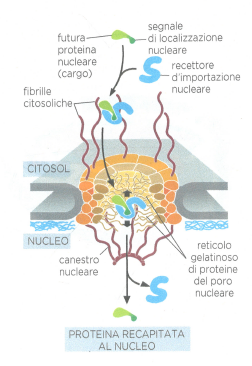
Il riconoscimento e l’attraversamento avvengono grazie a recettori citosolici del trasporto nucleare, appartenenti alla famiglia delle karioferine. I recettori di importazione nucleare (importine) si legano alle proteine cariche di NLS e le convogliano verso le fibrille citoplasmatiche dell’NPC, strutture filamentose che sporgono nel citosol e facilitano il reclutamento (Figura 05.18-05). L’avanzamento all’interno del canale risulta da interazioni transitorie, ad alta avidità ma bassa affinità, fra il recettore e i motivi FG delle nucleoporine: il recettore “salta” da un sito FG al successivo, aprendo localmente la matrice selettiva senza generare un vero foro aperto. Una volta nel nucleo, il carico viene rilasciato e il recettore ritorna nel citosol per un nuovo ciclo (Figura 05.18-05).
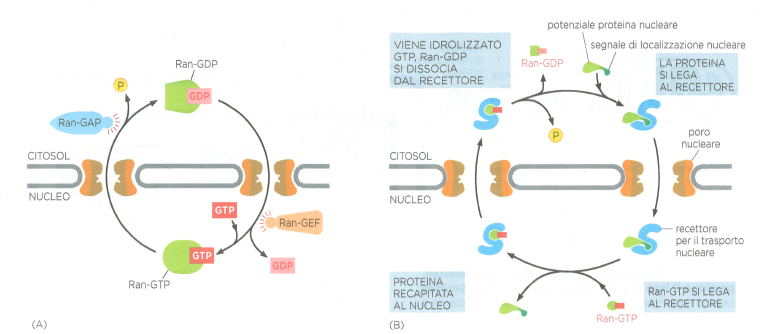
La direzionalità del trasporto dipende da un gradiente di stato nucleotidico della GTPasi monomerica Ran. La forma Ran–GTP è abbondante nel nucleo, mentre Ran–GDP prevale nel citosol (Figura 05.18-06). Tale asimmetria è mantenuta da fattori segregati: una GEF nucleare associata alla cromatina converte Ran–GDP in Ran–GTP, mentre una GAP citosolica accelera l’idrolisi di Ran–GTP a Ran–GDP. Nel ciclo d’importazione, il complesso importina–cargo si forma in citosol, attraversa l’NPC e, nel nucleo, l’associazione con Ran–GTP induce il distacco del cargo. Il complesso importina–Ran–GTP ritorna nel citosol dove l’idrolisi del GTP libera l’importina, pronta a un nuovo ciclo; il riciclo di Ran–GDP verso il nucleo è assicurato da trasportatori specifici (Figura 05.18-06). In tal modo l’energia chimica dell’idrolisi della GTP guida il processo in senso vettoriale.
Un principio analogo governa l’esportazione verso il citosol. I recettori di esportazione nucleare (exportine) riconoscono segnali di esportazione (NES), spesso ricchi di residui idrofobici, formano nel nucleo complessi stabili cargo–exportina–Ran–GTP e, una volta nel citoplasma, rilasciano il carico in seguito all’idrolisi della GTP legata. Alcuni tipi di RNA e ribonucleoproteine sfruttano sistemi dedicati: ad esempio, le subunità ribosomiali e gli tRNA dipendono da karioferine e Ran, mentre l’export degli mRNA utilizza complessi specifici e ATPasi che rimodellano i RNP al lato citoplasmatico, pur transitando sempre attraverso gli NPC.
Gli NPC raggiungono velocità notevoli: ciascun poro può trasferire simultaneamente in entrambe le direzioni un gran numero di carichi. Una peculiarità del trasporto nucleare è che le proteine attraversano il poro nella loro conformazione nativa e i precursori ribosomiali vengono esportati come particelle già assemblate, in netto contrasto con quanto avviene in altri organuli, dove l’attraversamento di membrane richiede spesso lo svolgimento della catena polipeptidica:
- Involucro nucleare: doppia membrana, lamina interna e continuità con l’RE esterno (Figura 05.18-03);
- NPC: circa 30 nucleoporine, matrice FG selettiva e trasporto mediato ad alta capacità (Figura 05.18-04);
- Segnali: NLS e NES riconosciuti da karioferine; NLS in genere non rimosso (Tabella 05.18-01);
- Energetica: gradiente Ran–GTP/Ran–GDP mantenuto da GEF nucleare e GAP citosolica, con idrolisi di GTP che conferisce direzionalità (Figura 05.18-06);
- Stato del carico: proteine importate ripiegate; complessi RNP esportati come particelle preassemblate.
| Funzione del segnale | Sequenza amminoacidica tipica |
|---|---|
| Importazione nel reticolo endoplasmatico | Met–Ser–Phe–Val–Ser–Leu–Leu–Val–Gly–Ile–Phe–Trp–Ala–Thr |
| Ritenzione nel lume del RE | Lys–Asp–Glu–Leu–COO⁻ |
| Importazione nei mitocondri | Met–Leu–Ser–Leu–Arg–Gln–Ser–Ile–Arg–Phe–Lys–Pro–Ala–Thr |
| Segnale per il nucleo (importazione) | Pro–Pro–Lys–Lys–Lys–Arg–Lys–Val |
| Segnale di esportazione dal nucleo | Met–Glu–Leu–Ser–Gln–Ala–Leu–Ala–Ser–Ser–Phe |
| Importazione nei perossisomi | Ser–Lys–Leu |
Sequenze segnale per il traffico intracellulare
Le proteine destinate a specifici compartimenti cellulari contengono brevi sequenze amminoacidiche che ne guidano il riconoscimento e il trasporto. Questi segnali molecolari permettono di indirizzare correttamente le proteine verso reticolo endoplasmatico, mitocondri, nucleo o perossisomi, garantendo la compartimentazione e la funzionalità dei processi cellulari.
| Funzione del segnale | Sequenza amminoacidica tipica |
|---|---|
| Importazione nel reticolo endoplasmatico | Met–Ser–Phe–Val–Ser–Leu–Leu–Val–Gly–Ile–Phe–Trp–Ala–Thr |
| Ritenzione nel lume del RE | Lys–Asp–Glu–Leu–COO⁻ |
| Importazione nei mitocondri | Met–Leu–Ser–Leu–Arg–Gln–Ser–Ile–Arg–Phe–Lys–Pro–Ala–Thr |
| Segnale per il nucleo (importazione) | Pro–Pro–Lys–Lys–Lys–Arg–Lys–Val |
| Segnale di esportazione dal nucleo | Met–Glu–Leu–Ser–Gln–Ala–Leu–Ala–Ser–Ser–Phe |
| Importazione nei perossisomi | Ser–Lys–Leu |
Sequenze segnale per il traffico intracellulare
Le proteine destinate a specifici compartimenti cellulari contengono brevi sequenze amminoacidiche che ne guidano il riconoscimento e il trasporto. Questi segnali molecolari permettono di indirizzare correttamente le proteine verso reticolo endoplasmatico, mitocondri, nucleo o perossisomi, garantendo la compartimentazione e la funzionalità dei processi cellulari.
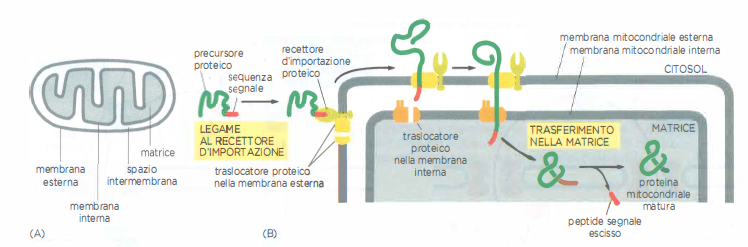
Mitocondri e cloroplasti sono circondati da due membrane, esterna e interna, e sono specializzati nella produzione di ATP; nei cloroplasti è presente anche il sistema tilacoidale. Pur possedendo un proprio genoma, la grande maggioranza delle loro proteine è codificata dal nucleo e sintetizzata nel citosol come precursori diretti agli organuli. Questi precursori espongono, in posizione N-terminale, sequenze segnale specifiche: nei mitocondri, una presequenza anfipatica capace di formare un’elica α con facce polare e idrofobica; nei cloroplasti, un peptide di transito ricco di residui idrossilati e povero di acidi. Il trasferimento avviene in siti di contatto tra le due membrane dell’involucro, dove complessi di traslocazione cooperano per attraversare i doppi strati lipidici; al termine, il segnale N-terminale viene rimosso da peptidasi dedicate (Figura 05.18-07).
A differenza dell’importazione nucleare, il passaggio attraverso le membrane mitocondriali e cloroplastiche richiede che le catene polipeptidiche siano non ripiegate. Ciò è reso possibile da chaperoni citosolici, che mantengono i precursori in uno stato di competenza all’import, e da chaperoni stromali o della matrice che ne sostengono il recupero conformazionale una volta oltrepassata la membrana. Nei mitocondri, l’inserimento nella matrice coinvolge i complessi TOM (membrana esterna) e TIM (membrana interna), assistiti dal potenziale di membrana interno e da un “motore” di importo dipendente da ATP. Nei cloroplasti, il trasferimento nello stroma è mediato dai complessi TOC e TIC, anch’essi coadiuvati da chaperoni e ATP.
La successiva distribuzione verso specifiche destinazioni interne richiede spesso segnali addizionali che diventano accessibili dopo la rimozione della presequenza primaria. Esempi includono: targeting alla membrana interna mitocondriale mediante sequenze di arresto del trasferimento o segnali interni multipli per proteine polipass, e indirizzamento al tilacoide nei cloroplasti tramite motivi che impiegano vie distinte (analoghe ai sistemi Sec o Tat, o a un percorso SRP cloroplastico). In tutti i casi, l’accuratezza del trasferimento dipende dal riconoscimento sequenziale dei segnali e dall’azione concertata delle macchine di traslocazione.
La crescita e l’omeostasi di mitocondri e cloroplasti richiedono anche l’approvvigionamento di lipidi. Sebbene una frazione di lipidi sia sintetizzata localmente (per esempio, cardiolipina nei mitocondri e galattolipidi nei cloroplasti), la maggior parte dei fosfolipidi di membrana proviene dall’RE, sede principale della biosintesi lipidica. Il trasferimento avviene tramite proteine che estraggono singole molecole da una membrana e le rilasciano in un’altra, spesso in corrispondenza di giunzioni di contatto ravvicinato tra RE e organuli. Questo flusso mirato consente di preservare le composizioni lipidiche caratteristiche dei vari compartimenti:
- Segnali N-terminali: presequenze mitocondriali anfipatiche e peptidi di transito cloroplastici rimossi dopo l’import (Figura 05.18-07);
- Macchine di traslocazione: TOM/TIM per i mitocondri, TOC/TIC per i cloroplasti, con chaperoni Hsp70/Hsp60 che assistono svolgimento e rifolding;
- Energia: ATP e, per i mitocondri, potenziale elettrochimico della membrana interna che favorisce il passaggio di sequenze cationiche;
- Smistamento introrganelle: segnali secondari dirigono verso membrane interne, esterne o tilacoidi, secondo meccanismi di avvio/arresto del trasferimento;
- Lipidi: forniti in gran parte dall’RE tramite proteine di trasferimento e contatti di membrana, con contributi sintetici specifici di ciascun organulo.
I perossisomi ospitano enzimi chiave per l’ossidazione di substrati potenzialmente tossici e per la biosintesi di fosfolipidi eterei, in particolare i plasmalogeni, componenti abbondanti della guaina mielinica degli assoni. La maggioranza delle proteine perossisomali è acquisita dal citosol mediante un sistema di importazione altamente selettivo. Per molte proteine matriciali, il segnale di targeting consiste in un breve motivo tripeptidico in posizione carbossiterminale ( Tabella 05.18-01), riconosciuto da recettori citosolici. In alternativa, un sottoinsieme di proteine utilizza un segnale N-terminale più lungo (PTS2), mediato da recettori specifici. Almeno uno di questi recettori, dopo aver legato il cargo, accompagna il complesso all’interno dell’organulo e in seguito viene riciclato nel citosol.
Analogamente a mitocondri e cloroplasti, la membrana perossisomale ospita un apparato di traslocazione proteica. In netto contrasto con i meccanismi di importazione mitocondriali e cloroplastici, molte proteine entrano nel perossisoma in forma nativa o quasi nativa, senza richiedere un completo disavvolgimento. Il poro di importazione, costituito da perossine di membrana, appare dinamico e transiente, e il processo rimane in parte enigmatico. L’energia necessaria è soprattutto legata al ciclo del recettore: ubiquitinazione regolatoria e attività di AAA-ATPasi di membrana (ad esempio Pex1/Pex6) estraggono il recettore dalla membrana e ne consentono il riutilizzo.
La biogenesi dei perossisomi è duplice: essi crescono e si dividono a partire da perossisomi preesistenti, ma possono anche originare de novo da vescicole che gemmano dal reticolo endoplasmatico (RE). La maggior parte delle proteine, incluse molte proteine di membrana, proviene direttamente dal citosol; tuttavia, una quota di proteine di membrana perossisomali viene inserita in vescicole derivate dall’RE, che successivamente si fondono con perossisomi presenti o maturano in nuovi perossisomi mediante importazione selettiva di proteine citosoliche.
Difetti nell’importazione perossisomiale provocano gravi patologie. La sindrome di Zellweger, la più severa tra le malattie del gruppo, deriva da mutazioni in geni delle perossine che bloccano l’ingresso delle proteine nei perossisomi. Ne conseguono marcate anomalie del sistema nervoso centrale, del fegato e del rene, spesso con esito letale nei primi mesi di vita. L’impatto clinico riflette il ruolo essenziale dei perossisomi nell’omeostasi lipidica e nella detossificazione cellulare.
| Funzione del segnale | Sequenza amminoacidica tipica |
|---|---|
| Importazione nel reticolo endoplasmatico | Met–Ser–Phe–Val–Ser–Leu–Leu–Val–Gly–Ile–Phe–Trp–Ala–Thr |
| Ritenzione nel lume del RE | Lys–Asp–Glu–Leu–COO⁻ |
| Importazione nei mitocondri | Met–Leu–Ser–Leu–Arg–Gln–Ser–Ile–Arg–Phe–Lys–Pro–Ala–Thr |
| Segnale per il nucleo (importazione) | Pro–Pro–Lys–Lys–Lys–Arg–Lys–Val |
| Segnale di esportazione dal nucleo | Met–Glu–Leu–Ser–Gln–Ala–Leu–Ala–Ser–Ser–Phe |
| Importazione nei perossisomi | Ser–Lys–Leu |
Sequenze segnale per il traffico intracellulare
Le proteine destinate a specifici compartimenti cellulari contengono brevi sequenze amminoacidiche che ne guidano il riconoscimento e il trasporto. Questi segnali molecolari permettono di indirizzare correttamente le proteine verso reticolo endoplasmatico, mitocondri, nucleo o perossisomi, garantendo la compartimentazione e la funzionalità dei processi cellulari.
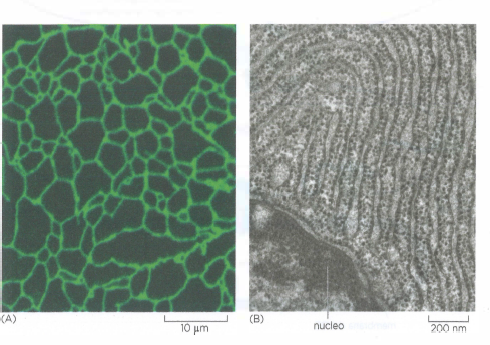
Il reticolo endoplasmatico rappresenta il sistema di membrane più esteso delle cellule eucariotiche (Figura 05.18-08) e costituisce la principale porta d’accesso alla via secretoria. Proteine dirette all’apparato di Golgi, a endosomi e lisosomi, nonché alla superficie cellulare, transitano inizialmente attraverso l’RE. Una volta trasferite nel lume o inserite nella membrana dell’RE, queste proteine non fanno più ritorno nel citosol: il loro percorso prosegue mediante vescicole di trasporto fino alla destinazione finale (Figura 05.18-01). Si riconoscono due categorie principali di proteine traslocate dal citosol all’RE:
- Proteine idrosolubili, che attraversano completamente la membrana per essere rilasciate nel lume dell’organelle;
- Proteine integrali di membrana, che inseriscono una o più regioni nel doppio strato lipidico e vi rimangono ancorate.
Le proteine solubili sono destinate alla secrezione o al lume di compartimenti della via secretoria; le proteine transmembrana restano invece nelle membrane dei vari organuli o della membrana plasmatica. La loro selezione dipende da una sequenza segnale per l’RE, generalmente un tratto idrofobo di almeno otto amminoacidi (Tabella 05.18-01), che promuove il reclutamento della macchina di traslocazione.
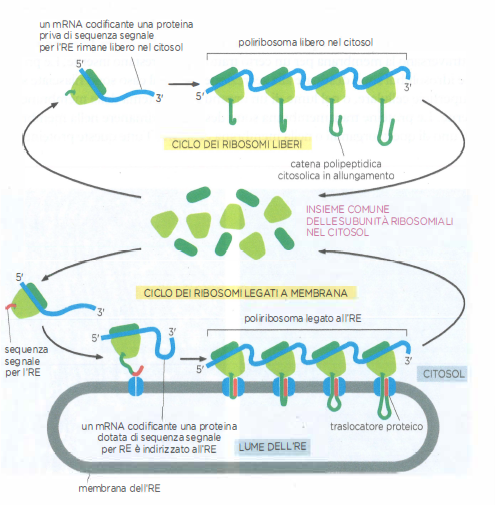
La traslocazione verso l’RE avviene in prevalenza in modo co-traduzionale: l’inserimento nel canale di traslocazione inizia prima del completamento della sintesi della catena polipeptidica. Di conseguenza, il ribosoma che traduce l’mRNA si associa alla membrana dell’RE, generando regioni di reticolo endoplasmatico ruvido per il tipico profilo granulare osservabile al microscopio elettronico (Figura 05.18-08).
Nel citosol coesistono ribosomi “liberi” e ribosomi “legati” a membrana. Entrambi sono identici per struttura e attività catalitica; differiscono esclusivamente per l’insieme di proteine sintetizzate. Quando un ribosoma inizia la traduzione di una proteina dotata di sequenza segnale per l’RE, la stessa sequenza ne indirizza il complesso verso la membrana dell’RE. L’energia per il trasferimento è fornita dall’allungamento della catena polipeptidica, che spinge il nascente polipeptide attraverso il canale di traslocazione. Poiché molte copie di ribosomi si associano a uno stesso mRNA, si formano poliribosomi; se la proteina possiede la sequenza per l’RE, l’intero poliribosoma si ancorerà alla membrana per l’inserimento simultaneo di più catene in crescita (Figura 05.18-09).
| Funzione del segnale | Sequenza amminoacidica tipica |
|---|---|
| Importazione nel reticolo endoplasmatico | Met–Ser–Phe–Val–Ser–Leu–Leu–Val–Gly–Ile–Phe–Trp–Ala–Thr |
| Ritenzione nel lume del RE | Lys–Asp–Glu–Leu–COO⁻ |
| Importazione nei mitocondri | Met–Leu–Ser–Leu–Arg–Gln–Ser–Ile–Arg–Phe–Lys–Pro–Ala–Thr |
| Segnale per il nucleo (importazione) | Pro–Pro–Lys–Lys–Lys–Arg–Lys–Val |
| Segnale di esportazione dal nucleo | Met–Glu–Leu–Ser–Gln–Ala–Leu–Ala–Ser–Ser–Phe |
| Importazione nei perossisomi | Ser–Lys–Leu |
Sequenze segnale per il traffico intracellulare
Le proteine destinate a specifici compartimenti cellulari contengono brevi sequenze amminoacidiche che ne guidano il riconoscimento e il trasporto. Questi segnali molecolari permettono di indirizzare correttamente le proteine verso reticolo endoplasmatico, mitocondri, nucleo o perossisomi, garantendo la compartimentazione e la funzionalità dei processi cellulari.
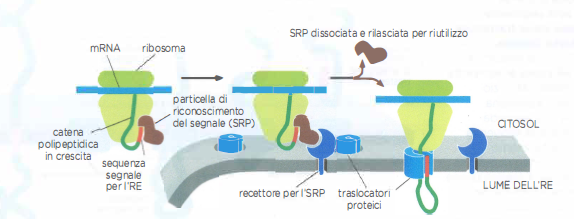
Il riconoscimento e l’aggancio delle catene nascenti alla membrana dell’RE coinvolgono due elementi proteici principali:
- La particella di riconoscimento del segnale, SRP (Signal Recognition Particle), un complesso ribonucleoproteico citosolico che lega sia il ribosoma sia la sequenza segnale emergente;
- Il recettore per SRP, localizzato sulla faccia citosolica della membrana dell’RE, che indirizza il complesso al traslocatore proteico.
Il legame dell’SRP alla sequenza segnale induce un temporaneo rallentamento dell’allungamento. Il complesso ribosoma–SRP viene quindi catturato dal recettore per SRP sulla superficie dell’RE; a seguito di interazioni dipendenti da nucleotidi guanilici, l’SRP si dissocia e il ribosoma viene trasferito al canale di traslocazione proteica (translocon) nella membrana dell’RE, consentendo la ripresa della sintesi con concomitante passaggio della catena nel lume (Figura 05.18-10).
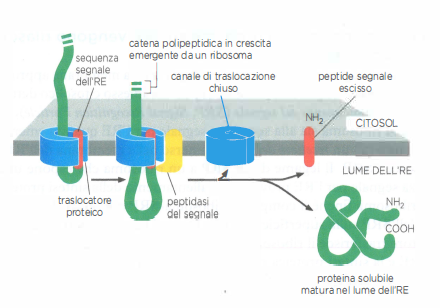
Nelle proteine solubili la sequenza segnale, in genere N-terminale, non solo dirige la catena al translocon, ma ne provoca anche l’apertura. Il peptide segnale rimane appoggiato al canale mentre il resto della proteina attraversa la membrana come un’ampia ansa. Durante la traslocazione, il peptide segnale viene idrolizzato da una peptidasi del segnale, esposta sul lato luminale, e il frammento viene poi rilasciato nel doppio strato lipidico, dove è rapidamente degradato. La traslocazione è assistita nel lume da chaperoni, come BiP, che favoriscono il corretto ripiegamento e prevengono aggregazioni premature.
Quando l’estremità carbossiterminale della catena oltrepassa il canale, la proteina viene liberata nel lume dell’RE come polipeptide solubile (Figura 05.18-11). Il translocon può aprirsi lateralmente per rilasciare segmenti idrofobi nella membrana, proprietà cruciale per l’integrazione delle proteine transmembrana descritta di seguito.
Non tutte le proteine destinate all’RE vengono rilasciate nel lume: una frazione rimane integrata nella membrana come proteine transmembrana. La loro topologia dipende da sequenze topogeniche che stabiliscono dove il trasferimento inizia e dove si arresta.
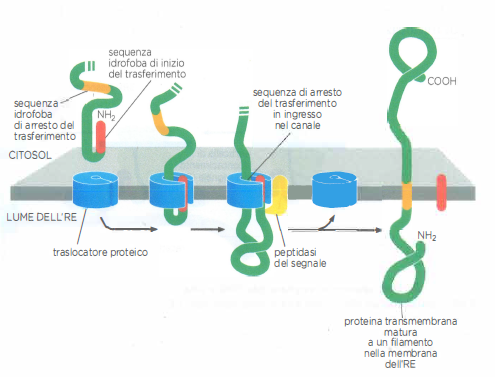
Nel caso più semplice, una proteina transmembrana a singolo passaggio con N-terminale luminale (tipo I) utilizza un peptide segnale N-terminale per avviare l’ingresso. La presenza, più a valle, di una sequenza idrofoba detta “arresto del trasferimento” interrompe il passaggio attraverso il canale. A questo punto, il translocon rilascia lateralmente il segmento idrofobo nel doppio strato lipidico; il peptide segnale N-terminale viene rimosso e la sequenza di arresto rimane come elica transmembrana che ancora la proteina. Il risultato è una proteina con estremità ammino-terminale nel lume ed estremità carbossi-terminale verso il citosol, topologia che rimane invariata lungo tutte le tappe di trasporto vescicolare (Figura 05.18-12).
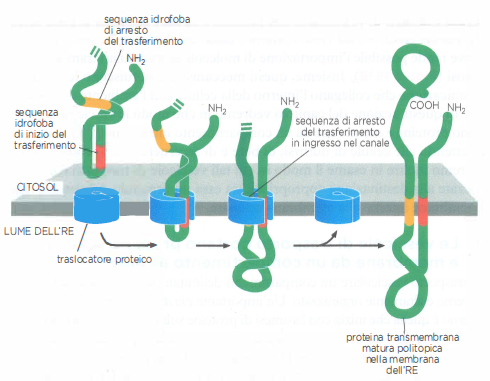
In molte proteine, invece, la sequenza che avvia la traslocazione è interna e funge da “segnale di avvio del trasferimento” o “signal anchor”; essa non viene scissa e rimane parte integrante del segmento transmembrana. L’orientamento della proteina (tipo II con N-terminale citosolico o tipo III con N-terminale luminale) dipende dalla distribuzione delle cariche nelle regioni fiancheggianti: il principio “positive-inside” favorisce il posizionamento delle cariche positive verso il citosol. Raggiunta una sequenza di arresto, il trasferimento si interrompe e le due sequenze idrofobe (inizio e arresto) vengono rilasciate nella membrana come eliche transmembrana (Figura 05.18-13).
Nelle proteine multipasso (politopiche) più complesse, la successione alternata di segnali di avvio e di arresto determina l’inserzione sequenziale di molteplici eliche α nel doppio strato: ogni segnale di avvio riapre il canale e ogni arresto lo richiude con rilascio laterale nel lipide. In questo modo, la catena nascente viene “intessuta” nella membrana durante la sintesi, definendo con precisione i tratti luminali e citosolici. Tale topologia, una volta stabilita all’RE, viene conservata durante l’intero percorso del traffico vescicolare fino alla destinazione finale.