Termodinamica
Definizione
Secondo la visione atomistica introdotta da John Dalton, le reazioni chimiche consistono nell’unire, separare o riorganizzare gli atomi; a distanza di due secoli questa interpretazione resta pienamente valida. Oggi, tuttavia, la comprensione dei processi chimici si integra con l’analisi delle variazioni di energia, elemento imprescindibile per descrivere perché e con quale velocità le reazioni avvengono. Un richiamo alla teoria cinetica dei gas, è utile: atomi e molecole sono in moto incessante e disordinato, collidono di frequente e la loro energia cinetica cresce all’aumentare della temperatura. A fini chimici, sono particolarmente rilevanti i seguenti aspetti:
- solo una frazione delle collisioni, quelle con energia pari o superiore a una soglia (energia di attivazione), è in grado di rompere i legami dei reagenti;
- dopo la rottura dei legami originari, la riorganizzazione degli atomi consente la formazione di nuovi legami, generando i prodotti;
- oltre all’energia, l’orientazione reciproca delle specie che collidono influisce sulla probabilità di esito reattivo, poiché i legami si formano in direzioni geometricamente specifiche.
Non è possibile accedere all’energia assoluta contenuta in un sistema chimico; ciò che è misurabile è la sua variazione al passaggio dallo stato iniziale allo stato finale. Diventa quindi cruciale delimitare con chiarezza il sistema e l’ambiente. Per sistema si intende la porzione dell’universo oggetto di studio; l’ambiente è tutto ciò che sta al di fuori. Si distinguono tre categorie operative: un sistema aperto scambia massa ed energia (tipicamente calore) con l’esterno, come accade per l’organismo umano o per una quantità d’acqua in una bottiglia aperta (Figura 04.06-01); un sistema chiuso consente scambi di energia ma non di materia, ad esempio la stessa bottiglia se chiusa ermeticamente in modo che il vapore non possa entrare né uscire (Figura 04.06-01); un sistema isolato, infine, non scambia né massa né energia con l’ambiente, come una bottiglia perfettamente isolata (Figura 04.06-01).
Durante una trasformazione, il sistema può cedere energia all’ambiente oppure assorbirla da esso. In termodinamica è utile distinguere tra calore e lavoro: il calore è il trasferimento di energia termica dovuto a una differenza di temperatura, mentre il lavoro è qualsiasi altro scambio energetico non termico. La prima legge della termodinamica si esprime come \( \Delta U = q + w \), dove \( \Delta U \) è la variazione di energia interna del sistema, \( q \) il calore scambiato e \( w \) il lavoro svolto su (o dal) sistema. A pressione costante, condizione comune nelle reazioni in soluzione o all’aria, il calore scambiato coincide con la variazione di entalpia: \( q_p = \Delta H \).
Il trasferimento di energia termica si manifesta attraverso variazioni di temperatura del sistema o dell’ambiente, grandezze che possono essere misurate con relativa facilità. Questo principio è alla base di quanto schematizzato in (Figura 04.06-02). Si consideri la combustione del metano, in cui metano e ossigeno reagiscono generando anidride carbonica e acqua. Trattando la reazione come sistema, l’incremento di temperatura dell’aria circostante segnala che una parte dell’energia potenziale chimica dei reagenti (associata ai legami) è stata convertita in energia cinetica delle molecole dell’ambiente, cioè in energia termica. Il flusso di energia dall’area di reazione verso l’ambiente è il calore, che fluisce spontaneamente dal corpo più caldo a quello più freddo.
In pratica, stimare accuratamente la temperatura dell’aria prima e dopo la reazione può risultare difficile. Per ovviare a ciò, si isola una porzione controllata dell’ambiente in grado di catturare il calore scambiato, così da determinare il calore di reazione. La calorimetria è la metodologia sperimentale dedicata a questa misura: il calore assorbito o ceduto da una massa \( m \) di materiale di capacità termica specifica \( c \) si calcola con \( q = m\,c\,\Delta T \); più in generale, per un apparato con capacità termica complessiva nota \( C \), vale \( q = C\,\Delta T \). Per la combustione del metano in condizioni standard, il processo è esotermico e la variazione di entalpia molare è circa \( \Delta H^\circ \approx -890,3 \) kJ·mol\(^{-1}\): nel linguaggio dei segni, \( q < 0 \) per il sistema, a indicare cessione di calore all’ambiente. Queste grandezze, determinate calorimetricamente, consentono di collegare la dinamica microscopica delle collisioni molecolari alla descrizione macroscopica dei flussi energetici osservabili.
Infine, è utile ricordare che, nel quadro della teoria cinetica, l’aumento di temperatura incrementa l’energia cinetica media delle particelle e la frazione di collisioni efficaci: per un gas ideale, l’energia cinetica traslazionale media è proporzionale alla temperatura assoluta, \( \langle E_\mathrm{k} \rangle = \tfrac{3}{2}k_\mathrm{B}T \). Questo legame tra moto molecolare, distribuzione delle energie e probabilità di superare l’energia di attivazione spiega perché il riscaldamento acceleri molte reazioni chimiche.
Processi che rilasciano o assorbono calore
Il primo principio della termodinamica afferma la conservazione dell’energia: l’energia totale dell’universo rimane costante. In chimica, questo principio si concretizza nello studio delle trasformazioni energetiche che accompagnano le reazioni. Consideriamo, a titolo generale, la trasformazione:
\[ A{-}B \;+\; C{-}D \;\longrightarrow\; A{-}D \;+\; C{-}B \]
I legami chimici immagazzinano energia potenziale; la rottura dei legami preesistenti richiede energia, mentre la formazione dei nuovi legami la rilascia. Se l’energia necessaria a spezzare i legami \(A{-}B\) e \(C{-}D\) è inferiore all’energia liberata generando \(A{-}D\) e \(C{-}B\), l’eccesso energetico viene ceduto all’ambiente: la reazione è esotermica e il contorno si riscalda. Viceversa, quando la somma delle energie per rompere i legami è superiore a quella rilasciata formando i prodotti, il sistema deve assorbire energia dall’esterno: la reazione è endotermica e l’ambiente si raffredda.
Un esempio tipico di processo esotermico è la combustione dell’idrogeno molecolare:
H\(_2\)(g) + 1/2 O\(_2\)(g) → H\(_2\)O(l) + 68,3 kcal ≃ 285,8 kJ (reazione esotermica)
Questa equazione termochimica indica che la formazione di 1 mol di acqua liquida da idrogeno e ossigeno libera circa 68,3 kcal sotto forma di calore a pressione costante. Invece, la decomposizione termica del carbonato di calcio costituisce un processo endotermico:
42,6 kcal + CaCO\(_3\)(s) → CaO(s) + CO\(_2\)(g) ≃ +178,3 kJ (reazione endotermica)
Qui, la scissione della struttura cristallina del carbonato richiede energia assorbita dal sistema. Oltre al calore, l’energia di reazione può manifestarsi in altre forme: processi chimici possono generare luce (per esempio in dispositivi LED chemiluminescenti) o fornire energia elettrica in una pila galvanica capace di alimentare un circuito.
In termini di bilancio di energia interna, vale la relazione fondamentale del primo principio: \[ \Delta U = q + w \] dove \(q\) è il calore scambiato con l’ambiente e \(w\) il lavoro (ad esempio di espansione/compressione). A pressione costante, condizione tipica delle reazioni chimiche in soluzione o in fase gas aperta, il calore scambiato coincide con la variazione di entalpia, \(q_p = \Delta H\).
Entalpia
L’entalpia, \(H\), è una funzione di stato definita come \(H = U + pV\). Nelle trasformazioni a pressione costante, la variazione di entalpia corrisponde al calore scambiato: \[ \Delta H_{\text{reazione}} = H_{\text{prodotti}} - H_{\text{reagenti}}. \] Per convenzione, quando il sistema cede calore all’ambiente \(\Delta H < 0\) (processo esotermico); quando lo assorbe \(\Delta H > 0\) (processo endotermico). Pertanto, per gli esempi precedenti si ha:
\(\Delta H\) (combustione di H\(_2\)) = −68,3 kcal;
\(\Delta H\) (decomposizione di CaCO\(_3\)) = +42,6 kcal.
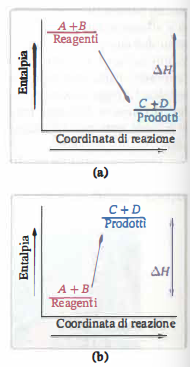
La (Figura 04.06-03) illustra i profili energetici di entalpia per processi esotermici (a) ed endotermici (b), mettendo in evidenza la differenza di livello energetico tra reagenti e prodotti.
Spontaneità e non spontaneità delle reazioni
Il solo segno di \(\Delta H\) non basta a stabilire la spontaneità di una reazione. Benché molti processi esotermici siano spontanei, esistono eccezioni; parimenti, non tutti i processi endotermici sono non spontanei. Accanto all’entalpia, un secondo fattore determina la direzione naturale dei processi: l’entropia.
Entropia
Il secondo principio della termodinamica afferma che, per un sistema isolato (o per l’universo considerato nel suo insieme), il disordine complessivo tende ad aumentare: \(\Delta S_{\text{universo}} \ge 0\). L’entropia, \(S\), quantifica il grado di dispersione dell’energia e di disordine del sistema. In termini qualitativi, passando da solido a liquido fino a gas l’entropia cresce, perché l’ordine a lungo raggio tipico dei solidi cristallini si attenua nei liquidi e scompare nei gas, dove le particelle esplorano un numero immensamente superiore di configurazioni possibili.
La descrizione statistica, introdotta da Boltzmann, lega l’entropia al numero di microstati accessibili, \(W\), mediante: \[ S = k_{\mathrm{B}} \ln W, \] a sottolineare che più configurazioni compatibili con lo stato macroscopico sono disponibili, maggiore è il disordine. Nella (Figura 04.06-04) e (Figura 04.06-05) sono presentati esempi di sistemi con differente grado di entropia.
L’entropia di reazione è data dalla differenza tra i valori dei prodotti e dei reagenti: \[ \Delta S_{\text{reazione}} = S_{\text{prodotti}} - S_{\text{reagenti}}. \] In generale, si osserva che processi in cui si formano più particelle gassose, o si passa da fasi più ordinate a meno ordinate, tendono ad avere \(\Delta S > 0\). Le reazioni che, al contempo, diminuiscono l’energia potenziale (\(\Delta H < 0\)) e aumentano il disordine (\(\Delta S > 0\)) risultano fortemente favorite dal punto di vista termodinamico. Viceversa, trasformazioni che richiedono energia e riducono l’entropia richiedono un apporto energetico esterno.
Per conciliare in un unico criterio i contributi di entalpia ed entropia, si utilizza l’energia libera di Gibbs, \(G\). La variazione di energia libera, \(\Delta G\), a temperatura \(T\) è: \[ \Delta G = \Delta H - T \Delta S, \] dove \(T\) è espressa in kelvin. Il segno di \(\Delta G\) predice la spontaneità: \(\Delta G < 0\) indica processo spontaneo, \(\Delta G > 0\) processo non spontaneo nelle condizioni considerate.
Ne derivano quattro casi limite, a seconda dei segni di \(\Delta H\) e \(\Delta S\):
- \(\Delta H > 0\) e \(\Delta S < 0\): \(\Delta G\) è sempre positivo, indipendente dalla temperatura; la reazione è non spontanea in ogni condizione;
- \(\Delta H < 0\) e \(\Delta S > 0\): \(\Delta G\) è sempre negativo; la reazione è spontanea in ogni condizione;
- \(\Delta H > 0\) e \(\Delta S > 0\): la spontaneità dipende dalla temperatura; è favorita a temperature sufficientemente alte, quando \(T\Delta S > \Delta H\);
- \(\Delta H < 0\) e \(\Delta S < 0\): la spontaneità dipende dalla temperatura; è favorita a temperature sufficientemente basse, quando \(T\Delta S < \Delta H\).
Energia libera standard di reazione. Si definisce energia libera standard \((\Delta G^\circ)\) la variazione di energia libera quando reagenti e prodotti si trovano in condizioni standard e la reazione si svolge a condizioni standard. La (Tabella 04.06-01) riporta le convenzioni comunemente adottate in chimica: temperatura di riferimento (solitamente 298,15 K), pressione di 1 bar per le fasi gassose, attività unitarie per i solidi e i liquidi puri, concentrazione 1 M per i soluti. In tali condizioni, \(\Delta G^\circ\) è ricavabile da \(\Delta H^\circ\) e \(\Delta S^\circ\) mediante \(\Delta G^\circ = \Delta H^\circ - T\Delta S^\circ\). Nelle soluzioni, lo stato standard chimico implica \([\mathrm{H}^+] = 1\ \mathrm{M}\), cioè pH = 0.
Poiché nei sistemi biologici il pH fisiologico è vicino a 7, si introduce lo stato standard biochimico, contraddistinto dall’apice primo: \(\Delta G^{\circ\prime}\), \(\Delta H^{\circ\prime}\), \(\Delta S^{\circ\prime}\). In questo caso \([\mathrm{H}^+] = 10^{-7}\ \mathrm{M}\) (pH = 7), mentre le restanti convenzioni rimangono analoghe a quelle chimiche. I valori \(\Delta G^{\circ\prime}\) descrivono in modo più realistico l’equilibrio e la direzione di marcia delle reazioni in ambiente cellulare.
Una relazione utile collega l’energia libera standard alla costante di equilibrio termodinamica \(K\): \[ \Delta G^\circ = -RT \ln K, \] dove \(R\) è la costante dei gas. Al di fuori delle condizioni standard, il criterio generale resta \(\Delta G = \Delta H - T\Delta S\). Si ricorda che la spontaneità termodinamica non implica rapidità: la velocità di reazione dipende dalla cinetica chimica e dall’energia di attivazione, distinta dal bilancio energetico globale.
Stati standard in chimica
| Stato della materia | Stato standard* |
|---|---|
| Gas | Pressione di 1 atm |
| Liquido | Liquido puro |
| Solido | Solido puro |
| Elemento | Forma allotropica più stabile a 25 °C e 1 atm |
| Soluzione | Concentrazione 1 M |
| Proteina (extra) | Soluzione tampone fisiologica (pH 7.4, 37 °C) |
| DNA/RNA (extra) | Doppia elica stabile in soluzione acquosa fisiologica |
| Elettrolita (extra) | Dissociazione standard in soluzione acquosa 1 M |
| *Temperatura di 25 °C e 1 atm. | |
| Tabella che riporta i criteri convenzionali utilizzati per definire gli stati standard. | |