Stato solido
Definizione
Nel solido le particelle costituenti sono disposte a distanza molto ridotta e soggette a forze attrattive sufficientemente intense da vincolarne il moto traslazionale. L’energia termica disponibile non basta, alle temperature ordinarie, a superare tali interazioni, per cui atomi, ioni o molecole oscillano attorno a posizioni di equilibrio ben definite. Questa organizzazione determina forma e volume propri, elevata rigidità meccanica e bassi coefficienti di dilatazione termica, pur in presenza di vibrazioni reticolari a livello microscopico.
L’incomprimibilità dei solidi è riconducibile alle ridottissime distanze intermolecolari e all’elevato modulo di comprimibilità, con variazioni di volume trascurabili anche a pressioni relativamente alte. All’aumentare della temperatura, l’incremento dell’energia vibratoria indebolisce l’efficacia delle forze di coesione e può condurre alla transizione allo stato liquido. La temperatura alla quale coesistono in equilibrio fasi solida e liquida è il punto di fusione, grandezza che riflette la natura e l’intensità delle interazioni intermolecolari e la struttura del solido. A parità di massa molecolare, sistemi polari o capaci di legami a idrogeno presentano in genere punti di fusione più elevati rispetto a materiali prevalentemente apolari.
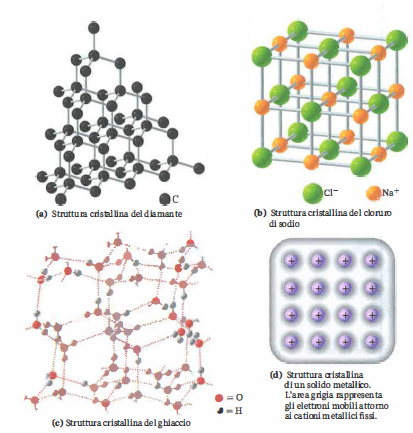
Si distinguono solidi cristallini, dotati di ordine a lungo raggio e periodicità reticolare, e solidi amorfi (o vetrosi), nei quali l’ordine è limitato a pochi strati di vicinato. Il diamante e il cloruro di sodio (Figura 02.03-01) rappresentano casi emblematici di cristalli con reticoli regolari, mentre vetri silicei, polimeri non cristallini e alcuni leganti idraulici costituiscono esempi tipici di solidi amorfi. Per questi ultimi è rilevante la temperatura di transizione vetrosa, al di sotto della quale il materiale si comporta come rigido e fragile, e al di sopra della quale mostra risposta meccanica più plastica. Nei solidi cristallini, proprietà come durezza, conduzione termica e comportamento meccanico possono dipendere dalla direzione cristallografica (anisotropia), nonché dalla presenza di difetti (vacanze, dislocazioni, bordi di grano) e di eventuali allotropi.
- Solidi ionici: formati da reticoli di cationi e anioni, stabilizzati da interazioni coulombiane di lungo raggio; presentano alte energie reticolari, elevati punti di fusione e durezza, ma risultano fragili per la tendenza a scorrimenti di piani che portano a repulsioni tra cariche uguali; sono isolanti allo stato solido e diventano buoni conduttori se fusi o disciolti in solventi polari, grazie alla mobilità degli ioni; esempi: cloruro di sodio, fluoruro di calcio, ossido di magnesio;
- Solidi a rete covalente: costituiti da estese reti tridimensionali di legami covalenti forti; manifestano punti di fusione molto elevati (frequentemente nell’intervallo 1 200 °C–2 000 °C), grande durezza e insolubilità nella maggior parte dei solventi; includono materiali isolanti (diamante) e semiconduttori (silicio, carburo di silicio, quarzo), con proprietà elettroniche descrivibili tramite bande di valenza e di conduzione e modulabili mediante drogaggio;
- Solidi molecolari: formati da molecole discrete aggregate da forze intermolecolari deboli (forze di London, interazioni dipolo-dipolo, legami a idrogeno); mostrano punti di fusione relativamente bassi, volatilità talora apprezzabile e bassa conducibilità elettrica; esempi rappresentativi sono lo zolfo rombico, lo iodio e il ghiaccio d’acqua (Figura 02.03-01), nel quale la rete di legami a idrogeno conferisce un punto di fusione più alto rispetto a molte altre molecole di massa simile;
- Solidi metallici: composti da nuclei positivi immersi in un “gas” di elettroni delocalizzati; la sovrapposizione di orbitali genera bande elettroniche parzialmente occupate, responsabili di elevata conducibilità elettrica e termica; la malleabilità e la duttilità derivano dallo scorrimento dei piani cristallini senza rottura del legame metallico; struttura cristallina (cubica a corpo centrato, cubica a facce centrate, esagonale compatta), purezza e presenza di leghe (per esempio rame, argento, ottone) modulano le proprietà meccaniche e fisiche.
Dal punto di vista geometrico, la periodicità dei solidi cristallini è descritta da celle elementari e reticoli di Bravais; la natura del reticolo e la coordinazione locale determinano densità, direzioni preferenziali di scorrimento e comportamento anisotropo. L’energia reticolare, la polarizzabilità e la massa delle specie coinvolte influiscono su grandezze termodinamiche e di trasporto.
La sublimazione è la transizione diretta dallo stato solido a quello gassoso e si verifica quando la pressione di vapore del solido, a una data temperatura, eguaglia la pressione esterna senza passare per la fase liquida. Alcuni solidi molecolari possiedono a temperatura ambiente pressioni di vapore sufficientemente elevate da rendere osservabile il fenomeno: l’anidride carbonica allo stato solido (ghiaccio secco) e composti aromatici come la naftalina lo illustrano chiaramente. Anche il ghiaccio e la neve, in condizioni di aria secca e temperature inferiori a 0 °C, possono diminuire di massa nel tempo per sublimazione, pur in assenza di fusione, convertendosi in vapore acqueo.
Il comportamento può essere razionalizzato mediante il diagramma di fase: al di sotto del punto triplo, la fase liquida non è termodinamicamente stabile e la trasformazione avviene tra solido e vapore. La dipendenza della pressione di vapore dalla temperatura è descritta, in prima approssimazione, dall’equazione di Clausius–Clapeyron integrata per la sublimazione: \[ \ln p_{\text{sub}} = -\frac{\Delta H_{\text{sub}}}{R}\frac{1}{T} + C, \] dove \(\Delta H_{\text{sub}}\) è l’entalpia molare di sublimazione, \(R\) la costante dei gas e \(C\) una costante di integrazione. Valori elevati di \(\Delta H_{\text{sub}}\) implicano pendenze ripide e pressioni di vapore più basse a parità di temperatura.
La sublimazione ha risvolti applicativi significativi: nella liofilizzazione di farmaci e alimenti, l’acqua congelata viene rimossa direttamente come vapore sotto vuoto, preservando struttura e principi attivi; deodoranti solidi e canfora mostrano perdita di massa per sublimazione in ambienti ventilati. La comprensione quantitativa del fenomeno richiede la misura di pressioni di vapore, calori latenti e la valutazione degli equilibri di fase in funzione di temperatura e pressione.