Stato liquido
Definizione
I liquidi presentano una comprimibilità estremamente ridotta: le particelle sono già impacchettate a distanze molto brevi e, anche in presenza di pressioni elevate, il volume varia in misura minima. In termini quantitativi, la comprimibilità isoterma \( \kappa_T \) dei liquidi comuni è dell’ordine di \(10^{-10}\,\text{Pa}^{-1}\); per l’acqua a 25 °C vale circa \(4,6 \times 10^{-10}\,\text{Pa}^{-1}\), corrispondente a un elevato modulo di comprimibilità (modulo di bulk) \(K = 1/\kappa_T\), indice della resistenza alla riduzione di volume. Tale proprietà ha conseguenze pratiche in idraulica e nei processi ad alta pressione, dove una minima variazione di volume richiede pressioni molto grandi. La viscosità misura l’opposizione interna di un liquido allo scorrimento. La viscosità dinamica \( \eta \) (unità SI: Pa·s) compare nella legge di Newton per lo sforzo tangenziale \( \tau = \eta \,\frac{\mathrm{d}v}{\mathrm{d}y} \), che definisce i fluidi newtoniani. Due fattori ne determinano l’entità:
- intensità e natura delle interazioni intermolecolari (forze di dipolo-dipolo, legami a idrogeno, forze di dispersione);
- forma e ingombro delle molecole, che condizionano l’attrito sterico tra strati adiacenti di fluido.
Molecole polari e/o in grado di formare estesi legami a idrogeno, oppure con geometrie ramificate e poco “scorrevoli”, manifestano in genere viscosità elevate rispetto a specie apolari e compatte. Il glicerolo (glicerina), triolo altamente polare, fornisce un esempio istruttivo: a 20 °C ha una viscosità di ordine \(10^{0}\)–\(10^{1}\) Pa·s, molto maggiore dell’acqua (\(\sim 0,89\) mPa·s a 25 °C) e di idrocarburi leggeri come quelli della benzina (\(\sim 0,3\)–\(0,6\) mPa·s).
 |
| Modello molecolare. Acido lattico (C₃H₆O₃). |
 |
| Struttura della glicerina (glicerolo). C₃H₈O₃. |
L’elevata viscosità del glicerolo deriva dalla sua forte polarità e dalla fitta rete di legami a idrogeno fra le tre funzioni alcoliche, che aumentano la coesione e lo smorzamento del moto relativo degli strati di liquido. Questa caratteristica risulta utile in formulazioni dermocosmetiche: un fluido più viscoso tende a restare aderente alla zona di applicazione, modulando il rilascio di umidità. Al contrario, miscele di idrocarburi apolari a bassa viscosità scorrono con facilità in condotti e ugelli, proprietà desiderabile per carburanti e solventi a rapida diffusione. La viscosità diminuisce generalmente all’aumentare della temperatura. L’incremento di energia cinetica riduce l’efficacia delle forze attrattive e facilita il “disincastro” molecolare. Spesso la dipendenza segue una legge di tipo Andrade/Arrhenius: \( \eta(T) = A \exp\!\big(\tfrac{E_a}{RT}\big) \), con \(E_a\) energia di attivazione viscosa. In applicazioni pratiche, anche additivi e composizione influenzano la risposta reologica; per esempio, oli lubrificanti sono progettati per mantenere \(\eta\) quasi costante su ampi intervalli di temperatura tramite modificatori di indice di viscosità.
All’interfaccia liquido–gas le molecole subiscono una risultante di forze coesive rivolta verso l’interno, poiché sono circondate da un numero minore di vicine rispetto al bulk. La tensione superficiale \( \gamma \) (N/m) quantifica l’energia necessaria per aumentare l’area superficiale di unità; equivale alla “pelle” elastica che tende a minimizzare la superficie del liquido. La forma quasi sferica delle goccioline in quiete riflette proprio la minimizzazione dell’energia superficiale a volume costante. La tensione superficiale dipende dalla natura delle interazioni intermolecolari e dalla temperatura: liquidi fortemente polari e con legami a idrogeno (es., acqua) mostrano valori elevati di \( \gamma \) rispetto a liquidi apolari. Per l’acqua pura a 20 °C, \( \gamma \approx 72,8 \) mN/m, e diminuisce con l’aumentare di \(T\) a causa dell’indebolimento della coesione superficiale. Su superfici idrofobiche e lisce (ad esempio, una carrozzeria appena cerata), le gocce tendono a “perlare”, evidenziando angoli di contatto elevati e una marcata coesione interna. La tensione può essere modulata tramite tensioattivi, molecole anfifiliche che si adsorbono all’interfaccia orientando i gruppi apolari verso l’aria e quelli polari verso l’acqua. Effetti principali:
- riduzione di \( \gamma \), che facilita la bagnabilità e la penetrazione del liquido in pori e fibre;
- formazione di micelle oltre la concentrazione micellare critica (CMC), con emulsione e solubilizzazione di sostanze idrofobe;
- stabilizzazione di interfacce e controllo di fenomeni come la schiumazione e i gradienti di tensione (effetto Marangoni).
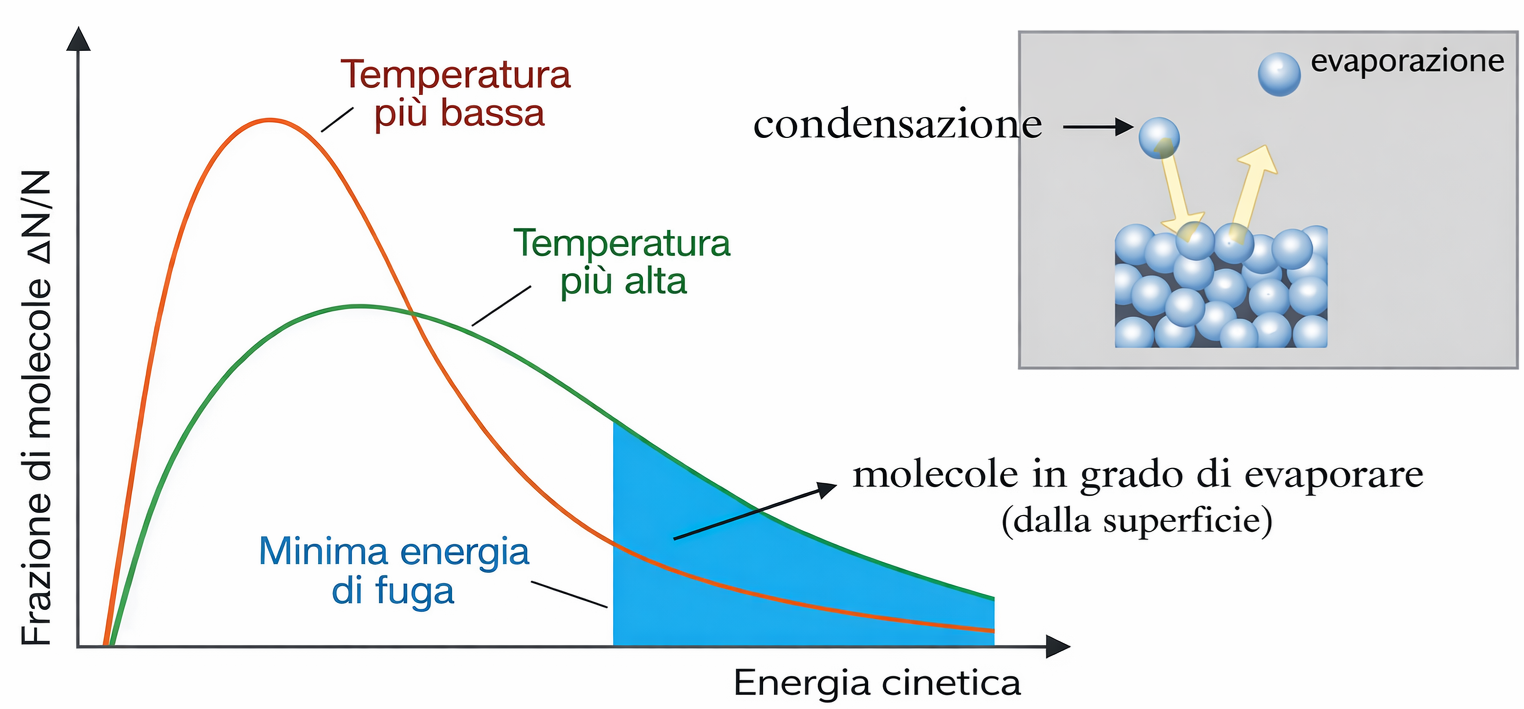
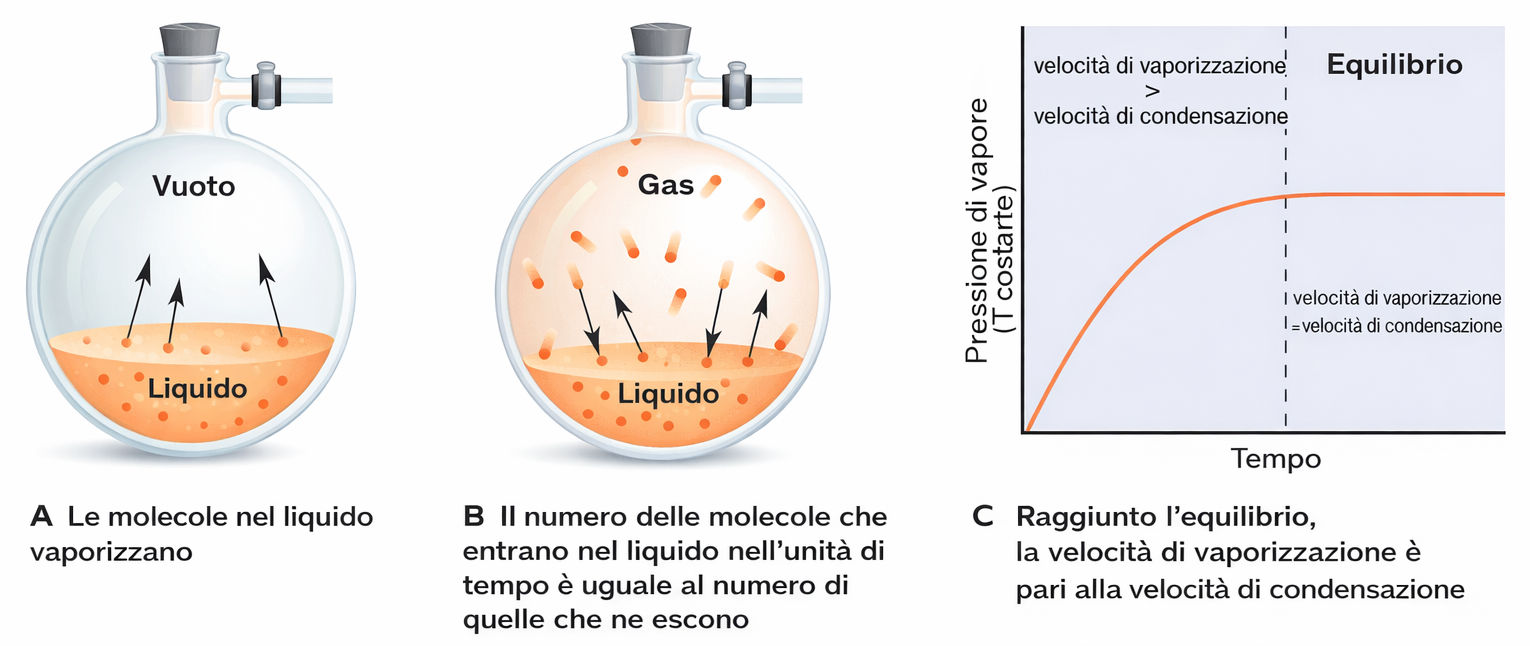
Consideriamo un liquido in un recipiente chiuso. Anche a temperatura inferiore al suo punto di ebollizione, una frazione delle molecole in superficie possiede energia sufficiente per lasciare la fase condensata ed entrare in fase gassosa (evaporazione). Il processo opposto, la ricattura delle molecole di vapore da parte del liquido, è la condensazione. L’origine statistica del fenomeno è illustrata dalla distribuzione delle energie cinetiche (Figura 02.02-01): pur avendo un’energia media fissata da \(T\), esiste una coda di molecole ad alta energia in grado di superare le attrazioni intermolecolari. Le trasformazioni elementari possono essere schematizzate come: \[ \mathrm{H_2O(l)} \xrightarrow{\Delta E} \mathrm{H_2O(g)}, \qquad \mathrm{H_2O(g)} \rightarrow \mathrm{H_2O(l)} + \Delta E. \] Dopo un certo tempo, le velocità di evaporazione e condensazione si uguagliano e si stabilisce un equilibrio dinamico fra le due fasi (Figura 02.02-02): \[ \mathrm{H_2O(l)} \rightleftharpoons \mathrm{H_2O(g)}. \] La pressione esercitata dal vapore alla temperatura considerata, quando l’equilibrio è raggiunto, è detta pressione di vapore del liquido. La relazione fra pressione di vapore e temperatura è fortemente non lineare e può essere descritta, in prima approssimazione, dall’equazione di Clausius–Clapeyron: \[ \ln p = -\frac{\Delta H_\mathrm{vap}}{R}\,\frac{1}{T} + C, \] dove \( \Delta H_\mathrm{vap} \) è l’entalpia molare di vaporizzazione. Interazioni intermolecolari più intense implicano \( \Delta H_\mathrm{vap} \) maggiore e, a parità di \(T\), una pressione di vapore minore. Il punto di ebollizione è la temperatura alla quale la pressione di vapore del liquido eguaglia la pressione esterna. Il punto di ebollizione normale corrisponde a una pressione di 1 atm (760 torr). Ne derivano alcune conseguenze operative:
- a quote elevate, dove la pressione atmosferica è inferiore a 1 atm, i liquidi bollono a temperature più basse;
- a pressioni superiori a 1 atm, come in pentole a pressione o autoclavi, l’ebollizione richiede temperature maggiori;
- liquidi polari e fortemente associati (es., acqua, alcoli poliossidrilati) hanno punti di ebollizione più alti dei liquidi apolari di massa molare simile, a causa delle forze coesive più forti.
Esempi quantitativi: a 90 kPa la temperatura di ebollizione dell’acqua è circa 96 °C, mentre in un ambiente a 2,0 atm essa sale a circa 120 °C. Analogamente, un solvente apolare con deboli forze di dispersione presenterà, alla stessa pressione esterna, un punto di ebollizione sensibilmente inferiore rispetto a un liquido polare di analoga massa molare. In sintesi, la compressibilità molto bassa, la viscosità dipendente da struttura e temperatura, la tensione superficiale legata alla coesione e la pressione di vapore determinano le principali risposte dei liquidi a stimoli meccanici e termici, oltre a controllare fenomeni quotidiani come la formazione di gocce, la bagnabilità dei solidi e le condizioni di ebollizione.
Le proprietà dei liquidi dipendono in misura determinante dalle forze intermolecolari. Oltre alle ben note attrazioni tra dipoli permanenti, che in sistemi polari riducono la pressione di vapore e innalzano il punto di ebollizione, esistono contributi attrattivi anche in sostanze non polari, molte delle quali risultano liquide o solide a temperatura ambiente. La coesione in questi composti è dovuta a interazioni deboli ma universali, scoperte e interpretate da Fritz London nel 1930, che scaturiscono dalle fluttuazioni quantistiche della densità elettronica: in ogni istante, la nuvola elettronica di una molecola o di un atomo può risultare asimmetrica, generando un dipolo istantaneo capace di indurre un dipolo in un vicino. Queste attrazioni, presenti in qualunque specie, polare o non polare, sono note come forze di dispersione di London. Nel linguaggio moderno, con “forze di van der Waals” si raccoglie l’insieme dei contributi attrattivi a corto raggio dovuti a: fluttuazioni elettroniche (London), interazioni tra dipoli permanenti mediati dalla rotazione termica (Keesom), e induzione di dipoli in specie polari o non polari (Debye). A distanza intermolecolare \(r\) sufficientemente grande rispetto alle dimensioni molecolari, tutte queste componenti scalano in media come \(-r^{-6}\). In particolare:
- dipolo permanente–dipolo permanente (Keesom): \(U_{\mathrm{K}} \propto -\dfrac{\mu_1^2 \mu_2^2}{3 k_{\mathrm{B}} T\, r^6}\), con una dipendenza esplicita dalla temperatura per via dell’orientamento termicamente mediato dei dipoli;
- dipolo permanente–dipolo indotto (Debye): \(U_{\mathrm{D}} \propto -\dfrac{\alpha\, \mu^2}{r^6}\), dove \(\alpha\) è la polarizzabilità;
- dipolo istantaneo–dipolo indotto (London): \(U_{\mathrm{L}} \propto -\dfrac{C_6}{r^6}\), con un coefficiente di London approssimabile da \(C_6 \approx \dfrac{3}{2}\,\dfrac{\alpha_1 \alpha_2 I_1 I_2}{I_1 + I_2}\), funzione di polarizzabilità ed energie di ionizzazione \(I_i\).
La forza delle interazioni di London cresce con la polarizzabilità, che tende ad aumentare con il numero di elettroni e con la “morbidezza” della nuvola elettronica. Ciò spiega, ad esempio, l’incremento marcato dei punti di ebollizione lungo il gruppo dei gas nobili: neon e xeno mostrano un salto notevole perché Xe è molto più polarizzabile di Ne. Anche la geometria conta: molecole allungate e con ampia superficie di contatto si attraggono di più dei loro isomeri compatti; per esempio, l’n-pentano bolle a 36,1 °C, mentre il neopentano, molto più sferico e con minore area di contatto, bolle a 9,5 °C. Le attrazioni dipolo-dipolo agiscono soltanto tra specie con dipolo permanente, mentre le forze di London operano per ogni molecola o atomo. Al di fuori delle interazioni di van der Waals, un caso particolare e più forte di interazione dipolare è il legame a idrogeno, di importanza cruciale per le proprietà di molti liquidi e per l’architettura dei sistemi biologici.
In numerosi liquidi polari le sole interazioni dipolo-dipolo non giustificano i punti di ebollizione osservati, spesso superiori a quanto previsto da massa e momento di dipolo. La discrepanza è attribuibile al legame idrogeno, che si stabilisce quando un idrogeno covalentemente legato a un eteroatomo molto elettronegativo e piccolo (tipicamente N, O o F) interagisce in modo direzionale con una coppia elettronica libera di un atomo vicino. Il risultato è una rete coesiva forte per standard intermolecolari: l’energia tipica di un legame a idrogeno in fase condensata è dell’ordine di 10–40 kJ·mol\(^{-1}\), molto inferiore a quella di un legame covalente ma spesso dominante tra le forze tra molecole. La presenza di un eteroatomo fortemente elettronegativo genera un legame X–H altamente polare, e dunque un intenso campo locale che facilita l’attrazione verso un accettore di legame. L’immagine seguente illustra il momento di dipolo in NH₃:
 |
| Polarità dell’ammoniaca. Momento dipolare e distribuzione di carica nella molecola di ammoniaca (NH₃). |
e la forte polarità del legame in HF:
| Distribuzione di carica e polarità nella molecola di fluoruro di idrogeno (HF) |
La direzionalità è un tratto distintivo: la configurazione energeticamente più favorevole è quasi lineare, X–H···Y con angolo H vicino a 180°. La capacità di una molecola di fungere da donatore (D, atomo X che porta H) e/o accettore (A, atomo Y con doppietto) determina quanti legami idrogeno può formare e la connettività della rete risultante. Un modo efficace per cogliere l’impatto del legame idrogeno è confrontare i punti di ebollizione di idruri isoelettronici in cui il legame H non si può formare o è molto debole, con quelli in cui esso è robusto. Consideriamo alcune serie:
- idruri del gruppo 16: H₂S (−60,7 °C), H₂Se (−41,3 °C), H₂Te (−2,2 °C) presentano ebollizioni molto inferiori rispetto all’acqua, per la quale il legame H conferisce un’anomala elevata coesione;
- idruri del gruppo 15: PH₃ (−87,7 °C) e AsH₃ (−62,5 °C) bollono ben al di sotto dell’ammoniaca, in cui il legame H, sebbene meno pervasivo rispetto all’acqua, è comunque significativo;
- alogenuroidi di idrogeno: HCl (−85,1 °C), HBr (−66,8 °C), HI (−35,4 °C) mostrano valori molto più bassi rispetto all’HF, nel quale il legame a idrogeno è possibile e stabilizzante.
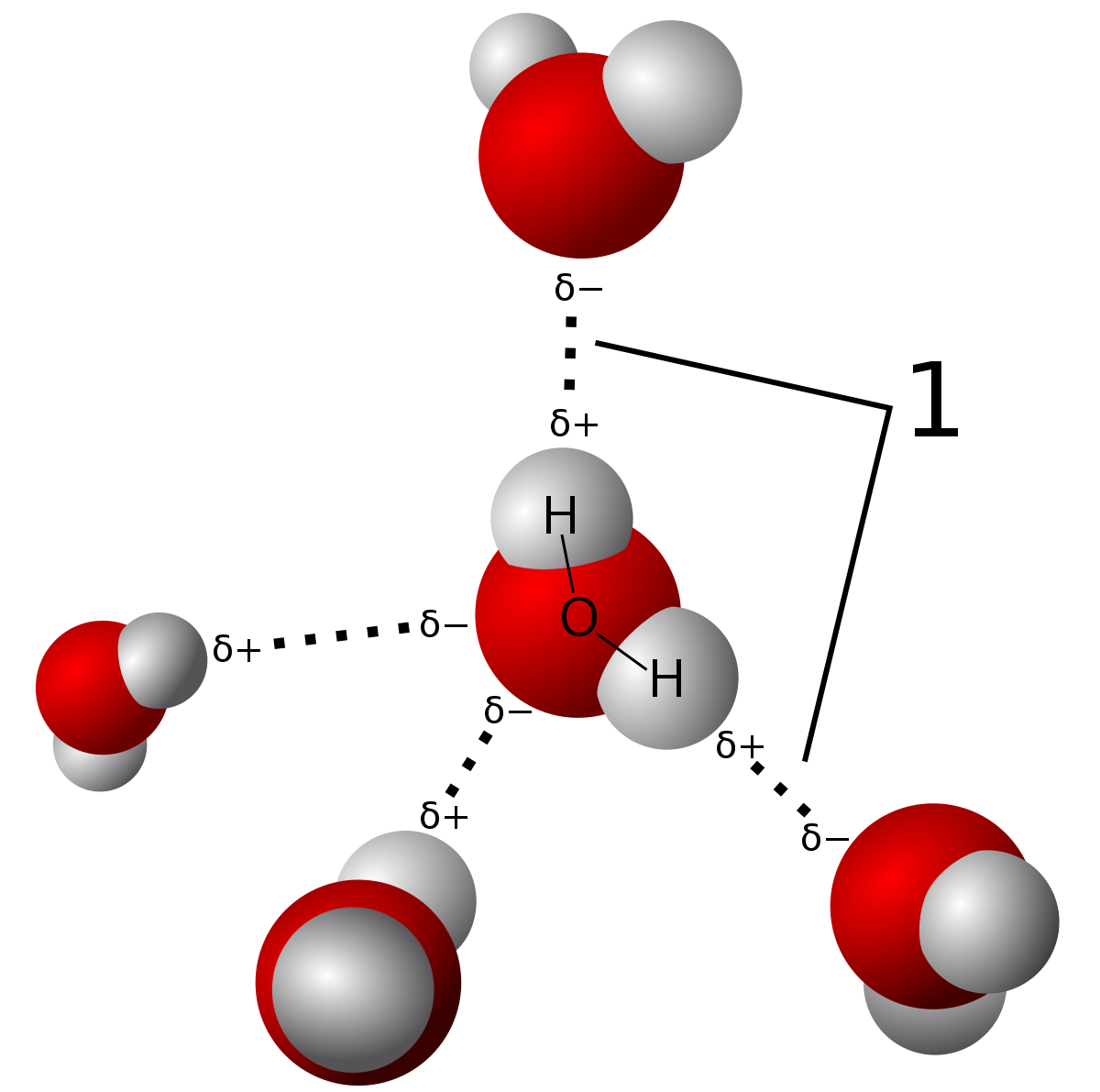
Il caso di H₂O, HF e NH₃ mette in luce come non basti l’elettronegatività per predire l’ordine dei punti di ebollizione. Pur avendo F l’elettronegatività più alta, HF non supera l’acqua. La ragione risiede nella connettività: una molecola d’acqua possiede due siti donatori (i due H legati a O) e due siti accettori (due doppietti su O) e può quindi impegnarsi fino a quattro legami a idrogeno, generando una rete tridimensionale estesa e altamente cooperativa. La complessità di tale reticolo, evidente nella (Figura 02.02-03), accresce l’energia coesiva del liquido e innalza il punto di ebollizione. L’ammoniaca dispone di tre H donatori ma di un solo doppietto disponibile su N: in media, ogni molecola può accettare un solo legame H, limitando la connettività complessiva. L’acido fluoridrico, al contrario, ha un solo H donatore e tre doppietti su F: il collo di bottiglia è il numero di siti donatori, che favorisce associazioni prevalentemente lineari o a catena piuttosto che una rete tridimensionale paragonabile a quella dell’acqua. La maggiore estensione e cooperatività del reticolo di legami H in H₂O si riflette in grandezze termodinamiche come l’entalpia di vaporizzazione, che per l’acqua a 1 atm vale circa 40,7 kJ·mol\(^{-1}\). Tali interazioni spiegano anche altre anomalie dell’acqua, tra cui elevata tensione superficiale, grande capacità termica e massimo di densità a 4 °C. Il legame a idrogeno è altresì pervasivo in ambito biologico: stabilizza strutture secondarie delle proteine (eliche α e foglietti β), controlla il riconoscimento molecolare e mantiene l’appaiamento complementare delle basi nel DNA (acido deossiribonucleico, vedi Paragrafo 19.2), dove migliaia di legami H cooperano per garantire integrità strutturale e fedeltà nella replicazione.