Soluzioni elettrolitiche e dissociazione elettrolitica
Definizione
Quando un soluto si disperde in un solvente può frammentarsi in specie cariche, gli ioni, che sono atomi o gruppi molecolari dotati di carica elettrica. In tali condizioni la soluzione è definita elettrolitica e il soluto prende il nome di elettrolita. La concentrazione di queste soluzioni, espressa come quantità di particelle per unità di volume, può essere indicata in g-ione/litro a 0 °C (osmole), dando luogo alla concentrazione osmolare. Un’altra grandezza largamente impiegata è il grammo-equivalente per litro di soluzione: un grammo-equivalente (g-Eq) rappresenta la frazione di grammo-ione che trasporta una carica elettrica pari alla costante di Faraday, F = N₀·e, dove N₀ = 6,02·10²³ è il numero di Avogadro ed e è la carica elementare dell’elettrone, e = 1,6·10⁻¹⁹ C; ne consegue F ≈ 96485 C. Per convenzione: 1 g-Eq corrisponde a 1 g-ione monovalente, 1/2 g-ione bivalente, 1/3 g-ione trivalente, e così via. Nella pratica analitica si usa spesso il milliequivalente per litro (mEq/L), pari a 10⁻³ Eq/L.
Tra la concentrazione osmolare e la concentrazione in equivalenti per litro di una soluzione ideale di un dato ione vale la relazione seguente:
\[C\left(\frac{Eq}{\text{litro}}\right) = \frac{C\left(\frac{g}{\text{litro}}\right) \cdot \text{valenza}(Z)}{\text{massa ione}(g)} = C(\text{osmole}) \cdot Z.\]
Esaminiamo ora il meccanismo fisico-chimico della dissociazione. Consideriamo un sale a legame ionico, come il cloruro di sodio (NaCl). Nel solido cristallino gli ioni Na⁺ e Cl⁻ sono organizzati in un reticolo stabilizzato da interazioni elettrostatiche. Allo scioglimento in acqua, il reticolo si disgrega e, per un elettrolita forte, la quasi totalità delle unità formula si separa nei due ioni costituenti, Na⁺ e Cl⁻. Il legame che tiene uniti gli ioni in un solido ionico è di natura coulombiana: cariche di segno opposto si attraggono con una forza data, in un mezzo dielettrico, dalla legge di Coulomb (si veda l’espressione in F = \frac{1}{4 \pi \varepsilon_0 \varepsilon_r} \frac{e^2}{r^2}):
\[F = \frac{1}{4\pi\varepsilon_o\varepsilon_r} \frac{e^2}{r^2},\]
dove r è la distanza tra le cariche e εᵣ è la costante dielettrica relativa del mezzo (Tabella 06.07-01). Nell’aria εᵣ ≈ 1, mentre nell’acqua εᵣ ≈ 80: l’interazione attrattiva fra ioni risulta pertanto attenuata di circa 80 volte in acqua rispetto all’aria, indebolendo il legame coulombiano.
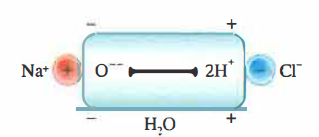
La sola riduzione dell’attrazione elettrostatica non basta tuttavia a giustificare la completa separazione degli ioni. Nei liquidi, l’agitazione termica produce urti incessanti fra le particelle; l’energia cinetica media cresce con la temperatura e gli urti tra ioni e molecole di solvente possono vincere il residuo vincolo coulombiano. Inoltre, l’acqua circonda gli ioni con gusci di solvatazione (idratazione), stabilizzandoli mediante interazioni dipolari: il polo parzialmente negativo della molecola d’acqua orienta verso cationi come Na⁺, mentre il polo positivo si dispone verso anioni come Cl⁻ (Figura 06.07-01). Questa solvatazione ostacola la ricombinazione ionica, rendendo la separazione più duratura.
Non sempre tutte le unità di soluto si dissociano, sia per ricombinazioni sia per equilibrio con la forma indissociata. Per quantificare il fenomeno si introduce il coefficiente di dissociazione elettrolitica δ, definito come rapporto tra il numero totale di particelle presenti in soluzione e il numero iniziale N di molecole di soluto immesse nel solvente:
\[\delta = \frac{v_+ + v_- + v_o}{N},\]
dove ν⁺, ν⁻ e ν₀ sono, rispettivamente, il numero di ioni positivi, di ioni negativi e di molecole indissociate in soluzione. Per una soluzione non elettrolitica si ha δ = 1, mentre nelle soluzioni elettrolitiche δ > 1; il valore massimo è pari al numero di ioni ottenibili dalla dissociazione completa della singola molecola (ad esempio, NaCl → Na⁺ + Cl⁻ implica δ = 2; H₂SO₄ → 2 H⁺ + SO₄²⁻ implica δ = 3). Si definisce inoltre grado di dissociazione α la frazione di molecole che si dissociano: α = 1 − (ν₀ / N). Vale α = 0 quando il soluto resta indissociato e α = 1 in caso di dissociazione totale.
La dipendenza di δ e α da variabili esterne è significativa. In prima approssimazione:
- l’aumento della temperatura incrementa l’energia cinetica delle particelle e favorisce la rottura dei legami ionici residui, accrescendo α;
- la polarità del solvente (εᵣ elevato) riduce l’attrazione coulombiana e stabilizza gli ioni solvatai, promuovendo la dissociazione;
- la diluizione, per gli elettroliti deboli, sposta l’equilibrio verso le specie ioniche (legge di diluizione di Ostwald), aumentando α;
- la forza ionica della soluzione influenza le interazioni tra ioni e, tramite i coefficienti di attività, può modificare l’effettivo grado di dissociazione osservato.
Gli elettroliti si classificano in forti e deboli in base a quanto è grande α in acqua alle condizioni standard. Gli elettroliti forti sono pressoché completamente dissociati: tra questi si annoverano sali come NaCl e KCl, acidi forti come HCl e H₂SO₄, e basi forti quali NaOH e KOH. Elettroliti deboli, come l’acido acetico o i bicarbonati, presentano una dissociazione parziale, con un equilibrio significativo tra forma molecolare e forme ioniche. Composti a legame marcatamente covalente e molte sostanze organiche polari ma non ionizzabili mostrano dissociazione trascurabile, con δ vicino a 1.
È utile collegare le grandezze di concentrazione all’assetto ionico in soluzione con un esempio numerico. Si consideri una soluzione 0,10 mol/L di MgCl₂ completamente dissociata: ogni unità formula genera 1 ione Mg²⁺ e 2 ioni Cl⁻. La concentrazione osmolare delle specie è allora C(osmole) = 0,10 osmole/L per Mg²⁺ e C(osmole) = 0,20 osmole/L per Cl⁻. Applicando (C \left( \frac{\text{Eq}}{\text{litro}} \right) = \frac{C \left( \frac{\text{g}}{\text{litro}} \right) \cdot \text{valenza} (Z)}{\text{massa ione} (\text{g})} = C (\text{osmole}) \cdot Z), si ottiene per il catione: C(Eq/L) = C(osmole)·Z = 0,10·2 = 0,20 Eq/L; per l’anione: C(Eq/L) = 0,20·1 = 0,20 Eq/L. In termini di milliequivalenti, entrambe le specie contribuiscono con 200 mEq/L, coerentemente con l’elettroneutralità della soluzione.
Il ruolo del mezzo acquoso merita un’ulteriore osservazione. L’elevata costante dielettrica (εᵣ ≈ 80) riduce l’energia potenziale elettrostatica tra ioni di carica ±e separati da una distanza r, secondo F = 1/(4π ε₀ εᵣ)·e²/r², rendendo più agevole il distacco. A ciò si somma l’energia di solvatazione, che compensa l’energia necessaria a separare gli ioni dal reticolo cristallino. L’insieme di questi contributi, unitamente agli urti termici, spiega perché molti sali, acidi forti e basi forti risultino elettroliti forti in acqua.
Le soluzioni contenenti ioni liberi (provenienti dalla dissociazione di uno o più soluti) conducono la corrente elettrica e si comportano da conduttori elettrolitici. Al contrario, un liquido molecolare puro privo di specie cariche libere è, in prima approssimazione, un isolante, poiché la concentrazione di ioni intrinseci è estremamente bassa.
| Sostanza / Tessuto | εr | Nota |
|---|---|---|
| Aria | 1.000590 | Riferimento quasi identico al vuoto, usato come base di confronto. |
| Acqua distillata | 81.07 | Elevata costante dielettrica, fondamentale per i processi biologici e biochimici. |
| Alcol etilico | 25.8 | Proprietà intermedia; usato come solvente e disinfettante. |
| Vetro | 7.0 | Materiale isolante con costante moderata. |
| Dimetilamina | 5.26 | Solvente organico, proprietà dielettriche relativamente basse. |
| Acetone | 20.7 | Ampiamente usato in laboratorio, caratterizzato da buona polarità. |
| Cloroformio | 4.8 | Bassa costante dielettrica, impiegato come solvente. |
| Membrana di assone | 9.0 | Rilevante nella trasmissione elettrica neuronale, influenza la conduzione nervosa. |
| Plasma sanguigno | ~68 | Elevata polarità, supporta la conduzione di ioni. |
| Tessuto muscolare | ~60 | Importante per l’elettrofisiologia e la stimolazione muscolare. |
| Tessuto adiposo | ~10 | Valore basso, agisce come isolante biologico. |
| Liquido cerebrospinale (CSF) | ~79 | Proprietà simili all’acqua, essenziale nei processi neurofisiologici. |
| Sangue intero | ~65 | Parametro critico per tecniche diagnostiche basate su campi elettrici (es. bioimpedenza). |
Permittività relativa di vari materiali
Indicazione dei valori della costante dielettrica relativa per diverse sostanze.