Ricezione del segnale: una molecola segnale si lega a un recettore proteico causando il suo cambiamento di forma
Definizione
Per gran parte della storia umana, senza disporre di conoscenze genetiche formali, si sono condotti veri e propri “esperimenti” sul DNA tramite incroci selettivi. Molte piante ornamentali, le spighe di mais con forme oggi familiari e le razze canine che popolano i cortili sono il risultato di selezione ripetuta per tratti desiderati, accumulata lungo innumerevoli generazioni (Figura 04.07-01). Solo con l’avvento, negli anni ’70 del XX secolo, delle tecniche di DNA ricombinante è divenuto possibile intervenire in modo mirato sui geni per ottenere organismi con caratteristiche definite.
Isolare e manipolare un gene richiede strategie sofisticate. A differenza di molte proteine che possono essere purificate come entità discrete, un gene occupa un breve tratto di una macromolecola di DNA molto più lunga. Anche i genomi procariotici, sebbene più compatti di quelli eucariotici, sono estesi: il genoma di Escherichia coli comprende circa 4,6 milioni di nucleotidi. Nei genomi eucariotici, oltre alla maggiore lunghezza, la presenza di introni, regioni regolative e sequenze ripetute complica ulteriormente l’isolamento di singole unità geniche.
La scoperta che ha reso affrontabile questo problema è quella delle endonucleasi di restrizione, enzimi batterici capaci di recidere il DNA a doppia elica in corrispondenza di sequenze bersaglio definite. Usandole, si ottiene una collezione riproducibile di frammenti specifici da qualunque genoma, inclusi quelli che contengono geni di interesse. Il frammento desiderato può essere quindi moltiplicato in copie identiche (amplificato) mediante clonaggio del DNA. Proprio l’amplificazione consente di separare un determinato gene dal resto del genoma e di analizzarlo sperimentalmente.
In questa prima parte vengono illustrati i principi alla base della generazione, dell’isolamento e della produzione in grande quantità di frammenti di DNA tramite clonaggio classico in batteri. Una seconda strategia, pur alternativa al clonaggio cellulare e condotta interamente in provetta, si basa su polimerasi del DNA particolari e consente di sintetizzare molte copie della sequenza target per reazione di amplificazione in vitro.
Come accade per molti strumenti cardine della biologia molecolare, anche le endonucleasi di restrizione furono identificate indagando un fenomeno biologico inatteso: alcuni batteri degradavano sistematicamente DNA “estraneo” introdotto dall’esterno. Lo studio del meccanismo alla base di questa distruzione selettiva portò all’individuazione di enzimi in grado di riconoscere particolari sequenze nucleotidiche e tagliare il DNA solo in corrispondenza di esse. Poiché tali attività impongono una vera e propria “restrizione” allo scambio di materiale genetico tra ceppi batterici, questi enzimi vennero denominati endonucleasi di restrizione. La comprensione di questo sistema di difesa ha aperto la strada a tecniche che hanno trasformato lo studio della cellula e dei geni.
Specie batteriche differenti producono endonucleasi con specificità diverse, ciascuna diretta contro una sequenza bersaglio definita (Figura 04.07-02). Il DNA della cellula ospite è protetto tramite un sistema complementare di modifica, tipicamente metilazioni delle stesse sequenze riconosciute, che impedisce il taglio: si parla di sistema restrizione-modificazione. Le sequenze bersaglio sono brevi, spesso palindromiche, e lunghe comunemente da 4 a 8 coppie di basi. Ciò comporta la presenza di numerosi siti distribuiti, in modo approssimativamente casuale, lungo una molecola di DNA. Il valore sperimentale di queste endonucleasi risiede nella loro riproducibilità: un dato enzima reciderà sempre la stessa molecola negli stessi punti, generando un insieme di frammenti identico da un campione all’altro.
La frequenza attesa dei tagli dipende dalla lunghezza della sequenza riconosciuta. Se si assume l’equiprobabilità delle quattro basi e l’assenza di bias di composizione, la probabilità che una specifica sequenza di lunghezza \(n\) si presenti in una posizione qualunque è \(p=(1/4)^n\); la distanza media tra siti è quindi \(E=1/p=4^n\). Per esempio, HaeIII riconosce un tetranucleotide e taglia in media una volta ogni \(4^4=256\) coppie di basi; un’endonucleasi con un sito ottanucleotide reciderà circa ogni \(4^8=65\,536\) coppie di basi. Questa differenza consente di scegliere l’enzima in base alla dimensione dei frammenti desiderata.
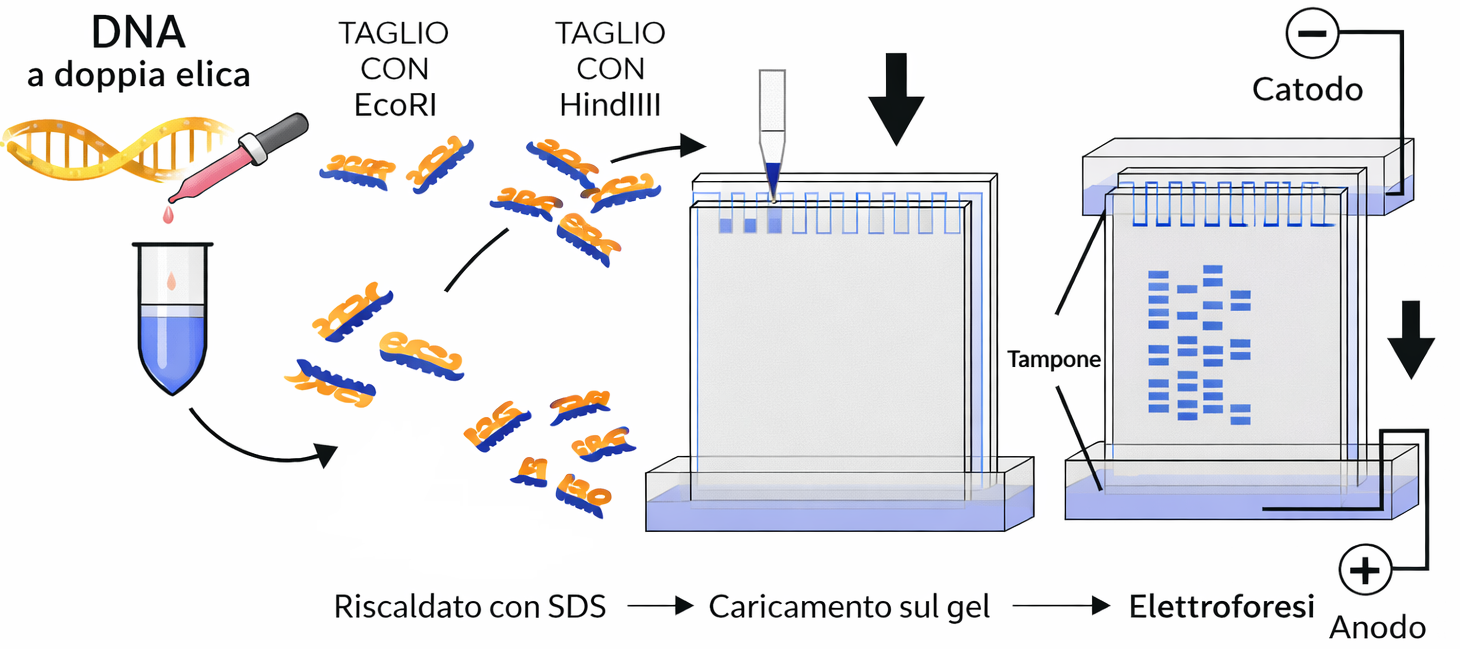
Gli enzimi di restrizione generano estremità diverse: alcuni, come HaeIII, producono estremità piatte (blunt), altri, come EcoRI, creano estremità coesive (“sticky”) con brevi sporgenze a singolo filamento. Le estremità coesive facilitano l’appaiamento specifico tra frammenti compatibili, caratteristica sfruttata nella costruzione di molecole ricombinanti.
Dopo la digestione enzimatica, i frammenti possono essere separati in base alla lunghezza mediante elettroforesi su gel, tecnica analoga a quella usata per le proteine. La miscela viene caricata in pozzetti all’estremità di un gel di agarosio o poliacrilammide, matrici che presentano una rete di pori di dimensione controllabile. Applicando un campo elettrico, il DNA, carico negativamente per via dei gruppi fosfato, migra verso l’anodo; i frammenti più lunghi attraversano la matrice più lentamente di quelli corti per effetto di setaccio molecolare. Dopo un intervallo di corsa appropriato, i frammenti risultano distribuiti lungo il gel in bande discrete ordinate per dimensione (Figura 04.07-03).
Poiché il DNA non è visibile a occhio nudo, si ricorre a coloranti intercalanti o leganti che fluorescono sotto luce UV o blu. L’incubazione con un tracciante consente di visualizzare bande che appaiono luminose all’illuminazione UV o nelle immagini acquisite (Figura 04.07-03). Un frammento di dimensione specifica può essere recuperato tagliando la banda corrispondente con una lama e purificando il DNA dal gel:
- Scelta della matrice: agarosio per frammenti da centinaia a decine di migliaia di coppie di basi; poliacrilammide per risoluzioni fini su frammenti corti;
- Condizioni di corsa: voltaggio, composizione del tampone e percentuale di gel influenzano velocità e risoluzione;
- Rilevazione: coloranti intercalanti con alta sensibilità e sistemi di illuminazione che minimizzano il danneggiamento del DNA, utili quando si devono recuperare i frammenti.
In molti intervalli dimensionali, la distanza migrata è approssimativamente proporzionale al logaritmo della lunghezza del frammento, permettendo la stima delle dimensioni mediante confronti con marcatori di peso molecolare.
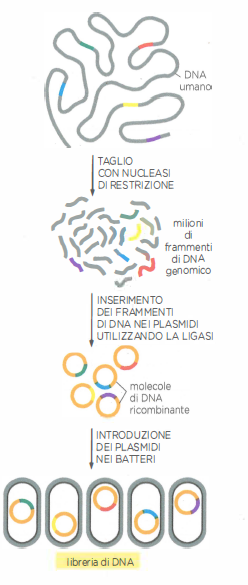
Una volta generati frammenti gestibili, il passo successivo è prepararli al clonaggio inserendoli in un vettore, ossia una molecola di DNA capace di replicare stabilmente in una cellula ospite. L’assemblaggio tra DNA di origine diversa produce una molecola chimerica, detta DNA ricombinante. Questo passaggio è fondamentale nell’approccio classico al clonaggio del DNA, poiché consente di propagare fedelmente il frammento di interesse in molte copie all’interno di batteri.
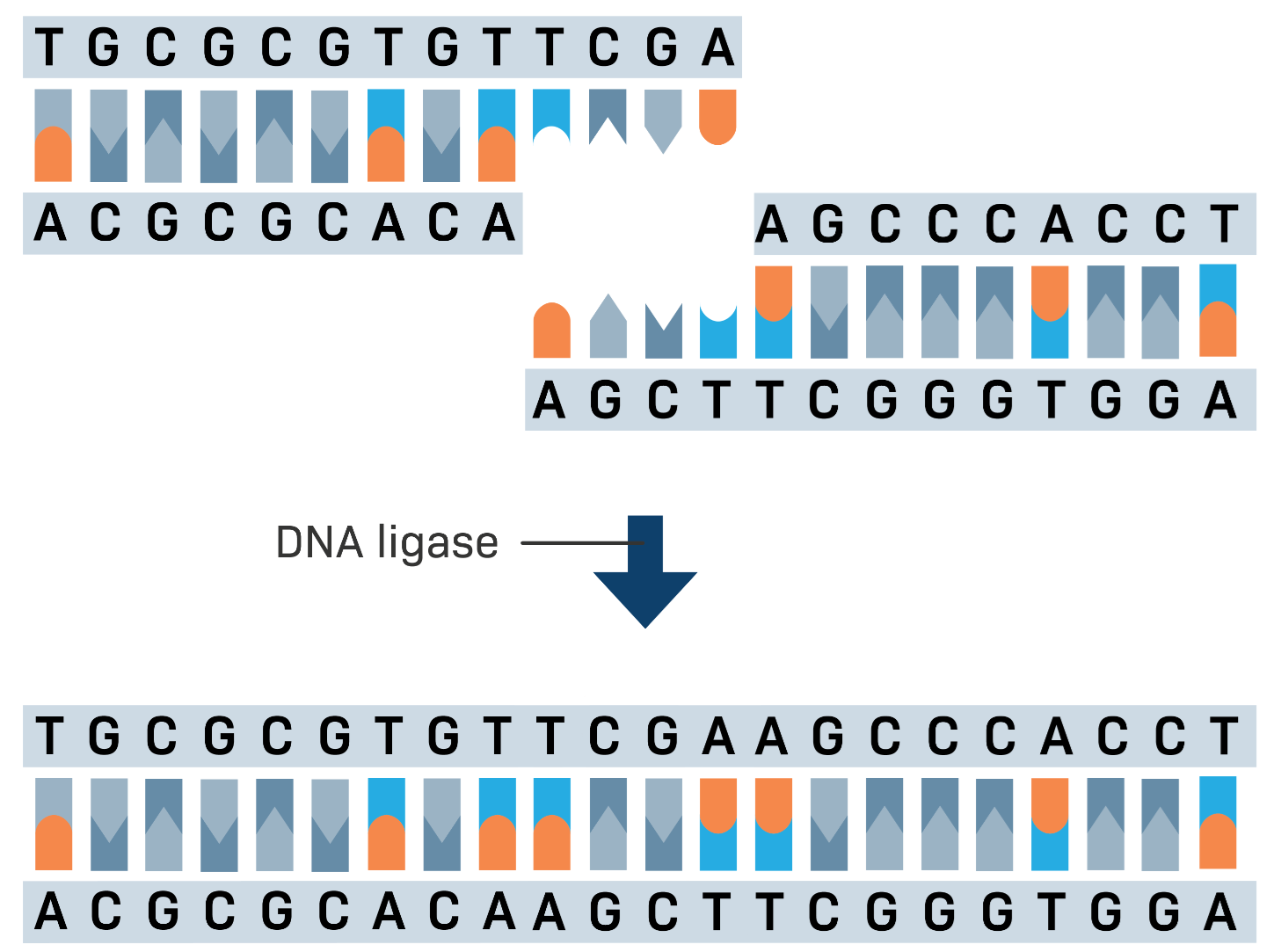
L’unione tra frammenti è mediata dalla DNA ligasi, enzima che nelle cellule sigilla le interruzioni del backbone fosfodiesterico durante replicazione e riparazione. In vitro, la ligasi catalizza la formazione del legame fosfodiestere tra estremità compatibili, chiudendo le “nicchie” generate dagli enzimi di restrizione e consentendo l’ottenimento di molecole ricombinanti che non esistono in natura (Figura 04.07-04). L’uso di estremità coesive complementari incrementa l’efficienza di giunzione, mentre le estremità piatte richiedono concentrazioni e condizioni di reazione più stringenti. Una volta ligato nel vettore, il DNA ricombinante può essere introdotto in cellule batteriche, in cui viene replicato insieme al vettore, rendendo possibile l’amplificazione del frammento bersaglio.
Accanto al clonaggio in cellule vive, esiste un approccio interamente in provetta, basato su DNA polimerasi termostabili che estendono primer specifici: tale metodo consente l’amplificazione selettiva di sequenze definite senza passare attraverso la cellula e rappresenta un complemento potente alle strategie di clonaggio tradizionali.
I vettori per il clonaggio sono tipicamente plasmidi, piccole molecole di DNA circolare presenti in molti batteri e capaci di replicarsi autonomamente grazie a una specifica origine di replicazione (ori) (Figura 04.07-05). L’indipendenza rispetto al cromosoma batterico consente a un inserto di DNA eterologo, integrato nel plasmide, di essere copiato molte volte all’interno di una singola cellula, generando un’elevata resa di materiale genetico. I plasmidi impiegati in laboratorio sono versioni ingegnerizzate di plasmidi naturali e includono, oltre all’ori, una regione ricca di siti di restrizione (spesso organizzata in un “polylinker” o multiple cloning site) per facilitare l’apertura e l’inserzione controllata del frammento di interesse.
Storicamente, molti plasmidi sono stati identificati per la presenza di geni che conferiscono resistenza agli antibiotici; tali determinanti, diffusi tramite trasferimento genico orizzontale, hanno contribuito all’ampia disseminazione della resistenza in popolazioni batteriche clinicamente rilevanti. Nei vettori moderni, i geni di resistenza (per esempio a ampicillina, kanamicina o cloramfenicolo) fungono da marcatori selettivi per isolare batteri che hanno acquisito il plasmide.
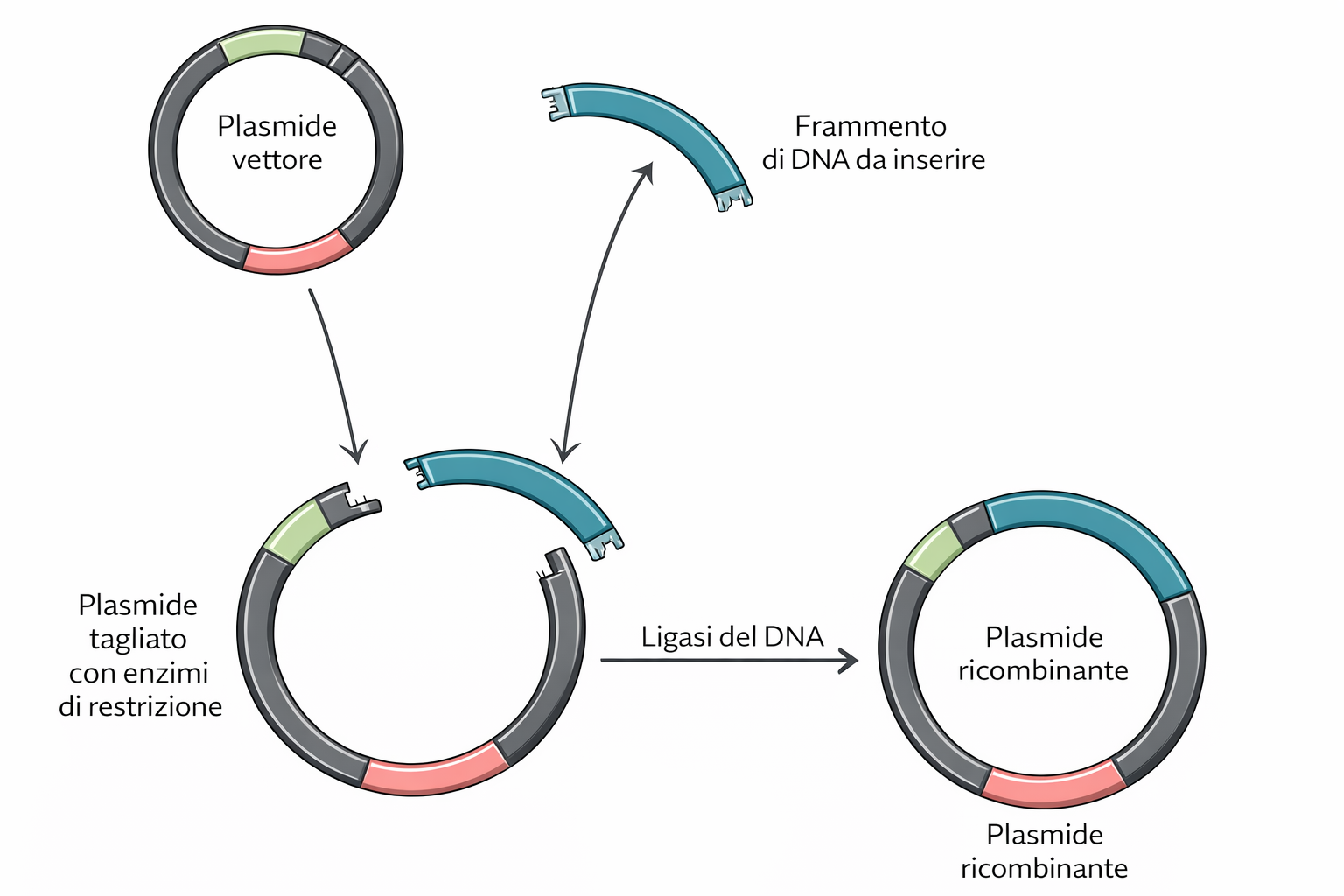
La costruzione di un DNA ricombinante implica l’apertura del plasmide purificato in un unico sito con un endonucleasi di restrizione e l’innesto del frammento di DNA da clonare con estremità compatibili; la DNA ligasi, in presenza di ATP, sigilla i giunti fosfodiesterici tra estremi coesivi o smussati, ripristinando la continuità del backbone (Figura 04.07-06). Per aumentare l’efficienza di clonaggio si impiegano, quando utile, strategie quali:
- clonaggio direzionale con due enzimi di restrizione diversi, per fissare l’orientamento dell’inserto;
- de-fosforilazione del vettore lineare per ridurre la ricircolarizzazione senza inserto;
- uso di sistemi di selezione per cloni ricombinanti, come la interruzione del gene lacZα (screening “blu-bianco”).
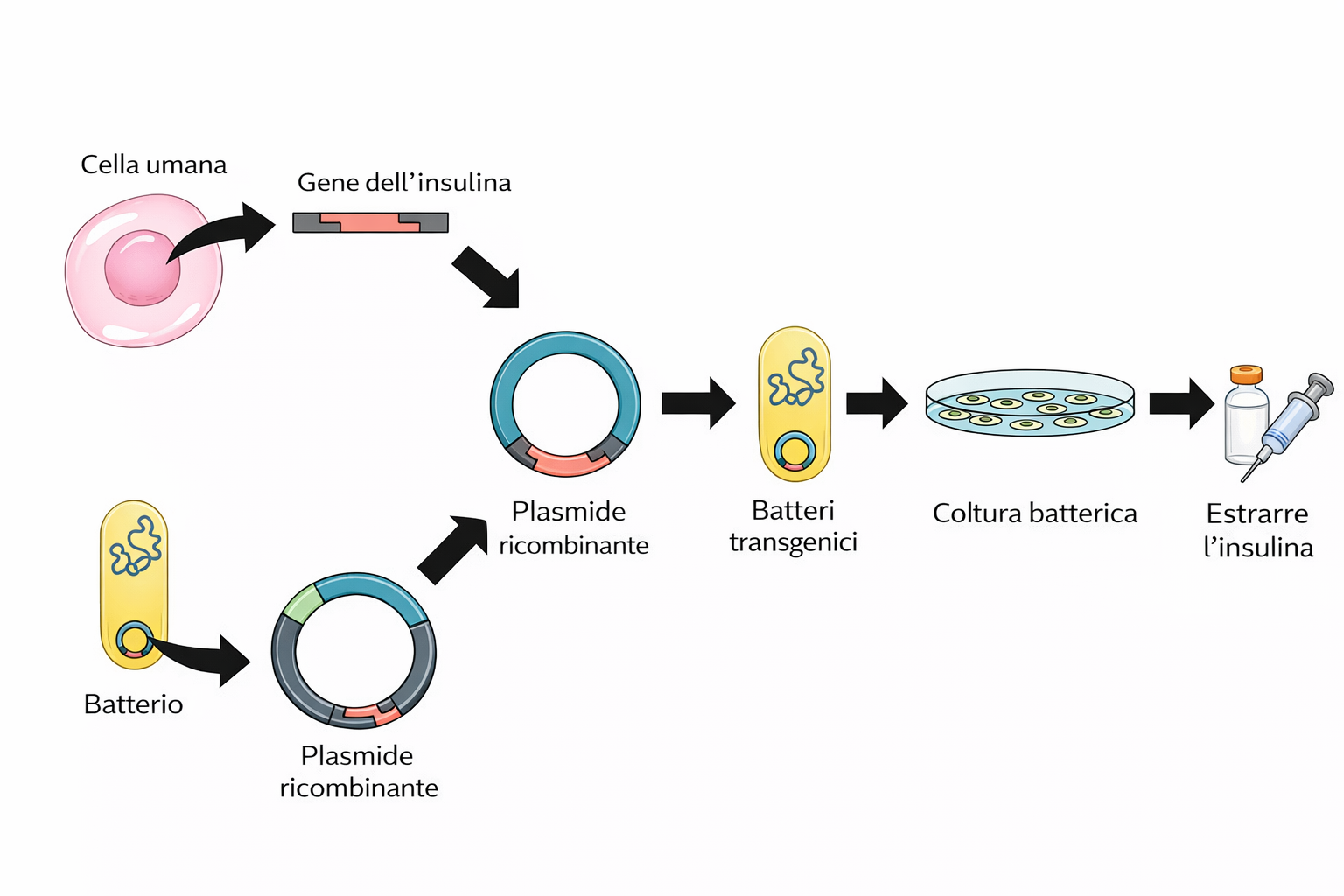
La molecola ricombinante viene quindi introdotta in batteri competenti sfruttando la trasformazione, un processo naturale di acquisizione di DNA esogeno. La competenza può essere indotta in laboratorio, ad esempio con trattamenti chimici e shock termico in Escherichia coli, oppure mediante elettroporazione. L’abilità del DNA di veicolare caratteri è stata dimostrata in esperimenti classici con Pneumococcus, in cui materiale genetico purificato da ceppi patogeni convertiva ceppi innocui in forme virulente, chiarendo il ruolo del DNA come sostanza genetica.
Le cellule trasformate vengono selezionate su terreni contenenti l’antibiotico appropriato e coltivate in brodi ricchi. Poiché il tempo di raddoppio di E. coli è di circa 30 minuti in condizioni ottimali, anche il numero di copie plasmidiche cresce rapidamente, talvolta sostenuto da origini di replicazione ad alto numero di copie. Dopo 24 ore, la coltura può contenere centinaia di milioni di plasmidi che portano l’inserto desiderato. I batteri vengono lisati (per esempio con lisi alcalina) e il DNA plasmidico viene separato dal cromosoma batterico di dimensioni molto maggiori (Figura 04.07-07). L’inserto può essere recuperato recidendo il plasmide con lo stesso enzima di restrizione usato per il clonaggio, e le specie di DNA (vettore e frammento) vengono separate mediante elettroforesi su gel (Figura 04.07-03). L’intera procedura consente di amplificare e purificare qualunque segmento di DNA, qualunque sia l’organismo di origine.
La digestione di un intero genoma con un enzima di restrizione genera un insieme numeroso di frammenti. Inserendo, in condizioni controllate, un singolo frammento per plasmide e trasformando E. coli a bassa concentrazione di DNA (in modo che ogni cellula riceva al massimo una molecola), si ottiene una popolazione di cloni che, collettivamente, costituisce una libreria di DNA. Quando i frammenti derivano dal DNA cromosomico totale, la collezione risultante, detta libreria genomica, rappresenta il genoma dell’organismo di partenza con un certo grado di copertura e ridondanza (Figura 04.07-08). Storicamente, librerie di questo tipo sono state fondamentali per il sequenziamento di genomi e per mappaggi fisici.
La dimensione minima di una libreria per ottenere una copertura desiderata P può essere stimata da: \[ N \ge \frac{\ln(1-P)}{\ln(1-f)}, \] dove f è la frazione del genoma contenuta in ciascun inserto medio. Questo formalismo guida la progettazione di librerie con probabilità elevata di includere qualsiasi locus.
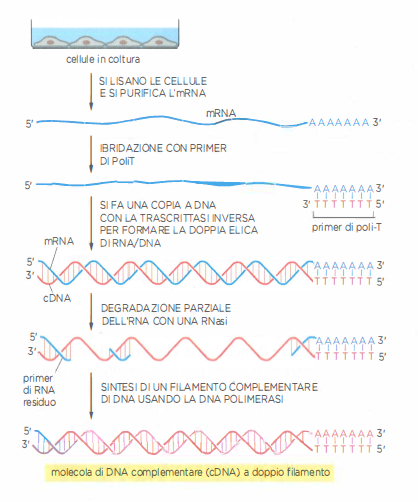
Per molte applicazioni è utile isolare soltanto sequenze codificanti. In batteri, l’espressione di geni eucariotici a partire da cloni genomici è inefficiente poiché le cellule procariotiche non rimuovono gli introni dai trascritti. Per produrre una proteina eucariotica in E. coli è quindi preferibile clonare la sola sequenza esonica continua. A tale scopo si costruisce una libreria di cDNA, nella quale le molecole rappresentano copie a doppio filamento degli mRNA presenti in uno specifico tipo cellulare o stato fisiologico. La preparazione prevede l’estrazione degli mRNA, spesso selezionati tramite la coda poli(A), la sintesi del primo filamento con una trascrittasi inversa e primer oligo(dT) o esameri casuali, e la successiva sintesi del secondo filamento tramite una DNA polimerasi (Figura 04.07-09). Le molecole di cDNA così ottenute vengono quindi clonate e propagate in batteri come descritto per i frammenti genomici (Figura 04.07-08).
Le differenze sostanziali tra librerie genomiche e di cDNA possono essere riassunte come segue:
- composizione: le librerie genomiche contengono un campione pressoché casuale dell’intero genoma, inclusi introni, sequenze ripetute, regioni regolative e spaziatrici; i cDNA rappresentano principalmente le regioni codificanti e, nei procarioti, sono direttamente traducibili;
- dipendenza dal tipo cellulare: i cloni genomici sono indipendenti dal tessuto di origine, mentre le librerie di cDNA riflettono il profilo trascrizionale del tipo cellulare analizzato;
- dinamica temporale: i cDNA cambiano con lo sviluppo, il ciclo cellulare e gli stimoli ambientali, consentendo analisi sull’espressione genica contestuale;
- dimensione degli inserti: i cloni genomici eucariotici possono essere voluminosi e difficili da maneggiare in plasmidi; per inserti molto grandi si ricorre a vettori dedicati (per esempio BAC), mentre i cDNA sono generalmente più compatti.
In ambito di espressione eterologa, i cDNA possono essere inseriti in vettori di espressione contenenti promotori batterici, siti di inizio traduzione e, se necessario, sequenze per tag di purificazione. Per ridurre la sovra-rappresentazione di mRNA altamente espressi, sono disponibili approcci di normalizzazione delle librerie, che appiattiscono l’abbondanza relativa dei trascritti.
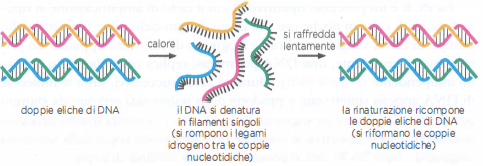
La capacità degli acidi nucleici di appaiarsi per complementarità delle basi consente di identificare con grande sensibilità sequenze specifiche di DNA o RNA. In condizioni fisiologiche, i due filamenti del DNA a doppia elica sono mantenuti insieme da legami idrogeno tra basi complementari; tali interazioni non covalenti si rompono riscaldando la soluzione fino a denaturare la doppia elica, tipicamente vicino a 90 °C. Abbassando poi la temperatura in condizioni opportune di salinità, i filamenti complementari possono rinaturare formando di nuovo la doppia elica, un processo detto ibridazione (Figura 04.07-10).
Per rilevare una sequenza specifica si impiega una sonda a singolo filamento (oligonucleotide o frammento più lungo) marcata con un tracciante radioattivo o fluorescente e complementare al bersaglio. La specificità dipende da lunghezza, contenuto in GC e condizioni di “stringenza” (temperatura e forza ionica). Per un oligonucleotide corto, una stima utile della temperatura di melting è: \[ T_m \approx 2\,(\#A+\#T) + 4\,(\#G+\#C)\;^\circ\text{C}, \] mentre per sonde più lunghe si impiegano modelli termodinamici più accurati. Aumentando la stringenza si discriminano anche singoli mismatch, caratteristica cruciale per distinguere varianti alleliche.
Le applicazioni dell’ibridazione includono:
- rilevazione di specifiche sequenze di DNA su membrane dopo separazione elettroforetica (Southern blot) e di RNA (Northern blot);
- localizzazione di trascritti o sequenze cromosomiche in cellule e tessuti mediante ibridazione in situ, con sonde fluorescenti o radioattive;
- progettazione di primer per la reazione a catena della polimerasi (PCR), nella quale l’annealing dei primer ai filamenti stampo guida la sintesi enzimatica della regione bersaglio.
La disponibilità di genomi annotati in banche dati pubbliche facilita la progettazione di sonde e primer altamente specifici. In un esempio pratico, un oligonucleotide di 24 basi con 50 % di GC avrà un \(T_m\) stimato vicino a 72 °C con la regola sopra, suggerendo condizioni di ibridazione e lavaggio appena inferiori per massimizzare il rapporto segnale/rumore. Combinata con il clonaggio e le librerie descritte in precedenza, l’ibridazione permette di isolare, quantificare e caratterizzare in modo mirato geni e trascritti di interesse.