Reazioni di ossido-riduzione
Definizione
Le reazioni di ossido-riduzione, o redox, descrivono trasformazioni in cui avviene un trasferimento netto di elettroni tra specie chimiche. In termini operativi, si distingue fra ossidazione, intesa come perdita di elettroni, eliminazione di atomi di idrogeno o acquisizione di atomi di ossigeno, e riduzione, intesa come acquisto di elettroni, acquisizione di idrogeno o perdita di ossigeno. Queste definizioni, coerenti con l’uso in chimica generale e fisica (IUPAC), permettono di interpretare sia reazioni ioniche sia processi che coinvolgono composti covalenti.
Quando il magnesio elementare, avente numero di ossidazione 0, reagisce con un alogeno come il cloro, esso si converte in ione magnesio Mg2+ aumentando il proprio numero di ossidazione a +2, cioè perdendo due elettroni. Viceversa, il cloro molecolare Cl2, con numero di ossidazione 0, riceve due elettroni e si trasforma in due ioni cloruro Cl− con numero di ossidazione −1. Le due trasformazioni si rappresentano in modo rigoroso mediante semireazioni che esplicitano il trasferimento elettronico.
\[ \text{Semireazione di ossidazione:}\quad \mathrm{Mg} \rightarrow \mathrm{Mg}^{2+} + 2\,e^- \]
\[ \text{Semireazione di riduzione:}\quad \mathrm{Cl}_2 + 2\,e^- \rightarrow 2\,\mathrm{Cl}^- \]
La somma algebrica delle due semireazioni produce l’equazione complessiva, nella quale gli elettroni, presenti come reagenti in una semireazione e come prodotti nell’altra, si elidono completamente:
\[ \text{Reazione complessiva:}\quad \mathrm{Mg} + \mathrm{Cl}_2 \rightarrow \mathrm{Mg}^{2+} + 2\,\mathrm{Cl}^- \]
In questa redox il magnesio agisce da agente riducente, poiché fornisce elettroni che consentono la riduzione del cloro; il cloro è l’agente ossidante, poiché accetta elettroni e provoca l’ossidazione del magnesio. In sintesi:
- agente ossidante: si riduce, acquista elettroni, induce l’ossidazione di un’altra specie;
- agente riducente: si ossida, cede elettroni, induce la riduzione di un’altra specie.
Quando sono coinvolti composti covalenti, il riconoscimento delle redox beneficia dell’uso sistematico dei numeri di ossidazione. Consideriamo la combustione del metano:
CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(g)
Pur non apparendo elettroni espliciti, la trasformazione è redox: il carbonio del metano passa da numero di ossidazione −4 a +4 nel biossido di carbonio, mentre l’ossigeno passa da 0 a −2 in CO2 e H2O. Una traccia operativa utile, specie in chimica organica, è osservare che l’ossidazione equivale a perdita netta di idrogeno e/o acquisto di ossigeno, mentre la riduzione è l’inverso. Nel caso riportato, il carbonio si ossida perché si lega a più ossigeno e a meno idrogeno.
Un secondo esempio riguarda l’ossidazione dei metalli da parte dell’ossigeno atmosferico. L’alluminio elementare (numero di ossidazione 0) forma ossido di alluminio in seguito a una reazione di combinazione:
4 Al(s) + 3 O2(g) → 2 Al2O3(s)
In Al2O3 l’alluminio ha numero di ossidazione +3, indicando un processo di ossidazione. È interessante notare che, a differenza del ferro, lo strato di Al2O3 è aderente e compatto, con effetto passivante: limita la prosecuzione della corrosione sottostante.
Per completezza, si ricorda che l’andamento spontaneo di molte redox può essere previsto dai potenziali standard di riduzione E°, misurati rispetto all’elettrodo standard a idrogeno: reazioni con ΔE° positivo risultano spontanee nelle condizioni standard, sebbene il profilo cinetico dipenda da barriere di attivazione e dalla presenza di catalizzatori.
Processi di ossidazione e riduzione sono alla base di fenomeni industriali, ambientali e biologici. La comprensione del trasferimento elettronico consente di interpretare la degradazione dei materiali, l’azione di detergenti e sbiancanti, le trasformazioni energetiche negli organismi e il funzionamento di celle elettrochimiche.
Corrosione
La corrosione metallica è un processo elettrochimico in cui atomi metallici si trasformano in ioni, alterando profondamente le proprietà meccaniche e chimiche del materiale. Spesso, sulla superficie del metallo si instaurano microcoppie galvaniche per disomogeneità di composizione o di aerazione: aree anodi cedono elettroni, aree catodi li ricevono, e un elettrolita (acqua con sali disciolti) chiude il circuito. Nel caso del ferro, l’ossidazione porta alla formazione di ossidi e idrossidi di ferro, comunemente indicati come ruggine:
4 Fe(s) + 3 O2(g) → 2 Fe2O3(s)
Le perdite economiche associate sono ingenti e includono la riduzione di integrità strutturale, la contaminazione dei processi e costi di manutenzione. Le strategie di mitigazione comprendono rivestimenti protettivi, passivazione, inibitori di corrosione, protezione catodica e progettazione dei materiali. Un esempio di protezione catodica è la zincatura: lo zinco, più riducente del ferro, si ossida preferenzialmente, proteggendo il substrato.
Agenti sbiancanti
Molti agenti sbiancanti operano come ossidanti, intervenendo sui cromofori, cioè sui sistemi elettronici coniugati responsabili del colore in molecole organiche. L’ipoclorito di sodio, NaClO, ampiamente impiegato in prodotti per il lavaggio, ossida tali cromofori riducendo l’estensione della coniugazione e convertendo molecole colorate in specie incolori o più solubili, facilitandone la rimozione. In alternativa, per tessuti delicati o applicazioni alimentari, si utilizzano perossidi (es. H2O2) che, in opportune condizioni di pH e temperatura, esercitano un’azione ossidante meno aggressiva sui substrati.
Nei sistemi viventi, il trasferimento sequenziale di elettroni è gestito da complessi proteici e cofattori redox. Nella respirazione aerobica, la catena di trasporto degli elettroni (mitocondriale) convoglia equivalenti riducenti da NADH e FADH2 all’ossigeno, attraverso centri metallici e chinoni. Il citocromo c, contenente un gruppo eme con ferro, alterna gli stati Fe(III)/Fe(II) in trasferimenti one-electron ben definiti:
citocromo c (Fe3+) + e− → citocromo c (Fe2+)
Lo ione ferro(II) del citocromo c può cedere l’elettrone a un centro Fe(III) della citocromo c ossidasi, realizzando un passaggio di carica tra proteine adiacenti:
citocromo c (Fe2+) + citocromo c ossidasi (Fe3+) → citocromo c (Fe3+) + citocromo c ossidasi (Fe2+).
La citocromo c ossidasi, al termine della catena, riduce l’ossigeno molecolare ad acqua secondo la stechiometria globale:
O2 + 4 e− + 4 H+ → 2 H2O
Il gradiente protonico generato dal flusso di elettroni viene poi convertito in lavoro chimico dall’ATP sintasi. L’ordine dei potenziali redox lungo la catena assicura la direzionalità del trasferimento, con O2/H2O come accettore finale ad alto potenziale di riduzione.
Metabolismo
Le trasformazioni metaboliche dell’etanolo costituiscono una sequenza redox ben caratterizzata nel fegato. L’etanolo viene dapprima ossidato ad acetaldeide dall’alcol deidrogenasi, quindi l’acetaldeide è ossidata ad acido acetico dall’aldeide deidrogenasi; l’acetato confluisce nel metabolismo energetico ed è infine mineralizzato a CO2 e H2O nel ciclo degli acidi tricarbossilici e nella catena respiratoria. La sequenza è riassunta nella figura che segue e procede con cofattori piridinici e flavinici come accettori di equivalenti riducenti.
 |
| Ossidazione dell’etanolo ad acido acetico. |
Queste tappe sono redox benché i reagenti e i prodotti siano elettricamente neutri: l’identificazione si basa sull’osservazione di perdita di idrogeno o guadagno di ossigeno. Nel passaggio da etanolo ad acetaldeide, la molecola perde due atomi di idrogeno equivalenti a due elettroni (con trasferimento di idruro a NAD+), segno di ossidazione del carbonio interessato. Analogamente, l’ossidazione dell’acetaldeide ad acetato comporta l’introduzione di un secondo legame C–O e un ulteriore aumento del numero di ossidazione del carbonio carbonilico.
Per la trattazione quantitativa di redox complesse, l’uso dei numeri di ossidazione e del metodo delle semireazioni consente di bilanciare correttamente massa e carica anche in ambienti non acquosi o in presenza di tamponi. In ambiente acido si impiegano H+ e H2O per bilanciare, mentre in ambiente basico si usano OH− e H2O. In ogni caso, gli elettroni compaiono solo nelle semireazioni e non nella reazione globale, riflettendo il fatto che, nel processo complessivo, non rimangono elettroni liberi.
Se una lamina di zinco metallico viene immersa in una soluzione acquosa contenente ioni rame(II), gli atomi di zinco si ossidano a ioni Zn²⁺, mentre gli ioni Cu²⁺ si riducono a rame metallico che si deposita sulla superficie dello zinco (Figura 05.06-01). Il bilancio redox complessivo è:
\[ \text{Zn}(s) + \text{Cu}^{2+}(aq) \rightarrow \text{Zn}^{2+}(aq) + \text{Cu}(s) \]
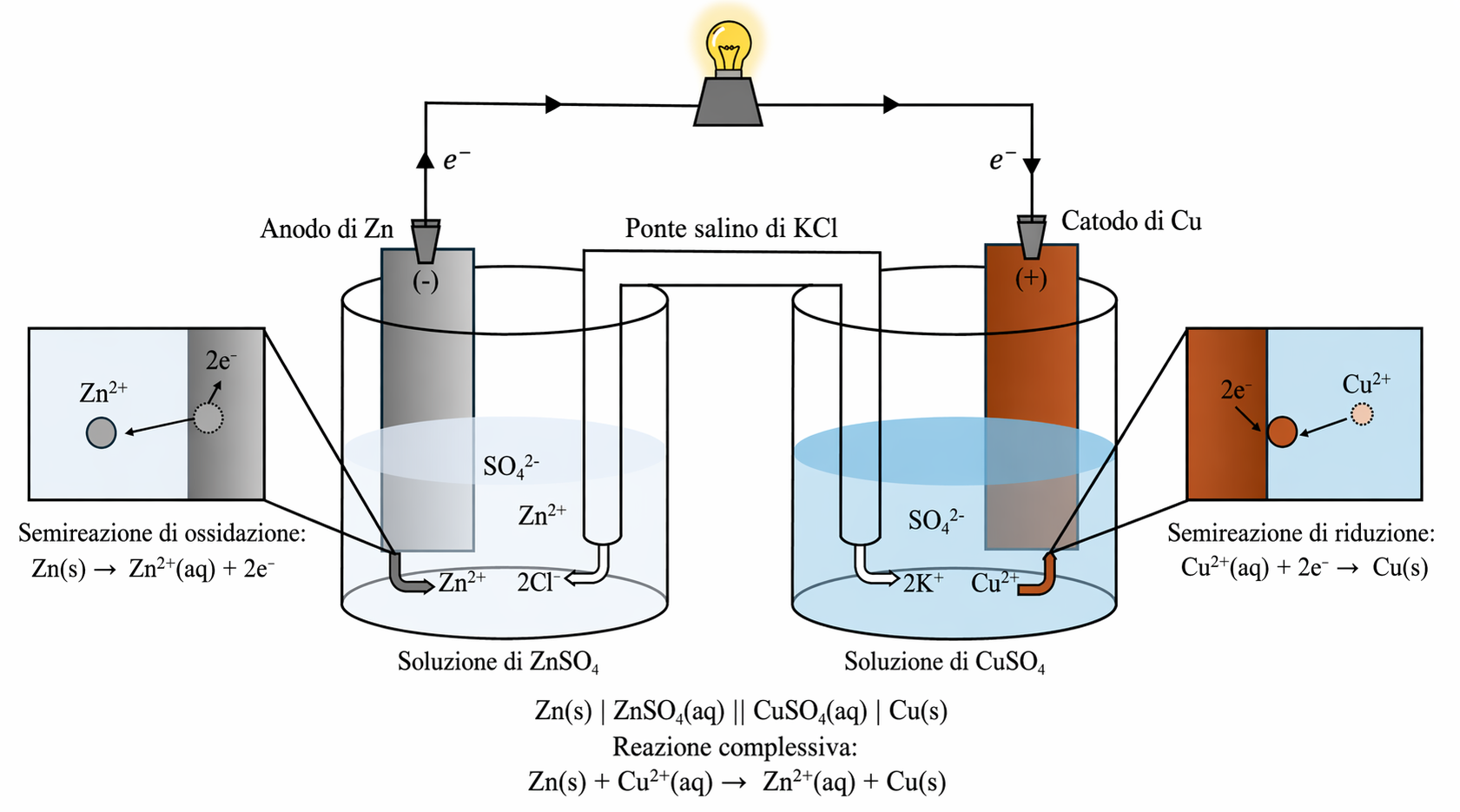
Nell’esperimento condotto in un unico recipiente, gli elettroni passano direttamente dallo zinco agli ioni Cu²⁺ in soluzione, con deposizione di Cu sulla superficie della lamina. Per convertire questa trasformazione chimica spontanea in lavoro elettrico, il trasferimento di elettroni deve avvenire attraverso un circuito esterno. A tale scopo si separano spazialmente i due processi di semireazione in due contenitori distinti e li si collega elettricamente con un conduttore metallico e ionicamente con un ponte salino. Se si collega semplicemente una lamina di zinco in un contenitore e una soluzione di solfato di rame(II) in un secondo contenitore tramite un filo di rame, non si osserva passaggio di corrente: il circuito non è chiuso e, soprattutto, la carica si accumula rapidamente in ciascun comparto, arrestando la reazione. L’inserimento di un ponte salino, un tubo riempito di elettrolita inerte (ad esempio KCl o KNO₃), ristabilisce l’elettroneutralità in ciascuna semicella e consente la circolazione continua di carica. Con questo accorgimento, il circuito è completo e la corrente fluisce nel circuito esterno (Figura 05.06-02).
L’insieme costituito dalle due semicelle, dal circuito esterno e dal ponte salino prende il nome di cella galvanica o voltaica (in onore di Luigi Galvani e Alessandro Volta), spesso indicata semplicemente come pila. Una cella galvanica trasforma l’energia chimica di una reazione redox spontanea in energia elettrica. In una semicella ha luogo l’ossidazione, nell’altra la riduzione; gli elettrodi sono le superfici solide dove si scambiano gli elettroni: l’anodo ospita l’ossidazione, il catodo la riduzione. Nel sistema di Daniell (pila di Daniell), che impiega Zn/Zn²⁺ e Cu²⁺/Cu, le semireazioni sono:
Anodo (ossidazione): \(\ \text{Zn}(s) \rightarrow \text{Zn}^{2+}(aq) + 2\,e^{-}\)
Catodo (riduzione): \(\ \text{Cu}^{2+}(aq) + 2\,e^{-} \rightarrow \text{Cu}(s)\)
La somma delle due semireazioni fornisce la reazione globale della cella di Daniell: \(\ \text{Zn}(s) + \text{Cu}^{2+}(aq) \rightarrow \text{Zn}^{2+}(aq) + \text{Cu}(s)\).
Nel circuito esterno gli elettroni fluiscono dall’anodo al catodo; la corrente convenzionale, per definizione, scorre in senso opposto. All’interno delle soluzioni, gli ioni si muovono per mantenere l’elettroneutralità: gli anioni del ponte salino migrano verso l’anodo, compensando l’aumento di carica positiva dovuto alla formazione di Zn²⁺, mentre i cationi del ponte salino si spostano verso il catodo, dove la riduzione di Cu²⁺ consuma carica positiva.
La differenza di energia potenziale elettrica tra i due elettrodi è misurata come potenziale di cella, forza elettromotrice o fem, indicata con \(E\). L’analogia meccanica è con una caduta d’acqua: il flusso è sostenuto da una differenza di potenziale, che nel caso elettrico si misura con un voltmetro, idealmente a circuito aperto per non perturbare la cella. Il potenziale di cella dipende dalla natura delle coppie redox, dalla temperatura e dalle attività (approssimabili con concentrazioni in soluzioni diluite). In condizioni non standard, la dipendenza dalla composizione è descritta dalla relazione di Nernst: \[ E = E^\circ - \frac{RT}{nF}\,\ln Q, \] dove \(E^\circ\) è il potenziale standard di cella, \(n\) il numero di elettroni scambiati, \(F\) la costante di Faraday, \(R\) la costante dei gas, \(T\) la temperatura assoluta e \(Q\) il quoziente di reazione.
La rappresentazione sintetica di una cella galvanica si ottiene tramite il diagramma di cella. Per la cella di Daniell in condizioni standard (attività unitarie, approssimate a 1 M per le specie in soluzione), si scrive:
\(\ \text{Zn}(s)\ \big|\ \text{Zn}^{2+}(1\,\text{M})\ \big\|\ \text{Cu}^{2+}(1\,\text{M})\ \big|\ \text{Cu}(s)\ \)
Nel diagramma, una linea verticale singola indica un confine di fase, ad esempio tra un metallo solido e i suoi ioni in soluzione; la doppia linea verticale rappresenta il ponte salino. Per convenzione, l’anodo è posto a sinistra e il catodo a destra; le specie sono elencate nell’ordine in cui si incontrano procedendo dall’elettrodo di ossidazione a quello di riduzione (Figura 05.06-02):
- anodo: sede dell’ossidazione, in una cella galvanica ha segno negativo per via della partenza degli elettroni nel circuito esterno;
- catodo: sede della riduzione, in una cella galvanica ha segno positivo;
- flussi di carica: gli elettroni scorrono dall’anodo al catodo nel circuito esterno, mentre gli ioni del ponte salino garantiscono l’elettroneutralità nelle soluzioni;
- ponte salino: contiene un elettrolita inerte ad alta mobilità ionica, non reattivo con le semicelle, e impedisce il mescolamento diretto delle soluzioni pur consentendo il passaggio di carica.
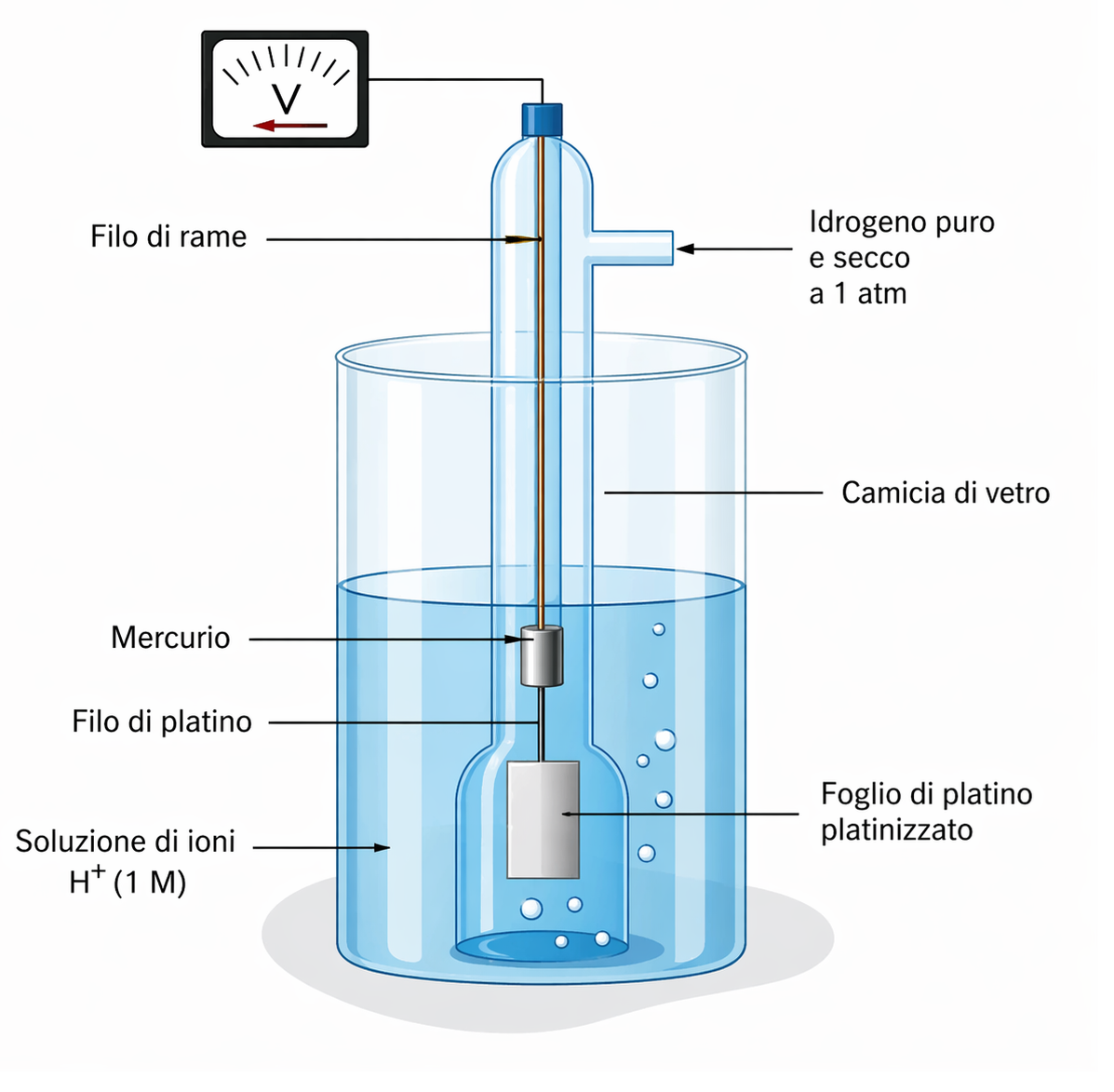
Quando le attività di Cu²⁺ e Zn²⁺ sono unitarie (soluzioni 1 M, gas a 1 atm) e la temperatura è 25 °C, la pila di Daniell presenta una forza elettromotrice pari a 1,10 V. Tale differenza di potenziale scaturisce dalla combinazione di due semireazioni di ossidoriduzione e può essere interpretata come somma algebrica dei potenziali ai due elettrodi. Sebbene il potenziale assoluto di un singolo elettrodo non sia misurabile, è possibile fissare convenzionalmente a zero il potenziale di un elettrodo di riferimento e riferire ad esso tutti gli altri. Il riferimento adottato è l’elettrodo standard a idrogeno (ESI, spesso SHE in letteratura), illustrato in (Figura 05.06-03).
Nell’ESI, idrogeno gassoso a 1 atm viene fatto gorgogliare su un elettrodo di platino immerso in una soluzione acquosa con attività di H⁺ unitaria. Il platino svolge duplice funzione: catalizza l’equilibrio di dissociazione/ricombinazione dell’idrogeno molecolare,
\[ \mathrm{H_2(g)} \rightleftharpoons 2\,\mathrm{H^+(aq)} + 2\,\mathrm{e^-}, \]
e fornisce la superficie conduttrice per lo scambio elettronico con il circuito esterno. Per definizione, in condizioni standard si assegna al potenziale di riduzione della coppia H⁺/H₂ il valore esatto di zero:
\[ 2\,\mathrm{H^+}(1\,\mathrm{M}) + 2\,\mathrm{e^-} \rightleftharpoons \mathrm{H_2}(1\,\mathrm{atm}) \qquad E^\circ = 0{,}00\ \mathrm{V}. \]
Il simbolo “\(^\circ\)” indica condizioni standard. Il potenziale standard di riduzione di qualunque altra semicoppia si determina collegando l’elettrodo d’interesse all’ESI e misurando la f.e.m. della cella. Se si accoppia, ad esempio, un elettrodo di zinco con l’ESI, si osserva che lo zinco metallico si consuma: lo Zn agisce da anodo, ossidandosi secondo
\[ \mathrm{Zn}(s) \rightleftharpoons \mathrm{Zn^{2+}}(aq) + 2\,\mathrm{e^-}. \]
Il diagramma di cella è:
Zn(s) | Zn²⁺(1 M) || H⁺(1 M) | H₂(1 atm) | Pt(s)
Alle condizioni standard la f.e.m. misurata è 0,76 V a 25 °C. Scrivendo le semireazioni:
\[ \text{Anodo (ossidazione):}\quad \mathrm{Zn}(s) \longrightarrow \mathrm{Zn^{2+}}(1\,\mathrm{M}) + 2\,\mathrm{e^-} \]
\[ \text{Catodo (riduzione):}\quad 2\,\mathrm{H^+}(1\,\mathrm{M}) + 2\,\mathrm{e^-} \longrightarrow \mathrm{H_2}(1\,\mathrm{atm}) \]
\[ \text{Totale:}\quad \mathrm{Zn}(s) + 2\,\mathrm{H^+}(1\,\mathrm{M}) \longrightarrow \mathrm{Zn^{2+}}(1\,\mathrm{M}) + \mathrm{H_2}(1\,\mathrm{atm}) \]
e applicando la convenzione IUPAC \( E^\circ_{\mathrm{cell}} = E^\circ_{\mathrm{catodo}} - E^\circ_{\mathrm{anodo}}, \) risulta:
\[ E^\circ_{\mathrm{cell}} = E^\circ_{\mathrm{H^+/H_2}} - E^\circ_{\mathrm{Zn^{2+}/Zn}} \quad\Rightarrow\quad 0{,}76\ \mathrm{V} = 0 - E^\circ_{\mathrm{Zn^{2+}/Zn}}, \]
da cui \( E^\circ_{\mathrm{Zn^{2+}/Zn}} = -0{,}76\ \mathrm{V}. \)
Un’analoga misura con un elettrodo di rame come catodo fornisce:
\[ \mathrm{Cu^{2+}}(aq) + 2\,\mathrm{e^-} \rightleftharpoons \mathrm{Cu}(s), \qquad E^\circ_{\mathrm{Cu^{2+}/Cu}} = +0{,}34\ \mathrm{V}, \]
con cella
Pt(s) | H₂(1 atm) | H⁺(1 M) || Cu²⁺(1 M) | Cu(s)
e f.e.m. standard di 0,34 V. Per la pila di Daniell (Figura 05.06-02), si combinano le due semicoppie:
\[ \text{Catodo (riduzione):}\quad \mathrm{Cu^{2+}}(1\,\mathrm{M}) + 2\,\mathrm{e^-} \longrightarrow \mathrm{Cu}(s) \]
\[ \text{Totale:}\quad \mathrm{Zn}(s) + \mathrm{Cu^{2+}}(1\,\mathrm{M}) \longrightarrow \mathrm{Zn^{2+}}(1\,\mathrm{M}) + \mathrm{Cu}(s) \]
e si ottiene \( E^\circ_{\mathrm{cell}} = 0{,}34\ \mathrm{V} - (-0{,}76\ \mathrm{V}) = 1{,}10\ \mathrm{V}. \) Come per la variazione di energia libera standard, il segno di \( E^\circ_{\mathrm{cell}} \) anticipa la direzione di spontaneità: valori positivi indicano processi che, alle condizioni standard, evolvono verso i prodotti; valori negativi implicano predominio dei reagenti all’equilibrio.
Nel contesto biochimico si adotta il potenziale standard biochimico \( E^{\circ'} \), definito con \( [\mathrm{H^+}] = 10^{-7}\ \mathrm{M} \) (pH 7, 298 K) e condizioni standard per gli altri componenti. La (Tabella 05.06-01) elenca potenziali standard di riduzione riferiti all’ESI con \( E^\circ = 0{,}00\ \mathrm{V}. \) Scorrendo la tabella verso l’alto aumentano i valori di \( E^\circ \) e la tendenza alla riduzione; verso il basso aumentano la tendenza all’ossidazione e la forza riducente delle specie poste a destra delle semicoppie:
- I valori tabulati di \( E^\circ \) si riferiscono alle semireazioni come riduzioni, scritte da sinistra a destra; quanto più \( E^\circ \) è positivo, tanto maggiore è l’attitudine della specie a essere ridotta;
- Le semireazioni sono reversibili: lo stesso elettrodo può comportarsi da anodo o da catodo a seconda del partner. L’ESI è catodo in coppia con Zn, mentre funge da anodo in presenza di Cu;
- Qualsiasi specie a sinistra in una semireazione ossiderà spontaneamente una specie posta a destra in una semireazione che compaia più in basso in (Tabella 05.06-01) (cosiddetta regola della diagonale). Nella pila di Daniell, Zn(s) riduce spontaneamente Cu²⁺(aq) a Cu(s), formando Zn²⁺(aq);
- I potenziali di elettrodo sono grandezze intensive: moltiplicare tutti i coefficienti stechiometrici non modifica \( E^\circ \). Per esempio, \( \mathrm{Ag^+}(1\,\mathrm{M}) + \mathrm{e^-} \rightleftharpoons \mathrm{Ag}(s) \) ha \( E^\circ = +0{,}80\ \mathrm{V} \) e lo stesso valore rimane se si scrive \( 2\,\mathrm{Ag^+} + 2\,\mathrm{e^-} \rightleftharpoons 2\,\mathrm{Ag}(s) \);
- Invertendo una semireazione si cambia il segno di \( E^\circ \), mentre il suo valore assoluto resta invariato.
È utile ricordare che i potenziali di elettrodo sono, in senso rigoroso, funzioni delle attività termodinamiche. In soluzioni diluite si approssimano spesso con le concentrazioni molari, ma a forza ionica elevata occorre considerare i coefficienti di attività per stime accurate.
Valori standard di riduzione a 25 °C
| Semireazione | E° (V) |
|---|---|
| F₂(g) + 2e⁻ → 2F⁻(aq) | +2.87 |
| O₃(g) + 2H⁺(aq) + 2e⁻ → O₂(g) + H₂O | +2.07 |
| Co³⁺(aq) + e⁻ → Co²⁺(aq) | +1.82 |
| H₂O₂(aq) + 2H⁺(aq) + 2e⁻ → 2H₂O | +1.77 |
| PbO₂(s) + 4H⁺(aq) + SO₄²⁻(aq) + 2e⁻ → PbSO₄(s) + 2H₂O | +1.70 |
| Ce⁴⁺(aq) + e⁻ → Ce³⁺(aq) | +1.61 |
| MnO₂(s) + 4H⁺(aq) + 2e⁻ → Mn²⁺(aq) + 2H₂O | +1.51 |
| Au³⁺(aq) + 3e⁻ → Au(s) | +1.50 |
| Cl₂(g) + 2e⁻ → 2Cl⁻(aq) | +1.36 |
| Cr₂O₇²⁻(aq) + 14H⁺(aq) + 6e⁻ → 2Cr³⁺(aq) + 7H₂O | +1.33 |
| MnO₄⁻(aq) + 4H⁺(aq) + 3e⁻ → MnO₂(s) + 2H₂O | +1.23 |
| O₂(g) + 4H⁺(aq) + 4e⁻ → 2H₂O | +1.23 |
| Br₂(l) + 2e⁻ → 2Br⁻(aq) | +1.07 |
| NO₃⁻(aq) + 4H⁺(aq) + 3e⁻ → NO(g) + 2H₂O | +0.96 |
| Hg²⁺(aq) + 2e⁻ → Hg(l) | +0.92 |
| Ag⁺(aq) + e⁻ → Ag(s) | +0.80 |
| Fe³⁺(aq) + e⁻ → Fe²⁺(aq) | +0.77 |
| O₂(g) + 2H₂O(l) + 2e⁻ → H₂O₂(aq) | +0.68 |
| MnO₄⁻(aq) + 2H₂O + 3e⁻ → MnO₂(s) + 4OH⁻(aq) | +0.59 |
| I₂(s) + 2e⁻ → 2I⁻(aq) | +0.54 |
| Ni³⁺(aq) + e⁻ → Ni²⁺(aq) | +0.50 |
| Cu²⁺(aq) + 2e⁻ → Cu(s) | +0.34 |
| AgCl(s) + e⁻ → Ag(s) + Cl⁻(aq) | +0.22 |
| SO₄²⁻(aq) + 4H⁺(aq) + 2e⁻ → SO₂(g) + 2H₂O | +0.20 |
| Cu⁺(aq) + e⁻ → Cu(s) | +0.15 |
| Sn⁴⁺(aq) + 2e⁻ → Sn²⁺(aq) | +0.15 |
| 2H⁺(aq) + 2e⁻ → H₂(g) | 0.00 |
| Pb²⁺(aq) + 2e⁻ → Pb(s) | –0.13 |
| Sn²⁺(aq) + 2e⁻ → Sn(s) | –0.14 |
| Ni²⁺(aq) + 2e⁻ → Ni(s) | –0.25 |
| Co²⁺(aq) + 2e⁻ → Co(s) | –0.28 |
| Cd²⁺(aq) + 2e⁻ → Cd(s) | –0.40 |
| Fe²⁺(aq) + 2e⁻ → Fe(s) | –0.44 |
| Cr³⁺(aq) + 3e⁻ → Cr(s) | –0.74 |
| Zn²⁺(aq) + 2e⁻ → Zn(s) | –0.76 |
| 2H₂O + 2e⁻ → H₂(g) + 2OH⁻(aq) | –0.83 |
| Mn²⁺(aq) + 2e⁻ → Mn(s) | –1.18 |
| Al³⁺(aq) + 3e⁻ → Al(s) | –1.66 |
| Be²⁺(aq) + 2e⁻ → Be(s) | –1.85 |
| Mg²⁺(aq) + 2e⁻ → Mg(s) | –2.37 |
| Ti²⁺(aq) + 2e⁻ → Ti(s) | –2.71 |
| Ca²⁺(aq) + 2e⁻ → Ca(s) | –2.87 |
| Ba²⁺(aq) + 2e⁻ → Ba(s) | –2.90 |
| K⁺(aq) + e⁻ → K(s) | –2.93 |
| Li⁺(aq) + e⁻ → Li(s) | –3.05 |
| Tabella che riporta i potenziali standard di riduzione misurati a 25 °C. | |
Valori standard di riduzione a 25 °C
| Semireazione | E° (V) |
|---|---|
| F₂(g) + 2e⁻ → 2F⁻(aq) | +2.87 |
| O₃(g) + 2H⁺(aq) + 2e⁻ → O₂(g) + H₂O | +2.07 |
| Co³⁺(aq) + e⁻ → Co²⁺(aq) | +1.82 |
| H₂O₂(aq) + 2H⁺(aq) + 2e⁻ → 2H₂O | +1.77 |
| PbO₂(s) + 4H⁺(aq) + SO₄²⁻(aq) + 2e⁻ → PbSO₄(s) + 2H₂O | +1.70 |
| Ce⁴⁺(aq) + e⁻ → Ce³⁺(aq) | +1.61 |
| MnO₂(s) + 4H⁺(aq) + 2e⁻ → Mn²⁺(aq) + 2H₂O | +1.51 |
| Au³⁺(aq) + 3e⁻ → Au(s) | +1.50 |
| Cl₂(g) + 2e⁻ → 2Cl⁻(aq) | +1.36 |
| Cr₂O₇²⁻(aq) + 14H⁺(aq) + 6e⁻ → 2Cr³⁺(aq) + 7H₂O | +1.33 |
| MnO₄⁻(aq) + 4H⁺(aq) + 3e⁻ → MnO₂(s) + 2H₂O | +1.23 |
| O₂(g) + 4H⁺(aq) + 4e⁻ → 2H₂O | +1.23 |
| Br₂(l) + 2e⁻ → 2Br⁻(aq) | +1.07 |
| NO₃⁻(aq) + 4H⁺(aq) + 3e⁻ → NO(g) + 2H₂O | +0.96 |
| Hg²⁺(aq) + 2e⁻ → Hg(l) | +0.92 |
| Ag⁺(aq) + e⁻ → Ag(s) | +0.80 |
| Fe³⁺(aq) + e⁻ → Fe²⁺(aq) | +0.77 |
| O₂(g) + 2H₂O(l) + 2e⁻ → H₂O₂(aq) | +0.68 |
| MnO₄⁻(aq) + 2H₂O + 3e⁻ → MnO₂(s) + 4OH⁻(aq) | +0.59 |
| I₂(s) + 2e⁻ → 2I⁻(aq) | +0.54 |
| Ni³⁺(aq) + e⁻ → Ni²⁺(aq) | +0.50 |
| Cu²⁺(aq) + 2e⁻ → Cu(s) | +0.34 |
| AgCl(s) + e⁻ → Ag(s) + Cl⁻(aq) | +0.22 |
| SO₄²⁻(aq) + 4H⁺(aq) + 2e⁻ → SO₂(g) + 2H₂O | +0.20 |
| Cu⁺(aq) + e⁻ → Cu(s) | +0.15 |
| Sn⁴⁺(aq) + 2e⁻ → Sn²⁺(aq) | +0.15 |
| 2H⁺(aq) + 2e⁻ → H₂(g) | 0.00 |
| Pb²⁺(aq) + 2e⁻ → Pb(s) | –0.13 |
| Sn²⁺(aq) + 2e⁻ → Sn(s) | –0.14 |
| Ni²⁺(aq) + 2e⁻ → Ni(s) | –0.25 |
| Co²⁺(aq) + 2e⁻ → Co(s) | –0.28 |
| Cd²⁺(aq) + 2e⁻ → Cd(s) | –0.40 |
| Fe²⁺(aq) + 2e⁻ → Fe(s) | –0.44 |
| Cr³⁺(aq) + 3e⁻ → Cr(s) | –0.74 |
| Zn²⁺(aq) + 2e⁻ → Zn(s) | –0.76 |
| 2H₂O + 2e⁻ → H₂(g) + 2OH⁻(aq) | –0.83 |
| Mn²⁺(aq) + 2e⁻ → Mn(s) | –1.18 |
| Al³⁺(aq) + 3e⁻ → Al(s) | –1.66 |
| Be²⁺(aq) + 2e⁻ → Be(s) | –1.85 |
| Mg²⁺(aq) + 2e⁻ → Mg(s) | –2.37 |
| Ti²⁺(aq) + 2e⁻ → Ti(s) | –2.71 |
| Ca²⁺(aq) + 2e⁻ → Ca(s) | –2.87 |
| Ba²⁺(aq) + 2e⁻ → Ba(s) | –2.90 |
| K⁺(aq) + e⁻ → K(s) | –2.93 |
| Li⁺(aq) + e⁻ → Li(s) | –3.05 |
| Tabella che riporta i potenziali standard di riduzione misurati a 25 °C. | |
Il legame tra potenziale di cella ed energia libera è dato da:
\[ \Delta G = -\,n\,F\,E_{\mathrm{cell}}, \]
dove \( n \) è il numero di moli di elettroni trasferiti e \( F \) è la costante di Faraday, pari alla carica di una mole di elettroni: \[ 1\,F = (6{,}022\times 10^{23}\ \mathrm{e^-\,mol^{-1}})\,(1{,}602\times 10^{-19}\ \mathrm{C\,e^{-1}}) \approx 9{,}6485\times 10^{4}\ \mathrm{C\,mol^{-1}} \approx 96\,500\ \mathrm{C\,mol^{-1}}. \] Poiché \( n > 0 \) e \( F > 0 \), un processo spontaneo ha \( \Delta G < 0 \) e dunque \( E_{\mathrm{cell}} > 0 \). Alle condizioni standard vale: \[ \Delta G^\circ = -\,n\,F\,E^\circ_{\mathrm{cell}}. \]
Combinando questa relazione con l’espressione termodinamica \( \Delta G^\circ = -RT\ln K \) si ottiene:
\[ -\,n\,F\,E^\circ_{\mathrm{cell}} = -RT\ln K \quad\Rightarrow\quad E^\circ_{\mathrm{cell}} = \frac{RT}{nF}\,\ln K. \]
A 298 K, utilizzando il logaritmo in base 10,
\[ E^\circ_{\mathrm{cell}} = \frac{0{,}0592}{n}\,\log K. \]
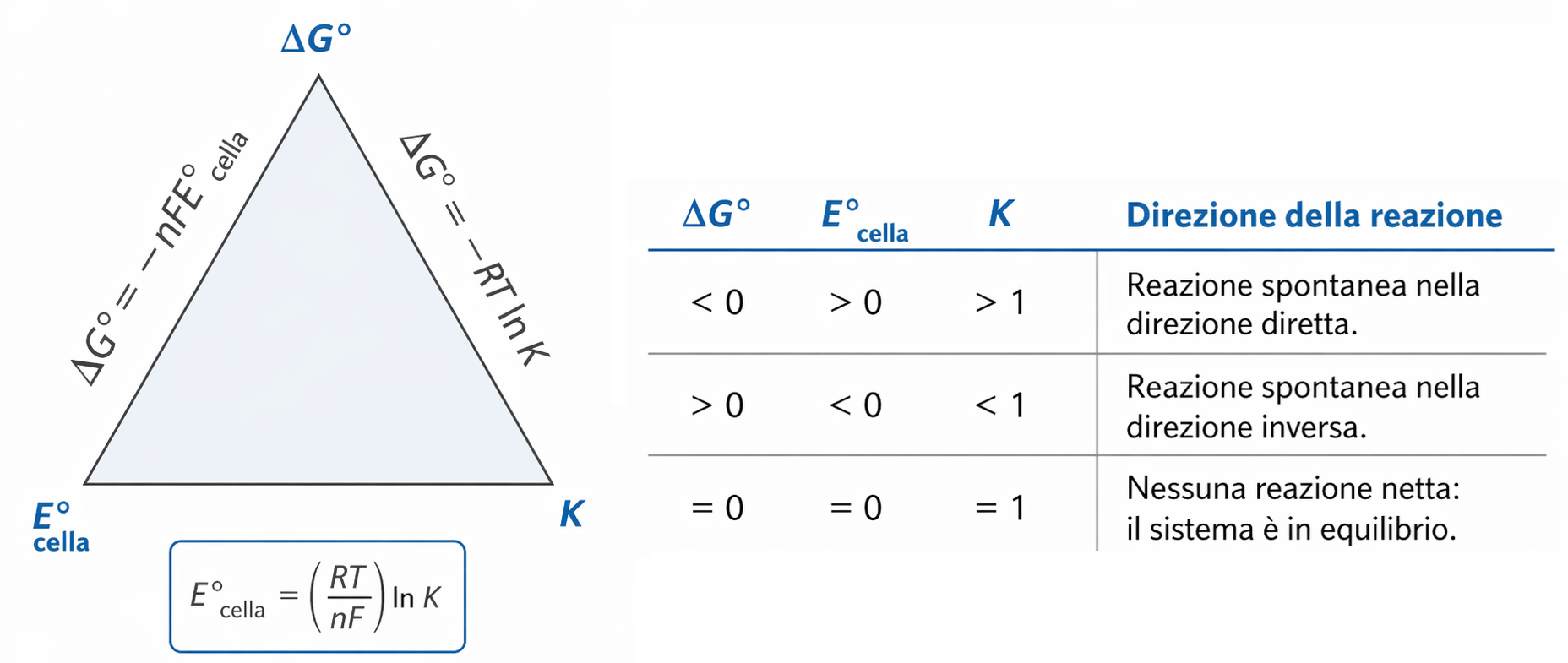
Conoscendo una qualunque tra \( \Delta G^\circ \), \( E^\circ_{\mathrm{cell}} \) e \( K \), le altre due si determinano con le formule riassunte in (Figura 05.06-04) e (Tabella 05.06-02).
Connessione tra energia libera, equilibrio ed elettrochimica
| ΔG° | K | E°cell | Reazione in condizioni standard |
|---|---|---|---|
| Negativo | > 1 | Positivo | Reazione spontanea, favorisce la formazione dei prodotti |
| 0 | = 1 | 0 | Reagenti e prodotti sono ugualmente favoriti (equilibrio dinamico) |
| Positivo | < 1 | Negativo | Reazione non spontanea, favorisce la formazione dei reagenti |
| Molto negativo | ≫ 1 | Fortemente positivo | Reazione praticamente completa → avviene quasi totalmente verso i prodotti |
| Molto positivo | ≪ 1 | Fortemente negativo | Reazione bloccata, procede solo se accoppiata a processi energetici (es. idrolisi ATP) |
| Tabella che mostra il rapporto tra ΔG⁰, la costante di equilibrio K e il potenziale standard della cella E°. | |||
L’equazione di Nernst consente di calcolare il potenziale \( E \) di un elettrodo o di una cella in condizioni non standard, tenendo conto delle attività delle specie ossidata e ridotta. Per una generica semicoppia: \[ \mathrm{Ox} + n\,\mathrm{e^-} \rightleftharpoons \mathrm{Red}, \] si ha:
\[ E = E^\circ - \frac{RT}{nF}\,\ln\!\left(\frac{a_{\mathrm{Red}}}{a_{\mathrm{Ox}}}\right) = E^\circ - \frac{RT}{nF}\,\ln\!\left(\frac{\text{[Red]}}{\text{[Ox]}}\right)\quad\text{(soluzioni diluite)}. \]
Espressa con logaritmo decimale a 298 K: \[ E = E^\circ - \frac{0{,}0592}{n}\,\log\!\left(\frac{\text{[Red]}}{\text{[Ox]}}\right). \]
Per la pila di Daniell, \( \mathrm{Zn}(s) + \mathrm{Cu^{2+}}(aq) \to \mathrm{Zn^{2+}}(aq) + \mathrm{Cu}(s) \), il quoziente di reazione è \( Q = \dfrac{[\mathrm{Zn^{2+}}]}{[\mathrm{Cu^{2+}}]} \) (perché i solidi hanno attività unitaria) e dunque:
\[ E_{\mathrm{cell}} = E^\circ_{\mathrm{cell}} - \frac{RT}{nF}\,\ln Q = E^\circ_{\mathrm{cell}} - \frac{0{,}0592}{2}\,\log\!\left(\frac{[\mathrm{Zn^{2+}}]}{[\mathrm{Cu^{2+}}]}\right). \]
Esempio numerico didatticamente equivalente: se \( [\mathrm{Zn^{2+}}]=0{,}010\ \mathrm{M} \) e \( [\mathrm{Cu^{2+}}]=1{,}0\ \mathrm{M} \), allora \( Q=0{,}010 \) ed \( E_{\mathrm{cell}} = 1{,}10\ \mathrm{V} - \tfrac{0{,}0592}{2}\,\log(0{,}010) \approx 1{,}10\ \mathrm{V} - 0{,}0296\,(-2) \approx 1{,}16\ \mathrm{V}. \)
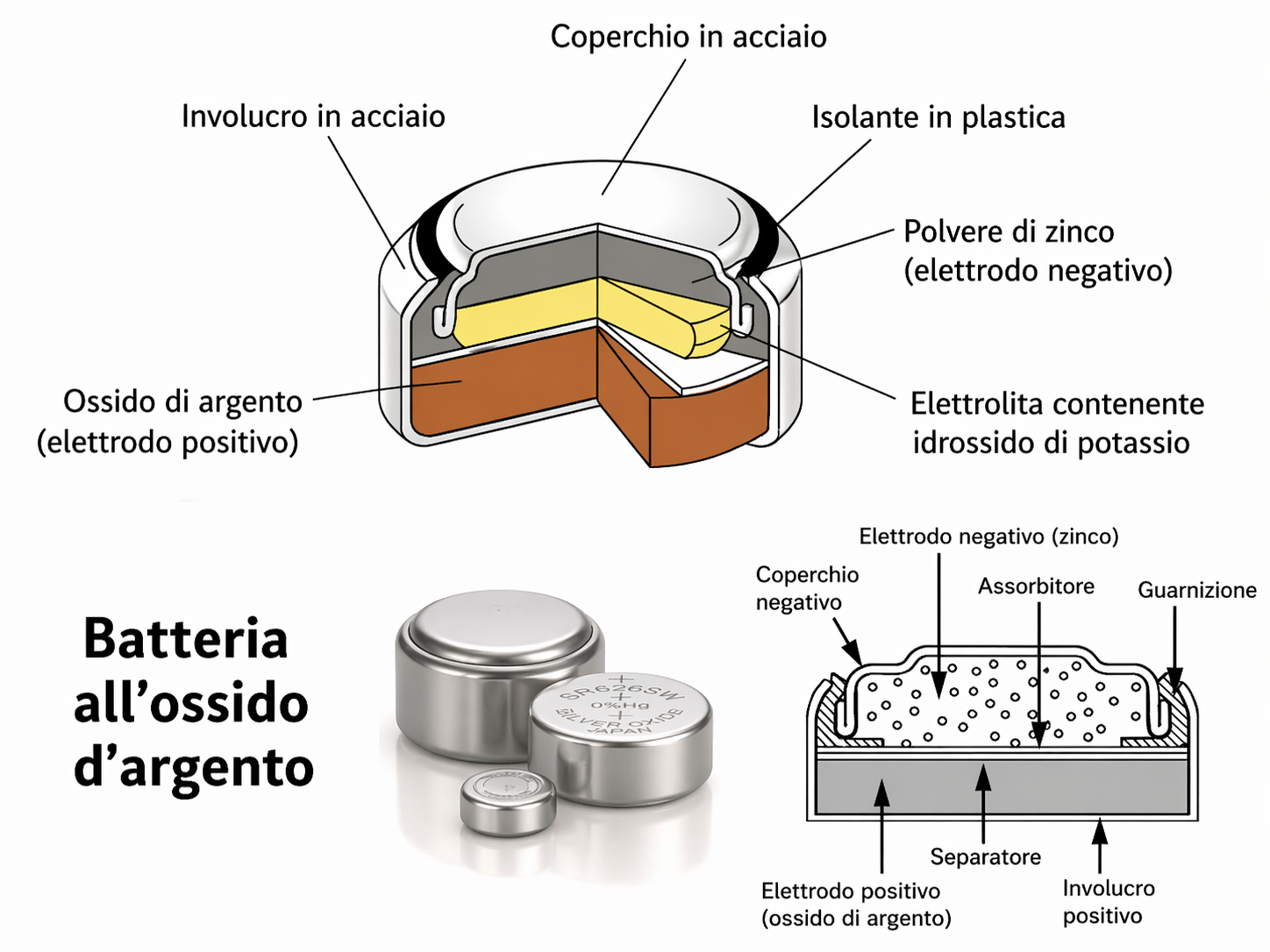
La stessa struttura di legge governa fenomeni biofisici: il potenziale transmembrana associato a un gradiente di ioni monovalenti segue una forma di Nernst, così come il mantenimento dei gradienti Na⁺/K⁺ attraverso la membrana plasmatica. Le celle galvaniche, disponibili come batterie di uso quotidiano, trasformano energia chimica in energia elettrica in modo sicuro ed efficiente. L’evoluzione tecnologica ha miniaturizzato e reso affidabili molti sistemi; la pila all’argento (Figura 05.06-05), per esempio, è sufficientemente stabile da essere integrata in dispositivi medici impiantabili come i pacemaker.
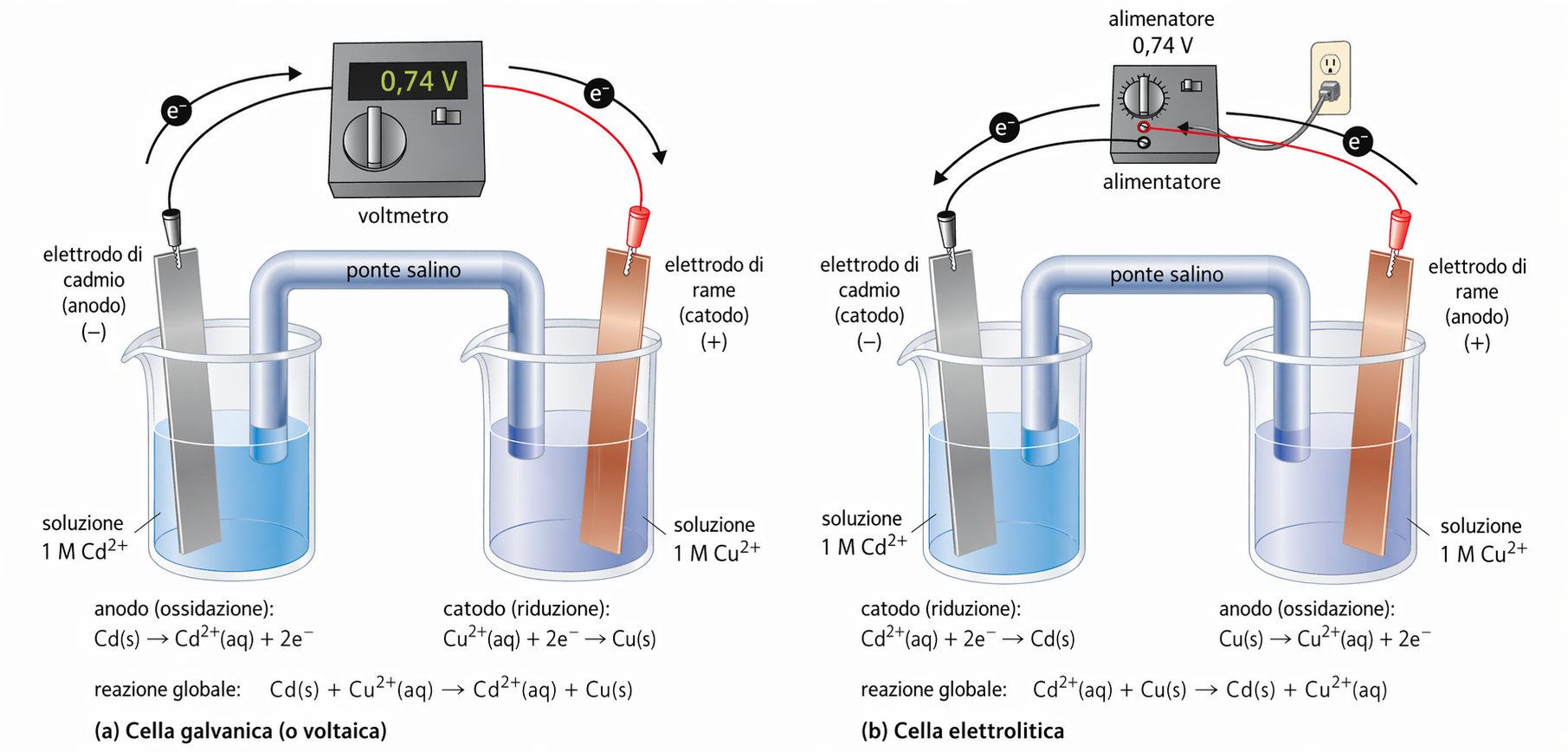
Per elettrolisi si intende l’impiego di energia elettrica esterna per forzare una reazione redox termodinamicamente non spontanea. Le batterie ricaricabili alternano due modalità: durante l’erogazione di corrente si comportano da celle galvaniche, mentre durante la ricarica il caricabatterie impone una differenza di potenziale opposta che inverte il flusso elettronico e rigenera i reagenti, attuando un processo elettrolitico. La (Figura 05.06-06) illustra il nesso tra funzionamento galvanico ed elettrolitico in una pila ricaricabile stagno/rame.
Oltre alla ricarica degli accumulatori, l’elettrolisi trova impieghi di rilievo in: deposizione elettrolitica di metalli (elettroplaccatura), raffinazione elettrolitica, produzione di sostanze di base (per esempio cloro-idrossido di sodio) e scissione dell’acqua. La direzione delle reazioni ai due elettrodi è determinata dal potenziale applicato: l’elettrodo collegato al polo positivo del generatore funge da anodo (ossidazione indotta), quello al polo negativo da catodo (riduzione indotta). Il criterio energetico rimane coerente con \( \Delta G = -n F E_{\mathrm{cell}} \): per innescare una trasformazione non spontanea occorre fornire dall’esterno una f.e.m. almeno pari, in modulo, alla f.e.m. opposta alla reazione desiderata, al netto delle cadute ohmiche e delle sovratensioni cinetiche.