Reazioni di aldeidi e chetoni
Definizione
La selettività è un aspetto cruciale: l’arresto della reazione allo stadio di aldeide richiede condizioni anidre e ossidanti “morbidi”. Tra i protocolli più usati per trasformare alcoli primari in aldeidi senza sovraossidazione si annoverano, a titolo di esempio: ossidazione con reagenti a base di Cr(VI) in ambiente anidro (come il reattivo di Collins), Swern e ossidazione con periodinani (Dess–Martin); per gli alcoli secondari, le stesse condizioni forniscono in modo netto i chetoni. In forma schematica:
\[ \begin{aligned} \text{RCH}_2\text{OH}\ &\xrightarrow{[O]}\ \text{RCHO}\ \xrightarrow{[O]}\ \text{RCOOH},\\ \text{R}_2\text{CHOH}\ &\xrightarrow{[O]}\ \text{R}_2\text{C{=}O}. \end{aligned} \]
In ambito di sintesi, sono frequenti anche percorsi alternativi, utili quando l’ossidazione dell’alcol non è praticabile o quando si desidera introdurre il gruppo carbonilico in una posizione specifica:
• ozonolisi selettiva di alcheni, con appropriato work-up, per ottenere aldeidi o chetoni in funzione della sostituzione dell’alchene;
• idratazione di alchini terminali o interni seguita da tautomeria, utile per accedere rispettivamente a chetoni metilici o a chetoni interni;
• acilazione di Friedel–Crafts su anelli aromatici per generare chetoni aril-alchilici con elevata regioselettività.
Le aldeidi sono suscettibili a ulteriore ossidazione fino agli acidi carbossilici; i chetoni, al contrario, in condizioni blande non progrediscono verso specie più ossidate. La differenza risiede nella presenza, nelle aldeidi, del legame C–H in alfa al carbonile che facilita il trasferimento di idrogeno durante il processo redox, legame assente nei chetoni. In termini generali:
\[ \text{RCHO} + [O] \longrightarrow \text{RCOOH}. \]
Questa elevata reattività rende talora difficoltosa l’isolazione delle aldeidi, poiché l’ossidazione tende a proseguire fino all’acido. Inoltre, l’ossigeno atmosferico può ossidare lentamente molte aldeidi già a temperatura ambiente, con conseguente ridotta stabilità allo stoccaggio. L’equazione complessiva di ossidazione di un’aldeide ad acido carbossilico esprime il trasferimento di due elettroni dal carbonile all’ossidante, spesso con partecipazione della base:
\[ \text{RCHO} + \text{H}_2\text{O} \xrightarrow{\text{ossidante}} \text{RCOO}^- + 2\text{H}^+ + 2e^-. \]
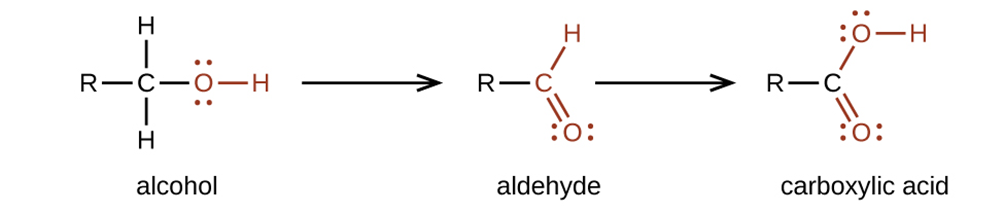 |
| Da alcool ad aldeide ad acido carbossilico. |
Tra gli agenti ossidanti di uso comune si annoverano il permanganato di potassio in ambiente basico e gli ossidanti a base di cromo esavalente. Esempi tipici includono:
• KMnO4 in soluzione alcalina (pH basico), capace di convertire rapidamente molte aldeidi negli anioni carbossilato corrispondenti;
• H2CrO4 o CrO3 in condizioni acquose o anidre, con elevato potere ossidante e rischio di sovraossidazione se non controllati;
• Ag2O in ambiente ammoniacale (reattivo di Tollens), selettivo per le aldeidi rispetto ai chetoni.
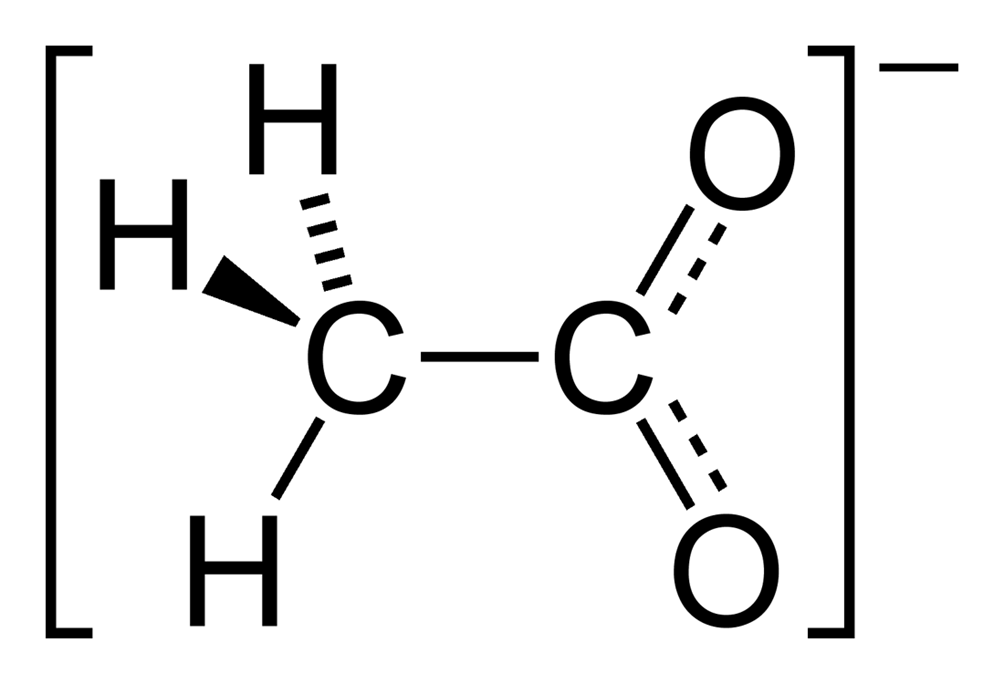 |
| L'etanale può reagire con il permanganato di potassio, H2O e OH- a formare Ione etanoato |
Un’illustrazione classica dell’ossidazione aromatica è la trasformazione della benzaldeide in acido benzoico, che procede agevolmente in presenza di ossidanti idonei e costituisce un passaggio cardine nella chimica dei derivati benzenici.
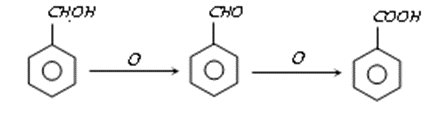 |
| Formazione di Acido benzoico da Benzaldeide. |
La discriminazione tra aldeidi e chetoni sfrutta proprio la diversa attitudine all’ossidazione. Il saggio di Tollens, o “specchio d’argento”, utilizza una soluzione basica di ioni complessati diargento, \(\text{[Ag(NH}_3\text{)}_2]^+\). In presenza di un’aldeide, il carbonile viene ossidato ad anione carbossilato e lo ione argento si riduce ad argento metallico che si deposita sulla superficie del recipiente, generando il caratteristico film lucente (Figura 07.03-01). I chetoni ordinari, non potendo essere ossidati ad acidi carbossilici in tali condizioni, non reagiscono.
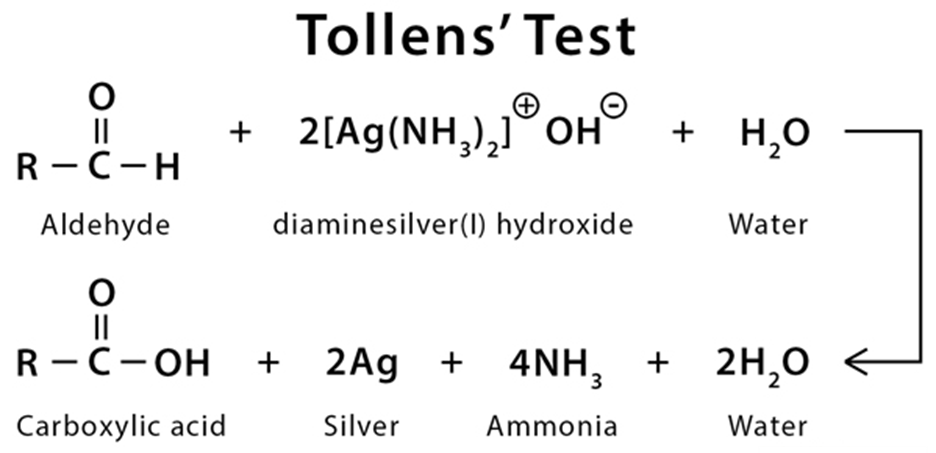 |
| Il saggio di Tollens (chiamato anche "specchio d'argento") è un saggio chimico per l'individuazione delle aldeidi in una soluzione basato sull'utilizzo del reattivo di Tollens. Tale reattivo è, di solito, idrossiammoniato d'argento (ovvero ione diamminoargento). |
Una stechiometria rappresentativa del saggio di Tollens è la seguente:
\[ \text{RCHO} + 2\,\text{[Ag(NH}_3\text{)}_2]^+ + 3\,\text{OH}^- \longrightarrow \text{RCOO}^- + 2\,\text{Ag(s)} + 4\,\text{NH}_3 + 2\,\text{H}_2\text{O}. \]
Un secondo saggio largamente impiegato è il reattivo di Benedict, soluzione tampone contenente Cu(II) complessato da citrato in ambiente alcalino. Le aldeidi riducono Cu(II) a Cu(I) con formazione di ossido rameoso, Cu2O, solido rosso-arancio, mentre i chetoni non reagiscono in condizioni standard. L’andamento cromatico (da blu intenso a rosso) fornisce un’indicazione qualitativa, talvolta semi-quantitativa, del potere riducente del campione. Una forma sintetica dell’equazione globale è:
\[ \text{RCHO} + 2\,\text{Cu}^{2+} + 5\,\text{OH}^- \longrightarrow \text{RCOO}^- + \text{Cu}_2\text{O(s)} + 3\,\text{H}_2\text{O}. \]
I monosaccaridi sono poliidrossialdeidi o poliidrossichetoni. Il glucosio, un aldoso, è il principale carboidrato circolante nel sangue e costituisce un substrato energetico primario. In condizioni patologiche, come nelle forme di diabete con glicosuria, il glucosio può essere presente nelle urine; storicamente il reattivo di Benedict è stato utilizzato per evidenziarlo, poiché la quantità di Cu2O precipitatasi cresce con la concentrazione del riducente nel campione (Figura 07.03-02). La reazione di ossidazione del gruppo aldeidico del D-glucosio a acido D-gluconico da parte di Cu(II) o Ag(I) è esemplificata nelle figure seguenti.
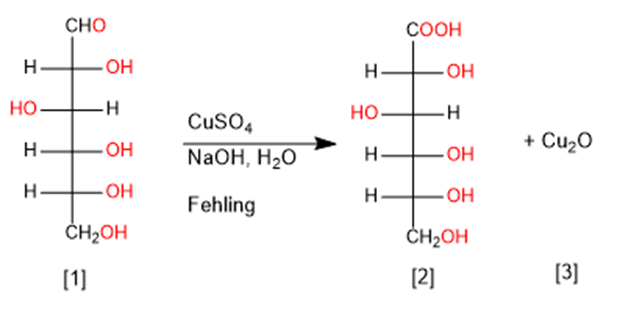 |
| Cu(II) e Ag(I) sono in grado di ossidare selettivamente il gruppo carbonilico degli aldosi ad acido carbossilico, generando precipitati di Cu 2 O e Ag elementare. [1] D-Glucosio. [2] Acido D-Gluconico. [3] Precipitato di ossido rameoso. |
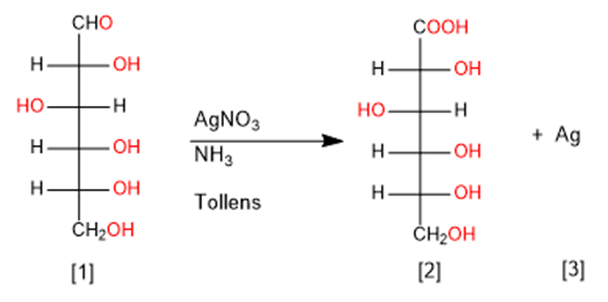 |
| Cu(II) e Ag(I) sono in grado di ossidare selettivamente il gruppo carbonilico degli aldosi ad acido carbossilico, generando precipitati di Cu 2 O e Ag elementare. [1] D-Glucosio. [2] Acido D-Gluconico. [3] Precipitato Elementale d'Argento (Specchio d'Argento) |
In sintesi, la preparazione e l’identificazione di aldeidi e chetoni ruotano intorno alla loro diversa reattività redox: controllo delle condizioni di ossidazione per la sintesi selettiva e impiego di saggi specifici, come Tollens e Benedict, per la distinzione analitica in laboratorio.
Aldeidi e chetoni sono suscettibili a riduzione del gruppo carbonilico, con formazione dei corrispondenti alcoli. Nelle equazioni di reazione è consuetudine indicare la presenza di un agente riducente con il simbolo [H] posto sopra la freccia. Tra le strategie più impiegate figura l’idrogenazione catalitica: il carbonile reagisce con idrogeno molecolare ad alta pressione, in presenza di catalizzatori metallici come nichel, platino o palladio, spesso con lieve riscaldamento. Il legame doppio C=O viene convertito in un legame singolo C–O, con protonazione dell’ossigeno e formazione del gruppo alcolico, in analogia concettuale alla riduzione di un alchene, pur con un diverso profilo elettronico e meccanicistico.
La reattività segue in genere l’ordine aldeidi > chetoni, riflettendo sia minore ingombro sterico sia maggiore elettrofilia del carbonio carbonilico nelle aldeidi. La selettività pratica dipende dalla natura del substrato, dal metallo catalitico, dalla pressione di H2 e dal solvente.
 |
| La riduzione di un’aldeide fornisce in via generale un alcol primario; |
 |
| La riduzione di un chetone conduce tipicamente a un alcol secondario; |
Per idrogenazione catalitica, un chetone si converte in un alcol secondario. Un esempio rappresentativo è la trasformazione della cicloesanone in cicloesanolo in presenza di nichel:
\[ \mathrm{C_6H_{10}O} + \mathrm{H_2} \xrightarrow{\mathrm{Ni}} \mathrm{C_6H_{11}OH} \]
Analogamente, l’idrogenazione di un’aldeide genera un alcol primario. Ad esempio, il propanale è ridotto a 1-propanolo in presenza di platino o palladio:
\[ \mathrm{CH_3CH_2CHO} + \mathrm{H_2} \xrightarrow{\mathrm{Pt}} \mathrm{CH_3CH_2CH_2OH} \]
Oltre all’idrogeno molecolare, sono ampiamente utilizzati riducenti idridici inorganici, che operano tramite trasferimento di \(\ce{H^-}\) al carbonio carbonilico seguito da protonazione in fase di work-up:
• Sodio boroidruro (\(\ce{NaBH4}\)): selettivo e gestibile in solventi protici come etanolo o metanolo; riduce efficacemente aldeidi e chetoni, con moderata reattività verso altri gruppi funzionali;
• Litio alluminio idruro (\(\ce{LiAlH4}\)): più potente, richiede solventi aprotici anidri (es. etere etilico, THF) e attento quench; riduce un ventaglio più ampio di funzioni, ma con minore chemoselettività;
• Varianti catalitiche e organometalliche (es. idrogenazioni asimmetriche con catalizzatori chirali) permettono il controllo enantioselettivo nella formazione di centri stereogenici;
• Il passaggio chiave in comune è l’addizione nucleofila all’orbitale \(\pi^*\) del C=O, con sviluppo di carica negativa su ossigeno e successiva protonazione.
Schema generale per la riduzione idridica di un chetone (work-up acido):
\[ \mathrm{R_2C{=}O} + \ce{H^-} \longrightarrow \mathrm{R_2C{-}O^-} \quad\overset{\ce{H_3O^+}}{\longrightarrow}\quad \mathrm{R_2CH{-}OH} \]
Stereoaspetti: l’attacco all’aldeide o al chetone, il cui carbonio è planare \(\mathrm{sp^2}\), può avvenire dalle due facce prochirali (Re/Si). In assenza di induttori chirali o effetti sterici marcati, la riduzione di un chetone prochirale fornisce spesso una miscela racemica di alcoli secondari. L’impiego di catalizzatori o reagenti chirali consente invece di privilegiare un enantiomero.
Confronto pratico tra metodiche comuni di riduzione del carbonile:
• Idrogenazione catalitica (H2/Ni, Pd, Pt): condizioni da lievi a pressurizzate; può ridurre anche doppi legami C=C, aspetto da considerare nella chemoselettività;
• \(\ce{NaBH4}\): elevata selettività per C=O in presenza di altri gruppi sensibili; indicato per miscele complesse e per substrati contenenti alogenuri o doppi legami coniugati meno reattivi;
• \(\ce{LiAlH4}\): utile quando il substrato è poco reattivo o quando sono presenti funzioni addizionali da ridurre; richiede rigoroso controllo operativo;
• Work-up: in genere si isola l’alcol dopo protonazione acquosa; il bilancio stechiometrico include l’ossidazione del riducente o l’attivazione di H2 sulla superficie metallica.
Un caso biologico di riduzione di un chetone si osserva in condizioni di ridotta disponibilità di ossigeno nei tessuti: durante intenso esercizio, il piruvato derivato dalla glicolisi viene ridotto a lattato dall’enzima lattato deidrogenasi (LDH). Il cofattore NADH fornisce equivalenti riducenti e si ossida a NAD+, rigenerando il pool necessario a sostenere il flusso glicolitico:
\[ \mathrm{Piruvato} + \mathrm{NADH} + \mathrm{H^+} \longrightarrow \mathrm{Lattato} + \mathrm{NAD^+} \]
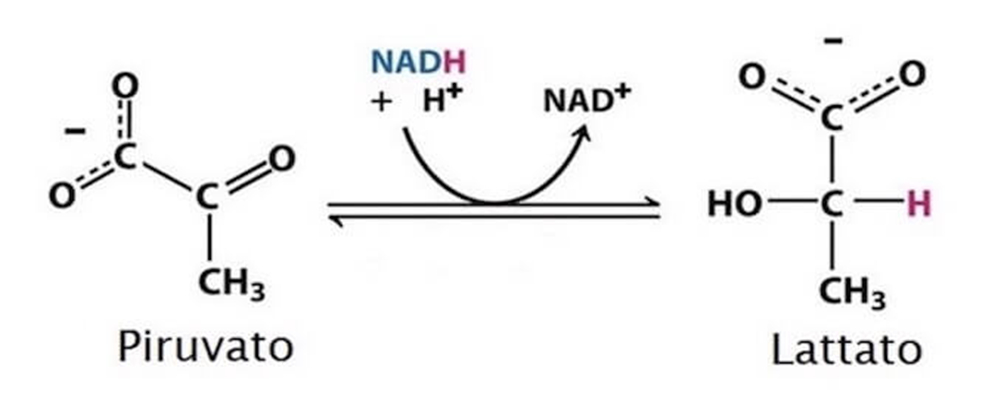 |
| La reazione che porta alla formazione da Piruvato a Lattato è mediata dalla Lattato-deidrogenasi ed utilizza NADH che diventa NAD+ |
La trasformazione più tipica del gruppo carbonilico consiste nell’addizione al doppio legame polare C=O. L’andamento elettronico ricorda, per certi versi, l’addizione ai doppi legami C=C, ma la forte polarizzazione del carbonile modifica profondamente la reattività: il carbonio carbonilico è elettrofilo, mentre l’ossigeno è nucleofilo di base. In condizioni acide, la protonazione dell’ossigeno aumenta l’elettrofilia del carbonio, accelerando l’attacco del nucleofilo. Convenzionalmente, un catalizzatore acido è indicato sovrafreccia come [H⁺] o \(\xrightarrow{H^+}\).
Un caso rilevante è l’addizione di un alcol a un’aldeide o a un chetone, che conduce dapprima a un emiacetale (o semichetale) e, in presenza di eccesso di alcol ed acido, all’acetale (o chetale). In termini meccanicistici, la sequenza acidocatalizzata comprende: protonazione del carbonile \(\big(\text{R}_2\text{C}=O + \text{H}^+ \rightleftharpoons \text{R}_2\text{C}(\!\!\!\!^{+}\!-\!OH)\big)\), attacco nucleofilo dell’alcol al carbonio carbonilico, deprotonazione a emiacetale; successiva protonazione dell’ossidrile emiacetalico, eliminazione di acqua e cattura di una seconda molecola di alcol per formare l’acetale. L’intero processo è reversibile e governato dall’equilibrio chimico.
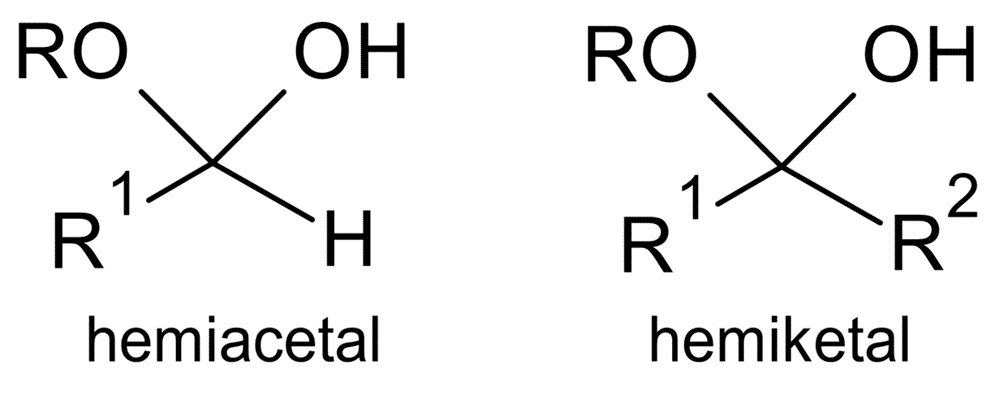 |
| Struttura generale di un emiacetale (a sinistra) e di un emichetale (a destra). |
Gli emiacetali isolati sono in genere instabili in ambiente acido e con eccesso di alcol: l’ossidrile emiacetalico viene sostituito da un gruppo –OR, fornendo un acetale. La trasformazione è un equilibrio reversibile che può essere spostato verso i prodotti rimuovendo l’acqua prodotta o usando un grande eccesso di alcol (principio di Le Chatelier).
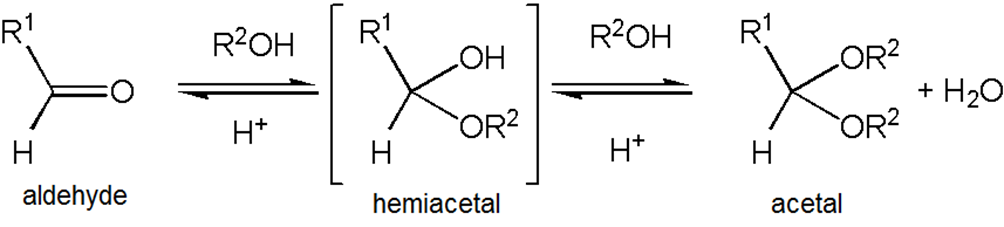 |
| Conversione da aldeide ad acetale |
Come esempio didattico, si consideri la formazione dell’acetale da butanale e etanolo in presenza di acido:
\(\text{CH}_3\text{CH}_2\text{CH}_2\text{CHO} + \text{CH}_3\text{CH}_2\text{OH} \;\rightleftharpoons\;[\text{H}^+] \;\text{CH}_3\text{CH}_2\text{CH}_2\text{CH}(OH)(OCH_2CH_3)\) (emiacetale)
\(\text{CH}_3\text{CH}_2\text{CH}_2\text{CH}(OH)(OCH_2CH_3) + \text{CH}_3\text{CH}_2\text{OH} \;\rightleftharpoons\;[\text{H}^+] \;\text{CH}_3\text{CH}_2\text{CH}_2\text{CH}(OCH_2CH_3)_2 + \text{H}_2\text{O}\) (acetale dietilico)
Analogamente, un chetone reagisce con due equivalenti di alcol per fornire un chetale; l’equilibrio è favorito da condizioni disidratanti o da rimozione azeotropica dell’acqua.
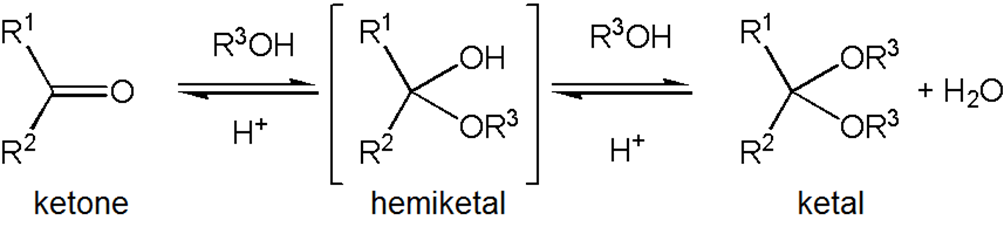 |
| Conversione da chetone a chetale |
Per esempio, il 2-butanone reagisce con metanolo in ambiente acido secondo le tappe seguenti:
\(\text{CH}_3\text{COCH}_2\text{CH}_3 + \text{CH}_3\text{OH} \;\rightleftharpoons\;[\text{H}^+] \;\text{CH}_3\text{C}(OH)(OCH_3)\text{CH}_2\text{CH}_3\) (semichetale)
\(\text{CH}_3\text{C}(OH)(OCH_3)\text{CH}_2\text{CH}_3 + \text{CH}_3\text{OH} \;\rightleftharpoons\;[\text{H}^+] \;\text{CH}_3\text{C}(OCH_3)_2\text{CH}_2\text{CH}_3 + \text{H}_2\text{O}\) (dimetilchetale)
Una classe di eccezioni importanti sono i carboidrati: grazie alla reazione intramolecolare tra il carbonile e un ossidrile opportunamente posizionato, i monosaccaridi a cinque o sei atomi di carbonio formano in acqua emiacetali o semichetali ciclici (forme furanosiche o piranosiche) energeticamente più stabili della forma aperta. L’ossigeno anomerico può dare ulteriori reazioni di acetilazione con l’ossidrile di un altro monosaccaride producendo un acetale (o chetale) intermonosaccaridico: nasce così un disaccaride, unito da un legame glicosidico C–O–C. Il centro anomerico può risultare α o β, con fenomeno di mutarotazione in soluzione:
• Le condizioni che spostano l’equilibrio verso acetali/chetali includono rimozione di H₂O, uso di alcol in grande eccesso, essiccanti acidi o trappole azeotropiche;
• Acetali e chetali sono stabili in ambiente basico e trovano impiego come gruppi protettivi del carbonile in sintesi organica.
Molte aldeidi e chetoni mostrano un equilibrio dinamico tra una forma chetonica (o aldeidica) e la corrispondente forma enolica, che differiscono per la posizione di un protone e del doppio legame. L’enolo possiede un doppio C=C coniugato a un gruppo –OH; in basi forti, l’enolo si deprotona a enolato, anione stabilizzato per risonanza tra ossigeno e carbonio α.
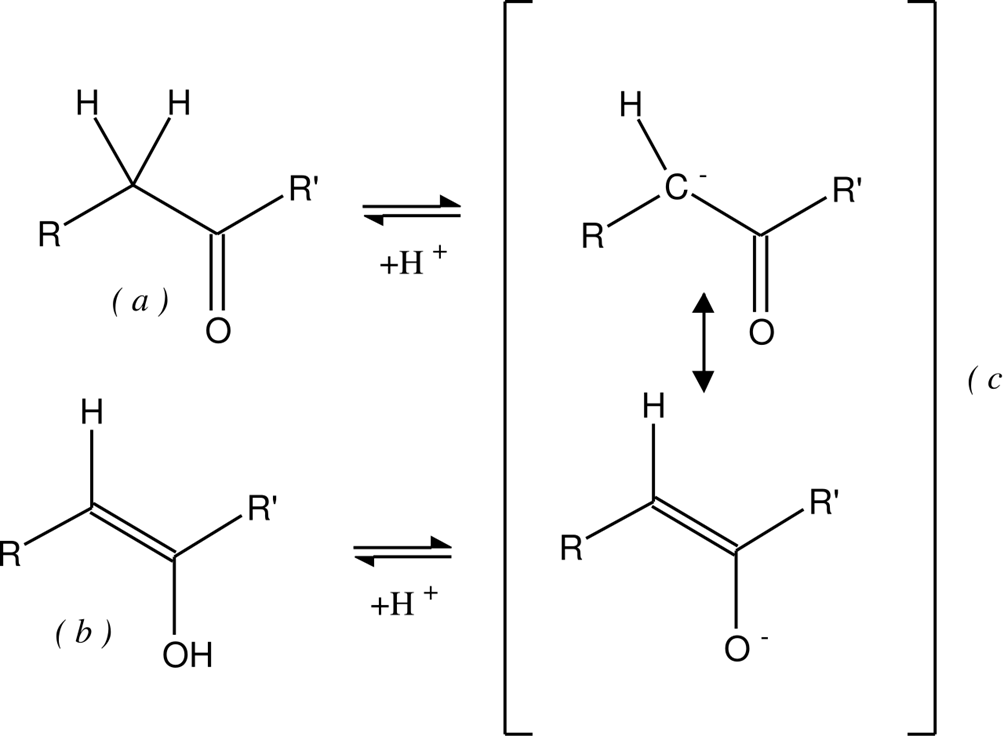 |
| Tautomeria cheto-enolica; (a) è il chetone o l'aldeide, (b) l'enolo corrispondente e (c) l'anione stabilizzato per risonanza |
Nella maggior parte delle aldeidi e dei chetoni non coniugati, l’equilibrio è fortemente spostato verso la forma chetonica, mentre l’enolo è presente in tracce. La catalisi acida o basica accelera l’interconversione: in acido via protonazione dell’ossigeno e successivo trasferimento del protone, in base via formazione di enolato e successiva protonazione sul carbonio.
Un enolo di rilevanza biochimica è il fosfoenolpiruvato (PEP), estere fosforico dell’enolo dell’acido piruvico, ad altissimo potenziale di trasferimento del gruppo fosforico. Il PEP si forma dall’azione dell’enolasi sul 2-fosfoglicerato nella glicolisi. Nella tappa terminale, la piruvato chinasi trasferisce il fosfato al’adenosina difosfato (ADP) generando adenosina trifosfato (ATP) e piruvato: l’energia di reazione è resa molto favorevole dalla tautomerizzazione dell’enolo di piruvato alla forma chetonica, che rimuove il prodotto reattivo e trascina l’equilibrio.
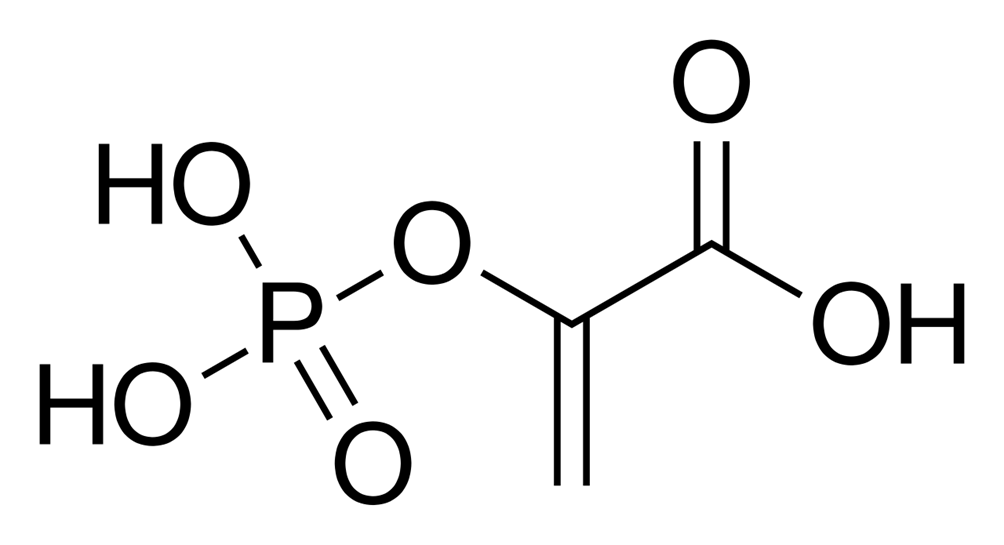 |
| Acido fosfoenolpiruvico |
Il fosfoenolpiruvato viene prodotto nel penultimo passaggio del percorso metabolico detto glicolisi, che costituisce il primo stadio nel metabolismo dei carboidrati. Nel passaggio finale della glicolisi, il gruppo fosforico viene trasferito dal fosfoenolpiruvato all'adenosindifosfato (ADP) che si trasforma in adenosintrifosfato (ATP), la principale fonte energetica nelle cellule.
La condensazione aldolica costruisce nuovi legami C–C a partire da aldeidi o chetoni contenenti almeno un idrogeno in α al carbonile. In condizioni basiche, l’ossidrile deprotona la posizione α generando l’enolato, che addiziona nucleofilicamente al carbonile di una seconda molecola (aldol addizione), formando una β-idrossialdeide o un β-idrossichetone. In molte condizioni, segue disidratazione a \(\alpha,\beta\)-enone coniugato (aldol condensazione).
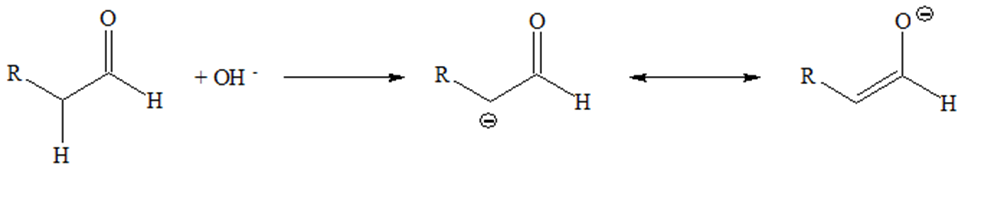 |
| La reazione aldolica è una reazione in cui due molecole di un'aldeide o di un chetone, che abbiano almeno un atomo di idrogeno in posizione α al gruppo carbonilico (C=O), si combinano tra loro formando una β-idrossialdeide o un β-idrossichetone. |
Per chiarezza didattica, si osservi la reazione tra acetone e benzaldeide (quest’ultima priva di idrogeni α): l’enolato dell’acetone attacca il carbonile aromatico, fornendo l’aldolo incrociato, 4-idrossi-4-fenil-2-butanone; un successivo riscaldamento può disidratare il prodotto a 4-fenil-3-buten-2-one (\(\alpha,\beta\)-enone coniugato).
Le reazioni tra due molecole identiche di chetone sono possibili quando il chetone presenta idrogeni α sufficientemente acidi; per esempio, l’auto-aldolazione del 2-butanone fornisce, in prima istanza, un β-idrossichetone, che sotto condizioni più rigide perde acqua generando l’enone coniugato. Il bilancio di atomi evidenzia in ogni caso la formazione di un nuovo legame C–C tra il carbonio α di una unità e il carbonio carbonilico dell’altra.
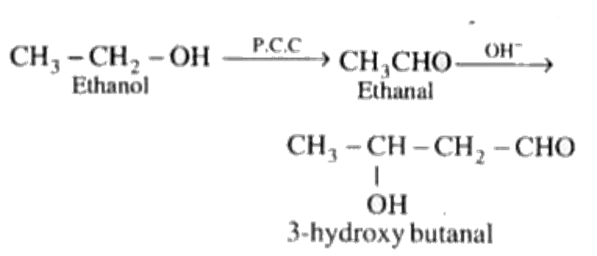 |
| La reazione di condensazione fra due molecole di etanale. |
In laboratorio la catalisi è spesso basica (es. idrossidi, alcoli in presenza di basi, oppure basi forti per controllare la chemioselettività), mentre in ambiente biologico la catalisi è enzimatica. Il legame C–C del metabolismo dei carboidrati è costruito dall’aldolasi, che nella glicolisi scinde il fruttosio-1,6-difosfato in gliceraldeide-3-fosfato (GAP) e diidrossiacetone fosfato (DHAP); nel verso opposto della gluconeogenesi, la stessa enzima catalizza la condensazione aldolica tra DHAP e GAP, generando fruttosio-1,6-difosfato.
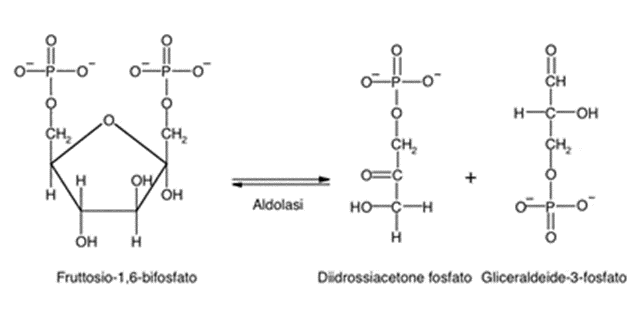 |
| Reazione catalizzata dall'aldolasi. |
La velocità e la specificità della trasformazione sono garantite dall’architettura del sito attivo dell’aldolasi. Il prodotto, fruttosio-1,6-difosfato, può essere instradato verso la sintesi di glucosio dopo idrolisi dei fosfati. Quando la glicemia scende, la gluconeogenesi fornisce nuovo glucosio per i tessuti glucosio-dipendenti; viceversa, nella glicolisi la sequenza procede nel senso opposto, confermando la reversibilità generale delle tappe aldoliche:
• Selettività: l’aldolazione incrociata richiede strategie di controllo (scelta dei partner, uso di basi forti non nucleofile, formazione di enolati non equilbrati) per limitare miscele di prodotti;
• Termodinamica: le β-idrossicarboniliche possono disidratarsi a enoni coniugati, spesso termodinamicamente favoriti;
• Ambiente di reazione: basi deboli promuovono equilibri enolato/enolo, basi forti generano enolati cinetici o termodinamici a seconda di solvente, temperatura e stechiometria.










