Reazioni degli alcani e dei cicloalcani
Definizione
Gli alcani e i cicloalcani, come tutti gli idrocarburi saturi, subiscono ossidazione completa in presenza di un eccesso di ossigeno molecolare. Tale processo, la combustione, richiede innesco termico o una scintilla e procede con forte sviluppo di calore, producendo anidride carbonica e acqua come unici prodotti quando l’ossigeno è in grande eccesso;
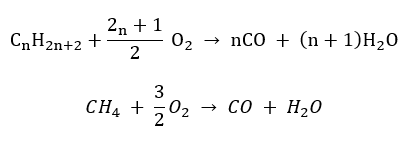 |
| Combustione incompleta degli alcani. |
Di seguito sono riportati due esempi rappresentativi: la combustione del metano e quella del cicloesano, rispettivamente il più semplice alcano e un cicloalcano privo di tensione d’anello significativa;
Reazione di combustione del metano:
\[ \mathrm{CH_4 + 2\,O_2 \;\xrightarrow{\Delta}\; CO_2 + 2\,H_2O + \text{calore}} \]
Reazione di combustione del cicloesano:
\[ \mathrm{C_6H_{12} + 9\,O_2 \;\xrightarrow{\Delta}\; 6\,CO_2 + 6\,H_2O + \text{calore}} \]
La combustione completa degli idrocarburi è fortemente esoergonica, con \(\Delta H^\circ_\text{comb} < 0\), e costituisce la base del loro impiego come combustibili in impianti termici, motori a combustione interna e sistemi di generazione elettrica. L’energia liberata dipende principalmente dal numero di legami C–H e C–C che vengono ossidati a C=O e O–H, e cresce al crescere della massa dell’idrocarburo;
In condizioni non ideali (apporto di ossigeno insufficiente, miscelazione incompleta, temperature non uniformi) si osserva combustione parziale con formazione di monossido di carbonio o addirittura di carbonio elementare (fuliggine):
\[ \mathrm{2\,CH_4 + 3\,O_2 \;\to\; 2\,CO + 4\,H_2O} \]
\[ \mathrm{C_xH_y \;\to\; C(s) + \ldots} \]
La combustione ad alta temperatura dell’aria promuove inoltre la formazione di ossidi di azoto (NOx) a partire da \(\mathrm{N_2}\) e \(\mathrm{O_2}\), che contribuiscono all’inquinamento atmosferico. Sul piano climatico, la liberazione di grandi quantità di \(\mathrm{CO_2}\) costituisce un fattore rilevante per l’aumento dell’effetto serra;
Gli aspetti operativi di una combustione efficiente includono:
- rapporto aria/combustibile in eccesso controllato per garantire ossidazione completa;
- adeguata turbolenza e miscelazione, al fine di ridurre le sacche locali di carenza di ossigeno;
- temperatura di fiamma sufficiente all’innesco ma limitata per contenere le emissioni di NOx;
- sistemi di post-trattamento dei fumi (ad esempio, ossidazione catalitica del CO), quando necessario.
Alcani e cicloalcani possono subire sostituzione radicalica con alogeni, in particolare cloro o bromo. L’alogenazione è una reazione di sostituzione omolitica in cui un atomo di idrogeno legato al carbonio viene rimpiazzato da un atomo di alogeno, con formazione di un alogenuro alchilico e di un acido alogenidrico:
\[ \mathrm{R{-}H + X_2 \;\xrightarrow{h\nu\ \text{o}\ \Delta}\; R{-}X + H{-}X} \]
Poiché i legami C–H e C–C di un alcano sono forti e non polari, l’attivazione richiede luce (UV) o calore, talvolta coadiuvati da iniziatori radicalici (perossidi). La reazione procede per catena radicalica, con fasi di innesco, propagazione e terminazione, schematicamente:
\[ \begin{aligned} &\text{Innesco:} && \mathrm{X_2 \;\xrightarrow{h\nu/\Delta}\; 2\,X\cdot} \\ &\text{Propagazione:} && \mathrm{R{-}H + X\cdot \;\to\; R\cdot + H{-}X} \\ & && \mathrm{R\cdot + X_2 \;\to\; R{-}X + X\cdot} \\ &\text{Terminazione:} && \mathrm{R\cdot + R\cdot \;\to\; R{-}R},\quad \mathrm{R\cdot + X\cdot \;\to\; R{-}X},\quad \mathrm{X\cdot + X\cdot \;\to\; X_2}. \end{aligned} \]
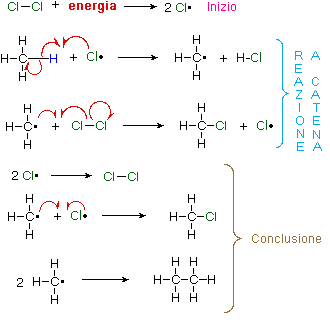 |
| Clorurazione radicalica del metano. |
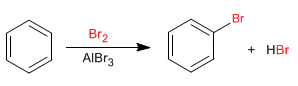 |
| Bromurazione del benzene. |
In pratica, il cloro reagisce più velocemente ma è meno selettivo, mentre il bromo è più lento e più selettivo per i centri radicalici più stabilizzati. La fluorurazione degli alcani è spesso troppo violenta e difficilmente controllabile, mentre la iodurazione risulta sfavorevole dal punto di vista termodinamico in molte condizioni;
Se l’alogeno è presente in eccesso o la reazione viene lasciata procedere a lungo, l’alogenuro primario prodotto può subire ulteriori sostituzioni, generando specie polialogenate. Ad esempio, nella bromurazione a catena del metano si possono ottenere, in sequenza, bromometano \(\mathrm{CH_3Br}\), dibromometano \(\mathrm{CH_2Br_2}\), tribromometano \(\mathrm{CHBr_3}\) e tetrabromometano \(\mathrm{CBr_4}\); il controllo stechiometrico e l’irraggiamento moderato riducono la formazione di prodotti secondari;
L’alogenazione di un alcano ramificato presenta esiti regioselettivi distinti in funzione del tipo di idrogeno coinvolto. Nel 2-metilpropano, la sostituzione di un idrogeno terziario sul carbonio-2 fornisce 2-cloro-2-metilpropano, mentre la sostituzione su un’idrogeno primario genera 1-cloro-2-metilpropano. Con il bromo, la maggiore preferenza per il centro terziario fa sì che il 2-bromoderivato prevalga nettamente nelle miscele di reazione;
Per alcani più complessi, ciascuna posizione contenente almeno un idrogeno è potenzialmente suscettibile di sostituzione radicalica, con distribuzioni di prodotto che riflettono sia il numero di idrogeni equivalenti sia la reattività intrinseca degli stessi. Un caso tipico è la bromurazione del propano, che porta a una miscela di 1-bromopropano e 2-bromopropano, in cui il derivato secondario tende a predominare per la maggiore stabilità del radicale intermedio secondario rispetto a quello primario;
Dal punto di vista applicativo, gli alogenuri alchilici sono intermedi di largo impiego in sintesi organica per reazioni di sostituzione e di eliminazione; l’industria farmaceutica sfrutta la loro reattività per introdurre funzionalità più complesse. Alcuni alogenuri alchilici polialogenati sono stati storicamente utilizzati come solventi, pesticidi o fluidi refrigeranti, pur con crescenti restrizioni regolatorie per motivi ambientali. Si considerino inoltre alcuni aspetti pratici e di sicurezza:
- l’impiego di luce UV (indicata come \(h\nu\) sopra la freccia di reazione) o calore (\(\Delta\)) come iniziatori è essenziale per l’avvio della catena radicalica;
- per minimizzare la polialogenazione, si opera con l’alogeno come reagente limitante e tempi di esposizione ridotti;
- la selettività segue in generale l’ordine di stabilità radicalica 3° > 2° > 1°, più marcato per il bromo che per il cloro;
- i sottoprodotti gassosi \(\mathrm{HCl}\) o \(\mathrm{HBr}\) sono corrosivi e richiedono idonei sistemi di abbattimento;
- l’alogenazione degli aromatici (come il benzene) segue un differente meccanismo elettrofilo catalizzato da acidi di Lewis, distinto dalla sostituzione radicalica degli alcani.








