Reazioni che coinvolgono alcheni e alchini
Definizione
Le trasformazioni più caratteristiche di alcheni e alchini sono le addizioni ai legami multipli carbonio–carbonio, in cui il sistema elettronico \( \pi \) viene impiegato per legare nuovi sostituenti. Nel quadro generale dell’addizione elettrofila, un alchene o un alchino agiscono come nucleofili verso un agente elettrofilo (per esempio H+), con successiva cattura di un controione nucleofilo. Tra le addizioni più diffuse agli alcheni si annoverano l’idrogenazione con H2, l’alogenazione con X2 (Cl2, Br2), l’idratazione con H2O in condizioni acido-catalizzate e l’addizione di acidi alogenidrici (HX). Queste reazioni riducono il grado di insaturazione e, nella maggior parte dei casi, procedono con cinetica e stereochimica ben definite, governate dalla stabilità degli intermedi cationici o degli ioni alonio a tre termini.
L’idrogenazione consiste nell’addizione di una molecola di idrogeno (H2) a un legame multiplo C=C o C≡C, con formazione di nuovi legami C–H e conseguente saturazione del substrato. Per gli alcheni, la rottura del legame \( \pi \) produce l’alcano corrispondente; il processo è tipicamente catalizzato eterogeneamente da metalli come platino, palladio su carbone o nichel, e richiede condizioni opportune di temperatura e pressione per favorire l’adsorbimento di reagenti e la dissociazione di H2.
Dal punto di vista stereochimico, l’idrogenazione catalitica degli alcheni avviene di norma in addizione sin, poiché entrambi gli atomi di idrogeno sono trasferiti dalla superficie metallica alla stessa faccia del doppio legame. Quando si passa agli alchini, l’aggiunta di \(2\) equivalenti di H2 porta a un alcano; tuttavia, regolando il catalizzatore è possibile arrestare la reazione allo stadio di alchene: il catalizzatore di Lindlar fornisce preferenzialmente alcheni cis, mentre riduzioni in metallo disciolto (Na/NH3 liquida) conducono spesso ad alcheni trans.
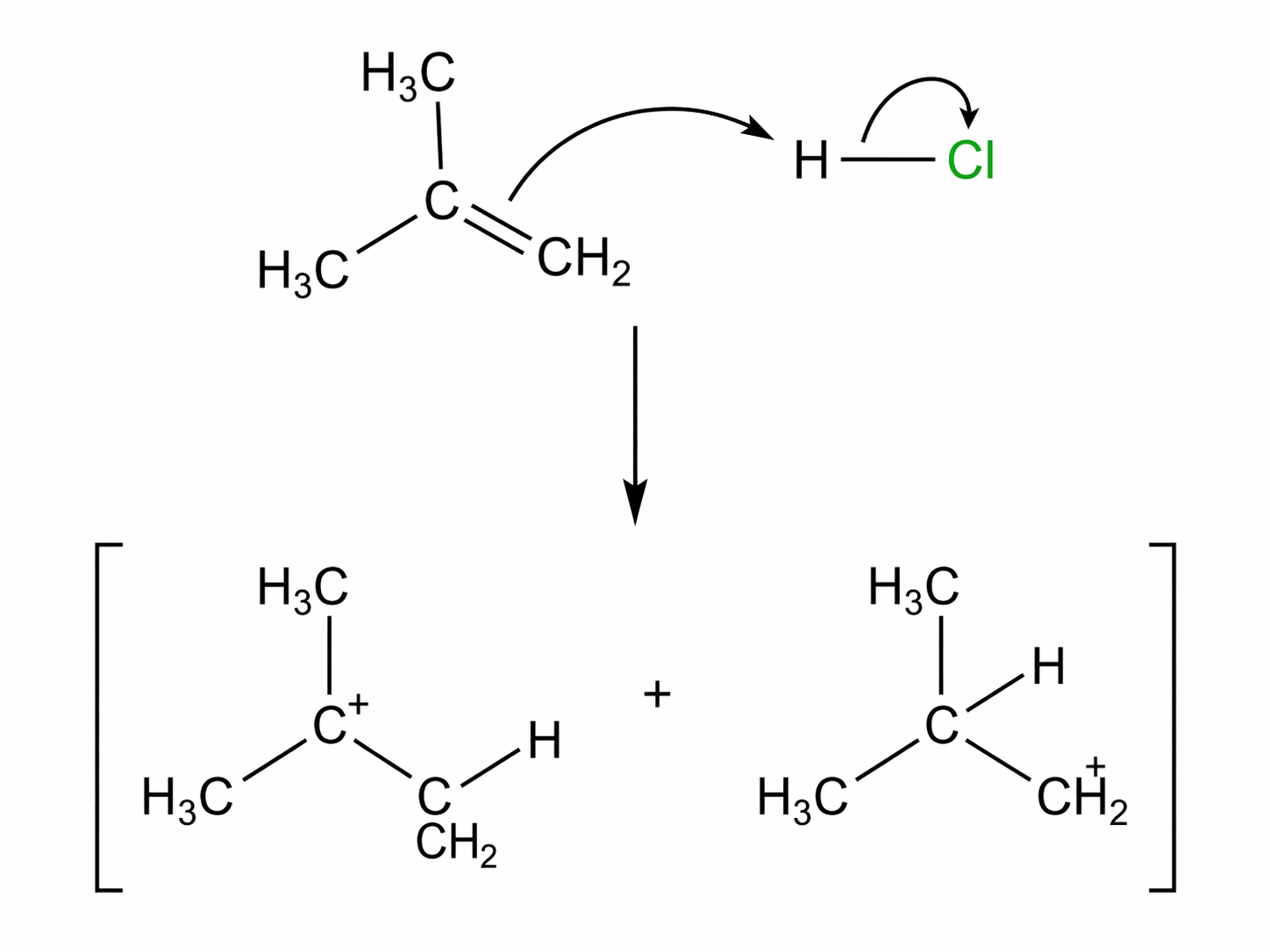
Passo 1. Protonazione dell’alchene (avvio dell’addizione elettrofila)
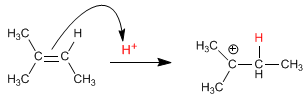 |
| Formazione del carbocatione negli alcheni. |
Passo 2. Attacco nucleofilo dell’acqua sull’intermedio carbocationico
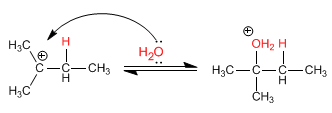 |
| Attacco nucleofilo dell’acqua al carbocatione. |
Passo 3. Deprotonazione dell’ossonio e formazione dell’alcol; l’acqua agisce da base.
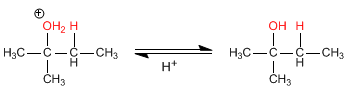 |
| Deprotonazione e formazione dell’alcol. |
La sequenza illustrata sopra mostra, a titolo esemplificativo, una tipica addizione elettrofila (idratazione acido-catalizzata) che condivide la logica generale del primo stadio delle addizioni: attivazione elettrofila del doppio legame, generazione di un intermedio ad alta energia e cattura nucleofila. Sebbene l’idrogenazione catalitica proceda su una superficie metallica e non attraverso carbocationi in soluzione, l’analogia concettuale aiuta a mettere in relazione la reattività dei legami \( \pi \) con l’esito stereochimico dell’addizione.
Le condizioni operative per l’idrogenazione degli alchini sono affini a quelle degli alcheni. Due moli di H2 si addizionano a un C≡C per dare l’alcano corrispondente, come riassunto dalla reazione generale:
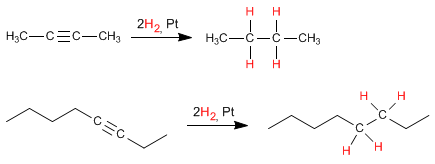 |
| Idrogenazione completa degli alchini. |
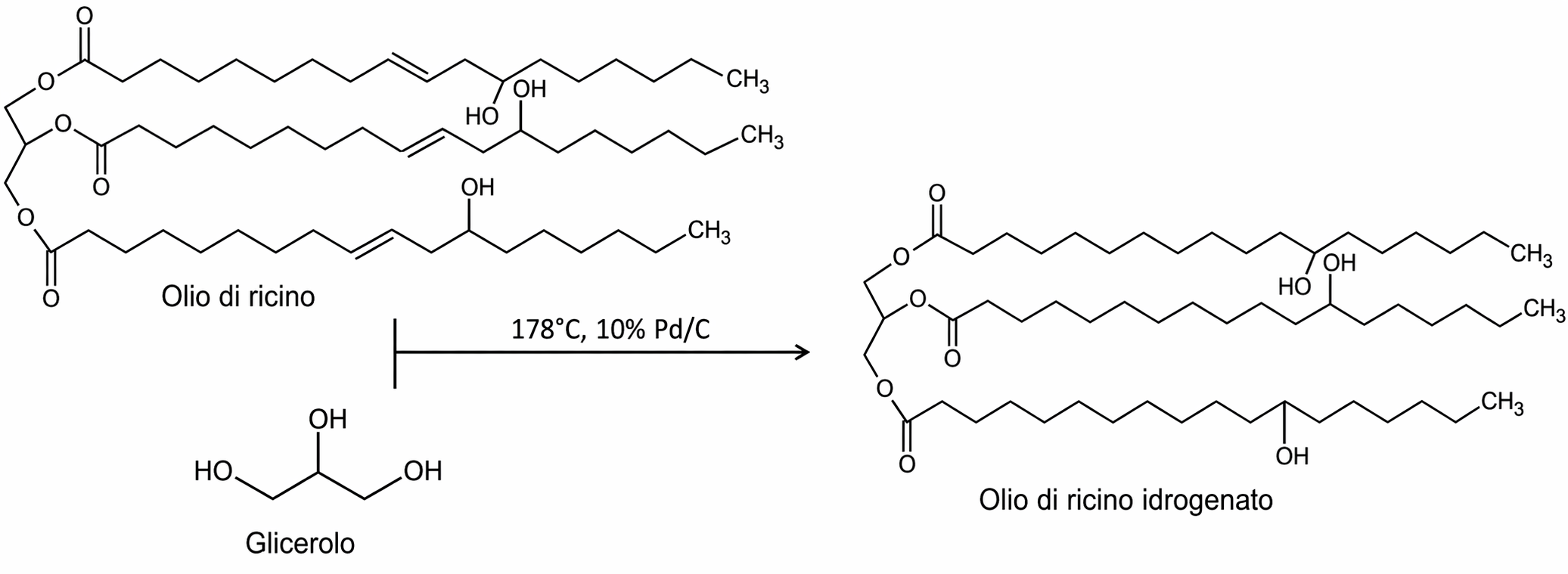
Un’applicazione industriale di rilievo è l’idrogenazione parziale di oli vegetali per la produzione di margarina (Figura 06.10-01). Gli oli sono ricchi di doppi legami e fondono a basse temperature, risultando liquidi a temperatura ambiente; l’addizione di H2 ai legami \( \pi \) incrementa la temperatura di fusione e produce miscele più solide. Durante questi processi possono verificarsi isomerizzazioni con formazione di acidi grassi trans, costituyenti rinvenibili in alcune margarine e oggetto di particolare attenzione nutrizionale:
- catalizzatori tipici: Pt, Pd/C, Ni; per idrogenazioni selettive degli alchini verso alcheni cis si impiega il catalizzatore di Lindlar;
- stereochimica: addizione sin per alcheni su superfici metalliche;
- controllo della selettività: variazione del catalizzatore, della pressione di H2 e della temperatura permette di fermarsi allo stadio di alchene o di procedere fino all’alcano;
- termidinamica: le idrogenazioni sono fortemente esoergoniche per la formazione di legami C–H e C–C più forti.
Cloro (Cl2) e bromo (Br2) reagiscono prontamente con i doppi legami degli alcheni. L’alogenazione procede a temperatura ambiente, senza bisogno di catalizzatori, in solventi poco nucleofili (ad esempio CCl4 o CH2Cl2):
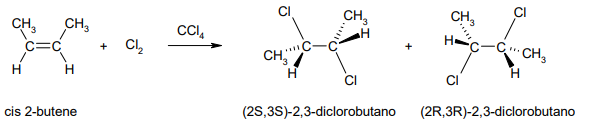 |
| Addizione elettrofila di Cl₂ a un alchene. |
Il meccanismo tipico prevede la formazione di un catione alonio a tre termini e un successivo attacco del controione alogenuro, con esito di addizione anti. L’alogenazione degli alchini è anch’essa possibile: l’ingresso di due molecole di X2 porta ai tetraaloalcani, passando attraverso l’alogenoalchene intermedio.
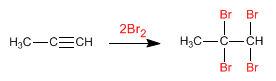 |
| Addizione di bromo a un alchino. |
L’addizione della prima molecola di alogeno avviene con stereochimica anti;
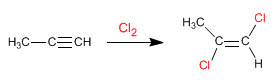 |
| Addizione parziale di Cl₂ a un alchino. |
Nella bromurazione dell’1-pentene, l’aspetto cromatico della miscela di reazione cambia nettamente: la soluzione di Br2 è rosso-bruna, mentre il prodotto finale è incolore (Figura 06.10-02). Questo comportamento è sfruttato come saggio qualitativo per l’insaturazione: la decolorazione del bromo indica consumo di Br2 per addizione al doppio o triplo legame. A parità di quantità di sostanza organica, un composto con più legami \( \pi \) consuma più bromo; ad esempio, un diene con due C=C o un alchino con un C≡C impiega circa il doppio di Br2 rispetto a un monoalchene, a parità di condizioni:
- meccanismo: formazione di ione bromonio o cloronio, seguita da apertura anti con X−;
- regio- e stereocontrollo: su alcheni dissimmetrici, l’attacco del nucleofilo privilegia la posizione più sostituita dell’intermedio, con anti-addizione netta;
- condizioni: solventi inerti e poco nucleofili migliorano la selettività ed evitano reazioni collaterali;
- saggio analitico: la perdita del colore del bromo è indicativa della presenza di insaturazioni e, in modo qualitativo, del loro numero.
L’addizione di acqua a un doppio legame carbonio–carbonio costituisce una tipica reazione di addizione elettrofila. In presenza di tracce di un acido forte, indicato genericamente come H+ (ad esempio H2SO4 o H3PO4), l’alchene viene protonato per formare un carbocatione, al quale l’acqua si addiziona come nucleofilo; la deprotonazione successiva genera un alcol come prodotto netto:
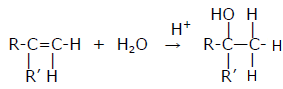 |
| Addizione di acqua a un alchino. |
Un caso semplice è l’idratazione dell’etene, che fornisce etanolo secondo il meccanismo descritto:
 |
| Idratazione di un alchene ad alcol. |
Per alcheni asimmetrici, la regiochimica è governata dalla stabilità del carbocatione intermedio. La regola empirica attribuita a Markovnikov, confermata dall’analisi meccanicistica, prevede che il protone si leghi preferenzialmente al carbonio del doppio legame che possiede il numero maggiore di atomi di idrogeno, poiché tale protonazione genera il carbocatione più stabile (terziario > secondario > primario). La molecola d’acqua attacca quindi il centro carbocationico più sostituito, e dopo deprotonazione si ottiene l’alcol Markovnikov. Ad esempio, per 1-butene si forma prevalentemente 2-butanolo: il protone si addiziona al carbonio terminale e l’ossidrile si colloca sul carbonio interno.
È utile ricordare che, quando si formano carbocationi, possono intervenire riarrangiamenti (migrazione di idruro o di un gruppo alchilico) che talvolta conducono ad alcoli strutturalmente diversi da quelli attesi per una semplice addizione. In alternativa alla via carbocationica, esistono strategie complementari (es. ossimercurazione–demercurazione; idroborazione–ossidazione) che modulano la regiochimica e riducono i riarrangiamenti, ma esse implicano condizioni e reagenti differenti dalla catalisi acida classica.
Processi di idratazione di doppi legami sono anche centrali in biochimica. Nel ciclo dell’acido citrico, l’enzima fumarasi catalizza l’addizione stereospecifica di H2O al fumarato per ottenere malato, integrando l’idratazione in un contesto di ossidoriduzioni coordinate alla produzione di equivalenti riducenti.
 |
| Idratazione del fumarato a L-malato. |
Un passaggio analogo si osserva nella β-ossidazione degli acidi grassi: l’enoyl‑CoA idratasi converte un trans‑Δ2-enoyl‑CoA nel corrispondente L‑3‑idrossiacil‑CoA mediante addizione di acqua, preparando il substrato alla successiva ossidazione. In entrambi i contesti, la chimica dell’addizione di H2O a un insaturo è adattata dall’ambiente enzimatico per ottenere selettività di sito e di faccia.
Per gli alchini, l’addizione diretta di acqua sotto catalisi acida non procede fino al diolo; dopo la prima addizione, si forma un enolo, caratterizzato dalla coesistenza del gruppo ossidrilico con un doppio legame C=C. L’enolo è generalmente instabile e va incontro rapidamente a tautomeria ceto–enolica, generando un carbonile (chetone o aldeide) più termodinamicamente favorevole. In forma schematica:
\[ \text{R–C}\equiv\text{CH} \;\xrightarrow[\text{H^+}]{\text{H}_2\text{O}}\; \underbrace{\text{R–CH{=}C(OH)H}}_{\text{enolo}} \;\rightleftharpoons\; \underbrace{\text{R–CO–CH}_3}_{\text{chetone}} \]
L’esito regiochimico segue criteri analoghi al caso degli alcheni: con catalizzatori adeguati (ad esempio Hg2+ in ambiente acido) l’idratazione di alchini terminali porta tipicamente a metilchetoni via tautomeria, mentre per alchini interni si ottengono chetoni sostituiti. L’immagine seguente illustra la sequenza addizione–tautomerizzazione:
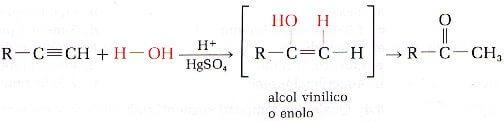 |
| Idratazione acido-catalizzata di un alchino. |
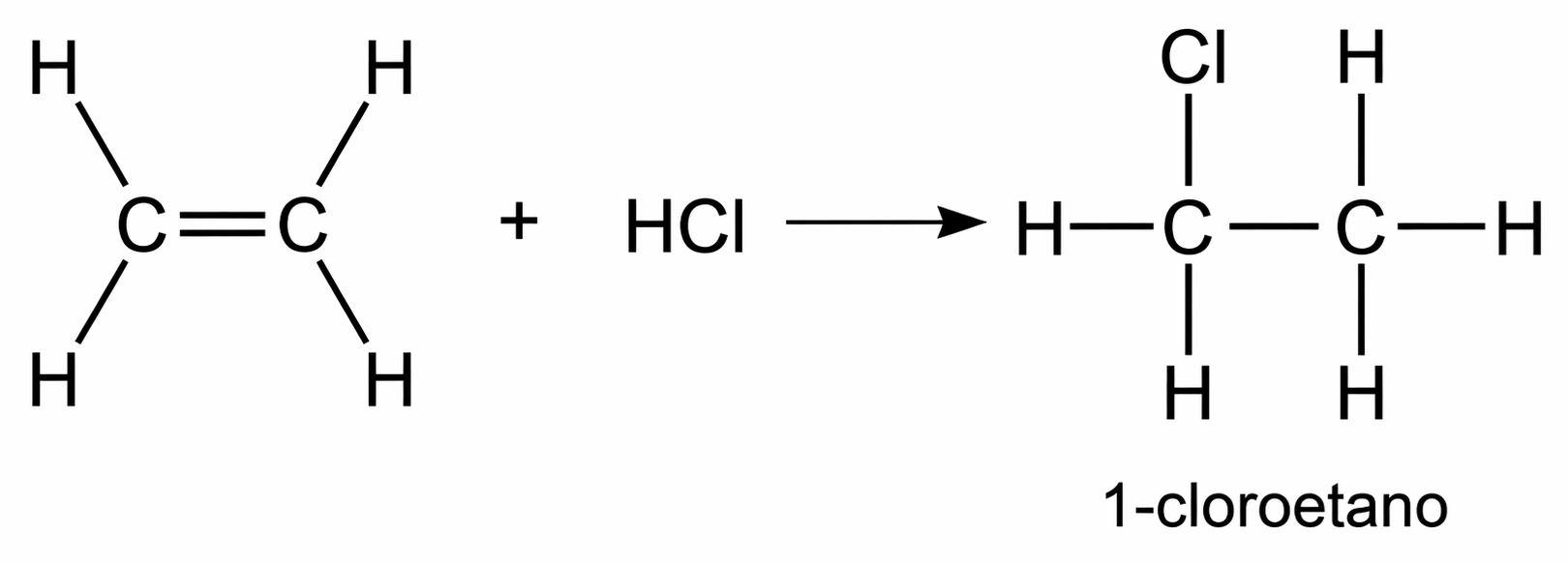
Gli alcheni reagiscono con acidi alogenidrici alogenuri (HX = HCl, HBr, HI) per fornire alogenuri alchilici. Il meccanismo standard è elettrofilo: protonazione del doppio legame con formazione di un carbocatione seguita dall’attacco del controanione X−. La trasformazione è rappresentata di seguito:
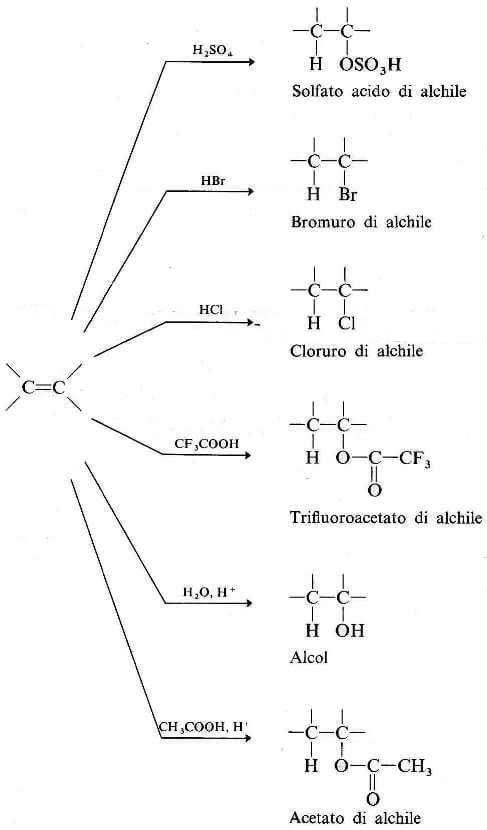 |
| Principali reazioni di addizione agli alcheni. |
Per alcheni asimmetrici, si applica la regioselettività di Markovnikov: l’idrogeno si lega al carbonio del doppio legame con la maggior disponibilità di idrogeni, generando il carbocatione più sostituito, mentre l’alogenuro si addiziona al centro più sostituito. La planarità del carbocatione intermedio implica perdita di informazione stereochimica al centro attaccato, con possibile formazione di miscele racemiche quando si generano centri chirali:
- Controllo cinetico: HCl, HBr e HI mostrano reattività crescente con la maggiore acidità e polarizzabilità dell’alogeno;
- Ristrutturazioni: sono possibili migrazioni di idruro o gruppi alchilici qualora conducano a carbocationi più stabili, modificando la struttura del prodotto;
- Eccezione radicalica: in presenza di perossidi e luce/riscaldamento, HBr può addizionarsi con regiochimica anti‑Markovnikov via catena radicalica; questa modalità richiede condizioni non acide e meccanismo distinto.
Nel complesso, idratazione e idroalogenazione illustrano come la stabilità intermedia del carbocatione e le condizioni operative (catalizzatore, solvente, temperatura) determinino l’orientamento e la selettività delle addizioni agli insaturi, principi ampiamente validi sia in sintesi organica sia nei sistemi biochimici.
Le addizioni agli alcheni procedono secondo un meccanismo di addizione elettrofila: il legame π del doppio legame C=C funge da sorgente di densità elettronica e interagisce con una specie elettrofila, tipicamente H+ o un acido di Lewis; per “elettrofilo” si intende una specie carente di elettroni (carica positiva o con orbitali vuoti) attratta da regioni ricche di carica. L’impatto iniziale dell’elettrofilo sul doppio legame provoca scissione eterolitica del legame π, con formazione di un nuovo legame σ C–H e di un carbocatione. Questo intermedio cationico, a sua volta, viene rapidamente intercettato da un nucleofilo (ad esempio OH−, Cl−, Br−), ossia una specie ricca di elettroni in grado di donare una coppia di non legame.
Nel caso di reagenti del tipo H–X (acido alogenidrico) o di sistemi che generano H+ in presenza di H2O (idratazione acido-catalizzata), l’addizione avviene in due stadi distinti, con un profilo energetico governato dalla prima tappa (Figura 06.10-03):
- Attacco elettrofilo: H+, derivato dalla dissociazione di H–X o generato dal catalizzatore acido, coordina al doppio legame; gli elettroni π formano un nuovo legame σ C–H, generando un carbocatione. Questa è la tappa più lenta (determinante della velocità), generalmente endoergonica e con stato di transizione alto in energia;
- Intrusione nucleofila: il nucleofilo (X− o H2O) attacca il centro cationico con formazione del legame C–X oppure, se interviene H2O, di un ossonio C–OH2+, che successivamente perde H+ rigenerando il catalizzatore e lasciando un gruppo ossidrilico in posizione vinilica. Questa tappa è rapida e fortemente esoergonica.
Nel complesso, l’addizione elettrofila è controllata dall’evento di protonazione del doppio legame. Per un alchene asimmetrico, sono in linea di principio possibili più orientazioni: la regola di Markovnikov stabilisce che l’idrogeno si lega al carbonio del doppio legame già più idrogenato, mentre il resto (X oppure –OH) si posiziona sul carbonio più sostituito. La ragione è meccanicistica: nella tappa lenta, il carbocatione che si forma preferenzialmente è quello più stabilizzato per effetti induttivi e iperconiugativi.
Un esempio didatticamente equivalente mostra l’addizione di HBr a 1-butene: la protonazione che conduce al carbocatione secondario (sul C-2) è favorita rispetto alla formazione del carbocatione primario (sul C-1), e l’attacco di Br− porta prevalentemente a 2-bromobutano rispetto a 1-bromobutano (Figura 06.10-04). La selettività di orientazione osservata è una marcata regioselettività, spesso prossima alla regiospecificità.
Il principio si formalizza nelle tappe elementari:
\[ \ce{R-CH2-CH=CH2 + H^+ -> R-CH2-CH(+)-CH3} \quad\text{(formazione del carbocatione, tappa lenta)} \] \[ \ce{R-CH2-CH(+)-CH3 + X^- -> R-CH2-CH(X)-CH3} \quad\text{(attacco nucleofilo, tappa veloce)} \]
La preferenza per carbocationi più sostituiti (terziari > secondari > primari) discende da:
- effetti induttivi dei gruppi alchilici, che distribuiscono parzialmente la carica positiva per polarizzazione del legame C–C;
- iperconiugazione, ossia sovrapposizione tra orbitali σ(C–H/C–C) adiacenti e l’orbitale p vacante del centro cationico, con delocalizzazione elettromerica che stabilizza l’intermedio.
Questi fattori, insieme al postulato di Hammond per la tappa lenta, giustificano la validità generale della regola di Markovnikov. Va ricordato che, in sistemi idonei, possono avvenire trasposizioni (migrazione di idruro o di metile) se ciò consente il passaggio a un carbocatione più stabile, modificando la regiocontrollo finale.
L’illustrazione dell’ordine di stabilità dei carbocationi è riportata di seguito.
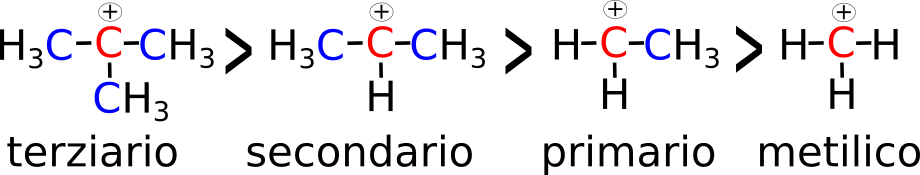 |
| Classificazione dei gruppi alchilici. |
Come caso di idratazione acido-catalizzata, il 2-metilpropene genera pressoché esclusivamente 2-metil-2-propanolo: la protonazione al carbonio più sostituito genera il catione tert-butile, fortemente stabilizzato, che viene poi catturato dall’acqua con successiva deprotonazione. L’orientazione osservata è in accordo con Markovnikov e con la maggiore stabilità del carbocatione tertiario:
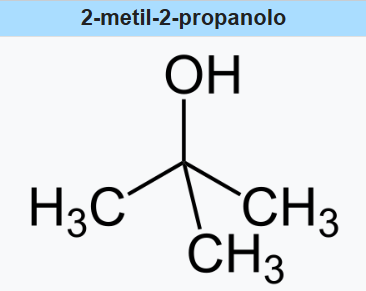 |
| Struttura del 2-metil-2-propanolo. |
Il profilo energetico complessivo e le alternative cationiche potenziali sono schematicamente richiamati nella (Figura 06.10-03) e (Figura 06.10-04).
I polimeri di addizione sono macromolecole ottenute per crescita radicalica, cationica o per coordinazione a partire da alcheni o alcheni sostituiti. La struttura ripetitiva (unità costitutiva) deriva dall’apertura successiva di doppi legami con formazione di legami σ lungo la catena. In notazione compatta:
\[ n\,\big(\ce{CH2=CH-R}\big)\;\longrightarrow\;\big[\ce{-CH2-CH(R)-}\big]_n \]
Un esempio classico di polimerizzazione cationica riguarda il 2-metilpropene, che polimerizza in condizioni acide forti o in presenza di acidi di Lewis a basse temperature. Le fasi elementari sono riorganizzabili nei tre stadi tipici della crescita a catena:
Fase 1. Innesco (protonazione del doppio legame) con generazione del catione tert-butile;
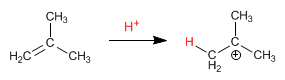 |
| Protonazione dell’alchene e formazione del carbocatione. |
Fase 2. Propagazione: l’alchene agisce da nucleofilo verso il carbocatione terminale, prolungando la catena;
Fase 3. Ulteriore propagazione per attacchi successivi di nuove molecole di alchene fino alla terminazione, con accumulo del polimero.
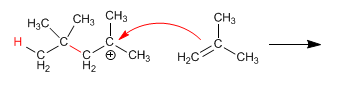 |
| Riarrangiamento del carbocatione. |
Poiché l’intermedio chiave è un carbocatione, questo schema è definito polimerizzazione cationica. Catalizzatori tipici sono acidi di Brønsted forti o sistemi di Lewis come BF3, AlCl3, spesso in presenza di co-ini ziatori, e temperature basse per limitare reazioni collaterali.
L’etene non genera intermedî cationici stabili, per cui non procede efficacemente per via cationica. Il polietilene si ottiene invece per via radicalica in condizioni di alta pressione e temperatura, oppure mediante catalizzatori di coordinazione. Nel meccanismo radicalico, perossidi o ossigeno innescano la formazione di radicali che attaccano il doppio legame avviando la catena.
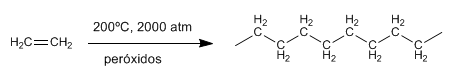 |
| Polimerizzazione dell’etene. |
Il polietilene, ottenuto dalla polimerizzazione dell’etilene (etene), è impiegato in bottiglie, giocattoli, guaine isolanti e, ad altissimo peso molecolare, anche in applicazioni biomediche (ad esempio componenti per protesi). La reazione complessiva può essere rappresentata come:
\[ n\,(\ce{CH2=CH2})\;\longrightarrow\;[-\ce{CH2-CH2}-]_n \]
Il polietilene si sintetizza a partire dall’etilene secondo la reazione:n(CH2=CH2)⟶[−CH2−CH2−]n
![{\displaystyle {\mathrm {n} ~(\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{2}}{=}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{2}}){}\mathrel {\longrightarrow } {}[{-}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{2}}{-}\mathrm {CH} {\vphantom {A}}_{\smash[{t}]{2}}{\vphantom {A}}^{-}]{\vphantom {A}}_{\smash[{t}]{n}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/96c3452d097b24bc6bcdf567eb1a0686d2cfd44d)
La molecola dell’etilene è caratterizzata dal doppio legame C=C, che richiede condizioni appropriate per l’apertura radicalica o la coordinazione al metallo, a seconda del processo adottato.
 |
| Unità ripetitiva del polietilene. |
Principali vie industriali per il polietilene:
Polimerizzazione radicalica ad alta pressione: temperature tipiche 80–300 °C, pressioni 1.000–3.000 bar, iniziatori radicalici come ossigeno o perossidi; impiegata per produrre polietilene a bassa e media densità;[6]
Polimerizzazione per coordinazione (bassa pressione): catalizzatori a base di metalli di transizione, in particolare sistemi Ziegler-Natta o Phillips; impiegata per ottenere polietilene ad alta densità;[4]
Tecnologie con catalizzatori metallocenici di prima e seconda generazione, spesso in fase gas o in soluzione, per controllare microstruttura e distribuzione di peso molecolare.
Il polipropilene, ottenuto dalla polimerizzazione del propene, rappresenta un materiale ampiamente diffuso in arredi, imballaggi e oggetti d’uso quotidiano. La presenza di un sostituente metilico su un atomo di carbonio alternato lungo la catena influenza la stereochimica di inserzione (isotattico, sindiotattico, atattico) (Tabella 06.10-01) e le proprietà meccaniche risultanti.
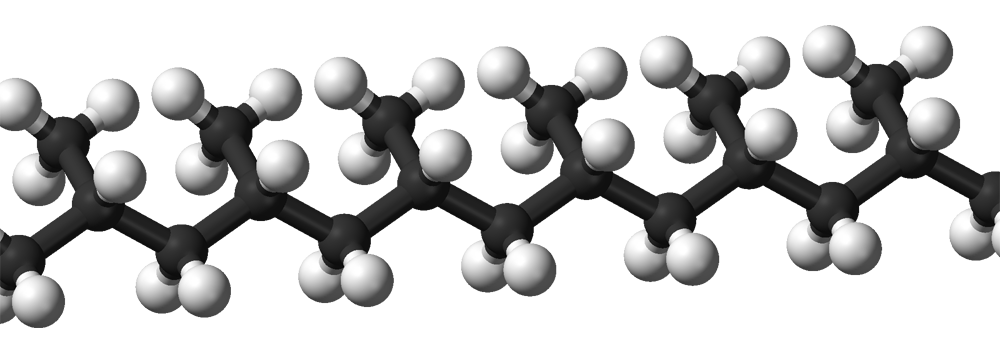 |
| Struttura tridimensionale del polietilene. |
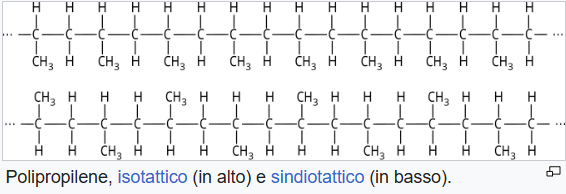 |
| Polipropilene isotattico e sindiotattico. |
Nota complementare: in condizioni radicaliche con perossidi, l’addizione di HBr ad alcheni può procedere con orientazione anti-Markovnikov per via catena-radicalica; tale percorso, tuttavia, non si applica a HCl o HI, e non opera nei processi di idratazione acido-catalizzata, nei quali restano valide le considerazioni cationiche sopra discusse.
Polimeri da reazione di addizione degli alcheni
| Nome del monomero | Formula | Polimero principale | Usi principali | Nota |
|---|---|---|---|---|
| Stirene | CH₂=CH–C₆H₅ | Polistirene (polistirolo) | Imballaggi, isolamento termico | Possibile rilascio di monomero libero; studiato per effetti irritativi e sospetto impatto neurotossico. |
| Acrilonitrile | CH₂=CH–CN | Poli(acrilonitrile) (Orlon) | Fibre sintetiche | Classificato come sostanza potenzialmente cancerogena; valutato in ambito di sicurezza occupazionale. |
| Metil-metacrilato | CH₂=C(CH₃)–COOCH₃ | Polimetil-metacrilato (PMMA; Plexiglas, Lucite) | Vetri di sicurezza, protesi, odontoiatria | Biocompatibile e ampiamente utilizzato in protesi ortopediche e restauri dentali. |
| Cloruro di vinile | CH₂=CH–Cl | Polivinilcloruro (PVC) | Tubi, pellicole, dispositivi medici | Monomero associato a tossicità epatica (angiosarcoma del fegato); il polimero inerte è molto usato in dispositivi sanitari. |
| Tetrafluoroetilene | CF₂=CF₂ | Politetrafluoroetilene (PTFE; Teflon) | Superfici antiaderenti, dispositivi chirurgici | Inerte e biocompatibile, impiegato in protesi vascolari e rivestimenti chirurgici. |
| Tabella che riporta le principali macromolecole ottenute attraverso processi di addizione di composti alchenici. | ||||