Reazioni acido-base: formazione di sali
Definizione
Un sale è un composto ionico ottenuto dalla neutralizzazione tra un acido e una base. In acqua, i sali si dissociano in ioni e, in molti casi, tali ioni interagiscono con il solvente. Si definisce idrolisi salina la reazione dell’anione, del catione, o di entrambi con le molecole d’acqua, con conseguente variazione della concentrazione di \( \text{H}^+ \) o di \( \text{OH}^- \), e quindi del pH della soluzione.
La direzione e l’entità dell’idrolisi dipendono dalla forza dell’acido e della base di partenza: gli anioni coniugati di acidi deboli tendono a comportarsi da basi, mentre i cationi coniugati di basi deboli mostrano comportamento acido. Per contro, specie derivate da acidi e basi forti risultano inerti nei confronti dell’acqua:
- anionI di acidi deboli → idrolisi basica, pH > 7;
- cationi di basi deboli → idrolisi acida, pH < 7;
- ioni provenienti da acidi e basi forti → idrolisi trascurabile, pH circa 7 a 25 °C;
- se entrambi gli ioni sono idrolizzabili (acido debole/base debole), il pH dipende dal confronto tra \( K_a \) e \( K_b \).
Nota termodinamica: il valore di \( K_w \) e quindi il pH di neutralità dipendono dalla temperatura; a 25 °C \( K_w = 1{,}0 \times 10^{-14} \).
I sali costituiti da cationi di metalli alcalini o alcalino-terrosi (ad esclusione di Be²⁺) associati a basi coniugate di acidi forti (per esempio \( \text{Cl}^- \), \( \text{Br}^- \), \( \text{ClO}_4^- \)) non reagiscono in modo apprezzabile con l’acqua; le loro soluzioni acquose risultano, in buona approssimazione, neutre a 25 °C.
Ad esempio, sciogliendo perclorato di sodio:
\(\text{NaClO}_4(s) \;\;\rightleftharpoons\;\; \text{Na}^+(aq) + \text{ClO}_4^-(aq)\)
\(\text{Na}^+\) è uno ione spettatore e \(\text{ClO}_4^-\) è base coniugata di un acido forte; nessuno dei due promuove la formazione di \( \text{H}^+ \) o \( \text{OH}^- \). Soluzioni di questo tipo (per esempio RbBr, LiClO₄, Ca(ClO₄)₂) presentano pH prossimo a 7, fatte salve le variazioni dovute alla temperatura e a effetti di forza ionica.
Eccezioni importanti riguardano cationi piccoli e altamente carichi come Al³⁺ o Be²⁺, che acidificano l’acqua tramite idrolisi dei complessi idrati \([\text{M(H}_2\text{O)}_n]^{m+}\).
Se l’anione del sale è la base coniugata di un acido debole, l’equilibrio con l’acqua produce \( \text{OH}^- \). Un esempio tipico è il fluoruro di sodio:
\(\text{NaF}(s) \;\;\rightleftharpoons\;\; \text{Na}^+(aq) + \text{F}^-(aq)\)
\(\text{Na}^+\) è inerte; lo ione fluoruro, base coniugata di HF (acido debole), idrolizza secondo:
\(\text{F}^-(aq) + \text{H}_2\text{O}(l) \;\;\rightleftharpoons\;\; \text{HF}(aq) + \text{OH}^-(aq)\)
La formazione di \( \text{OH}^- \) rende la soluzione basica. La costante di equilibrio dell’idrolisi è la basicità dello ione, legata a \( K_a \) dell’acido coniugato per:
\[ K_b(\text{F}^-) \;=\; \frac{K_w}{K_a(\text{HF})} \;\approx\; \frac{1{,}0 \times 10^{-14}}{6{,}8 \times 10^{-4}} \;\approx\; 1{,}5 \times 10^{-11}. \]
Altri sali con idrolisi basica includono NaCN e KCH₃COO (acetato di potassio); in tutti i casi, l’anione proviene da un acido debole e sottrae protoni all’acqua generando \( \text{OH}^- \).
Quando il catione del sale è l’acido coniugato di una base debole, l’interazione con l’acqua produce \( \text{H}^+ \) (o \( \text{H}_3\text{O}^+ \)), acidificando la soluzione. Consideriamo il bromuro di ammonio:
\(\text{NH}_4\text{Br}(s) \;\;\rightleftharpoons\;\; \text{NH}_4^+(aq) + \text{Br}^-(aq)\)
\(\text{Br}^-\) è base coniugata di un acido forte e non idrolizza; lo ione ammonio, acido coniugato di NH₃ (base debole), segue:
\(\text{NH}_4^+(aq) + \text{H}_2\text{O}(l) \;\;\rightleftharpoons\;\; \text{NH}_3(aq) + \text{H}_3\text{O}^+(aq)\)
La costante di acidità di \(\text{NH}_4^+\) è legata alla basicità dell’ammoniaca:
\[ K_a(\text{NH}_4^+) \;=\; \frac{K_w}{K_b(\text{NH}_3)} \;=\; \frac{1{,}0 \times 10^{-14}}{1{,}8 \times 10^{-5}} \;=\; 5{,}6 \times 10^{-10}. \]
Esempi analoghi sono il cloruro di metilammonio (CH₃NH₃Cl) e il nitrato di anilinio; il tratto comune è un catione che rilascia protoni all’acqua.
Per sali derivanti da acidi deboli e basi deboli, sia il catione sia l’anione idrolizzano. La direzione del pH dipende dal confronto tra \( K_a \) del catione e \( K_b \) dell’anione. Un esempio è il fluoruro di ammonio, \(\text{NH}_4\text{F}\): \(\text{NH}_4^+\) tende ad acidificare, \(\text{F}^-\) a basificare:
- se \( K_a(\text{catione}) > K_b(\text{anione}) \) → soluzione acida;
- se \( K_a(\text{catione}) < K_b(\text{anione}) \) → soluzione basica;
- se \( K_a(\text{catione}) \approx K_b(\text{anione}) \) → pH prossimo a 7.
Un’espressione utile (validità a diluizione moderata) è: \[ \text{pH} \;\approx\; 7 \;+\; \tfrac{1}{2}\bigl(\text{p}K_a(\text{acido debole}) - \text{p}K_b(\text{base debole})\bigr), \] che discende dalla combinazione degli equilibri di idrolisi con \( K_w \).
- scrivere la dissociazione del sale e identificare lo ione potenzialmente idrolizzabile;
- scrivere l’equilibrio di idrolisi pertinente e la costante (\( K_a \) o \( K_b \)), usando \( K_b = K_w/K_a \) o \( K_a = K_w/K_b \) quando serve;
- impostare il bilancio di materia con una tabella ICE e risolvere l’equilibrio, verificando le approssimazioni rispetto a \( K \);
- calcolare \( \text{[H}^+\text{]} \) o \( \text{[OH}^-\text{]} \) e ricavare il pH, ricordando che \( \text{pH} + \text{pOH} = 14{,}00 \) a 25 °C.
Questa procedura ricalca i metodi impiegati per acidi e basi deboli e utilizza le stesse relazioni di equilibrio, con l’avvertenza di considerare la forza ionica quando le concentrazioni non sono molto diluite.
Quando un sale deriva dalla combinazione di una base debole con un acido debole, entrambi gli ioni, il catione e l’anione, tendono a idrolizzarsi in acqua. Il valore del pH non è fissato a priori, ma riflette la competizione tra le due idrolisi e dunque la forza relativa della base e dell’acido coniugati. Poiché la trattazione esatta richiede la risoluzione simultanea di più equilibri, risulta spesso conveniente basarsi su criteri qualitativi robusti, di seguito sintetizzati:
- se l’anione deriva da un acido più debole rispetto alla base coniugata del catione (cioè se \(K_b(\text{anione}) > K_a(\text{catione})\)), l’idrolisi dell’anione è predominante e la soluzione risulta basica, con eccesso di \(\text{OH}^-\);
- se l’acidità del catione è relativamente maggiore (\(K_b(\text{anione}) < K_a(\text{catione})\)), prevale l’idrolisi del catione e la soluzione è acida, con eccesso di \(\text{H}_3\text{O}^+\);
- quando le propensioni all’idrolisi sono confrontabili (\(K_b(\text{anione}) \approx K_a(\text{catione})\)), il pH risulta prossimo alla neutralità, con lievi scostamenti che dipendono dalla concentrazione e dall’autoionizzazione dell’acqua.
Esempi rappresentativi di sali formati da acidi e basi entrambi deboli includono NH4F, NH4HCOO e il formiato di piridinio (C5H6N+ HCOO−), nei quali tanto NH4+ o C5H6N+ quanto F− o HCOO− sono soggetti a idrolisi.
In molte condizioni diluite, un’approssimazione utile per questi sali è:
\[ \text{pH} \approx 7 + \tfrac{1}{2}\log\!\left(\frac{K_b(\text{base debole})}{K_a(\text{acido debole})}\right), \]
dove \(K_b(\text{base debole})\) è la costante di basicità della base da cui deriva il catione (p.es. NH3 per NH4+) e \(K_a(\text{acido debole})\) è la costante di acidità dell’acido da cui proviene l’anione (p.es. HF per F−). Questa relazione, comune nei manuali di analitica quantitativa, è valida quando l’autoionizzazione dell’acqua è trascurabile e \(K_a\) e \(K_b\) non sono troppo simili.
Alcuni anioni presentano comportamento anfotero, potendo agire sia da acidi sia da basi. Un caso didatticamente importante è lo ione idrogenocarbonato, HCO3− (Tabella 05.04-01), per il quale sono accessibili entrambe le semireazioni:
\[ \text{HCO}_3^-(aq) + \text{H}_2\text{O}(l) \;\rightleftharpoons\; \text{H}_3\text{O}^+(aq) + \text{CO}_3^{2-}(aq) \qquad K_{a2} = 4{,}8 \times 10^{-11} \]
\[ \text{HCO}_3^-(aq) + \text{H}_2\text{O}(l) \;\rightleftharpoons\; \text{H}_2\text{CO}_3(aq) + \text{OH}^-(aq) \qquad K_b = \frac{K_w}{K_{a1}} = 2{,}4 \times 10^{-8} \]
Poiché per HCO3− risulta \(K_b > K_{a2}\), l’idrolisi basica è favorita: una soluzione di NaHCO3 è quindi debolmente basica. Per gli ioni anfiprotici di un acido diprotico, il pH a equilibrio si stima con buona approssimazione come media aritmetica delle prime due pKa:
\[ \text{pH} \approx \frac{\text{p}K_{a1} + \text{p}K_{a2}}{2} = \tfrac{1}{2}\text{p}K_{a1} + \tfrac{1}{2}\text{p}K_{a2}. \]
Per acidi poliprotici come l’acido fosforico, gli ioni H2PO4− e HPO42− sono entrambi anfoteri. Di conseguenza, per NaH2PO4 si impiega la media di pKa1 e pKa2, mentre per Na2HPO4 si usa la media di pKa2 e pKa3:
\[ \text{pH} \approx \frac{\text{p}K_{a2} + \text{p}K_{a3}}{2} = \tfrac{1}{2}\text{p}K_{a2} + \tfrac{1}{2}\text{p}K_{a3}. \]
Tali relazioni approssimate, ampiamente adottate nei testi di chimica generale e analitica, risultano preziose anche per stimare il punto isoelettrico degli amminoacidi.
Costanti di ionizzazione a 25 °C
| Nome dell’acido | Formula | Ka | Base coniugata | Kb |
|---|---|---|---|---|
| Acido cloridrico | HCl | Molto grande | Cl⁻ | Molto piccola |
| Acido nitrico | HNO₃ | Molto grande | NO₃⁻ | Molto piccola |
| Acido solforico | H₂SO₄ | Molto grande | HSO₄⁻ | Molto piccola |
| Acido perclorico | HClO₄ | Molto grande | ClO₄⁻ | Molto piccola |
| Ione idrossonio | H₃O⁺ | Molto grande | H₂O | Molto piccola |
| Acido ossalico | H₂C₂O₄ | 6.5 × 10⁻² | HC₂O₄⁻ | 1.5 × 10⁻¹³ |
| Acido solforoso | H₂SO₃ | 1.3 × 10⁻² | HSO₃⁻ | 7.7 × 10⁻¹³ |
| Acido ortofosforico | H₃PO₄ | 7.5 × 10⁻³ | H₂PO₄⁻ | 1.3 × 10⁻¹² |
| Acido fluoridrico | HF | 7.1 × 10⁻⁴ | F⁻ | 1.4 × 10⁻¹¹ |
| Acido acetilsalicilico (aspirina) | C₉H₈O₄ | 3.0 × 10⁻⁴ | C₉H₇O₄⁻ | 3.3 × 10⁻¹¹ |
| Acido formico | HCOOH | 1.7 × 10⁻⁴ | HCOO⁻ | 5.9 × 10⁻¹¹ |
| Acido acetico | CH₃COOH | 1.8 × 10⁻⁵ | CH₃COO⁻ | 5.6 × 10⁻¹⁰ |
| Acido carbonico | H₂CO₃ | 4.2 × 10⁻⁷ | HCO₃⁻ | 2.4 × 10⁻⁸ |
| Ione idrogenosolfito | HSO₃⁻ | 6.3 × 10⁻⁸ | SO₃²⁻ | 1.6 × 10⁻⁷ |
| Acido solfidrico | H₂S | 9.5 × 10⁻⁸ | HS⁻ | 1.1 × 10⁻⁷ |
| Ione diidrogenofosfato | H₂PO₄⁻ | 6.2 × 10⁻⁸ | HPO₄²⁻ | 1.6 × 10⁻⁷ |
| Acido lattico | C₃H₆O₃ | 1.4 × 10⁻⁴ | C₃H₅O₃⁻ | 7.1 × 10⁻¹¹ |
| Acido piruvico | C₃H₄O₃ | 3.2 × 10⁻³ | C₃H₃O₃⁻ | 3.1 × 10⁻¹² |
| Acido cianidrico | HCN | 4.9 × 10⁻¹⁰ | CN⁻ | 2.0 × 10⁻⁵ |
| Ione idrogenocarbonato | HCO₃⁻ | 4.8 × 10⁻¹¹ | CO₃²⁻ | 2.1 × 10⁻⁴ |
| Ione idrogenofosfato | HPO₄²⁻ | 4.8 × 10⁻¹³ | PO₄³⁻ | 2.1 × 10⁻² |
| Ione idrogenosolfuro | HS⁻ | 1.0 × 10⁻¹⁹ | S²⁻ | 1 × 10⁵ |
| Ione idrossido | OH⁻ | Trascurabile | O²⁻ | Molto grande |
| Tabella che riporta i valori di ionizzazione di vari acidi monoprotici e poliprotici e delle rispettive basi coniugate. | ||||
Per neutralizzazione si intende la reazione stechiometrica tra ioni idrossonio e ioni idrossido che porta alla formazione di acqua, con eventuale presenza di ioni spettatori che costituiscono il sale in soluzione. Per una coppia acido forte–base forte, entrambi completamente dissociati, l’equazione ionica netta è:
\[ \text{H}_3\text{O}^+(aq) + \text{OH}^-(aq) \;\longrightarrow\; 2\,\text{H}_2\text{O}(l). \]
Ad esempio, nella miscela HCl(aq) + NaOH(aq), gli ioni Na+ e Cl− non partecipano alla trasformazione (ioni spettatori) e rimangono invariati in soluzione. Quando le moli di \(\text{H}_3\text{O}^+\) e di \(\text{OH}^-\) sono equivalenti, si raggiunge il punto equivalente. Per acido forte e base forte, in condizioni ideali, il pH al punto equivalente è prossimo a 7; per combinazioni che coinvolgono specie deboli, invece, il pH all’equivalenza può discostarsi in modo significativo dalla neutralità per effetto dell’idrolisi del sale risultante.
Procedura per la titolazione acido–base (acido forte con base forte)
- Si trasferisce in una beuta, con pipetta tarata, un volume noto del campione acido a concentrazione incognita, ad esempio 20,00 mL;
- Si aggiunge un opportuno indicatore acidobase che vari colore in prossimità del punto equivalente; per titolazioni forte–forte sono idonei indicatori il cui intervallo di viraggio intercetta la ripida variazione di pH attorno a 7, come il blu di bromotimolo o la fenolftaleina (Figura 05.04-01);
- Si riempie una buretta con una soluzione standard di base forte, per esempio NaOH 0,2000 mol·L−1, e si eroga il titolante sotto agitazione controllando l’avanzamento del colore;
- Al punto equivalente, le moli di \(\text{OH}^-\) aggiunte eguagliano le moli iniziali di \(\text{H}_3\text{O}^+\) presenti nel campione: la soluzione risulta, idealmente, neutra (pH ≈ 7) e il viraggio dell’indicatore segnala l’endpoint sperimentale;
- Si registra con cura il volume erogato dalla buretta, ad esempio 19,85 mL, tenendo conto dell’incertezza di lettura (tipicamente ±0,05 mL);
- La concentrazione dell’acido si calcola per via stechiometrica dai volumi misurati e dalla molarità del titolante. In presenza di reazioni 1:1 (H+ : OH−), vale \(C_\text{acido} = C_\text{base}\,V_\text{base}/V_\text{acido}\), con volumi espressi in unità coerenti.
È buona pratica impiegare una base standardizzata con uno standard primario e distinguere tra punto equivalente (condizione stechiometrica) ed endpoint (segnale dell’indicatore), minimizzando l’errore di titolazione con una scelta oculata dell’indicatore e una corretta tecnica operativa.
La definizione di Brønsted–Lowry interpreta le basi come accettori di protoni e gli acidi come donatori di protoni. Tale prospettiva, pur efficace, non abbraccia tutte le interazioni acidobase. La formulazione di G. N. Lewis amplia il quadro identificando come base una specie che dona una coppia di elettroni e come acido una specie che accetta una coppia di elettroni: ogni reazione acidobase di Lewis coincide quindi con la formazione di un nuovo legame coordinativo tramite condivisione di una coppia elettronica.
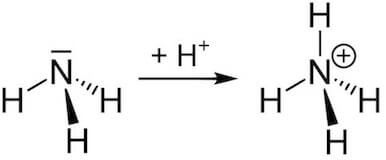 |
| Protonazione dell’ammoniaca. |
Nella protonazione di NH3, l’azoto offre la sua coppia non condivisa al protone: NH3 agisce da base di Lewis e H+ è un acido di Lewis. In generale, ogni acido di Brønsted è anche un acido di Lewis perché il protone accetta una coppia elettronica dal partner basico.
La forza della definizione di Lewis emerge in reazioni prive di trasferimento di H+. Un esempio paradigmatico è l’addotto tra BF3, che possiede un orbitale vuoto sul boro, e l’ammoniaca, donatrice di coppia elettronica:
 |
| Risonanza del benzene e lunghezze di legame. |
In questo caso BF3 è un acido di Lewis e si forma un legame dativo B–N. In modo analogo, molti cationi metallici, in particolare di metalli di transizione con orbitali d disponibili, si comportano da acidi di Lewis coordinandosi a basi di Lewis (leganti) neutre o anioniche. Un classico equilibrio di complessazione è:
\[ \text{Ag}^+(aq) + 2\,\text{NH}_3(aq) \;\rightleftharpoons\; [\text{Ag}(\text{NH}_3)_2]^+(aq), \]
dove NH3 è base di Lewis e Ag+ è acido di Lewis. Molti catalizzatori in sintesi organica sono acidi di Lewis, come AlCl3, che attiva substrati elettrofili favorendo la formazione di complessi reattivi. Questi concetti, consolidati nei manuali universitari di chimica inorganica e organica, consentono di interpretare in modo unitario reattività e catalisi anche in assenza di protoni.








