Radioattività
Definizione
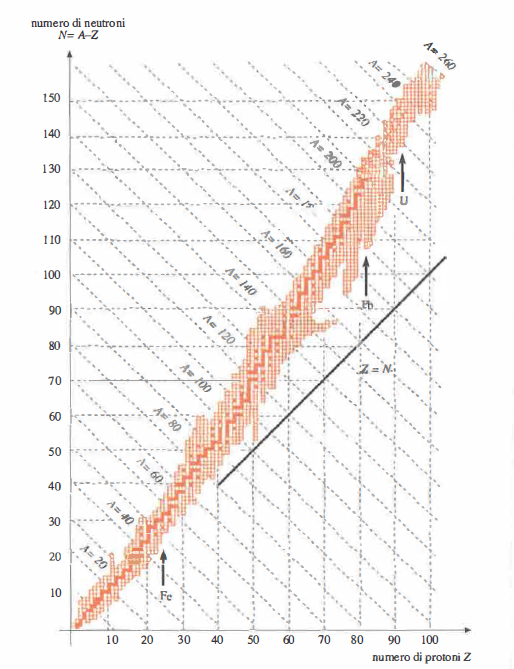
Nel nucleo atomico coesistono due interazioni di natura diversa: l’attrazione a corto raggio dovuta alla forza nucleare forte, che lega tra loro nucleoni (protoni e neutroni), e la repulsione coulombiana tra protoni, che cresce con il numero atomico Z. All’aumentare di Z, la repulsione elettrica diviene preponderante su scale nucleari sempre più ampie; la stabilità è allora garantita solo da un eccesso relativo di neutroni, i quali contribuiscono al legame senza introdurre repulsione elettrica. Se si rappresentano tutti i nuclidi nel piano numero atomico Z–numero di neutroni N, si ottiene l’andamento mostrato in (Figura 07.16-01): la “striscia di stabilità” devia progressivamente dalla bisettrice N = Z e presenta una pendenza maggiore di 1, evidenziando che per valori elevati di Z sono necessari più neutroni per mantenere il nucleo legato.
La posizione di un nuclide rispetto alla striscia di stabilità è indicativa del suo comportamento: un difetto di neutroni rispetto ai protoni (nuclidi proton-ricchi) o, al contrario, un eccesso di neutroni (nuclidi neutron-ricchi) rende il nucleo instabile. Un neutrone libero, per esempio, non è stabile e si trasforma secondo \(n \rightarrow p + e^- + \bar{\nu}_e\), emettendo un elettrone e un antineutrino elettronico. L’instabilità nucleare si manifesta mediante trasformazioni spontanee, spesso attraverso più stadi successivi, verso configurazioni più legate. Tali trasformazioni prendono il nome di decadimenti o disintegrazioni radioattive.
Nel dominio dei nuclei pesanti, la repulsione coulombiana diviene così intensa da non poter più essere compensata neppure da un ulteriore aumento di neutroni: nessun isotopo con Z > 92 è stabile in senso rigoroso. Più in generale, gli elementi oltre il piombo non possiedono isotopi stabili; quelli presenti in natura sono a vita lunga e appartengono a catene di decadimento di nuclidi primordiali. La (Figura 07.16-01) riassume questo quadro: la stabilità è confinata in una regione ristretta del piano N–Z, mentre al di fuori di essa i nuclidi tendono a trasformarsi fino a raggiungere nuclei più stabili.
Le principali modalità di decadimento e le loro conseguenze su numero di massa A e numero atomico Z sono:
- decadimento α: emissione di un nucleo di elio \(^{4}\mathrm{He}\) (2 protoni e 2 neutroni); comporta \(A \rightarrow A-4\) e \(Z \rightarrow Z-2\);
- decadimento β⁻: un neutrone si converte in protone con emissione di elettrone \(e^-\) e antineutrino \(\bar{\nu}_e\); implica \(Z \rightarrow Z+1\) e \(A\) invariato;
- decadimento β⁺ (o cattura elettronica EC): un protone si trasforma in neutrone con emissione di positrone \(e^+\) e neutrino \(\nu_e\), oppure mediante cattura di un elettrone atomico; comporta \(Z \rightarrow Z-1\) e \(A\) invariato;
- emissione γ: rilassamento del nucleo da uno stato eccitato con emissione di fotoni ad alta energia; non modifica né A né Z;
- emissione di neutroni: espulsione di uno o più neutroni, tipica di nuclei fortemente eccitati o molto neutron-ricchi; produce \(A \rightarrow A-1\) (o meno uno per ciascun neutrone emesso) con Z costante.
Queste trasformazioni obbediscono alla conservazione della carica elettrica, del numero barionico e dell’energia. In termini energetici, il decadimento avviene quando la differenza di massa tra stato iniziale e finale, via \(E = \Delta m\,c^2\), consente l’emissione delle particelle e della radiazione.
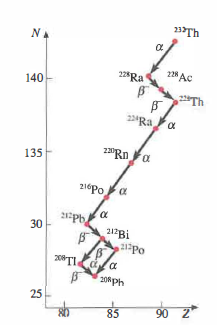
Un esempio significativo è la serie di decadimenti del torio \(^{232}\mathrm{Th}\), che procede attraverso molte tappe con emissioni α e β fino a raggiungere un nuclide stabile; la successione è illustrata in (Figura 07.16-02). In tali catene, ogni stadio ridisegna il bilancio tra N e Z, avvicinando progressivamente il nucleo alla regione di stabilità.
Tutti gli elementi presenti sulla Terra contengono, in tracce, isotopi radioattivi che producono un fondo continuo di radiazioni naturali. A questo contributo si sommano le radiazioni cosmiche, composte da particelle e fotoni di elevata energia provenienti dallo spazio. Alcuni radionuclidi naturali vengono incessantemente rigenerati dall’interazione della radiazione cosmica con l’atmosfera e la litosfera, sostenendo cicli di produzione e decadimento. La parte prevalente della radioattività naturale, tuttavia, deriva da radionuclidi primordiali ancora presenti fin dalla formazione della Terra, quali l’uranio \(^{238}\mathrm{U}\) e \(^{235}\mathrm{U}\), il torio \(^{232}\mathrm{Th}\) e il potassio \(^{40}\mathrm{K}\), insieme ai loro prodotti di decadimento.
La radioattività artificiale nasce invece da processi nucleari indotti dall’attività umana. Radionuclidi possono essere generati in reazioni nei reattori nucleari, durante esplosioni nucleari o tramite fasci di particelle prodotti da acceleratori. Queste tecnologie consentono, tra l’altro, la sintesi di radioisotopi utilizzati come traccianti e per scopi terapeutici in medicina nucleare, oltre che per applicazioni industriali e di ricerca.