Proprietà delle soluzioni
Definizione
Una soluzione liquida è un sistema monofasico e omogeneo, otticamente trasparente, nel quale le entità del soluto sono disperse a livello molecolare o ionico nel solvente. Il termine “limpido” indica l’assenza di una seconda fase visibile o di torbidità, mentre “incolore” segnala soltanto l’assenza di assorbimento nel visibile; di conseguenza, una soluzione può essere limpida e al tempo stesso colorata, a seconda della natura delle specie disciolte.
Quando il soluto genera ioni in soluzione, si ottiene una soluzione elettrolitica, capace di condurre la corrente elettrica. Gli elettroliti forti (per esempio molti sali in acqua) sono completamente dissociati, mentre gli elettroliti deboli (per esempio alcuni acidi e basi deboli) sono solo parzialmente ionizzati. Un sale come il bromuro di potassio, a contatto con acqua, dà luogo alla formazione di ioni idratati secondo la schematizzazione: \[ \mathrm{KBr(s)} \xrightarrow{\mathrm{H_2O}} \mathrm{K^+(aq)} + \mathrm{Br^-(aq)}. \] La conducibilità specifica cresce con la concentrazione ionica e con la mobilità degli ioni, ed è una misura sperimentale diretta della presenza di specie cariche in soluzione.
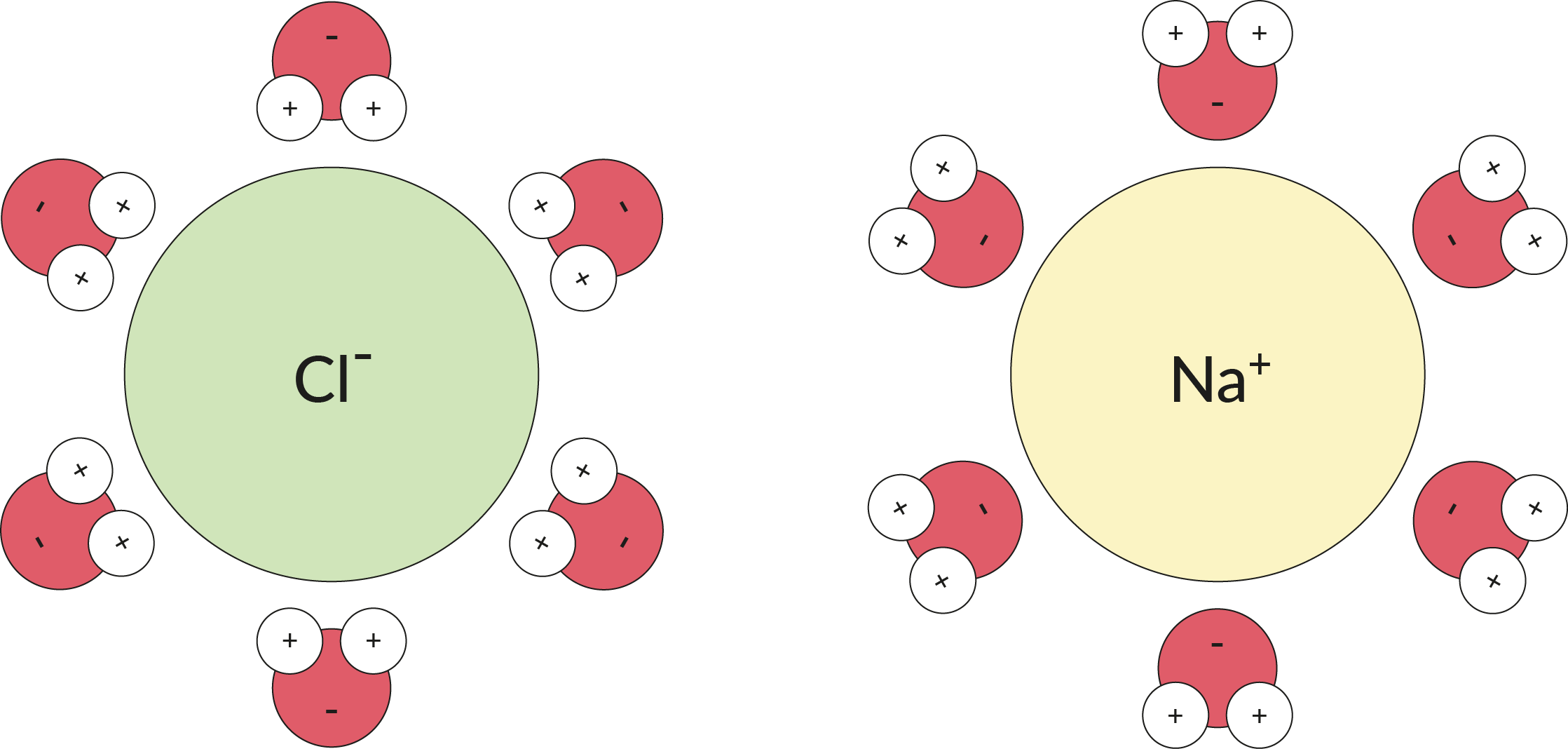 |
| Idratazione ionica di Na+ e Cl− : interazioni ione-dipolo con le molecole d’acqua. |
Al contrario, una soluzione non elettrolitica contiene soluti molecolari che non danno ioni in soluzione e, pertanto, non conducono la corrente elettrica in modo apprezzabile. Un esempio tipico è la dissoluzione del saccarosio: \[ \mathrm{C_{12}H_{22}O_{11}(s)} \xrightarrow{\mathrm{H_2O}} \mathrm{C_{12}H_{22}O_{11}(aq)}, \] in cui le molecole restano integre e sono solvatare senza dissociarsi.
Dal punto di vista macroscopico, le soluzioni liquide presentano alcune proprietà distintive:
- omogeneità su scala ottica, con composizione uniforme in ogni porzione del volume;
- impossibilità di separare soluto e solvente per semplice filtrazione, poiché le dimensioni delle particelle disperse sono confrontabili con quelle del solvente e attraversano il mezzo poroso;
- assenza di sedimentazione del soluto nel tempo, grazie alla diffusione termica e al moto browniano che mantengono una distribuzione casuale e stabile;
- trasparenza alla luce in assenza di specie assorbenti nel visibile; quando il soluto assorbe, la soluzione appare colorata senza perdere limpidezza.
Il volume di una soluzione non è, in generale, la somma dei volumi dei componenti puri. La mescolanza induce nuove interazioni tra molecole di solvente e di soluto (legami a idrogeno, interazioni dipolari, dispersione), che portano a contrazione o a lieve espansione del volume. Una descrizione quantitativa si ottiene tramite i volumi parziali molari: il volume totale è \[ V = \sum_i \bar V_i\, n_i, \] dove \(\bar V_i\) è il volume parziale molare del componente \(i\) e \(n_i\) la sua quantità di sostanza. Un esempio concreto è l’unione di etanolo e acqua: miscelando 50,0 mL di etanolo con 50,0 mL di acqua si osserva un volume finale inferiore a 100,0 mL per contrazione, dovuta al miglior impacchettamento molecolare e alla ristrutturazione della rete di legami a idrogeno.
Un liquido trasparente in un becher può essere una sostanza pura, una soluzione vera o un sistema colloidale. Solo un’analisi chimica stabilisce con certezza se è presente un unico componente (ad esempio acqua bidistillata) oppure una miscela. Nelle soluzioni, le specie disperse sono molecole o ioni di dimensioni inferiori alla scala colloidale e hanno distribuzione completamente uniforme; i colloidi sono dispersioni finemente suddivise ma non perfettamente omogenee su scala nanometrica.
La classificazione dimensionale è utile per distinguere i sistemi:
- soluzioni vere: particelle disperse con diametro minore di \(1 \times 10^{-9}\) m (1 nm), completamente trasparenti e non separabili per filtrazione ordinaria;
- colloidi: particelle con diametro compreso tra \(1 \times 10^{-9}\) m e \(2 \times 10^{-7}\) m (1–200 nm), come sol, gel ed emulsioni, stabili per effetto del moto browniano e/o di repulsioni elettrostatiche;
- sospensioni: particelle con dimensioni superiori a \(2 \times 10^{-7}\) m, che nel tempo sedimentano formando una fase solida distinta.
Soluzioni e colloidi possono apparire simili a occhio nudo, ma differiscono per l’interazione con la luce. Le particelle colloidali sono sufficientemente grandi da diffondere la radiazione incidente, rendendo il mezzo opalescente: è il cosiddetto effetto Tyndall. La diffusione dei raggi solari nella nebbia, costituita da microgocce d’acqua disperse nell’aria, ne è un esempio comune; la foschia è la luce diffusa da tali goccioline. Le soluzioni, contenendo specie troppo piccole per disperdere la luce in modo significativo, non mostrano questo fenomeno e restano otticamente limpide. L’osservazione delle proprietà di scattering permette quindi di distinguere facilmente una soluzione da una sospensione colloidale (Figura 03.01-01).
Le sospensioni sono miscele eterogenee instabili: le particelle, molto più grandi di quelle colloidali, tendono a depositarsi per gravità generando un precipitato in contatto con il liquido soprastante. Un esempio è una dispersione di particelle di argilla in acqua, che necessita di agitazione continua per rimanere apparentemente uniforme.
La capacità di un soluto di disperdersi in un solvente dipende in larga misura dalla compatibilità delle loro interazioni intermolecolari: specie chimiche con caratteristiche elettroniche e strutturali affini mostrano tendenzialmente una maggiore miscibilità. La struttura molecolare, la presenza di gruppi polari o funzionali in grado di formare legami a idrogeno e il “contesto” del solvente (costante dielettrica, polarizzabilità) consentono una previsione qualitativa. Il grado di solubilità, cioè la quantità massima di soluto che può essere presente in una data quantità di solvente a una temperatura specificata, fornisce invece una misura quantitativa e dipende da diversi fattori:
- Differenza di polarità tra soluto e solvente, e natura delle interazioni specifiche (legami a idrogeno, interazioni ione–dipolo, forze di dispersione): maggiore è la dissimilarità, minore è la solubilità attesa;
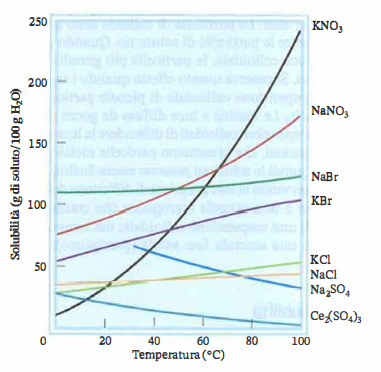
- Temperatura: l’incremento di temperatura spesso, ma non universalmente, accresce la solubilità dei solidi in liquidi (Figura 03.01-02), con effetti talvolta marcati. Per esempio, la solubilità del KCl in acqua aumenta sensibilmente scaldando la soluzione, passando da valori dell’ordine di qualche decina di grammi per 100 g di acqua a 0 °C a valori prossimi al raddoppio a 100 °C;
- Pressione: per solidi e liquidi disciolti in liquidi l’effetto della pressione è generalmente modesto, mentre per i gas la solubilità cresce in modo direttamente proporzionale alla pressione parziale del gas sopra il liquido, principio sfruttato nella produzione di bevande effervescenti confezionate sotto anidride carbonica a pressione elevata.
Una soluzione che contiene la massima quantità di soluto compatibile con l’equilibrio a una data temperatura è detta satura. I valori tabulati di solubilità (ad esempio, grammi di soluto per 100 g o 100 mL di solvente) corrispondono alla concentrazione della soluzione satura a quella temperatura. Scaldando una soluzione satura di un solido, la quantità di soluto che può rimanere in soluzione in un dato volume di solvente in genere aumenta; raffreddando, la solubilità spesso diminuisce e l’eccesso di soluto tende a separarsi come precipitato.
In alcune circostanze, dopo un raffreddamento delicato o in assenza di siti di nucleazione, l’eccesso può rimanere temporaneamente in soluzione: si formano così soluzioni sovrasature, metastabili e sensibili a perturbazioni meccaniche o all’aggiunta di un “cristallo seme”; una lieve sollecitazione fa precipitare rapidamente il soluto in eccesso fino al ripristino della condizione satura stabile.
Se si introduce un eccesso di solido in un solvente, ha luogo inizialmente una rapida dissoluzione. Con il tempo, cresce anche la velocità del processo inverso, la ricristallizzazione dalla soluzione. Quando la velocità di dissoluzione e quella di precipitazione si eguagliano, si stabilisce un equilibrio dinamico: la composizione della soluzione non varia più nel tempo, pur perdurando un continuo scambio di particelle tra fase solida e fase liquida. Questa condizione definisce in modo rigoroso la soluzione satura, ossia una soluzione in equilibrio dinamico con il soluto non disciolto.
Dal punto di vista cinetico, al saldo nullo tra i flussi corrisponde \( r_{\text{diss}} = r_{\text{prec}} \). Per elettroliti debolmente solubili, l’equilibrio può essere rappresentato come dissociazione del solido in ioni in soluzione e descritto tramite il prodotto di solubilità \(K_s\); per soluti molecolari prevalgono invece interazioni specifiche con il solvente. Agitazione, frantumazione del solido o variazioni della superficie esposta accelerano l’avvicinamento all’equilibrio ma non ne modificano il valore finale a temperatura e pressione fissate.
La solubilità dei gas in liquidi, a temperatura costante e per soluzioni diluite, è regolata dalla legge di Henry, che stabilisce la proporzionalità tra la concentrazione di equilibrio del gas disciolto e la sua pressione parziale nella fase gassosa in contatto con il liquido:
\( c = k_H \, p \)
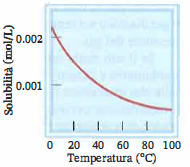
dove \( c \) è la concentrazione molare del gas nel liquido, \( p \) la pressione parziale del gas e \( k_H \) la costante di Henry (dipendente dalla coppia gas–solvente e dalla temperatura). In formulazione alternativa si usa la frazione molare \( x \): \( p = H \, x \), con \( H \) costante di Henry espressa in unità diverse. Per molti sistemi, \( k_H \) diminuisce al diminuire della temperatura, riflettendo l’aumento di solubilità dei gas a freddo (Figura 03.01-03).
Un esempio numerico illustra l’uso della legge: alla temperatura di 25 °C, per l’anidride carbonica in acqua si può assumere \( k_H \approx 3{,}3 \times 10^{-2} \,\text{mol·L}^{-1}\text{·atm}^{-1} \). In una bevanda confezionata sotto \( p = 4{,}0 \) atm di CO₂, la concentrazione di equilibrio è \( c \approx 0{,}13 \) mol·L⁻¹. All’apertura, la pressione parziale del gas scende rapidamente verso il valore atmosferico, il nuovo equilibrio richiede una concentrazione molto più bassa e l’eccesso di CO₂ esce dalla soluzione formando bolle.
L’influenza della temperatura è cruciale nelle applicazioni fisiologiche. Negli alveoli polmonari, dove il sangue scorre a temperatura pressoché costante, le concentrazioni di equilibrio di ossigeno e anidride carbonica sono determinate dalle rispettive pressioni parziali dell’aria alveolare secondo la legge di Henry, mentre il trasporto e il consumo metabolico mantengono il gradiente necessario allo scambio. Il rapido raggiungimento dell’equilibrio tra aria e sangue capillare assicura un’efficiente ossigenazione e la rimozione della CO₂ prodotta dai tessuti.
In sintesi, la pressione governa in modo diretto la quantità di gas disciolta, la temperatura ne modula sensibilmente il valore di equilibrio e le interazioni specifiche gas–solvente determinano la costante di Henry per ogni sistema.