Programmi di espressione genica differenziata portano alla formazione di tipologie cellulari diverse in un organismo pluricellulare
Definizione
I filamenti di actina sono presenti in tutte le cellule eucariotiche e costituiscono l’ossatura dinamica di numerose attività che coinvolgono la superficie cellulare. La loro funzione è imprescindibile per processi come la migrazione su substrati, l’inglobamento di particelle voluminose mediante fagocitosi e la separazione della cellula in due durante la citocinesi. Benché singolarmente instabili, i filamenti di actina acquistano stabilità e organizzazione quando interagiscono con specifiche proteine leganti l’actina, dando origine a strutture durature quali l’apparato contrattile muscolare.
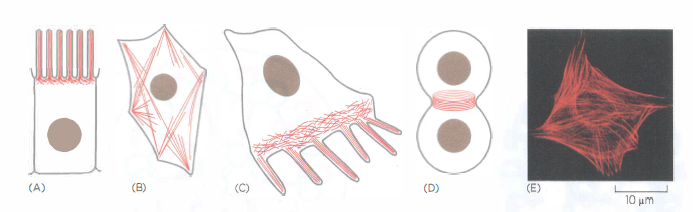
In base al repertorio di proteine associate, i filamenti di actina si organizzano in architetture distinte: strutture rigide e relativamente stabili, come i microvilli dell’orletto a spazzola dell’epitelio intestinale (Figura 05.29-01); fasci contrattili citoplasmatici che operano come “unità muscolari” intracellulari (Figura 05.29-01); strutture transitorie e altamente dinamiche, ad esempio le protrusioni al margine anteriore di un fibroblasto in migrazione (Figura 05.29-01) o l’anello contrattile che, nelle cellule animali, innesca la strozzatura alla fine della mitosi (Figura 05.29-01).
La maggior parte dei movimenti dipendenti dall’actina emerge dall’interazione con proteine motrici della famiglia della miosina. Sebbene actina e tubulina siano proteine differenti, condividono principi generali di assemblaggio e disassemblaggio e, in collaborazione con le rispettive proteine motrici, generano forze e rimodellamenti strutturali con logiche sorprendentemente affini. Tali processi sono integrati con l’adesione al substrato e con segnali molecolari che convergono sui regolatori dell’actina (ad esempio GTPasi della famiglia Rho), modulando la topologia del citoscheletro in tempo e spazio.
Al microscopio elettronico i filamenti di actina (F-actina) appaiono come sottili corde di circa 7 nm di diametro, costituite da una doppia elica di monomeri di actina globulare (G-actina) identici e orientati in modo uniforme lungo l’asse del polimero. Tale orientazione conferisce al filamento una polarità intrinseca, distinguendo un’estremità “barbuta” o più (+) da un’estremità “appuntita” o meno (−) (Figura 05.29-02). Questa polarità è funzionalmente cruciale per le cinetiche di crescita e di motilità dipendente da miosina.
Rispetto ai microtubuli, i filamenti di actina sono più sottili, più flessibili e normalmente più corti; sono tuttavia molto più numerosi, cosicché la somma delle loro lunghezze all’interno di una cellula supera ampiamente quella dei microtubuli. Raramente si presentano isolati: proteine impalcatura e di collegamento li organizzano in fasci paralleli o in reti ramificate, che conferiscono al citoplasma periferico una resistenza meccanica e una plasticità superiori a quelle dei singoli filamenti. Parametri fisici come la lunghezza di persistenza, dell’ordine di pochi micrometri per l’actina, aiutano a spiegare la facilità con cui questi polimeri si incurvano e si adattano a geometrie cellulari complesse.
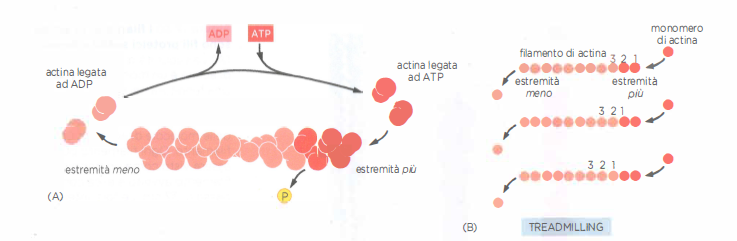
L’assemblaggio dell’actina presenta tre fasi concettuali, analoghe a quelle osservate per la tubulina: nucleazione, allungamento e stato stazionario. I monomeri di actina liberi si associano preferenzialmente in forma legata ad ATP e si aggiungono a entrambe le estremità del filamento, con una velocità maggiore all’estremità più. Subito dopo l’incorporazione, l’ATP viene idrolizzato ad ADP con rilascio ritardato di Pi, evento che riduce l’affinità tra subunità e tende a destabilizzare il polimero, come avviene per l’idrolisi del GTP nei microtubuli.
La dinamica di crescita a ciascuna estremità i può essere descritta da: \[ v_i = k_{\mathrm{on},i}\,C - k_{\mathrm{off},i}, \] dove C è la concentrazione di G-actina disponibile, mentre \(k_{\mathrm{on},i}\) e \(k_{\mathrm{off},i}\) sono le costanti di associazione e dissociazione specifiche per l’estremità. Ne deriva una concentrazione critica \(C_{c,i} = k_{\mathrm{off},i}/k_{\mathrm{on},i}\). Poiché in genere \(C_{c,+} < C_{c,-}\), esiste un intervallo di concentrazioni \[ C_{c,+} < C < C_{c,-} \] in cui il filamento cresce al polo più e si accorcia al polo meno, mantenendo lunghezza media costante: è il treadmilling. In termini qualitativi, le subunità “fluiscono” lungo il filamento dalla estremità più verso quella meno (Figura 05.29-03).
Il modello del “cappuccio ATP” spiega la stabilità relativa della regione terminale ricca di ATP/ADP·Pi, che contrasta la perdita di subunità; quando il cappuccio si riduce o scompare, prevalgono eventi di depolimerizzazione. La cellula sfrutta questa labilità per rimodellare rapidamente il citoscheletro: un aumento locale di C, o l’attivazione di nucleatori, produce espansione di reti e fasci; la prevalenza di actina-ADP e di proteine che favoriscono la dissociazione promuove il disassemblaggio.
Piccole molecole naturali modulano potentemente queste dinamiche (Tabella 05.29-01). Esempi rilevanti comprendono:
- citocalasine, che cappano l’estremità più inibendo l’ulteriore allungamento e inducendo accorciamento del filamento;
- latrunculine, che sequestrano la G-actina diminuendo la concentrazione libera disponibile e bloccando la polimerizzazione;
- falloidina, che si lega all’F-actina stabilizzandola e ostacolando la depolimerizzazione.
L’esposizione anche a basse concentrazioni di tali composti arresta rapidamente fenomeni dipendenti dall’actina, come protrusioni lamellipodiali e migrazione cellulare, a testimonianza di quanto l’equilibrio tra assemblaggio e disassemblaggio sia essenziale per la funzione.
| Sostanza | Effetto sui filamenti di actina |
|---|---|
| Falloidina | Si lega ai filamenti di actina stabilizzandoli e prevenendone la depolimerizzazione |
| Citochalasin | Blocca l’estremità positiva dei filamenti, impedendo l’allungamento e quindi la polimerizzazione |
| Latrunculina | Si lega ai monomeri di actina sequestrandoli e inibendo la formazione di nuovi filamenti |
Sostanze che influenzano i filamenti di actina
Alcuni composti naturali modulano la dinamica dei microfilamenti di actina. Stabilizzando o impedendo la polimerizzazione, queste sostanze interferiscono con processi cellulari fondamentali come migrazione, divisione e mantenimento della forma cellulare. Per questo motivo sono utilizzate sia in ricerca sia in applicazioni terapeutiche sperimentali.
Nelle cellule animali l’actina rappresenta circa il 5 % delle proteine totali; approssimativamente metà si trova come filamenti e metà come monomeri citosolici. Tale quota monomerica, pur superiore alla concentrazione critica misurata in vitro, non polimerizza indiscriminatamente grazie a proteine regolatrici che fissano i monomeri o ne controllano l’accesso alle estremità dei filamenti.
Tra i principali modulatori:
- proteine che sequestrano o “precaricano” i monomeri, come timosina β4 (sequestro) e profilina (favorisce lo scambio ADP→ATP e la consegna selettiva all’estremità più);
- nucleatori, tra cui il complesso ARP (Actin-Related Protein) che genera reti ramificate con angoli caratteristici e le formine che avviano fasci lineari e promuovono l’allungamento processivo delle estremità più;
- proteine impalcatura e di crosslinking, come fimbrina e villina nei fasci serrati dei microvilli, α-actinina nei fasci contrattili, filamina e spettina nel cortex dove creano reticoli a gel sotto la membrana plasmatica;
- fattori di capping, ad esempio CapZ all’estremità più e tropomodulina all’estremità meno, che stabilizzano la lunghezza dei filamenti;
- proteine di frammentazione e depolimerizzazione, come cofilina e gelsolina, capaci di tagliare l’F-actina e favorire il turnover, convertendo strutture simili a gel in stati più fluidi;
- adattatori membranali, inclusi i membri della famiglia ERM (ezrina, radixina, moesina), che connettono l’actina corticale alle proteine transmembrana e ne trasmettono le tensioni;
- miosine, con ruoli motori e di trasporto: miosina II genera contrazione in fasci antiparalleli (come nell’anello contrattile), mentre miosine I e V partecipano al traffico di vescicole e all’organizzazione della membrana; nelle cellule vegetali le miosine ad alta processività sostengono movimenti di organuli lungo actina, con valore preminente rispetto ai microtubuli.
Attraverso combinazioni diverse di queste attività, l’actina costruisce dispositivi cellulari emblematici. Esempi includono i microvilli intestinali (Figura 05.29-01), sostenuti da fasci paralleli stabilizzati e collegati alla membrana; i fasci contrattili citoplasmatici (Figura 05.29-01), in cui filamenti antiparalleli scivolano l’uno sull’altro per azione di miosina II; le protrusioni dinamiche della periferia cellulare (Figura 05.29-01), generate da nucleazione ramificata e rapido turnover; l’anello contrattile (Figura 05.29-01), che stringe l’istmo citoplasmatico nella citocinesi. Nel loro insieme, cortex e fasci actinici determinano la meccanica della cellula, regolando tensione, elasticità e capacità di generare forza utile al movimento e alla divisione.
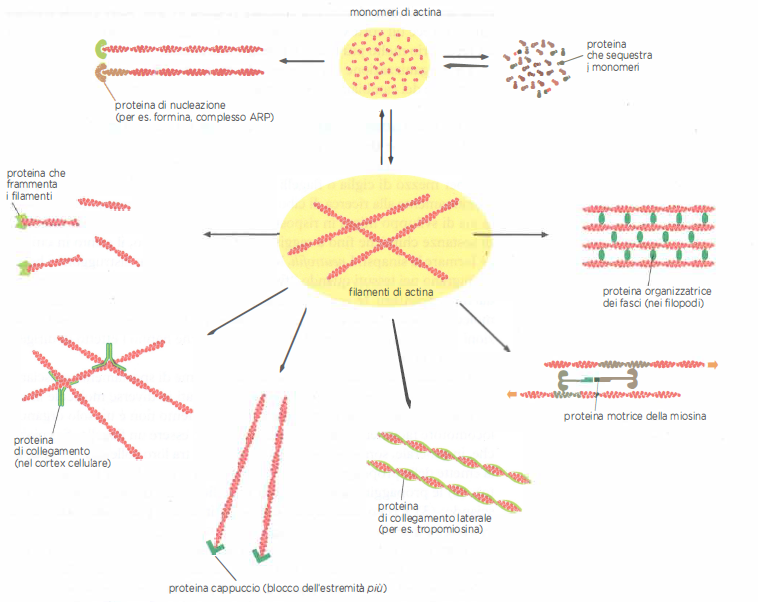
La riorganizzazione spaziale e temporale di tali strutture dipende dall’integrazione tra concentrazione locale di monomeri, stato del nucleotide, attività dei nucleatori e azione coordinata di proteine di capping, crosslinking e frammentazione (Figura 05.29-04). Questo controllo multilivello consente all’actina di funzionare sia come materiale strutturale sia come substrato dinamico per le proteine motrici, dall’orlo corticale coinvolto nella locomozione al sistema contrattilo delle cellule muscolari.
L’actina è ubiquitaria nel citoplasma delle cellule eucariotiche, ma raggiunge la massima concentrazione in un sottile strato immediatamente al di sotto della membrana plasmatica, il cortex cellulare. In questa regione i filamenti di actina, connessi a proteine di legame e a fattori di cross-linking, costituiscono una maglia elastica che stabilizza la superficie cellulare, contribuisce alla tensione corticale e fornisce resistenza alle deformazioni. Negli eritrociti, la tipica morfologia a disco biconcavo si mantiene grazie a una rete altamente ordinata di actina e spectrina, ancorata alla membrana mediante complessi proteici specifici; tale architettura garantisce robustezza meccanica con costi energetici minimi. In molte altre cellule animali il cortex è più spesso e composito, arricchito da proteine che collegano il citoscheletro alla membrana (ad esempio i fattori ERM), consentendo una gamma più ampia di forme e una risposta dinamica alle forze esterne. La riorganizzazione rapida dei filamenti corticali è il principio molecolare che sottende i cambiamenti di forma, l’endocitosi dipendente dalla tensione di membrana e la locomozione.
Molte cellule eucariotiche si spostano aderendo e scivolando su un substrato, piuttosto che nuotare mediante ciglia o flagelli. Esempi comprendono ameboidi predatori che inseguono particelle di cibo, coni di crescita assonali che seguono gradienti di fattori guida e leucociti che rispondono a segnali chemiotattici rilasciati da patogeni. Nei neutrofili, per esempio, il riconoscimento di chemiotattivi da parte di recettori di superficie innesca circuiti di segnalazione che modulano localmente l’assemblaggio dei filamenti di actina, polarizzando la cellula verso la sorgente del segnale.
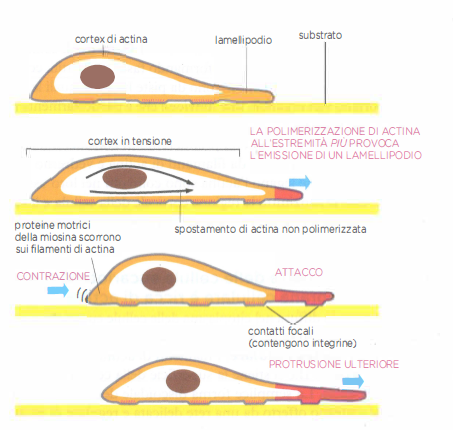
La locomozione per strisciamento non dipende da un unico organello motile, ma emerge dal coordinamento spaziale e temporale di processi distribuiti. In termini generali, tre eventi interconnessi sono indispensabili (Figura 05.29-05):
- protrusione del bordo anteriore (margine guida), mediante estroflessioni di membrana sostenute da polimerizzazione di actina;
- formazione di adesioni transitorie al substrato, che “agganciano” le protrusioni alla superficie;
- trazione del corpo cellulare e rilascio del bordo posteriore, così che la cellula avanzi in modo coordinato.
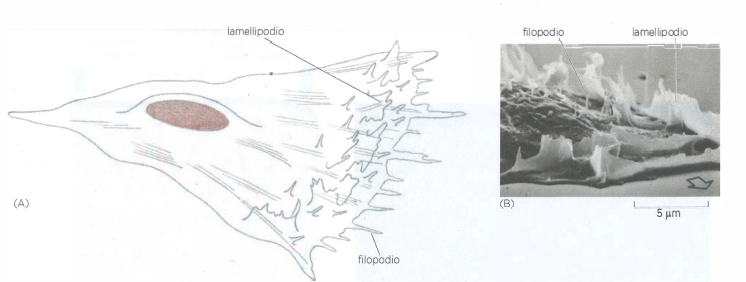
La protrusione del margine guida è alimentata dalla crescita dei filamenti di actina verso la membrana. Nei fibroblasti in coltura si osservano lamellipodi, sottili ventagli ricchi di una rete densa e ramificata di actina, con le estremità “barbed” orientate verso la membrana. Molte cellule emettono anche filopodi, prolungamenti sottili e rigidi (spessore circa 0,1 μm; lunghezza tipica 5–10 μm) formati da fasci lassi di 10–20 filamenti disposti con le estremità in crescita rivolte verso l’esterno (Figura 05.29-01). Nel cono di crescita assonale i filopodi possono estendersi fino a 50 μm, favorendo l’esplorazione dell’ambiente. Lamellipodi e filopodi sono altamente dinamici: si formano e si ritirano con velocità dell’ordine di 1 μm/s, grazie a un rapido turnover dell’actina e a un meccanismo di “cricchetto browniano” che converte la polimerizzazione in spinta meccanica.
Quando una protrusione incontra un substrato idoneo, avviene l’aderenza mediata da integrine: tali recettori transmembrana si legano a componenti della matrice extracellulare o a molecole sulla superficie di cellule adiacenti e, sul versante citoplasmatico, reclutano complessi adattatori (ad esempio talina, kindlin, vinculina) che connettono l’actina alle adesioni nascenti (Figura 05.29-05). L’ancoraggio così generato funge da “frizione molecolare” che trasforma il flusso retrogrado dell’actina in trazione in avanti. La retrazione del bordo posteriore e la coesione del corpo cellulare richiedono la contrazione dell’actomiosina, come discusso oltre. Le cellule che migrano rapidamente, come i cheratociti di pesce, esemplificano l’efficienza di questo ciclo protrusione–adesione–trazione, mentre macrofagi e cellule epiteliali mostrano versioni più lente ma robustamente regolabili (Figura 05.29-06), (Figura 05.29-05).
In termini cinetici, la velocità di avanzamento locale può essere approssimata da \( v \approx \delta \,[k_{\mathrm{on}}\,C - k_{\mathrm{off}}] \), dove \( \delta \) è l’incremento per monomero aggiunto, \( k_{\mathrm{on}} \) e \( k_{\mathrm{off}} \) sono le costanti di associazione e dissociazione all’estremità barbed, e \( C \) è la concentrazione locale di actina-ATP disponibile. La modulazione di questi parametri da parte di proteine accessorie e segnali di membrana consente un controllo fine della protrusione.
Il margine guida è un cantiere molecolare in cui molte proteine che legano l’actina orchestrano nucleazione, allungamento, ramificazione e turnover dei filamenti. Nei lamellipodi, il complesso Arp2/3 nuclea nuovi filamenti a partire dai lati di filamenti preesistenti, generando un reticolo ramificato con angolo caratteristico vicino a 70°. L’attivazione del complesso Arp2/3 richiede fattori di nucleazione (NPF), come le proteine della famiglia WASP/WAVE, che integrano i segnali di membrana con la dinamica del citoscheletro. L’assemblaggio anteriore e il disassemblaggio posteriore producono un “treadmilling” di rete che spinge in avanti il lamellipodio (Figura 05.29-07).
I filopodi, al contrario, dipendono da proteine formine, che rimangono processivamente associate all’estremità barbed dei filamenti e ne promuovono l’allungamento lineare, prevenendo la formazione di rami. Cross-linker come fascin consolidano i fasci paralleli tipici dei filopodi, conferendo rigidità al prolungamento. Le formine agiscono anche in altri contesti di actina non ramificata, incluso l’anello contrattile del solco di divisione nelle cellule animali, dove coordinano l’assemblaggio durante la citocinesi.
Ulteriori regolatori modulano la disponibilità e la qualità dei monomeri e dei filamenti: profilina carica i monomeri con ATP e li convoglia verso le estremità barbed; proteine “capping” limitano l’allungamento stabilizzando le estremità in crescita; cofilina promuove severing e depolimerizzazione di filamenti ricchi di ADP, accelerando il rinnovamento; le proteine Ena/VASP riducono il capping localmente e favoriscono l’estensione protrusiva. L’equilibrio tra questi fattori determina se prevalgono lamellipodi, filopodi o strutture ibride.
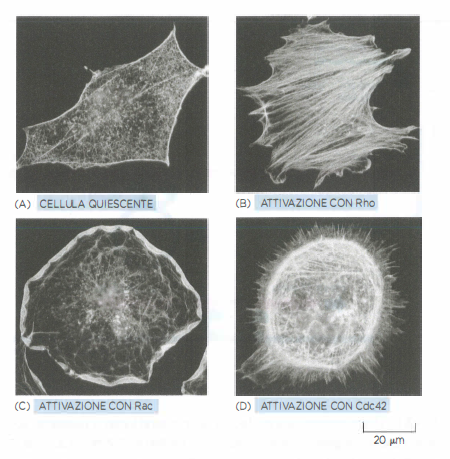
L’organizzazione dell’actina è strettamente controllata da segnali extracellulari che, tramite recettori di membrana (ad esempio GPCR o recettori tirosin–chinasi), attivano vie intracellulari convergenti sulla famiglia di GTPasi monomeriche Rho. Queste proteine funzionano come interruttori molecolari ciclici: nello stato attivo legano GTP, nello stato inattivo GDP. L’attivazione e lo spegnimento sono regolati da GEF (che favoriscono il caricamento di GTP), GAP (che accelerano l’idrolisi di GTP) e GDI (che sequestrano le GTPasi nel citosol). Nel contesto dell’actina, membri distinti della famiglia generano firmate morfologiche differenti: l’attivazione di Cdc42 stimola la formazione di filopodi; l’attivazione di Rac1 promuove lamellipodi e ruffling di membrana; l’attivazione di RhoA (“Rho” canonica) induce fasci di stress fibers e rinforzo delle adesioni tramite integrine, aumentando la contractilità dell’actomiosina (Figura 05.29-05).
Questi output derivano, in parte, dall’attivazione di effettori specifici: Rac1 e Cdc42 reclutano complessi WAVE/WASP che attivano Arp2/3; RhoA attiva ROCK, che fosforila la catena leggera della miosina II e inibisce la miosina fosfatasi, aumentando la tensione, e stimola formino mDia per promuovere filamenti lineari. La distribuzione spaziale di lipidi di membrana, come PIP3 generato da PI3K, crea gradienti che orientano la polarità del citoscheletro verso fonti chemiotattiche. L’aggregazione di integrine in adesioni focali, stabilizzata da talina e vinculina, fornisce ulteriori feedback meccanochimici che rafforzano le protrusioni direzionali (Figura 05.29-08).
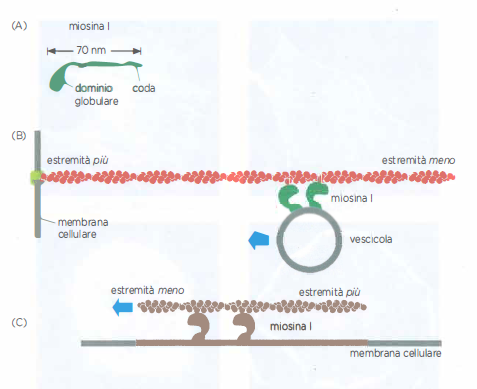
Le miosine sono motori molecolari dipendenti da actina che convertono l’energia dell’idrolisi di ATP in lavoro meccanico, muovendosi dalle estremità “pointed” verso le estremità “barbed” dei filamenti. Le due sottofamiglie più diffuse nelle cellule non muscolari sono miosina I e miosina II. La miosina I è tipicamente monomerica e possiede una testa motoria con attività ATPasica e una coda variabile che determina i carichi trasportati o i partner di membrana (Figura 05.29-09). Alcune isoforme collegano vescicole a binari di actina per il trasporto intracellulare direzionale (Figura 05.29-09); altre ancorano e rimodellano la membrana plasmatica rispetto al reticolo corticale, contribuendo al controllo della tensione e della morfologia della superficie (Figura 05.29-08).
La miosina II è più complessa: forma dimeri con code avvolte a coiled-coil che possono autoassemblarsi in filamenti bipolari capaci di scorrere antiparallelamente i filamenti di actina, generando contrazione. Nelle cellule non muscolari, filamenti di miosina II “non muscolare” si organizzano in fasci che costituiscono stress fibers, cinture corteciali e l’anello contrattile della citocinesi, fornendo la trazione necessaria per migrazione e cambi di forma. Nel muscolo scheletrico, una variante specializzata di miosina II forma i sarcomeri, l’unità contrattile alla base delle contrazioni potenti e ripetibili. In tutti i casi, il ciclo meccanico testata–actina segue sequenze di legame–colpo di forza–distacco sincronizzate con lo stato di ATP/ADP–Pi, e la regolazione della fosforilazione delle catene leggere modula la forza e la cinetica del motore.
La cooperazione tra polimerizzazione di actina al fronte, adesioni mediate da integrine e contrazione dell’actomiosina al retro produce il movimento netto: un esempio emblematico di come processi biochimici e meccanici, opportunamente integrati, traducano segnali esterni in lavoro cellulare direzionale.