pH: una scala di misura dell’acidità e della basicità
Definizione
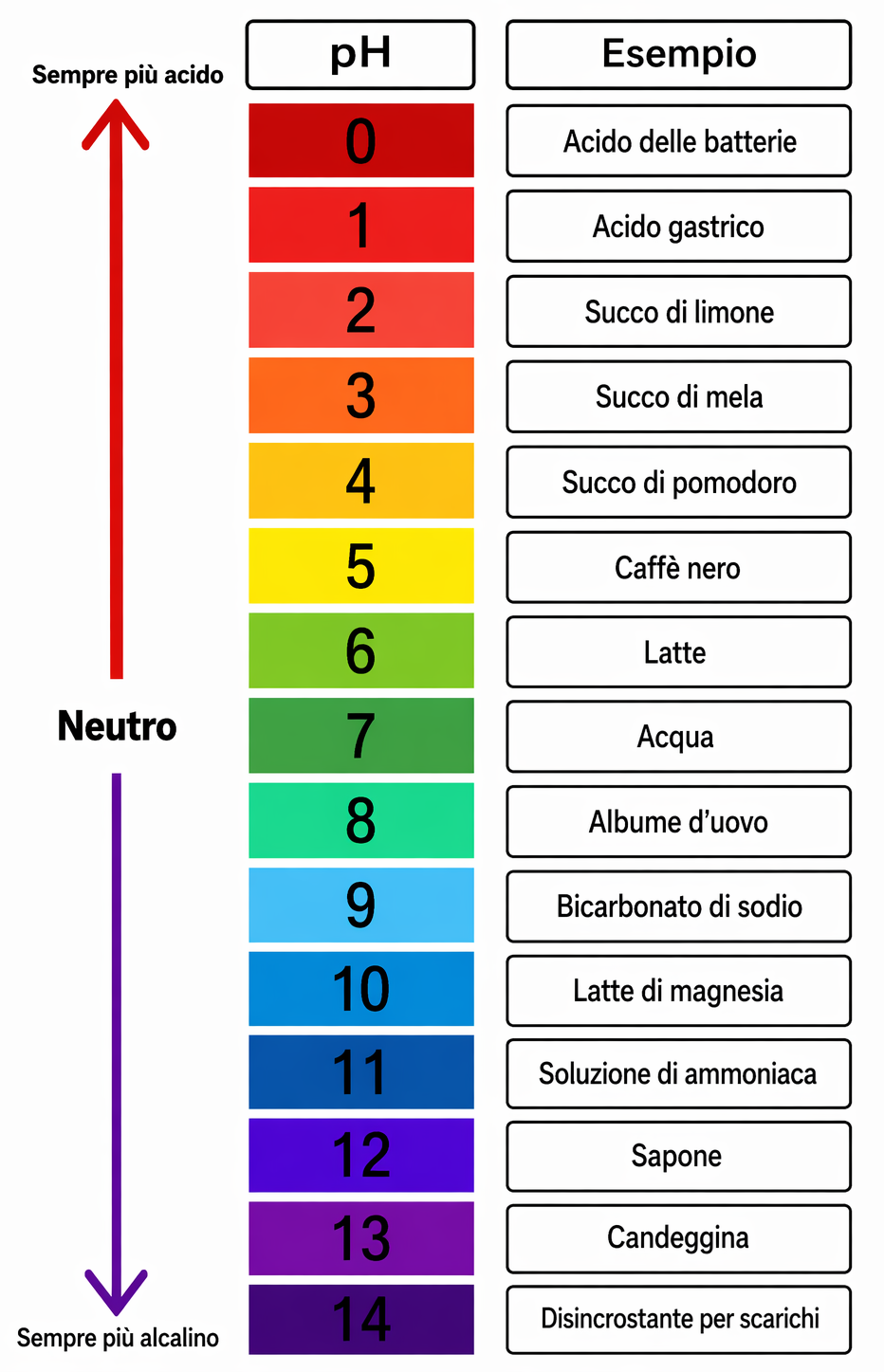
La scala del pH fornisce una misura logaritmica della “forza” acida o basica di una soluzione acquosa, in relazione alla concentrazione (più propriamente, all’attività) degli ioni idrossonio \( \mathrm{H_3O^+} \). In modo del tutto analogo a come la temperatura esprime lo stato termico, il pH esprime lo stato acido-base del sistema. Nelle soluzioni diluite a 25 °C, i valori di pH si collocano tipicamente fra 0 (acidità elevata) e 14 (basicità marcata). Il valore intermedio, pH = 7, individua una condizione di neutralità in cui l’effetto acido e quello basico si bilanciano. La (Figura 05.02-01) presenta alcuni esempi di soluzioni acquose e i relativi pH.
Per organizzare le idee, risultano utili le seguenti osservazioni di base:
- l’aggiunta di un acido (donatore di protoni) aumenta \( [\mathrm{H_3O^+}] \) e, di conseguenza, diminuisce \( [\mathrm{OH^-}] \);
- l’aggiunta di una base (accettore di protoni) diminuisce \( [\mathrm{H_3O^+}] \) e aumenta \( [\mathrm{OH^-}] \);
- in condizioni di neutralità, \( [\mathrm{H_3O^+}] = [\mathrm{OH^-}] \);
- per l’acqua a 25 °C vale sempre \( [\mathrm{H_3O^+}]\,[\mathrm{OH^-}] = 1{,}0 \times 10^{-14} \), il cosiddetto prodotto ionico dell’acqua, \( K_\mathrm{w} \);
- in acqua pura a 25 °C, \( [\mathrm{H_3O^+}] = [\mathrm{OH^-}] = 1{,}0 \times 10^{-7} \,\mathrm{mol\,L^{-1}} \), da cui pH = 7,00;
- in soluzioni molto concentrate o in solventi diversi dall’acqua, il pH può assumere valori anche inferiori a 0 o superiori a 14.
Il pH può essere determinato in modo approssimato o con elevata precisione. Una stima rapida si ottiene mediante carte indicatrici (indicatori universali), che cambiano colore al variare del pH. Per misure accurate si impiega il pH‑metro: un elettrodo vetroso sensibile a \( \mathrm{H_3O^+} \), accoppiato a un elettrodo di riferimento, rileva una differenza di potenziale elettrico proporzionale al pH secondo l’equazione di Nernst. Lo strumento va calibrato con soluzioni tampone certificate (ad esempio pH 4,00; 7,00; 10,00) per compensare deriva e dipendenza dalla temperatura. La dinamica di risposta dell’elettrodo, a 25 °C, è di circa 59,16 mV per unità di pH. Il principio operativo è illustrato nella (Figura 05.02-02).
Quando è nota la concentrazione (o, in prima approssimazione per soluzioni diluite, l’attività) degli ioni idrossonio, il pH è definito da:
\( \displaystyle \mathrm{pH} = -\log_{10} a_{\mathrm{H_3O^+}} \approx -\log_{10} [\mathrm{H_3O^+}] \).
In modo analogo, il pOH è definito da:
\( \displaystyle \mathrm{pOH} = -\log_{10} [\mathrm{OH^-}] \).
Le due grandezze sono collegate dal prodotto ionico dell’acqua:
\( \displaystyle \mathrm{pH} + \mathrm{pOH} = \mathrm{p}K_\mathrm{w} \approx 14{,}00 \) a 25 °C.
Quando si conosce \( [\mathrm{OH^-}] \), si ricava il pH passando per \( \mathrm{pOH} \) oppure usando direttamente \( [\mathrm{H_3O^+}] = K_\mathrm{w}/[\mathrm{OH^-}] \). È importante ricordare che \( K_\mathrm{w} \) dipende dalla temperatura; il valore 1,0 × 10⁻¹⁴ vale a 25 °C.
Indicazioni utili per interpretare la scala:
- una soluzione 1,0 M di acido forte (completamente dissociato) ha pH approssimativamente 0;
- una soluzione 1,0 M di base forte presenta pH approssimativamente 14;
- ogni variazione di dieci volte della concentrazione di \( \mathrm{H_3O^+} \) comporta una variazione di 1 unità di pH;
- la diluizione di un acido fa aumentare il pH; la diluizione di una base fa diminuire il pH;
- per soluzioni non ideali o molto concentrate, occorre usare le attività invece delle concentrazioni per evitare errori sistematici.
Esempi numerici:
- se \( [\mathrm{H_3O^+}] = 2{,}5 \times 10^{-3} \,\mathrm{mol\,L^{-1}} \), allora \( \mathrm{pH} = -\log_{10}(2{,}5 \times 10^{-3}) \approx 2{,}60 \);
- se \( [\mathrm{OH^-}] = 3{,}0 \times 10^{-5} \,\mathrm{mol\,L^{-1}} \), allora \( \mathrm{pOH} = 4{,}52 \) e \( \mathrm{pH} = 14{,}00 - 4{,}52 = 9{,}48 \).
Il controllo del pH è un requisito centrale in numerosi contesti scientifici, tecnologici e ambientali, poiché il grado di protonazione delle specie chimiche condiziona equilibrio, cinetica e selettività delle reazioni. Alcuni esempi rappresentativi sono i seguenti:
- Agricoltura: la disponibilità di nutrienti nel suolo (ad esempio fosfati, microelementi) dipende dal pH; pratiche agronomiche e ammendanti vengono adottati per mantenere il terreno nel range ottimale per le colture;
- Fisiologia: il pH ematico è finemente regolato (circa 7,35–7,45); scostamenti anche inferiori a un’unità alterano l’attività enzimatica e l’equilibrio acido‑base, con esiti potenzialmente letali;
- Industria: fermentazioni, galvanica, formulazione di detergenti, trattamento delle superfici e sintesi chimiche richiedono pH controllato per massimizzare resa, purezza e sicurezza di processo;
- Servizi idrici: potabilizzazione e depurazione necessitano di specifici intervalli di pH per ottimizzare coagulazione, disinfezione, adsorbimento e abbattimento degli inquinanti;
- Piogge acide: acido nitrico e acido solforico, generati dall’ossidazione degli ossidi di azoto e di zolfo e poi disciolti nelle precipitazioni, abbassano il pH di acque e suoli, con effetti negativi su ecosistemi acquatici e foreste.
In conclusione, ogni processo che avviene in soluzione acquosa è, in misura variabile, sensibile al pH: misurarlo correttamente e mantenerlo nel valore desiderato è parte integrante di un controllo chimico rigoroso.