Ossidazione e riduzione nei sistemi viventi
Definizione
Nei sistemi viventi, ossidazione e riduzione descrivono trasferimenti di elettroni intimamente connessi al metabolismo. In termini generali, si parla di ossidazione quando una specie perde elettroni, e di riduzione quando li acquista. Nelle molecole organiche, dove gli elettroni non sono sempre tracciabili esplicitamente, la variazione dello stato di ossidazione del carbonio si riconosce pragmaticamente da: aumento dei legami del carbonio con atomi più elettronegativi (in particolare l’ossigeno) oppure perdita di idrogeno per ossidazione; diminuzione dei legami con ossigeno o guadagno di idrogeno per riduzione. Questo criterio riflette l’incremento o la diminuzione della densità elettronica attorno al carbonio, coerentemente con le definizioni formali di numero di ossidazione.
L’ordinamento seguente rende intuitiva la progressione di ossidazione del carbonio in composti comuni: alcani (più ridotti) → alcoli → composti carbonilici (aldeidi o chetoni) → acidi carbossilici (più ossidati). In questa sequenza, ogni passo verso destra comporta, in media, perdita di idrogeno o acquisizione di ossigeno; viceversa, il percorso inverso implica riduzione.
| Reazioni di ossidazione: procedendo da un alcano a un alcol e oltre, il carbonio aumenta il proprio stato di ossidazione. |
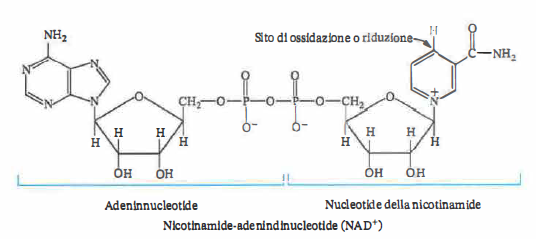
In biochimica, trasformazioni come alcano → alcol, alcol → aldeide/chetone, aldeide → acido carbossilico sono dunque ossidazioni, mentre i processi inversi sono riduzioni. Queste reazioni sono catalizzate da enzimi della classe delle ossidoriduttasi, che trasferiscono elettroni, spesso sotto forma di equivalenti riducenti di idrogeno. Tali trasferimenti richiedono frequentemente coenzimi specifici, capaci di accettare o donare elettroni in modo reversibile. Tra i cofattori più diffusi figura il nicotinamide adenina dinucleotide, NAD+ (Figura 07.06-01), che opera tipicamente attraverso il trasferimento di un idruro.
Dal punto di vista meccanicistico, NAD+ non cattura “un atomo di idrogeno” neutro, bensì accetta uno ione idruro \( \mathrm{H^-} \) (due elettroni e un protone) dal substrato, generando NADH; un secondo protone viene rilasciato in soluzione, come sintetizzato dalla stechiometria:
\[ \mathrm{Substrato\ (ridotto)} + \mathrm{NAD^+} \longrightarrow \mathrm{Substrato\ (ossidato)} + \mathrm{NADH} + \mathrm{H^+}. \]
Un esempio emblematico è l’ossidazione dell’L‑malato a ossalacetato catalizzata dalla malato deidrogenasi nel ciclo dell’acido citrico, accoppiata alla riduzione di NAD+ a NADH. In termini molecolari, un idruro è trasferito dal C‑2 del malato all’anello nicotinammidico di NAD+, con formazione di ossalacetato:
\[ \mathrm{L\text{-}malato} + \mathrm{NAD^+} \longrightarrow \mathrm{ossalacetato} + \mathrm{NADH} + \mathrm{H^+}. \]
 |
| Ossidazione dell’L‑malato a ossalacetato catalizzata dalla malato deidrogenasi, con formazione concomitante di NADH. |
La reattività di NAD+/NADH è coerente con il suo potenziale redox standard biochimico, che lo rende un accettore/donatore versatile in reazioni deidrogenative. Sebbene la trasformazione del malato sia endotermodinamica a condizioni standard (ΔG°’ positivo), in vivo procede grazie alla rimozione rapida dell’ossalacetato nelle tappe successive e a un elevato rapporto \(\mathrm{[NAD^+]/[NADH]}\) nel compartimento mitocondriale.
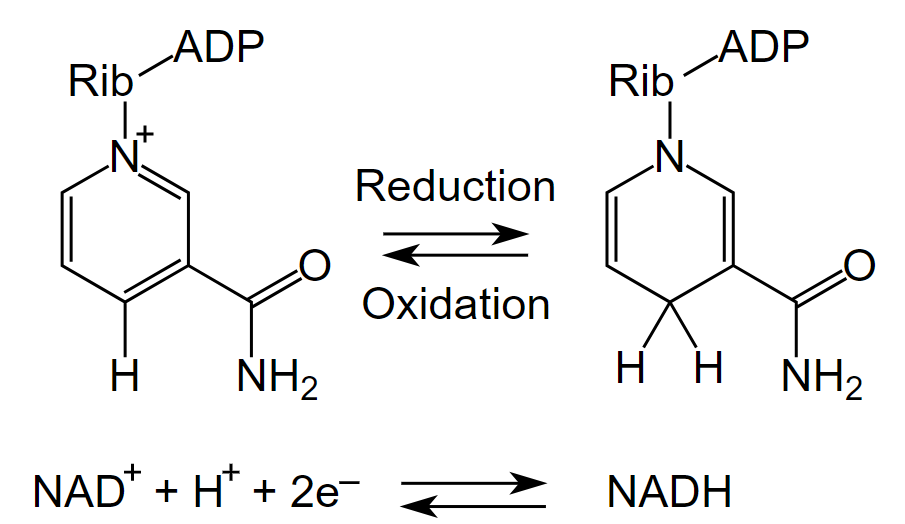 |
| Schema di riduzione: NAD+ accetta un idruro dal substrato ridotto, generando NADH e rilasciando un protone libero. |
Accanto a NAD+, altre coppie redox supportano il metabolismo cellulare. In forma sintetica:
- NADP+/NADPH, attivo soprattutto nelle vie anaboliche e nella difesa antiossidante;
- FAD/FADH2 e FMN/FMNH2, legati a flavoproteine capaci di trasferire uno o due elettroni;
- Ubichinone/ubichinolo (coenzima Q), mobile nella membrana mitocondriale e cruciale per la catena di trasporto degli elettroni;
- Centri ferro‑zolfo ed eme, mediatori di trasferimenti mono‑elettronici.
Indicatori operativi di ossidazione del carbonio in biochimica comprendono:
- incremento dei legami C–O o C–N e riduzione dei legami C–H;
- formazione di doppi legami C=O a partire da alcoli o la conversione di aldeidi in acidi per addizione di ossigeno;
- trasferimenti di idruro a cofattori nicotinammidici o di elettroni a flavine e chinoni.
Come esempio numerico di stato di ossidazione formale, consideriamo il passaggio da etanolo a etanale (acetaldeide). Assegnando al carbonio terminale (quello ossidato) le convenzioni di numero di ossidazione, si osserva un aumento di due unità, coerente con la rimozione complessiva di due elettroni trasferiti a NAD+ nella reazione catalizzata da una alcol deidrogenasi. Tale analisi, pur semplificata, spiega perché l’aggiunta di ossigeno o la rimozione di idrogeno siano ottimi traccianti del flusso elettronico nelle vie metaboliche.
In sintesi, le ossidoriduzioni nelle cellule si realizzano attraverso reti enzimatiche che coordinano trasferimenti di elettroni/idrogeno con coenzimi specializzati, collegando l’energia chimica dei substrati alla produzione di equivalenti riducenti (NADH, FADH2) e, in ultima analisi, alla generazione di ATP mediante fosforilazione ossidativa.