Nomenclatura IUPAC e nomi comuni
Definizione
Secondo le raccomandazioni IUPAC per la nomenclatura organica, il nome sistematico di un’aldeide si ottiene applicando le regole generali dei composti a catena, con priorità funzionale al gruppo formile \( -\mathrm{CHO} \). Di seguito si sintetizzano i passaggi fondamentali:
- Si seleziona come catena principale la sequenza continua di atomi di carbonio più lunga che includa il carbonio del gruppo carbonilico aldeidico, e la si denomina come l’alcano corrispondente;
- Si converte la desinenza dell’alcano in quella tipica delle aldeidi: la vocale finale viene sostituita da -ale (per esempio: etano → etanale, propano → propanale);
- La numerazione delle posizioni parte dal carbonio del gruppo formile, che assume locante 1; tale locante non si riporta esplicitamente per il suffisso -ale poiché è sottinteso;
- I sostituenti presenti sulla catena si indicano come prefissi con i rispettivi locanti, precedendo il nome del composto e rispettando l’ordine alfabetico; eventuali insaturazioni si indicano con -en-, -in-, ecc., posizionate e numerate in accordo alle regole IUPAC.
Quando sono presenti più gruppi aldeidici sulla stessa struttura, si adottano i suffissi -dial, -trial, e così via (ad esempio: butandiale per una catena a quattro atomi con due gruppi -CHO). Se il gruppo aldeidico non può essere considerato come funzione principale, lo si esprime come prefisso formil-; nelle strutture cicliche con -CHO direttamente sul ciclo, è ammesso l’uso della desinenza -carbaldeide (per esempio, cicloesancarbadeide), mentre per alcuni sistemi aromatici sono consentiti nomi conservati di largo impiego, quali benzaldeide, in linea con le preferenze IUPAC.
Esempio didattico: l’aldeide CHO–CH(CH3)–CH2–CH2–Cl si denomina 4-cloro-2-metilbutanale; l’insaturazione impone ulteriori indicazioni, come in CHO–CH=CH–CH3, che si nomina but-2-enale, con eventuale specificazione E/Z per l’alchene quando necessario. La priorità del gruppo -CHO fa sì che altre funzioni, come -OH o alcheni, vengano trattate rispettivamente come prefisso (idrossi-) o come parte del suffisso secondario (en-, in-), secondo le regole di precedenza funzionale IUPAC.
 |
| Schema generale di un’aldeide: R indica un residuo alifatico o aromatico legato al gruppo formile. |
 |
| La formaldeide (nome IUPAC: metanale) rappresenta il membro più semplice della classe. |
Denominazione IUPAC (sistematica) | Nome tradizionale | Numero CAS | Formula |
|---|---|---|---|
| Metanale | Formaldeide | 50-00-0 | H-CHO |
| Etanale | Acetaldeide | 75-07-0 | CH3-CHO |
| Propanale | Propionaldeide | 123-38-6 | CH3CH2-CHO |
| Butanale | Butirraldeide | 123-72-8 | CH3(CH2)2-CHO |
| 2-metilpropanale | Isobutiraldeide | 78-84-2 | CH3CH(CH3)-CHO |
| Pentanale | Valeraldeide | 110-62-3 | CH3(CH2)3-CHO |
| Esanale | Capraldeide | 66-25-1 | CH3(CH2)4-CHO |
| Eptanale | Enantaldeide | 111-71-7 | CH3(CH2)5-CHO |
| Ottanale | Caprilaldeide | 124-13-0 | CH3(CH2)6-CHO |
| Decanale | Caprinaldeide | 112-31-2 | CH3(CH2)8-CHO |
| Propenale | Acroleina | 107-02-8 | CH2=CH-CHO |
| trans-2-butenale | Crotonaldeide | 123-73-9 | CH3CH=CH-CHO |
| 2-metilpropenale | Metacroleina | 78-85-3 | CH2=C(CH3)-CHO |
| Benzaldeide | Benzaldeide | 100-52-7 | C6H5-CHO |
Il nome tradizionale di molte aldeidi deriva dal corrispondente acido carbossilico noto con nomenclatura comune: così, dall’acido acetico si ottiene “acetaldeide”, dall’acido propionico “propionaldeide”, e così via. Nella (Tabella 07.11-01) sono riportati i nomi comuni dei primi membri della serie omologa. Nel sistema non sistematico, un’aldeide sostituita si nomina anteponendo il nome del sostituente a quello dell’aldeide della stessa catena, e la posizione del sostituente si indica mediante lettere greche a partire dal carbonio adiacente al gruppo formile: α per il primo, β per il secondo, γ per il terzo, δ per il quarto, ecc. Per esempio, un sostituente metilico in α rispetto al gruppo -CHO si indicherà come α-metil-.
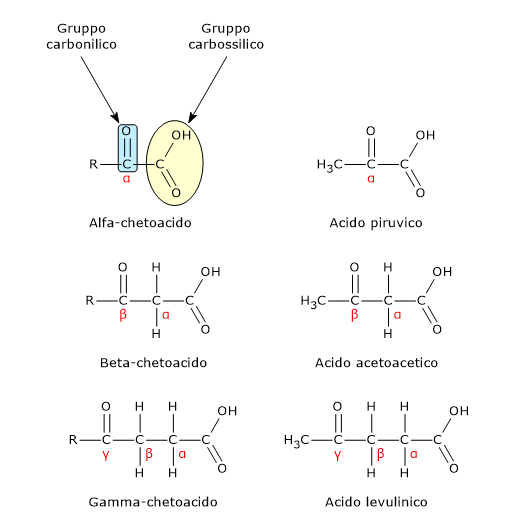 |
| Notazione posizionale α, β, γ, δ lungo la catena a partire dal carbonio adiacente al gruppo formile. |
Nota terminologica e priorità funzionale (IUPAC 2013):
- il gruppo aldeidico ha priorità rispetto a alcoli, alcheni, alchini ed eteri per l’assegnazione del suffisso;
- le insaturazioni si includono nel suffisso (-en-, -in-) con i relativi locanti, mantenendo il locante 1 per -CHO sottinteso; quando necessario, si antepongono descrittori E/Z per la geometria degli alcheni e R/S per i centri stereogenici;
- in sistemi ciclici, il gruppo -CHO direttamente legato all’anello si può nominare con -carbaldeide; su anelli aromatici, sono ammessi nomi conservati ampiamente accettati (per esempio, benzaldeide), in coerenza con le preferenze IUPAC.
Aldeidi: denominazioni e formule
| Nome IUPAC | Nome comune | Formula strutturale |
|---|---|---|
| Metanale | Formaldeide | H–C(=O)–H |
| Etanale | Acetaldeide | CH₃–C(=O)–H |
| Propanale | Propionaldeide | CH₃CH₂–C(=O)–H |
| Butanale | Butirraldeide | CH₃CH₂CH₂–C(=O)–H |
| Pentanale | Valeraldeide | CH₃CH₂CH₂CH₂–C(=O)–H |
| Esanale (extra) | Caproaldeide | CH₃(CH₂)₄–C(=O)–H |
| Benzaldeide (extra) | Benzaldeide | C₆H₅–C(=O)–H |
| Tabella che riporta i nomi sistematici, i nomi tradizionali e le formule di alcune aldeidi. | ||
La denominazione dei chetoni segue principi affini a quelli delle aldeidi, ma con regole specifiche per il gruppo carbonilico in posizione interna. In nomenclatura IUPAC, il suffisso caratteristico è “-one”, che sostituisce la desinenza dell’alcano corrispondente, e la posizione del gruppo C=O è indicata mediante un numero, quando necessario. La catena principale viene scelta in modo da includere il carbonile e viene numerata nel verso che assegna al carbonio carbonilico il locante più basso disponibile. Eventuali sostituenti sono elencati come prefissi, in ordine alfabetico, ciascuno con il proprio locante.
 |
| Schema generale di un chetone. |
| Formula | IUPAC | Nome Tradizionale |
| CH3COCH(CH3)2 | 3-metil-2-butanone | metil-isopropil-chetone |
| CH3CH2COCH2CH3 | 3-pentanone | dietilchetone |
| C6H5COCH3 | 1-feniletan-1-one | acetofenone |
| (CH2)5CO | cicloesanone | cicloesanone |
Secondo la IUPAC, il nome di un chetone lineare deriva dall’alcano di riferimento con l’aggiunta del suffisso “-one”; il locante del carbonile precede la desinenza se esistono più posizioni possibili (per esempio, pentan-3-one e pentan-2-one designano isomeri diversi). La numerazione della catena privilegia sempre il carbonio del C=O, che deve ricevere il numero più basso consentito dal sistema di locanti. Nei composti ciclici, il carbonio carbonilico è convenzionalmente il C-1 e il locante può essere omesso quando non sussistono ambiguità (ad esempio, cicloesanone).
Quando i sostituenti su entrambi i lati del carbonile sono esplicitati come gruppi, la IUPAC ammette anche la nomenclatura di classe funzionale, che enuncia i due radicali seguiti dalla parola “chetone” (per esempio, fenil-metil-chetone; per il composto arilico simmetrico, “difenilchetone”, noto come benzofenone). Se sono presenti più gruppi C=O in una stessa molecola, si impiegano i suffissi “-dione”, “-trione”, ecc., specificando i locanti, come in butano-2,3-dione. In presenza di funzioni di priorità superiore per la denominazione (ad esempio acidi carbossilici), il gruppo carbonilico del chetone può essere indicato come sostituente “oxo-” con relativo locante, mantenendo il suffisso della funzione principale:
- Scelta della catena madre: deve includere il carbonile e massimizzare la lunghezza in conformità alle regole generali della IUPAC;
- Numerazione: si assegna il locante più basso possibile al carbonio del C=O;
- Sostituenti: elencati in ordine alfabetico con locanti, prima del nome della catena principale con suffisso “-one”;
- Composti ciclici: il carbonile è in posizione 1 per convenzione, con locante spesso sottinteso;
- Più carbonili: si usano i suffissi “-dione”, “-trione”, ecc., con indicazione delle posizioni;
- Doppi legami concomitanti: si combinano i suffissi (“-enone”, “-dienone”) e si numerano insaturazioni e carbonile con la regola del più basso insieme di locanti.








