Nomenclatura e scrittura delle formule dei composti
Definizione
Per i solidi ionici, la formula chimica rappresenta l’unità di formula, ossia il più semplice rapporto intero tra cationi e anioni nel reticolo cristallino. La scrittura impiega simboli degli elementi e pedici numerici per indicare le quantità relative; il pedice 1 non si riporta. Esempi didattici sono CaF2 e K2S: nel primo caso, uno ione Ca2+ si associa a due ioni F-, nel secondo, due K+ si bilanciano con uno S2-. A differenza delle molecole covalenti, l’unità di formula non corrisponde a un’entità isolata, ma descrive la composizione ripetuta nel reticolo esteso. La condizione di elettroneutralità impone che la somma algebrica delle cariche sia nulla: \(\sum_i n_i z_i = 0\), dove \(n_i\) è il numero di ioni del tipo \(i\) e \(z_i\) la loro carica.
Determinazione della formula a partire dagli ioni presenti
Una volta identificati gli ioni costituenti, la formula si ottiene imponendo la neutralità complessiva. Le cariche dei principali ioni monoatomici si deducono dal gruppo del sistema periodico: metalli alcalini (+1), alcalino-terrosi (+2), alluminio (+3), alogeni (-1), calcogeni (-2). I metalli di transizione possono presentare più stati di ossidazione:
- bilanciare le cariche fino a ottenere somma zero, scegliendo i minimi rapporti interi possibili (ridotti ai termini più piccoli);
- utilizzare, se utile, la “regola dell’incrocio” delle cariche come scorciatoia, verificando poi la riduzione ai minimi termini;
- per ioni poliatomici, trattare lo ione come un’unità indivisibile e racchiudere tra parentesi se compare con pedice maggiore di 1;
- verificare con \(\sum_i n_i q_i = 0\) che la neutralità sia rispettata.
Esempi: Sr2+ e N3- portano a Sr3N2; Al3+ e O2- danno Al2O3. Con ioni poliatomici: Ca2+ e NO3- → Ca(NO3)2; NH4+ e PO43- → (NH4)3PO4.
Denominazione dei composti a legame ionico
I composti ionici sono costituiti da cationi e anioni. Nei composti binari, il nome si costruisce indicando per primo l’anione con il suffisso -uro applicato alla radice del non metallo (per esempio: cloruro, bromuro, solfuro), seguito dalla preposizione “di” e dal nome del metallo che fornisce il catione. Tra i binari rientrano anche diversi ossidi metallici, contenenti lo ione ossido, O2-, per i quali si usa la forma “ossido di …”. Gli ioni monoatomici più frequenti sono raccolti nella (Tabella 01.14-01), con evidenza per quelli di rilievo biologico (Figura 01.14-01).
Molti metalli, specialmente quelli di transizione, formano più cationi con diversa carica. Per evitare ambiguità, si adottano due sistemi: il metodo di Stock, oggi preferito dalle raccomandazioni IUPAC, e la nomenclatura tradizionale. Nel sistema di Stock si indica tra parentesi tonde, in numeri romani, lo stato di ossidazione del metallo subito dopo il suo nome, per esempio “stagno(IV)” o “cobalto(II)”. Nella nomenclatura comune, meno utilizzata, si impiega il suffisso -oso per la carica minore e -ico per la maggiore (per esempio “stannoso” vs “stannico”, “cobaltos” vs “cobaltic” nell’uso storico). Esempi e corrispondenze sono sintetizzati nella (Tabella 01.14-02).
Numerosi sali includono ioni poliatomici, ossia insiemi di atomi legati covalentemente con una carica netta, positiva o negativa, che interagiscono elettrostaticamente con ioni di segno opposto. Classici esempi sono idrossido (OH-), nitrato (NO3-), solfato (SO42-), carbonato (CO32-) e ammonio (NH4+). Gli ioni più comuni sono riportati nella (Tabella 01.14-03); la comprensione dei loro nomi risulterà più immediata affrontando la nomenclatura degli acidi ossigenati. Di seguito, alcune formule con i rispettivi nomi (Figura 01.14-02):
- (NH4)2SO4: solfato di ammonio;
- CaCO3: carbonato di calcio;
- KNO3: nitrato di potassio;
- Al(OH)3: idrossido di alluminio;
- BaSO4: solfato di bario.
Dalla denominazione alla formula chimica
Per ricavare la formula a partire dal nome, è necessario riconoscere gli ioni coinvolti, ricordarne cariche e formule, e combinare le specie in modo che la carica totale sia zero. Le seguenti indicazioni risultano utili:
- identificare l’anione dal suffisso (-uro per i binari, -ato/-ito per molti ossianioni) e il catione dal nome del metallo o dello ione ammonio;
- se presente un numero romano, attribuirlo allo stato di ossidazione del metallo e quindi alla carica dello ione (per ioni semplici carica = numero romano);
- bilanciare le cariche con i minimi rapporti interi, usando parentesi per gli ioni poliatomici ripetuti;
- controllare la neutralità con \(\sum_i n_i z_i = 0\).
Esempi: “fosfuro di calcio” → Ca2+ e P3- → Ca3P2; “solfato di ferro(III)” → Fe3+ e SO42- → Fe2(SO4)3; “nitrito di sodio” → Na+ e NO2- → NaNO2; “ossido di rame(II)” → Cu2+ e O2- → CuO. In presenza di più unità dello stesso ione poliatomico, si impiegano parentesi: ad esempio, “nitrato di piombo(II)” → Pb2+ e NO3- → Pb(NO3)2.
Cationi e anioni più diffusi
| Catione | Nome | Anione | Nome |
|---|---|---|---|
| H⁺ | Ione idrogeno | H⁻ | Ione idruro |
| Li⁺ | Ione litio | F⁻ | Ione fluoruro |
| Na⁺ | Ione sodio | Cl⁻ | Ione cloruro |
| K⁺ | Ione potassio | Br⁻ | Ione bromuro |
| Cs⁺ | Ione cesio | I⁻ | Ione ioduro |
| Be²⁺ | Ione berillio | S²⁻ | Ione solfuro |
| Mg²⁺ | Ione magnesio | N³⁻ | Ione nitruro |
| Ca²⁺ | Ione calcio | P³⁻ | Ione fosfuro |
| Ba²⁺ | Ione bario | O²⁻ | Ione ossido |
| Al³⁺ | Ione alluminio | ||
| Ag⁺ | Ione argento | ||
| Fe²⁺ / Fe³⁺ | Ione ferro | CO₃²⁻ | Ione carbonato |
| Zn²⁺ | Ione zinco | PO₄³⁻ | Ione fosfato |
| Cu²⁺ | Ione rame | HCO₃⁻ | Ione bicarbonato |
| Tabella che riporta gli ioni monoatomici maggiormente presenti. | |||
Denominazioni sistematiche e tradizionali di ferro e rame
| Formula | Carica ionica | Nome del catione | Nome del composto |
|---|---|---|---|
| FeCl₂ | 2⁺ | Ferro(II) | Cloruro di ferro(II) |
| FeCl₃ | 3⁺ | Ferro(III) | Cloruro di ferro(III) |
| Cu₂O | 1⁺ | Rame(I) | Ossido di rame(I) |
| CuO | 2⁺ | Rame(II) | Ossido di rame(II) |
| SnCl₂ | 2⁺ | Stagno(II) | Cloruro di stagno(II) |
| SnCl₄ | 4⁺ | Stagno(IV) | Cloruro di stagno(IV) |
| Formula | Carica ionica | Nome del catione | Nome del composto |
| FeCl₂ | 2⁺ | Ferroso | Cloruro ferroso |
| FeCl₃ | 3⁺ | Ferrico | Cloruro ferrico |
| Cu₂O | 1⁺ | Rameoso | Ossido rameoso |
| CuO | 2⁺ | Rameico | Ossido rameico |
| SnCl₂ | 2⁺ | Stannoso | Cloruro stannoso |
| SnCl₄ | 4⁺ | Stannico | Cloruro stannico |
| Tabella che riporta le indicazioni dei nomi secondo il metodo Stock e le denominazioni comuni dei cationi di Fe e Cu e dei loro composti corrispondenti. | |||
Ioni poliatomici
| Ione | Nome |
|---|---|
| H₃O⁺ | Idrossonio |
| NH₄⁺ | Ammonio |
| NO₂⁻ | Nitrito |
| NO₃⁻ | Nitrato |
| SO₃²⁻ | Solfito |
| SO₄²⁻ | Solfato |
| HSO₄⁻ | Idrogenosolfato |
| OH⁻ | Idrossido |
| CN⁻ | Cianuro |
| PO₄³⁻ | Fosfato (ortofosfato) |
| HPO₄²⁻ | Idrogenofosfato |
| H₂PO₄⁻ | Diidrogenofosfato |
| CO₃²⁻ | Carbonato |
| HCO₃⁻ | Idrogenocarbonato |
| ClO⁻ | Ipoclorito |
| ClO₂⁻ | Clorito |
| ClO₃⁻ | Clorato |
| ClO₄⁻ | Perclorato |
| CH₃COO⁻ (o C₂H₃O₂⁻) | Acetato |
| MnO₄⁻ | Permanganato |
| Cr₂O₇²⁻ | Dicromato |
| CrO₄²⁻ | Cromato |
| O₂²⁻ | Perossido |
| SCN⁻ | Tiocianato |
| BO₃³⁻ | Borato |
| Principali cationi e anioni poliatomici. | |
Denominazione dei composti covalenti
I composti covalenti risultano prevalentemente dall’interazione tra elementi non metallici. A differenza dei composti ionici, che nello stato solido organizzano una rete cristallina estesa, le specie covalenti si presentano di norma come insiemi di molecole individuali in fase solida, liquida o gassosa; tale carattere molecolare è un tratto distintivo della covalenza. Quando il composto contiene esattamente due elementi si parla di composto binario. Per i binari covalenti si applica una sistematica parallela a quella degli ionici, con alcune differenze. In linea generale:
- si nomina per primo l’elemento più elettropositivo (di solito quello che compare per primo nella formula), seguito dalla preposizione “di”;
- il secondo elemento si indica con la radice del nome seguita dal suffisso “-uro”, con l’eccezione dell’ossigeno, per il quale si usa “ossido”;
- si usano prefissi numerici greci per specificare il numero di atomi di ciascun elemento, come riportato nella (Tabella 01.14-04);
- il prefisso “mono-” si omette di norma sul primo elemento, ma si utilizza abitualmente sul secondo quando è presente un solo atomo (esempio: monossido);
- per ragioni eufoniche, in presenza di vocali contigue si applicano contrazioni: mono- + ossido → monossido; penta- + ossido → pentossido.
È frequente che la stessa coppia di elementi generi più composti stoichiometricamente diversi; per evitare ambiguità si impiegano i prefissi della (Tabella 01.14-04). Esempi didatticamente utili includono: “tetrafluoruro di silicio”, SiF4; “esafluoruro di zolfo”, SF6; “monossido di azoto”, NO, distinto dal “biossido di azoto”, NO2. Per i composti con ossigeno si adotta la forma “ossido di …” con i prefissi appropriati (esempio: “diossido di zolfo”, SO2).
Formulazione dei composti covalenti
Molte specie molecolari sono note con nomi d’uso consolidati che coesistono o sostituiscono la denominazione sistematica. Alcuni esempi diffusi sono: H2O2 (perossido di idrogeno), CH3OH (metanolo), HCOOH (acido formico), C12H22O11 (saccarosio). Tali denominazioni, benché non sistematiche, sono così radicate da richiedere memorizzazione. Viceversa, quando il nome contiene i prefissi numerici, la conversione al corrispondente formula-molecolare è meccanica. Per tradurre un nome sistematico in formula si può procedere come segue:
- identificare il primo elemento e il suo prefisso, se presente, e assegnare il pedice corrispondente (se il prefisso manca, si intende 1);
- identificare il secondo elemento (in forma “-uro” o “ossido”) e il suo prefisso, attribuendo il pedice indicato;
- verificare che l’ordine degli elementi rispetti la convenzione dell’elemento più elettropositivo per primo; in alternativa, adottare la sequenza tradizionale nota per la coppia (per esempio, C prima di O).
Esempi: “trifluoruro di boro” → BF3; “tetrafluoruro di selenio” → SeF4; “monossido di carbonio” → CO. L’uso coerente dei prefissi della (Tabella 01.14-04) consente univocità tra nome e formula.
Denominazione degli acidi
In ambiente acquoso, un acido è una sostanza che genera ioni idrogeno, H+. Gli acidi binari, o idracidi, sono costituiti da idrogeno e un non metallo (generalmente un alogeno o un calcogeno). Esempi tipici sono HF, HCl, HBr, HI, H2Se. Alcuni idracidi comprendono specie pseudoalogenuri, come HN3 (acido azidico). Per questi composti coesistono denominazioni tradizionali e sistematiche conformi alla prassi IUPAC. Gli acidi contenenti idrogeno, ossigeno e un altro non metallo sono detti ossiacidi. Essi si collegano concettualmente agli ossidi acidi (anidridi) del non metallo: l’idratazione dell’anidride fornisce l’ossoacido corrispondente. Ad esempio:
\( \mathrm{SO_3 + H_2O \rightarrow H_2SO_4} \)
Nella scrittura della formula dell’ossoacido è comune riportare gli elementi nell’ordine H–non metallo–O, con pedici coerenti con la somma degli atomi reagenti. La denominazione tradizionale impiega i suffissi -oso e -ico per indicare, rispettivamente, il contenuto di ossigeno minore o maggiore all’interno di una stessa serie; i prefissi ipo- e per- estendono l’escursione al minimo e massimo stato di ossidazione osservato per il non metallo. La denominazione IUPAC ammette anche forme come “ossido di …, idrato”, ma nell’uso didattico è diffusa la nomenclatura tradizionale degli ossiacidi. Il sistema fosforico costituisce un caso peculiare: dalle anidridi del fosforo si ottengono serie meta-, piro- e orto- in funzione del grado di idratazione. Per l’acido ortofosforico:
\( \mathrm{P_2O_5 + 3\,H_2O \rightarrow 2\,H_3PO_4} \), ovvero \( \mathrm{H_6P_2O_8} \) diviso per 2 fornisce \( \mathrm{H_3PO_4} \).
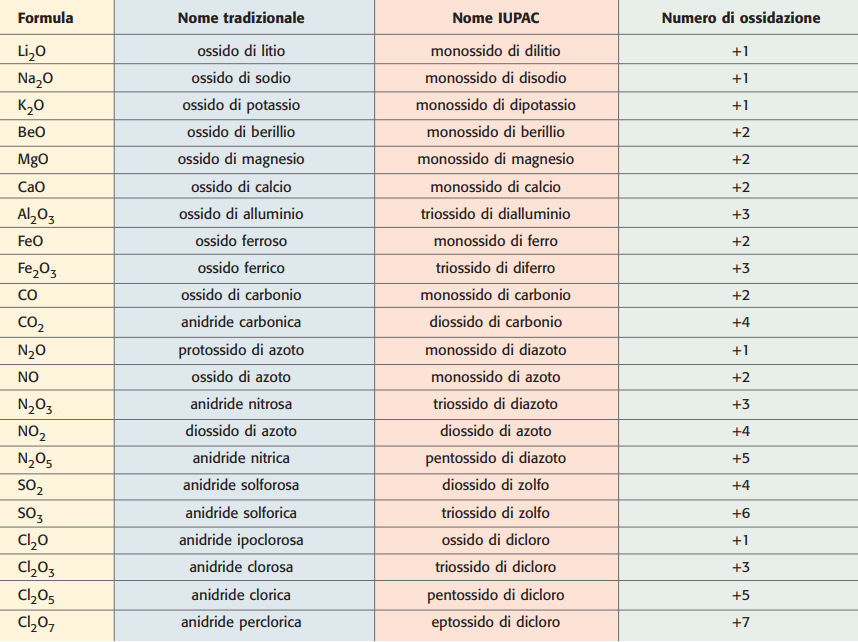
Di seguito si riportano esempi rappresentativi di anidridi e ossiacidi correlati, diversi ma analoghi a quelli tipici:
B2O3 anidride borica → H3BO3 acido borico;
SeO2 anidride seleniosa → H2SeO3 acido selenioso;
SeO3 anidride selenica → H2SeO4 acido selenico;
I2O5 anidride iodica → HIO3 acido iodico;
Br2O anidride ipobromosa → HBrO acido ipobromoso;
Br2O3 anidride bromosa → HBrO2 acido bromoso;
Br2O5 anidride bromica → HBrO3 acido bromico;
Br2O7 anidride perbromica → HBrO4 acido perbromico.
Possiamo ora riconsiderare la relazione con gli anioni poliatomici menzionati nella (Tabella 01.14-03). Le formule degli anioni si ottengono sottraendo uno o più H+ dall’ossoacido corrispondente; la trasformazione dei suffissi segue la regola -oso → -ito e -ico → -ato. Ad esempio a partire da H2SO4 (acido solforico) si hanno:
- l’anione solfato, SO42−, rimuovendo entrambi gli H+;
- l’anione idrogenosolfato, HSO4−, rimuovendo un solo H+.
Denominazione delle basi
Una base in soluzione acquosa libera ioni idrossido, OH−. Gli idrossidi metallici si ottengono per reazione dell’ossido basico del metallo con l’acqua. Ad esempio, l’ossido di calcio reagisce vigorosamente secondo:
\( \mathrm{CaO + H_2O \rightarrow Ca(OH)_2} \)
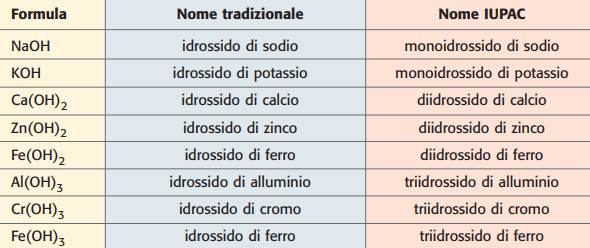
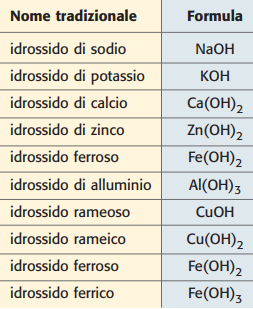
La nomenclatura segue le stesse convenzioni degli ossidi e dei sali per i metalli a multipla valenza: nel sistema di Stock si indica tra parentesi la valenza del metallo in numeri romani; la nomenclatura tradizionale impiega i suffissi -oso/-ico. Esempi: Fe(OH)2, “idrossido di ferro(II)” o “idrossido ferroso”; Fe(OH)3, “idrossido di ferro(III)” o “idrossido ferrico”. L’idrossido di rame può comparire come Cu(OH)2 (“rame(II)”, “rameico”), mentre Pb(OH)2 si denomina “idrossido di piombo(II)” (Figura 01.14-03).
I sali sono composti ionici di reazione tra acidi e basi forti o deboli. Come esempio di neutralizzazione:
\( \mathrm{KOH + HNO_3 \rightarrow KNO_3 + H_2O} \)
Il “nitrato di potassio” deriva così dall’interazione fra idrossido di potassio e acido nitrico. Analogamente, con acido solforico si ottiene \( \mathrm{Na_2SO_4} \) da \( \mathrm{2\,NaOH} \) e \( \mathrm{H_2SO_4} \), con formazione di \( \mathrm{2\,H_2O} \).
Prefissi numerici nei composti
| Prefisso | Numero di atomi | Nota di interesse biochimico |
|---|---|---|
| Mono- | 1 | Utilizzato per indicare la presenza di un singolo atomo (es. monossido di carbonio, CO) |
| Di- | 2 | Compare in composti con due atomi identici o gruppi (es. diossido di carbonio, CO₂) |
| Tri- | 3 | Usato in molecole con tre sostituenti (es. triiodotironina, T₃, ormone tiroideo) |
| Tetra- | 4 | Tipico in molecole come tetrafosfato (ATP, fonte di energia cellulare) |
| Penta- | 5 | Indica cinque atomi/gruppi, come nel pentafosfato |
| Esa- | 6 | Esametafosfati e composti ciclici complessi |
| Epta- | 7 | Compare in strutture complesse come eptaidrati (es. solfato di magnesio eptaidrato) |
| Otta- | 8 | Presente in composti coordinati, come ossidi metallici ottaidrati |
| Nona- | 9 | Più raro, ma compare in complessi poliatomici |
| Deca- | 10 | Tipico nei decaidrati (es. borace decaidrato, Na₂B₄O₇·10H₂O) |
| Undeca- | 11 | Prefisso aggiunto: usato in chimica organica per catene di 11 atomi di carbonio |
| Dodeca- | 12 | Prefisso aggiunto: usato in biologia molecolare (es. dodecapeptidi, piccoli ormoni/proteine) |
| Tabella che riporta i prefissi greci impiegati per specificare la quantità di atomi in una molecola. | ||
Prefissi numerici nei composti
| Prefisso | Numero di atomi | Nota di interesse biochimico |
|---|---|---|
| Mono- | 1 | Utilizzato per indicare la presenza di un singolo atomo (es. monossido di carbonio, CO) |
| Di- | 2 | Compare in composti con due atomi identici o gruppi (es. diossido di carbonio, CO₂) |
| Tri- | 3 | Usato in molecole con tre sostituenti (es. triiodotironina, T₃, ormone tiroideo) |
| Tetra- | 4 | Tipico in molecole come tetrafosfato (ATP, fonte di energia cellulare) |
| Penta- | 5 | Indica cinque atomi/gruppi, come nel pentafosfato |
| Esa- | 6 | Esametafosfati e composti ciclici complessi |
| Epta- | 7 | Compare in strutture complesse come eptaidrati (es. solfato di magnesio eptaidrato) |
| Otta- | 8 | Presente in composti coordinati, come ossidi metallici ottaidrati |
| Nona- | 9 | Più raro, ma compare in complessi poliatomici |
| Deca- | 10 | Tipico nei decaidrati (es. borace decaidrato, Na₂B₄O₇·10H₂O) |
| Undeca- | 11 | Prefisso aggiunto: usato in chimica organica per catene di 11 atomi di carbonio |
| Dodeca- | 12 | Prefisso aggiunto: usato in biologia molecolare (es. dodecapeptidi, piccoli ormoni/proteine) |
| Tabella che riporta i prefissi greci impiegati per specificare la quantità di atomi in una molecola. | ||
Prefissi numerici nei composti
| Prefisso | Numero di atomi | Nota di interesse biochimico |
|---|---|---|
| Mono- | 1 | Utilizzato per indicare la presenza di un singolo atomo (es. monossido di carbonio, CO) |
| Di- | 2 | Compare in composti con due atomi identici o gruppi (es. diossido di carbonio, CO₂) |
| Tri- | 3 | Usato in molecole con tre sostituenti (es. triiodotironina, T₃, ormone tiroideo) |
| Tetra- | 4 | Tipico in molecole come tetrafosfato (ATP, fonte di energia cellulare) |
| Penta- | 5 | Indica cinque atomi/gruppi, come nel pentafosfato |
| Esa- | 6 | Esametafosfati e composti ciclici complessi |
| Epta- | 7 | Compare in strutture complesse come eptaidrati (es. solfato di magnesio eptaidrato) |
| Otta- | 8 | Presente in composti coordinati, come ossidi metallici ottaidrati |
| Nona- | 9 | Più raro, ma compare in complessi poliatomici |
| Deca- | 10 | Tipico nei decaidrati (es. borace decaidrato, Na₂B₄O₇·10H₂O) |
| Undeca- | 11 | Prefisso aggiunto: usato in chimica organica per catene di 11 atomi di carbonio |
| Dodeca- | 12 | Prefisso aggiunto: usato in biologia molecolare (es. dodecapeptidi, piccoli ormoni/proteine) |
| Tabella che riporta i prefissi greci impiegati per specificare la quantità di atomi in una molecola. | ||
Ioni poliatomici
| Ione | Nome |
|---|---|
| H₃O⁺ | Idrossonio |
| NH₄⁺ | Ammonio |
| NO₂⁻ | Nitrito |
| NO₃⁻ | Nitrato |
| SO₃²⁻ | Solfito |
| SO₄²⁻ | Solfato |
| HSO₄⁻ | Idrogenosolfato |
| OH⁻ | Idrossido |
| CN⁻ | Cianuro |
| PO₄³⁻ | Fosfato (ortofosfato) |
| HPO₄²⁻ | Idrogenofosfato |
| H₂PO₄⁻ | Diidrogenofosfato |
| CO₃²⁻ | Carbonato |
| HCO₃⁻ | Idrogenocarbonato |
| ClO⁻ | Ipoclorito |
| ClO₂⁻ | Clorito |
| ClO₃⁻ | Clorato |
| ClO₄⁻ | Perclorato |
| CH₃COO⁻ (o C₂H₃O₂⁻) | Acetato |
| MnO₄⁻ | Permanganato |
| Cr₂O₇²⁻ | Dicromato |
| CrO₄²⁻ | Cromato |
| O₂²⁻ | Perossido |
| SCN⁻ | Tiocianato |
| BO₃³⁻ | Borato |
| Principali cationi e anioni poliatomici. | |