Negli eucarioti l’espressione genica può essere controllata a più livelli
Definizione
I filamenti intermedi costituiscono una componente del citoscheletro con spiccata resistenza alla trazione, essenziale per limitare i danni da stiramento e distribuire gli stress meccanici all’interno dei tessuti. Il loro diametro, prossimo a 10 nm, è intermedio tra quello dei filamenti di actina e dei filamenti spessi di miosina osservati nel muscolo, da cui deriva la denominazione storica di “intermedi”. A differenza di altri elementi del citoscheletro, tollerano trattamenti estrattivi severi, come alte concentrazioni saline e detergenti non ionici (ad esempio Triton X-100), che destabilizzano microtubuli e microfilamenti; ciò riflette la loro peculiare architettura e l’intensa rete di interazioni laterali che li stabilizza. Nei metazoi sono diffusi nel citoplasma della maggior parte delle cellule, dove formano un reticolo continuo che si addensa in regione perinucleare e si estende verso la periferia cellulare. In corrispondenza delle giunzioni di adesione tra cellule, in particolare i desmosomi, i filamenti intermedi si ancorano alla membrana plasmatica contribuendo alla coesione dei tessuti soggetti a carico meccanico (Figura 05.27-01). Strutture affini li collegano anche alla matrice extracellulare nei punti di contatto detti emidesmosomi. All’interno del nucleo, le lamine nucleari — una classe specializzata di filamenti intermedi — organizzano una rete continua che sostiene l’involucro nucleare e coopera con complessi di collegamento nucleo-citoscheletro nel trasmettere forze tra citoplasma e nucleo. I filamenti intermedi sono espressi in famiglie tessuto-specifiche con funzioni meccaniche e regolative convergenti:
- cheratine negli epiteli, indispensabili per l’integrità dell’epidermide e degli annessi cutanei;
- vimentina e proteine correlate in cellule mesenchimali e endoteliali;
- desmina nel muscolo striato e liscio, dove contribuisce all’allineamento dei sarcomeri;
- neurofilamenti nei neuroni, cruciali per il calibro assonale;
- lamine A/C e B nel nucleo, costitutive della lamina nucleare.
Mutazioni in queste proteine causano fenotipi meccanici marcati; ad esempio, alterazioni di cheratine specifiche determinano fragilità epiteliale con bolle cutanee in seguito a traumi modesti, evidenziando il ruolo cardine dei filamenti intermedi nel sostenere i tessuti.
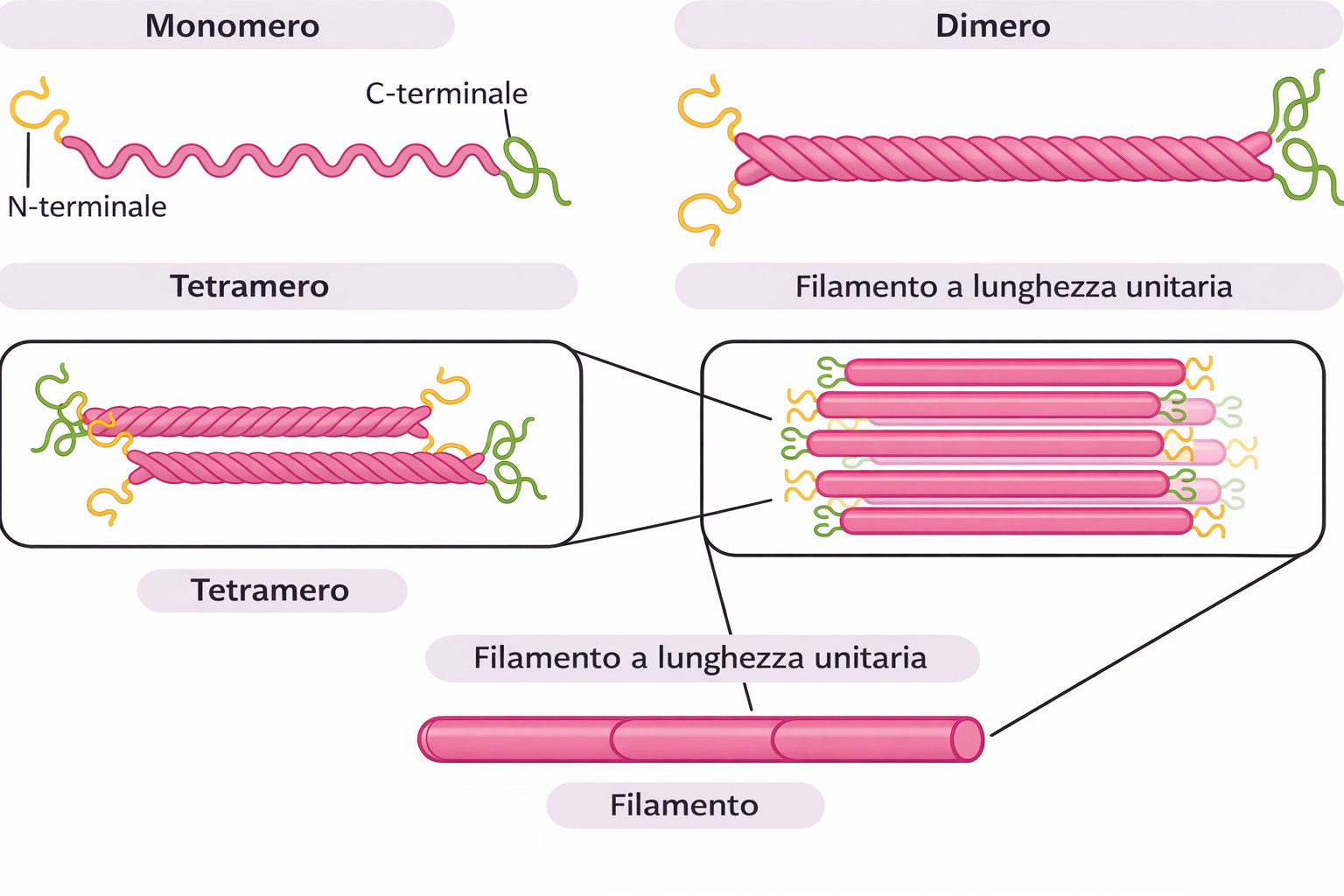
La forma e la funzione dei filamenti intermedi derivano dall’assemblaggio gerarchico di subunità proteiche fibrose in una struttura simile a una fune. Ogni subunità presenta tre regioni: una “testa” N-terminale e una “coda” C-terminale prevalentemente disordinate e accessibili, e un dominio centrale allungato a bastoncello con struttura ad α-elica. Quest’ultimo consente l’appaiamento di due monomeri in un dimero a coiled-coil stabile, nel quale le eliche si avvolgono reciprocamente (Figura 05.27-02). Due dimeri disposti in orientamento opposto (antiparallelo) si associano formando un tetramero laterale privo di polarità intrinseca (Figura 05.27-02). I tetrameri, unità solubili chiave dell’assemblaggio, si allineano testa-coda lungo l’asse del filamento e, simultaneamente, interagiscono l’uno con l’altro su più registri laterali (Figura 05.27-02). La maturazione del filamento comporta l’impacchettamento di più tetrameri in una struttura cilindrica di circa 10 nm di diametro, comparabile a una corda composta da molteplici trefoli avvolti e sfalsati (Figura 05.27-02). In sezione trasversale il filamento comprende diverse decine di catene α-elicoidali, con un’elevata densità di contatti che conferisce robustezza al traliccio proteico. L’orientamento antiparallelo dei dimeri all’interno dei tetrameri rende indistinguibili le due estremità del filamento, il quale risulta strutturalmente apolare. Questa caratteristica contrasta con la marcata polarità dei microtubuli e dei filamenti di actina, alla base del trasporto motore direzionale su quelle strutture. Nel caso dei filamenti intermedi, l’assemblaggio e il rimodellamento non richiedono legame a nucleotidi come ATP o GTP; la dinamica è modulata prevalentemente da interazioni non covalenti distribuite lungo i domini a bastoncello e da regolazioni post-traduzionali, come fosforilazioni delle regioni terminali, che possono favorire l’assemblaggio o la disassemblazione in risposta a segnali cellulari. La notevole resistenza alla trazione e la capacità di deformarsi elasticamente derivano dalla combinazione di:
- interazioni laterali multiple tra tetrameri, che ripartiscono lo stress lungo l’intero fascio;
- scorrimento controllato dei sottofili interni, che consente estensioni notevoli prima della rottura;
- teste e code variabili fra le diverse famiglie, esposte sulla superficie, che mediano agganci a complessi di adesione e a proteine ponte (ad esempio plectina) verso microtubuli e filamenti di actina.
La somiglianza nelle dimensioni e nell’organizzazione del dominio centrale tra le varie famiglie spiega la convergenza verso filamenti con diametro e architettura comparabili, mentre la diversità delle regioni terminali determina la specificità degli interattori e l’integrazione con organelli e membrane. In sintesi, l’impalcatura a “cavo” dei filamenti intermedi, unita alla loro apolarità e alle peculiari superfici di interazione, li rende insostituibili nel rinforzare la cellula e nell’assicurare continuità meccanica tra citoplasma, giunzioni di adesione e involucro nucleare, come illustrato nelle Figure 05.27-01 e 05.27-02.
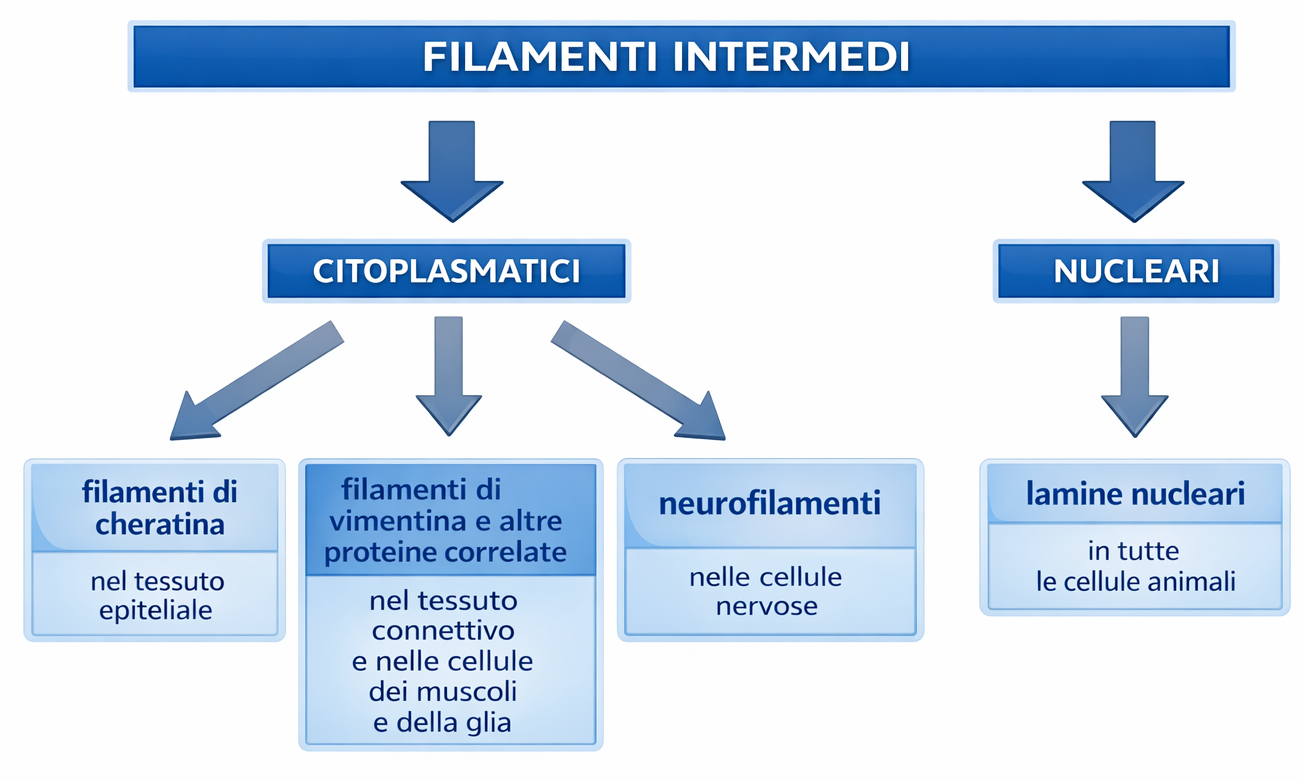
I filamenti intermedi, con diametro di circa \(10\,\text{nm}\), rappresentano l’ossatura più elastica del citoscheletro e sono particolarmente abbondanti nelle cellule esposte a sollecitazioni fisiche ripetute. Negli assoni dei neuroni, lunghi e sottili, costituiscono un sistema di rinforzo longitudinale; sono ricchi nelle fibre muscolari, dove contribuiscono all’integrità delle miofibrille, e negli epiteli, inclusa l’epidermide, in cui contrastano l’azione di forze di taglio. La loro capacità di allungarsi e di ripartire gli sforzi localizzati protegge cellule e membrane da rotture. Dal punto di vista meccanico, il contributo dei filamenti intermedi ricorda i materiali compositi rinforzati: come fibre robuste inserite in una matrice (per esempio, fibra di vetro o armatura in acciaio nel calcestruzzo) aumentano la resistenza alla trazione del materiale, così i filamenti intermedi, immersi nel citoplasma, conferiscono tenacità all’intero volume cellulare. Sulla base della composizione proteica e della localizzazione, si distinguono quattro grandi classi (Figura 05.27-03):
- filamenti di cheratina, caratteristici delle cellule epiteliali;
- filamenti di tipo vimentina e correlati, nelle cellule del connettivo, nelle cellule muscolari e nella glia;
- neurofilamenti, specifici dei neuroni;
- lamine nucleari, che formano un rivestimento continuo sul lato interno dell’involucro nucleare.
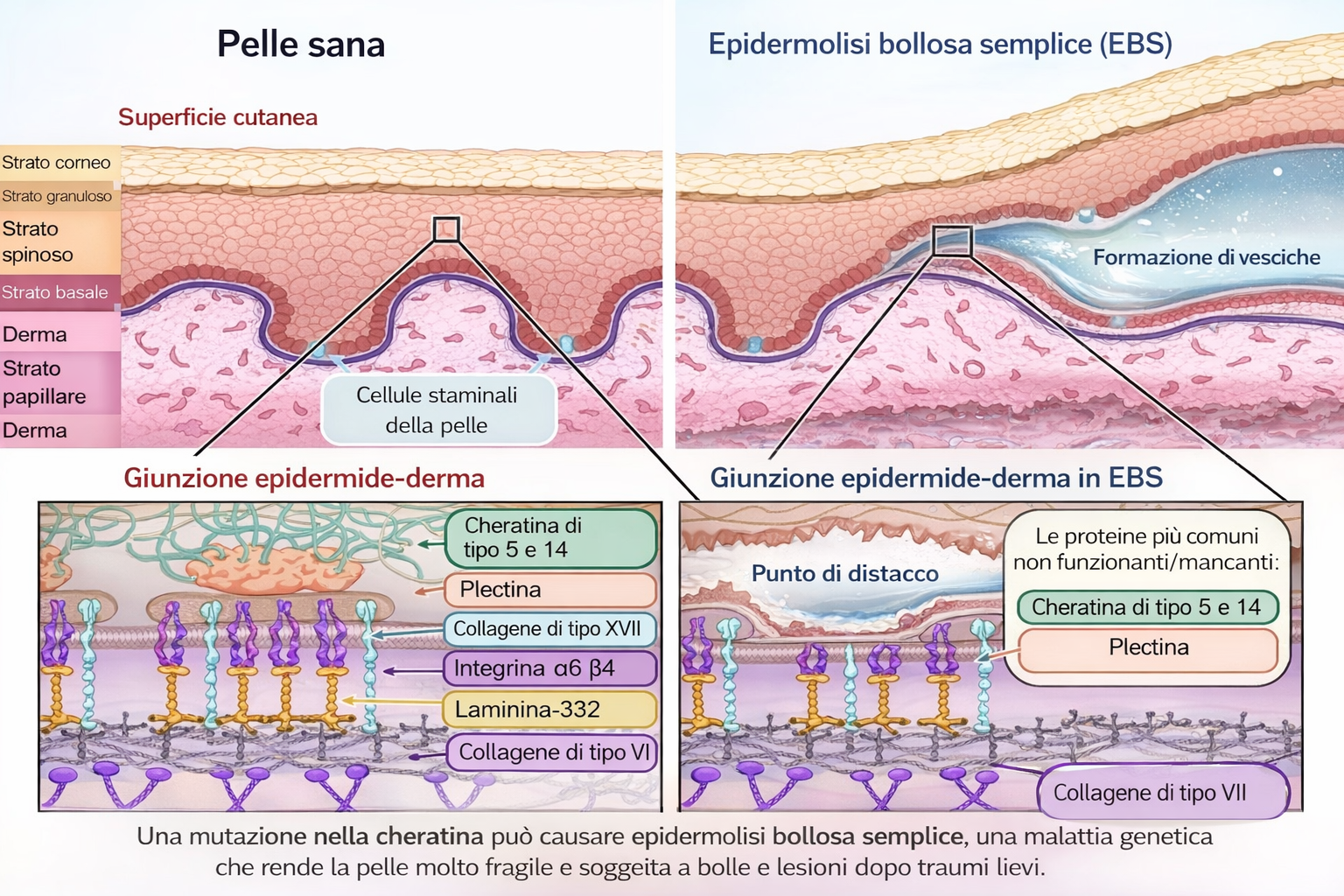
I primi tre gruppi risiedono nel citoplasma, mentre le lamine appartengono al nucleo. Tutti si assemblano per polimerizzazione di subunità proteiche omologhe che formano dapprima dimeri a coiled-coil, poi tetrameri sfalsati, quindi protofilamenti che si associano lateralmente nel filamento finale privo di polarità chimica. Tra le classi citoplasmatiche, le cheratine mostrano la maggiore diversità. Negli epiteli dei vertebrati coesistono combinazioni specifiche di cheratine di tipo I (acide) e di tipo II (basiche), che si assemblano in eterodimeri: l’epitelio della lingua, la cornea o il rivestimento intestinale possiedono “firme” cheratiniche distinte, mentre varianti altamente specializzate costituiscono peli, penne e unghie. In una cellula epiteliale, fasci di filamenti di cheratina attraversano il citoplasma e si ancorano ai desmosomi, giunzioni di adesione che collegano cellule adiacenti (Figura 05.27-01); alle estremità basali, nei tessuti aderenti alla membrana basale, le cheratine si collegano anche agli emidesmosomi. Le regioni globulari di testa e coda delle subunità cheratiniche sporgono dal filamento e mediano interazioni laterali con altre strutture cellulari, irrigidendo il reticolo complessivo che, a livello tissutale, distribuisce le tensioni quando, per esempio, la cute viene stirata. La rilevanza fisiologica di tale architettura è testimoniata dall’epidermolisi bollosa semplice: mutazioni in geni di cheratina dell’epidermide (tipicamente KRT5 o KRT14) compromettono l’assemblaggio dei filamenti intermedi e rendono la pelle estremamente fragile, così che anche un modesto trauma induce la formazione di bolle. Un fenotipo analogo si ottiene in topi transgenici che esprimono una cheratina mutante negli strati epidermici (Figura 05.27-04). Alterazioni dei neurofilamenti sono implicate in patologie del sistema nervoso. I neurofilamenti, composti da subunità come NF-L, NF-M e NF-H, determinano il calibro assonale e sostengono il trasporto lungo l’assone. Nella sclerosi laterale amiotrofica (SLA, malattia di Lou Gehrig) è stata osservata un’anomala accumulazione di neurofilamenti nei neuroni motori, sia nei corpi cellulari sia negli assoni. Tali depositi sono associati a disfunzioni del trasporto assonale, degenerazione delle proiezioni nervose e progressiva debolezza muscolare tipica della malattia.
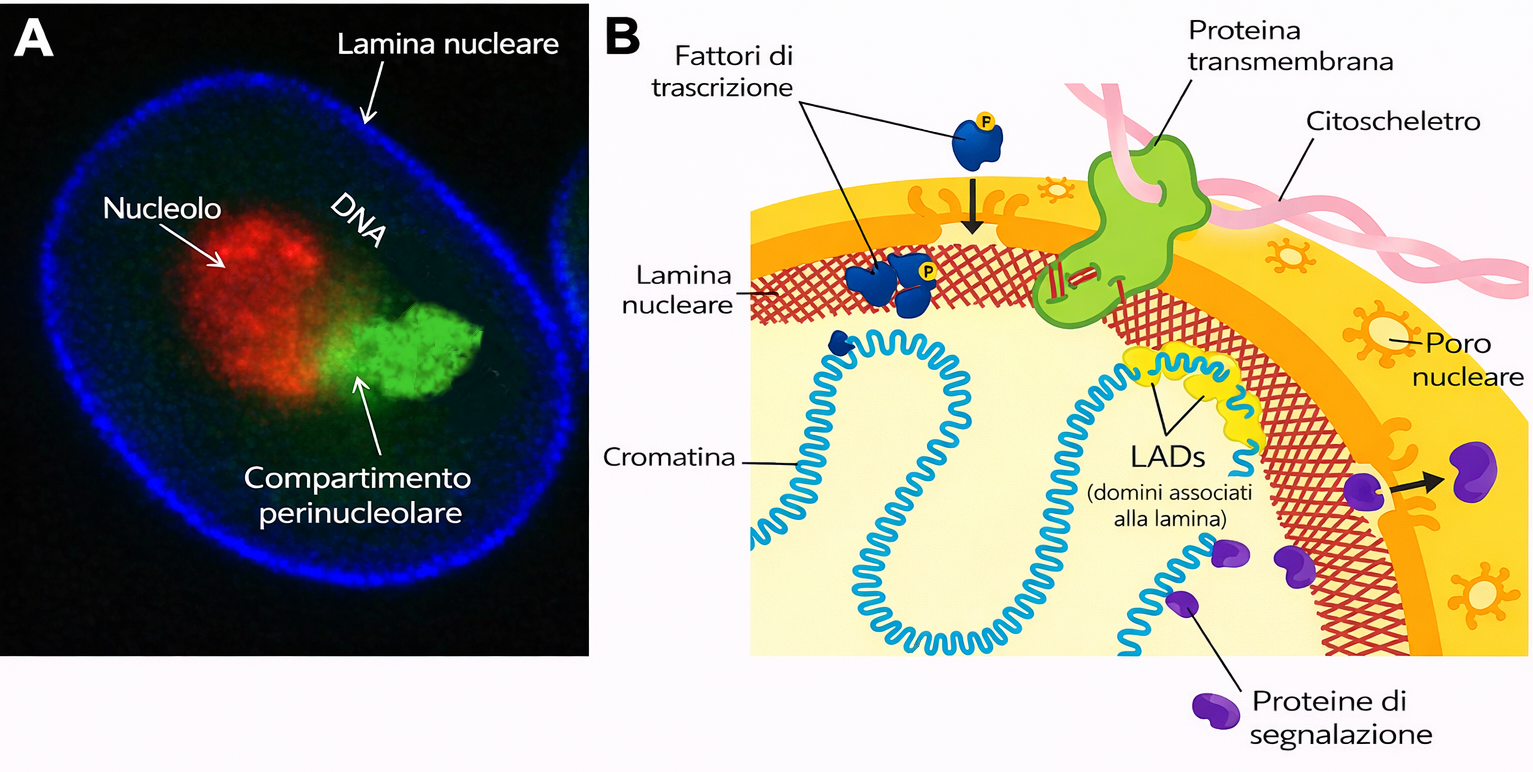
Mentre nel citoplasma i filamenti intermedi si organizzano in fasci simili a cavi, all’interno del nucleo formano una maglia bidimensionale adesa alla faccia interna della membrana nucleare interna (Figura 05.27-05). Questa struttura, detta lamina nucleare, è composta da lamine di tipo A/C e di tipo B (da non confondere con la laminina della matrice extracellulare) e funge da impalcatura per l’involucro nucleare, contribuendo insieme all’organizzazione della cromatina periferica. La lamina nucleare va incontro a cicli controllati di assemblaggio e disassemblaggio durante la mitosi. L’ingresso in mitosi è accompagnato da fosforilazione delle lamine da parte di chinasi mitotiche, in particolare Cdk1, che indebolisce i legami laterali tra tetrameri e determina la disgregazione del reticolo. Al termine della divisione, la defosforilazione a opera di fosfatasi favorisce la riassemblaggio della rete e la ricostituzione dell’involucro nelle cellule figlie. Anche vari filamenti intermedi citoplasmatici si disassemblano transitoriamente durante la mitosi, coordinando la riorganizzazione globale del citoscheletro. Mutazioni nelle lamine, specialmente nel gene LMNA, causano laminopatie, tra cui forme di progeria. Nella progeria di Hutchinson-Gilford, che rientra clinicamente nelle progerie, la produzione di una forma aberrante di lamina A (progerina) destabilizza il nucleo. I bambini affetti presentano pelle sottile e grinzosa, perdita precoce di capelli e denti e sviluppano con l’età alterazioni cardiovascolari severe (Figura 05.27-06). L’instabilità meccanica del nucleo e anomalie nell’organizzazione della cromatina possono compromettere la divisione cellulare, aumentare la morte cellulare e modificare l’espressione genica, contribuendo al quadro clinico. Poiché la lamina nucleare partecipa al posizionamento dei domini cromosomici e funge da piattaforma per complessi regolatori, le sue alterazioni si ripercuotono su processi quali il movimento dei cromosomi, la riparazione del DNA e la regolazione trascrizionale.
I filamenti intermedi sono ulteriormente stabilizzati da proteine accessorie che li fascicolano e li collegano ad altri elementi del citoscheletro. Tra queste, la plectina svolge un ruolo centrale: organizza i filamenti intermedi in fasci resistenti e crea connessioni con microtubuli, filamenti di actina e siti di adesione quali i desmosomi (Figura 05.27-07). Pur non essendo indispensabile per la nucleazione dei filamenti, la plectina è essenziale per integrare i vari reticoli citoscheletrici in un sistema meccanicamente continuo. Mutazioni del gene PLEC, che codifica la plectina, provocano una grave patologia multisistemica: i pazienti presentano una combinazione di caratteristiche riconducibili a epidermolisi bollosa semplice (difetto delle cheratine epidermiche), a distrofia muscolare (interessamento dei filamenti intermedi muscolari) e a degenerazione delle vie nervose periferiche (coinvolgimento dei neurofilamenti). Nei modelli murini, l’assenza di plectina determina morte precoce con bolle cutanee ed alterazioni delle musculature scheletrica e cardiaca, confermando la funzione cruciale di collegamento esercitata da questa proteina. La continuità meccanica si estende fino al nucleo attraverso complessi proteici che attraversano l’involucro nucleare e accoppiano i citoscheletri citoplasmatici all’interno nucleare. Tali complessi, organizzati in sistemi LINC (Linker of Nucleoskeleton and Cytoskeleton), comprendono proteine SUN sulla membrana nucleare interna e proteine KASH/Nesprine sulla membrana esterna; insieme, si collegano alla lamina nucleare e a cromosomi da un lato e a microtubuli, actina e filamenti intermedi dall’altro. La plectina e altre proteine di ancoraggio si interfacciano con questi complessi, stabilendo ponti che coordinano la posizione del nucleo, il suo movimento durante la migrazione cellulare, la trasduzione meccanica e l’architettura globale del citoscheletro.