Membrana cellulare: potenziale di riposo e trasporto passivo
Definizione
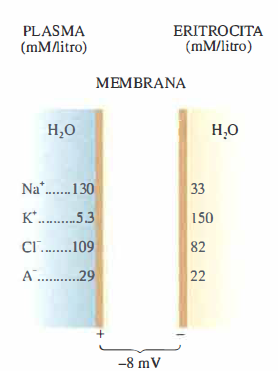
In questa sezione vengono esaminati gli equilibri elettrochimici che si instaurano attraverso la membrana cellulare. Come riferimento quantitativo ci concentreremo sulla membrana delle cellule muscolari dei Mammiferi, pur ricordando che il comportamento qualitativo è condiviso da molte altre cellule, sebbene con parametri differenti, come evidenziato, per esempio, dal confronto con gli eritrociti (Figura 06.13-03); (Tabella 06.13-01).
La membrana cellulare è un bilayer fosfolipidico in cui sono immerse proteine integrali e periferiche. Tra queste, i canali ionici costituiscono vie selettive che consentono a specifiche specie di attraversare la membrana. I canali possono essere modulati da variazioni del potenziale transmembrana (canali voltaggio-dipendenti) o dall’interazione con ligandi extracellulari o intracellulari (canali ligando-dipendenti, recettori ionotropici). A differenza dei canali, i trasportatori accoppiati e le pompe elettrogeniche realizzano trasferimenti contro gradiente utilizzando energia metabolica, e rientrano nei meccanismi di trasporto attivo.
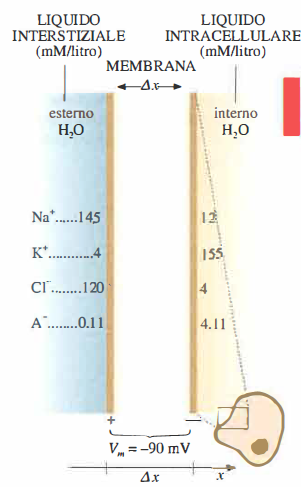
Il potenziale di riposo \(V_m\) è la differenza di potenziale elettrico tra citoplasma e liquido interstiziale in condizioni stazionarie. Esso si misura con microelettrodi ad alta impedenza e, nelle fibre muscolari dei Mammiferi, vale tipicamente circa −90 mV, con il lato citosolico negativo rispetto all’esterno.
Ai fini elettrici, i compartimenti intra- ed extracellulare sono ben approssimati da soluzioni acquose contenenti ioni monovalenti: Na⁺ e K⁺ come cationi, Cl⁻ e anioni organici impermeanti A⁻ come anioni. Altre specie possono essere trascurate per la presente analisi. I due compartimenti si comportano come conduttori elettrolitici, mentre il bilayer lipidico, per la sua scarsa permeabilità agli ioni, è un isolante con resistività elevata.
Il segno negativo del potenziale di riposo riflette un eccesso di cariche negative accumulate in prossimità della faccia interna della membrana. La quantità di carica separata è tuttavia piccolissima rispetto alla concentrazione totale di elettroliti, così che l’elettroneutralità globale dei fluidi è praticamente rispettata, come già discusso a proposito delle pressioni oncotiche.
Struttura funzionale, permeabilità e meccanismi passivi
Le concentrazioni ioniche ai due lati della membrana non coincidono (Figura 06.13-01). Per ciascuno ione permeante coesistono due contributi di trasporto, entrambi passivi:
- diffusione lungo il gradiente di concentrazione, che genera un flusso dalla regione più concentrata a quella meno concentrata;
- migrazione elettrica indotta dal campo transmembrana, che spinge gli ioni secondo il segno della loro carica e l’orientamento del potenziale.
Ulteriori motori passivi come gradienti di pressione idrostatica o differenze di pressione osmotica, nel caso della membrana cellulare, sono trascurabili in condizioni fisiologiche, potendosi assumere \(\Delta \pi \approx 0\) e \(\Delta p \approx 0\).
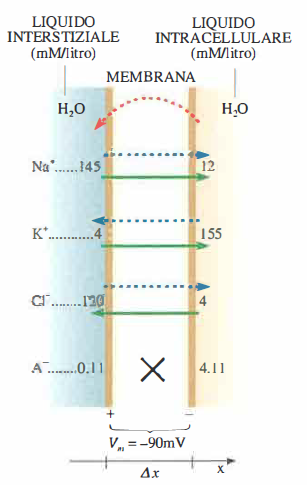
Il flusso diffusive e quello elettrico (Figura 06.13-02) per uno ione S possono essere rappresentati come:
\[J_{\text{DsM}} = -P_s \Delta[S],\]
\[J_{\text{EsM}} = \mu_s \{S\} \frac{V_e - V_i}{\Delta x} = -\mu_s \{S\} \frac{V_m}{\Delta x},\]
dove, per semplicità, distinguiamo soluti efficacemente permeanti (α = 1, ε = 1 oppure φ = 0) da soluti impermeanti, come gli anioni proteici A⁻ (φ = 1). La simbologia è la seguente:
\[\begin{array}{ll}V_i - V_e = V_m & \text{d.d.p. fra l'interno e l'esterno della membrana cellulare, chi-}\\\ &\text{mata potenziale di membrana } V_m;\\\{\text{S}\} & \text{concentrazione di soluto S nella membrana;}\\\Delta\{\text{S}\} & \text{differenza di concentrazione fra l'interno e l'esterno;}\\\Delta x & \text{spessore della membrana;}\\P_{\text{S}} & \text{permeabilità della membrana al soluto S, definita da:}\\& P = \alpha D_M / \Delta x \quad (14.16);\\\mu_{\text{S}} & \text{mobilità ionica dello ione S;}\\Z & \text{valenza dello ione S;}\\e & \text{carica elettrica elementare.}\end{array}\]
Poiché il coefficiente di diffusione nel bilayer (\(D_M\)) è ordini di grandezza inferiore rispetto a quello in soluzione, è lecito assumere che gli ioni si distribuiscano quasi istantaneamente in modo omogeneo all’interno di ciascun compartimento e che il collo di bottiglia del trasporto risieda nella membrana.
Ordini di grandezza delle permeabilità e regime stazionario
Per le cellule muscolari, le permeabilità tipiche sono:
\[P_{\text{Na}} = 10^{-8} \text{ cm/s} \quad \text{e} \quad P_{\text{K}} = 10^{-6} \text{ cm/s},\]
mentre una lamina d’acqua dello stesso spessore presenta valori di P di circa 10 cm/s per entrambi gli ioni. In diversi tipi cellulari \(P_{\text{Cl}}\) può collocarsi tra \(10^{-7}\) e \(10^{-6}\) cm/s, a seconda dell’espressione di canali per il cloro (dati in linea con manuali classici di fisiologia e biofisica: Guyton & Hall; Hille; Ganong).
In condizioni stazionarie il flusso netto di ogni specie attraverso la membrana è nullo e \(V_m\) rimane costante nel tempo. Come suggerito in (Figura 06.13-02), per K⁺ e Cl⁻ la diffusione e la migrazione elettrica sono tra loro antagoniste e possono raggiungere un bilanciamento, mentre per Na⁺ i due contributi spingono nella stessa direzione e, da soli, non consentono uno stato stazionario compatibile con il valore osservato di \(V_m\). Per gli anioni impermeanti A⁻, essendo assente il passaggio attraverso la membrana, la questione dell’equilibrio di flusso non si pone.
Equilibrio per singola specie: equazione di Nernst
Per una singola specie ionica permeante, in equilibrio elettrochimico, il potenziale elettrico ai due lati della membrana è descritto dall’equazione di Nernst, che deriva dall’uguaglianza tra il lavoro compiuto dal campo elettrico e la variazione di energia chimica dovuta al gradiente di concentrazione. In forma generale si scrive:
\[
V_1 - V_2 = V_m = \frac{RT}{zF} \ln\!\left(\frac{[S]_e}{[S]_i}\right)
\]
dove:
\(R\) è la costante dei gas (\(8.31\,\text{J·mol}^{-1}\text{·K}^{-1}\)),
\(T\) la temperatura assoluta (in kelvin),
\(z\) la valenza dello ione,
\(F\) la costante di Faraday (\(96487\,\text{C·mol}^{-1}\)),
\([S]_e\) e \([S]_i\) le concentrazioni esterna e interna dello ione considerato.
Applicando l’equazione di Nernst ai principali ioni coinvolti nei potenziali di membrana si ottengono i seguenti valori:
\[
V_{\text{Na}} = \frac{RT}{(+1)F} \ln\!\left(\frac{145}{12}\right)
= 26 \times 10^{-3} \ln\!\left(\frac{145}{12}\right)
= 0.066\,\text{V} = +66\,\text{mV}
\]
Per il sodio (Na⁺) il potenziale d’equilibrio risulta positivo, indicando una tendenza del sodio a entrare nella cellula (dove la concentrazione interna è minore).
\[
V_{\text{Cl}} = \frac{RT}{(-1)F} \ln\!\left(\frac{120}{4}\right)
= -26 \times 10^{-3} \ln\!\left(\frac{120}{4}\right)
= -0.090\,\text{V} = -90\,\text{mV}
\]
Per il cloro (Cl⁻), che è uno ione negativo, il potenziale risulta negativo, coerente con la sua tendenza a muoversi in direzione opposta a quella del sodio.
\[
V_{\text{K}} = \frac{RT}{(+1)F} \ln\!\left(\frac{4}{155}\right)
= 26 \times 10^{-3} \ln\!\left(\frac{4}{155}\right)
= -0.097\,\text{V} = -97\,\text{mV}
\]
Per il potassio (K⁺), il potenziale di Nernst risulta anch’esso negativo, poiché la concentrazione intracellulare è molto più elevata rispetto a quella extracellulare, e quindi il potassio tende a uscire dalla cellula per diffusione.
In sintesi, l’equazione di Nernst consente di calcolare il potenziale di equilibrio di ciascuno ione in funzione delle sue concentrazioni intra- ed extracellulari, e rappresenta il contributo fondamentale alla formazione del potenziale di membrana a riposo nelle cellule biologiche.
Questi risultati chiariscono il ruolo dei meccanismi passivi: per Cl⁻ si ottiene un potenziale vicino a quello misurato, segno che diffusione e campo elettrico si compensano. Per K⁺ si raggiunge un valore molto prossimo al potenziale di riposo, il che suggerisce che la permeabilità al potassio domina in condizioni basali. Per Na⁺, invece, l’equilibrio di Nernst richiederebbe \(V_m \approx +66\) mV, di segno opposto rispetto al valore a riposo: i soli meccanismi passivi non possono mantenere le concentrazioni osservate.
Contributo del trasporto attivo ed equilibrio stazionario
Per spiegare la discrepanza relativa al sodio è necessario introdurre un processo competitivo con i flussi passivi: il trasporto attivo (freccia rossa tratteggiata in (Figura 06.13-02). La pompa Na⁺/K⁺-ATPasi trasferisce, per ogni molecola di ATP idrolizzata, 3 Na⁺ verso l’esterno e 2 K⁺ verso l’interno. Questo ciclo è elettrogenico (produce un contributo aggiuntivo di alcuni mV all’iperpolarizzazione) e, soprattutto, conserva i gradienti transmembrana di Na⁺ e K⁺ nel lungo termine, rendendo possibile uno stato stazionario in cui i flussi passivi si bilanciano con i flussi attivi.
In termini quantitativi, la gran parte del valore di \(V_m\) nelle fibre muscolari deriva dalla maggiore permeabilità a K⁺ rispetto a Na⁺, mentre la Na⁺/K⁺-ATPasi fornisce un piccolo contributo diretto al potenziale e un grande contributo indiretto al mantenimento dei gradienti (testi di riferimento: Hille, Guyton & Hall, Ganong, Kandel).
Esempio alternativo di calcolo didattico
Per illustrare la sensibilità di \(V_{\text{Nernst}}\) alle concentrazioni, consideriamo valori diversi da quelli delle figure, ma fisiologicamente plausibili. Se \([\text{K}^+]_e = 5\) mM e \([\text{K}^+]_i = 140\) mM, allora a 37 °C:
\(V_{K} = \frac{RT}{F}\ln\frac{[\text{K}^+]_e}{[\text{K}^+]_i} = 26 \text{ mV} \cdot \ln\left(\frac{5}{140}\right) \approx -89 \text{ mV}\).
Se \([\text{Na}^+]_e = 140\) mM e \([\text{Na}^+]_i = 10\) mM, allora \(V_{Na} \approx +70\) mV; se \([\text{Cl}^-]_e = 110\) mM e \([\text{Cl}^-]_i = 10\) mM, con \(Z=-1\), si ottiene \(V_{Cl} \approx -66\) mV. Questi esempi, diversi dai numeri delle figure, conducono a conclusioni didatticamente equivalenti: K⁺ tende a fissare \(V_m\) a valori negativi, Na⁺ spingerebbe verso potenziali positivi, Cl⁻ si allinea a \(V_m\) stabilito dalle altre permeabilità.
Equazione di Goldman-Hodgkin-Katz (approfondimento)
Quando più specie ioniche sono simultaneamente permeanti, il potenziale di riposo può essere descritto dalla relazione di Goldman-Hodgkin-Katz (GHK), che pesa ciascuna concentrazione con la corrispondente permeabilità:
\[ V_m = \frac{RT}{F} \ln \left( \frac{P_{\text{K}}[\text{K}^+]_e + P_{\text{Na}}[\text{Na}^+]_e + P_{\text{Cl}}[\text{Cl}^-]_i}{P_{\text{K}}[\text{K}^+]_i + P_{\text{Na}}[\text{Na}^+]_i + P_{\text{Cl}}[\text{Cl}^-]_e} \right), \]
dove la posizione delle concentrazioni del cloro al numeratore e al denominatore è invertita rispetto ai cationi per via della valenza negativa. Se \(P_{\text{K}} \gg P_{\text{Na}}\) e \(P_{\text{K}} \gtrsim P_{\text{Cl}}\), \(V_m\) risulta vicino a \(V_K\), in accordo con i dati delle cellule muscolari. Questa formulazione, derivata dall’approssimazione di costanza del campo elettrico all’interno della membrana, è un riferimento standard in biofisica (Hille).
Il caso degli eritrociti
Negli eritrociti il potenziale a riposo è prossimo a −8 mV. Tale valore è sostanzialmente coerente con l’equilibrio di Nernst per Cl⁻ e HCO₃⁻, che sono relativamente più permeanti in questa membrana; al contrario, le concentrazioni di Na⁺ e K⁺ non sono in equilibrio e richiedono trasporto attivo per essere mantenute, analogamente a quanto discusso per il muscolo. Il ruolo del trasportatore anionico AE1 nello scambio Cl⁻/HCO₃⁻ contribuisce alla rapida equilibratione degli anioni e alla vicinanza di \(V_m\) al potenziale di equilibrio del cloro.
Osservazioni conclusive sui meccanismi passivi
In sintesi:
- la diffusione lungo gradiente e la migrazione elettrica sono sufficienti a spiegare l’equilibrio per Cl⁻ e in larga misura per K⁺;
- per Na⁺ i due flussi cooperano, impedendo il raggiungimento di uno stato stazionario compatibile con \(V_m\) senza l’intervento di trasporto attivo;
- gli anioni organici A⁻, impermeanti, possono mantenere concentrazioni differenti ai due lati della membrana senza violare l’elettroneutralità macroscopica;
- la piccolissima separazione di cariche che origina \(V_m\) è coerente con l’ipotesi di neutralità globale delle soluzioni e con l’elevata resistività del bilayer lipidico.
Questi principi sono validi, con differenze quantitative, anche per altri tipi cellulari, come indicato in (Figura 06.13-03) e (Tabella 06.13-01).
Lo schema di (Figura 06.13-02) illustra i contributi dei diversi meccanismi per ciascuno ione; la freccia tratteggiata rossa rappresenta il trasporto attivo necessario per il sodio. In condizioni stazionarie (J_{EaM} + J_{DsM} = 0.), il potenziale di membrana si mantiene costante nel tempo perché il bilancio tra flussi passivi e attivi è nullo per ogni specie.
| Ione | Formula (copia-incolla testuale) | Risultato |
|---|---|---|
| Sodio (Na⁺) | VmNa = (RT / ZF) · ln(130 / 33) = 26·10⁻³ · ln(130 / 33) | +36 mV |
| Cloro (Cl⁻) | VmCl = (26 / –1) · 10⁻³ · ln(109 / 82) | –7.4 mV |
| Potassio (K⁺) | VmK = (26 / +1) · 10⁻³ · ln(5.3 / 150) | –90 mV |
| Bicarbonato (HCO₃⁻) | VmHCO₃ = (26 / –1) · 10⁻³ · ln(29 / 22) | –7.2 mV |
Calcolo del potenziale di membrana negli eritrociti
Determinazione di Vm negli eritrociti utilizzando l’equazione di Nernst.
| Ione | Formula (copia-incolla testuale) | Risultato |
|---|---|---|
| Sodio (Na⁺) | VmNa = (RT / ZF) · ln(130 / 33) = 26·10⁻³ · ln(130 / 33) | +36 mV |
| Cloro (Cl⁻) | VmCl = (26 / –1) · 10⁻³ · ln(109 / 82) | –7.4 mV |
| Potassio (K⁺) | VmK = (26 / +1) · 10⁻³ · ln(5.3 / 150) | –90 mV |
| Bicarbonato (HCO₃⁻) | VmHCO₃ = (26 / –1) · 10⁻³ · ln(29 / 22) | –7.2 mV |
Calcolo del potenziale di membrana negli eritrociti
Determinazione di Vm negli eritrociti utilizzando l’equazione di Nernst.