L’RNA non codificante svolge molteplici ruoli nel controllo dell’espressione genica
Definizione
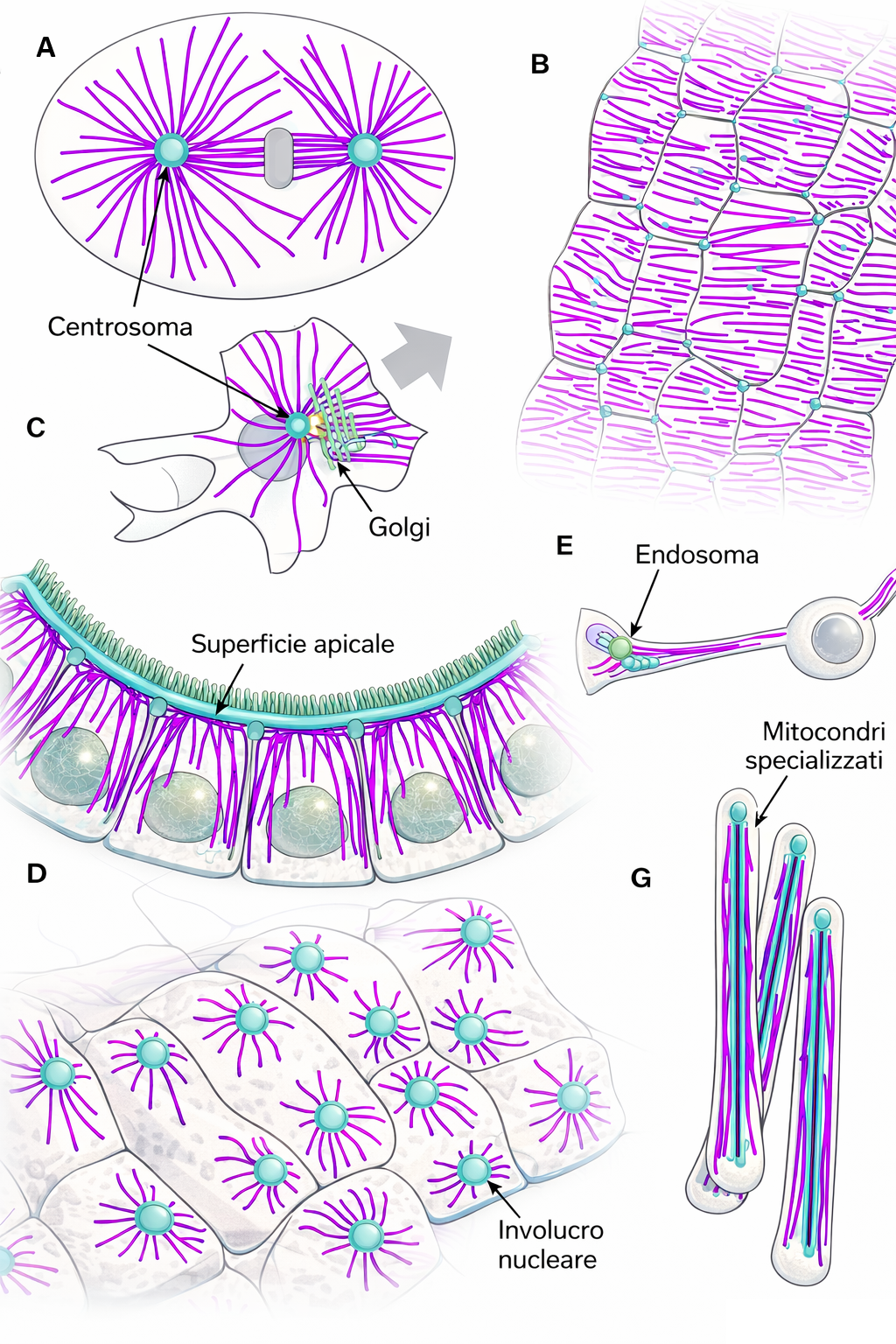
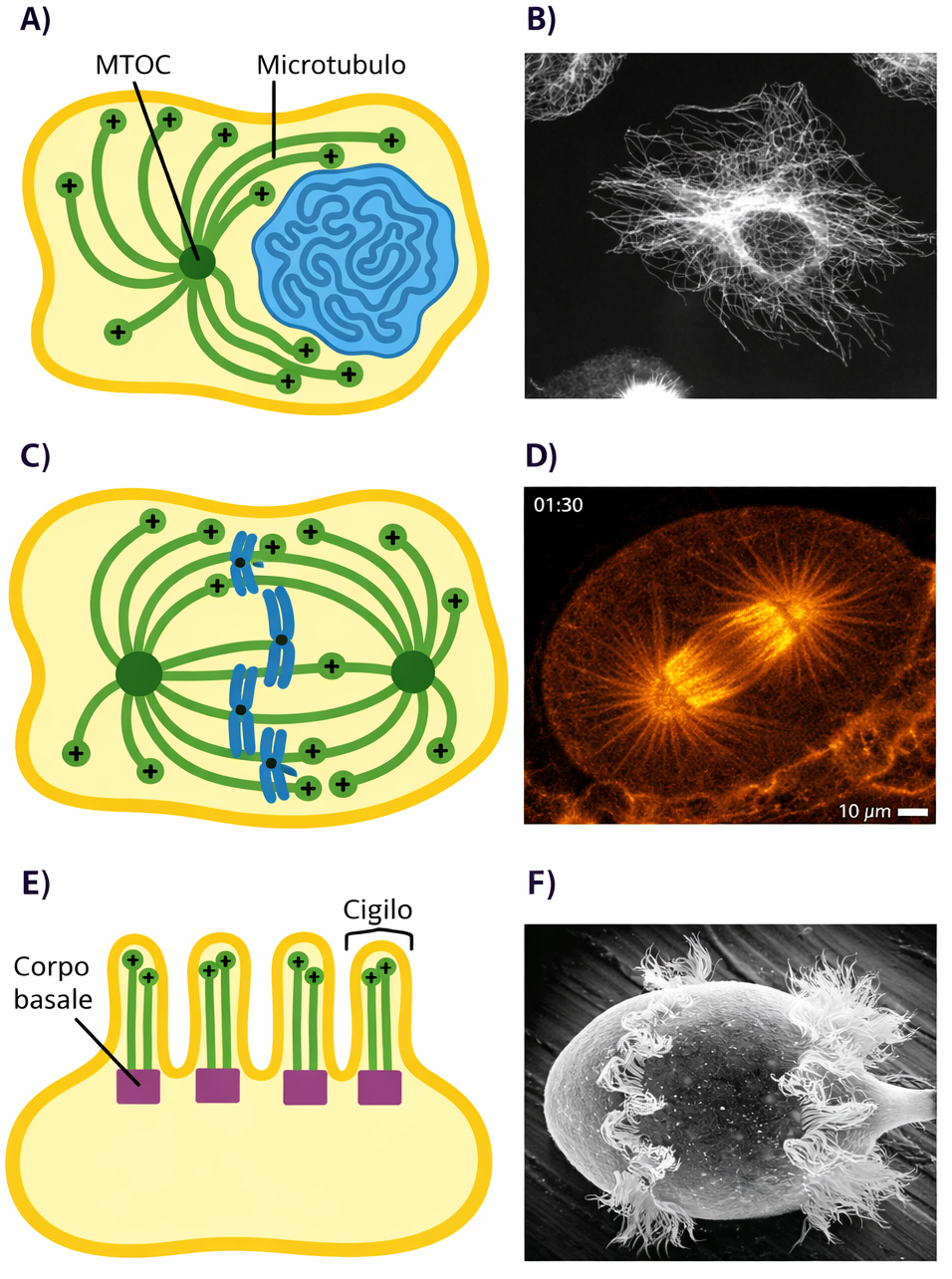
I microtubuli costituiscono il principale sistema di organizzazione spaziale delle cellule eucariotiche. Sono polimeri tubolari, lunghi e relativamente rigidi, capaci di rimodellarsi con rapidità: possono smontarsi in una regione del citoplasma e riformarsi altrove, riorientando in tempi brevi l’architettura cellulare. Nelle cellule animali, la polimerizzazione avviene perlopiù dal centrosoma, un complesso situato in posizione pericentrosomiale o vicino al nucleo, da cui si irradiano verso la periferia una fitta rete di microtubuli (Figura 05.28-01). Questa rete funge da sistema di “binari” per il trasporto guidato di vescicole, organuli e complessi macromolecolari, contribuendo al posizionamento degli organuli membranosi e alla definizione dell’asimmetria cellulare. Durante la mitosi, i microtubuli citoplasmatici vengono riconfigurati nel fuso mitotico, una macchina dinamica responsabile della segregazione equa dei cromosomi nelle due cellule figlie, in stretta coordinazione con la citodieresi (Figura 05.28-01). In altre circostanze, i microtubuli stabilizzano strutture persistenti, quali ciglia e flagelli (Figura 05.28-01), prolungamenti sottili che sporgono dalla superficie cellulare e generano movimento coordinato per la locomozione o per la movimentazione dei fluidi extracellullari; la loro impalcatura interna, altamente ordinata e stabile, si basa su fasci microtubulari associati in modo permanente a proteine motrici. È opportuno ricordare che i flagelli batterici, pur avendo funzione propulsiva, sono di natura molecolare e organizzazione completamente diverse. La funzione dei microtubuli come piattaforma organizzativa del citoplasma dipende dall’interazione con proteine accessorie, in particolare proteine motrici e regolatori dell’estremità, che indirizzano il traffico intracellulare e modulano la dinamica del polimero. Nelle sezioni seguenti vengono trattati la struttura e l’assemblaggio del polimero microtubulare, il ruolo del centrosoma come centro organizzatore e, infine, la particolare architettura ciliare e flagellare, in cui i microtubuli sono integrati con motori che alimentano il battito.
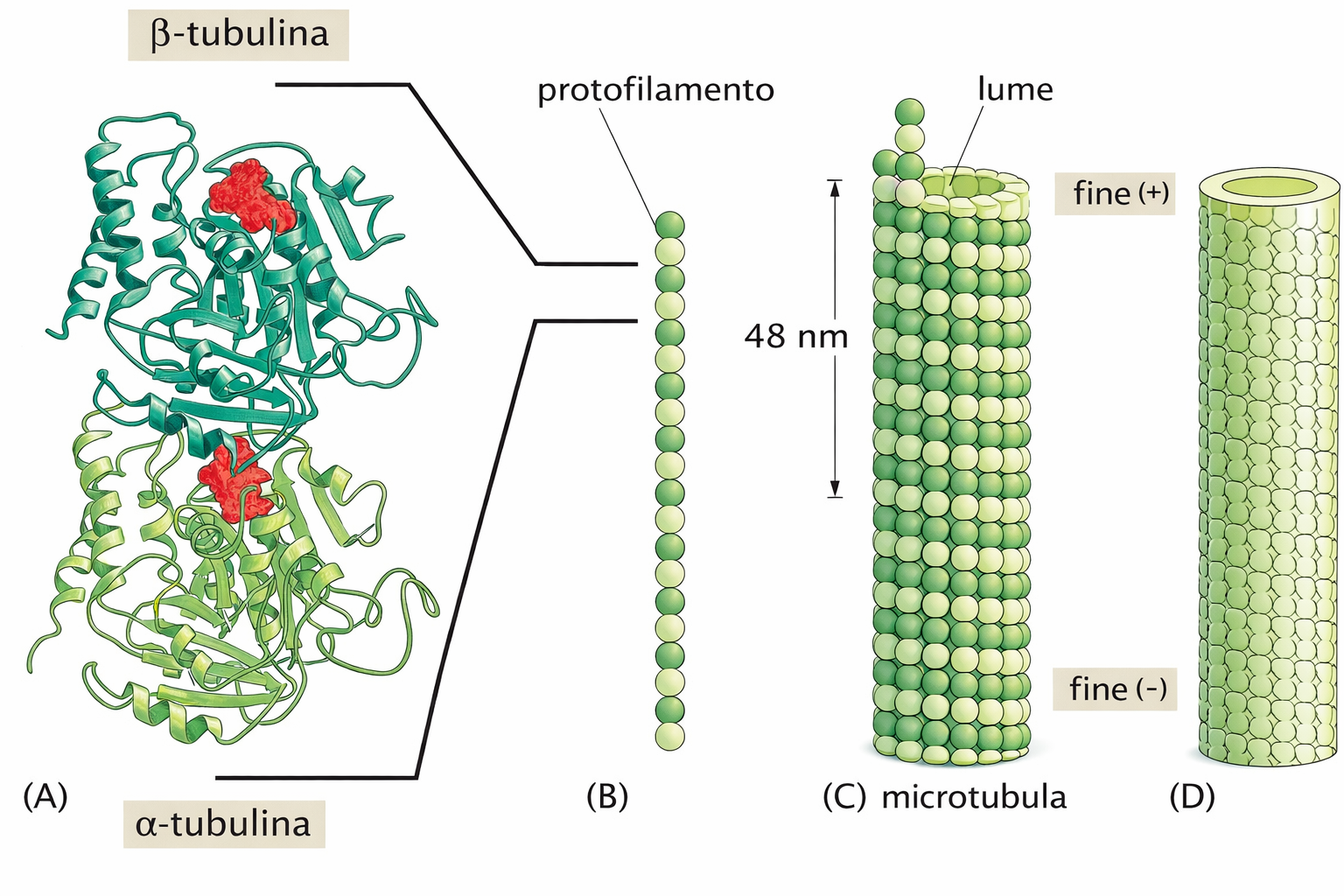
I microtubuli sono formati da eterodimeri di tubulina, composti da tubulina α e tubulina β, associati tramite legami non covalenti. Gli eterodimeri si allineano testa-coda lungo il lato longitudinale costituendo protofilamenti; tredici protofilamenti accostati lateralmente danno luogo al cilindro cavo caratteristico (Figura 05.28-02). La disposizione alternata delle subunità α e β lungo ogni protofilamento conferisce polarità intrinseca: un’estremità espone la tubulina β, l’altra la tubulina α. Poiché tutti i protofilamenti sono co-orientati, l’intero microtubulo presenta polarità strutturale definita, con un’estremità “più” (+) e una “meno” (−). Questa polarità ha rilievo funzionale. In condizioni in vitro, a concentrazioni adeguate di tubulina, l’allungamento avviene a entrambe le estremità, ma la velocità di crescita alla estremità più è maggiore: \( v_{+} > v_{-} \). Inoltre, la tubulina β lega GTP che, una volta incorporato nella rete, viene idrolizzato a GDP con rilascio di fosfato: \( \mathrm{GTP} \rightarrow \mathrm{GDP} + \mathrm{P_i} \). La differenza conformazionale tra il “mantello” di GTP e lo stato GDP contribuisce alla labilità del polimero e alla sua instabilità dinamica, con eventi alternati di crescita e disassemblaggio. La direzionalità del trasporto intracellulare è ancorata a questa asimmetria: molte chinesine avanzano verso l’estremità più, mentre le dineine citoplasmatiche procedono verso l’estremità meno, assicurando la distribuzione ordinata di cargo nel citoplasma. La polarità, dunque, non è un semplice tratto geometrico ma un principio organizzativo che determina dove e come i microtubuli si accrescono, come interagiscono con proteine motrici e quali percorsi di traffico definiscono all’interno della cellula.
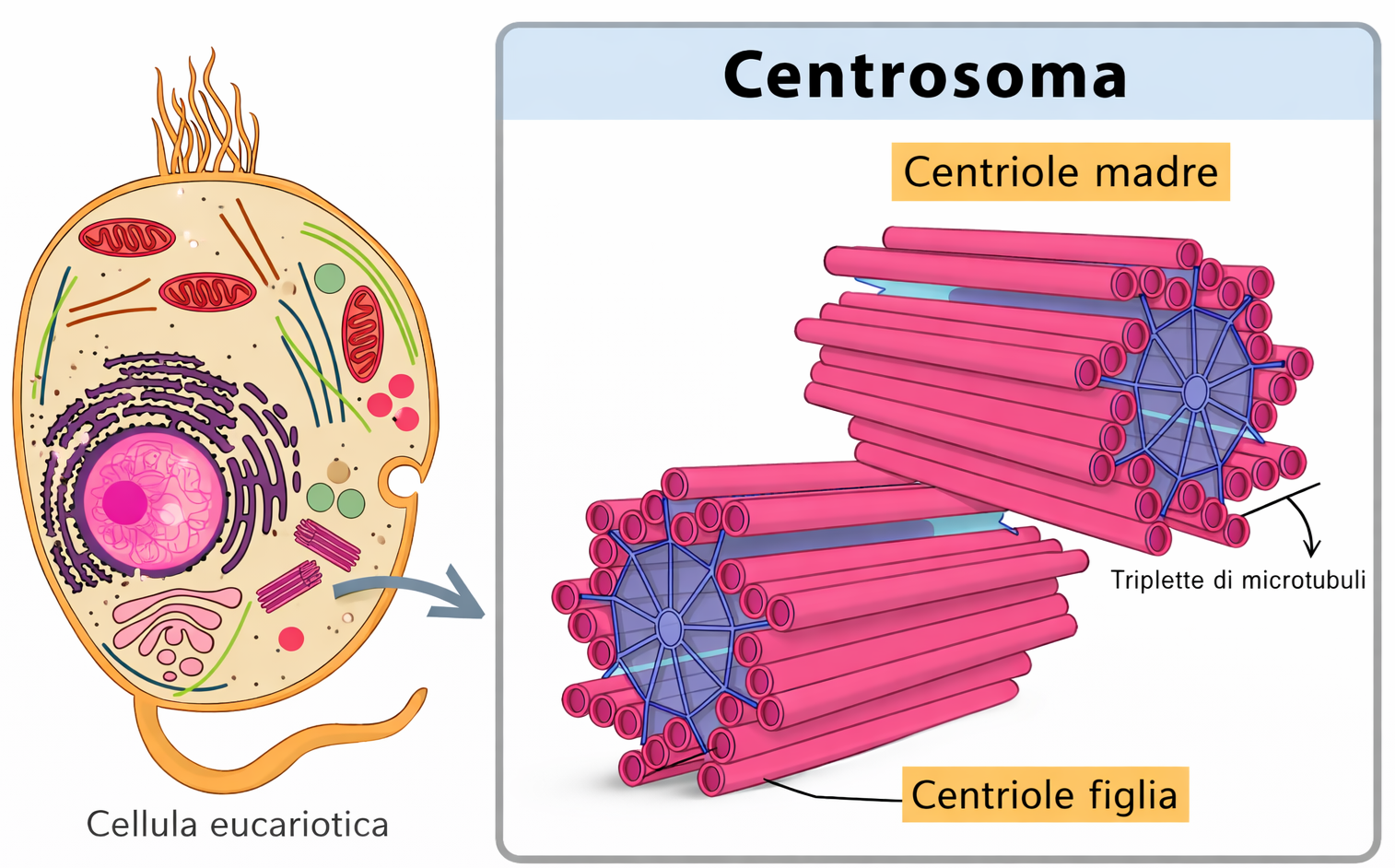
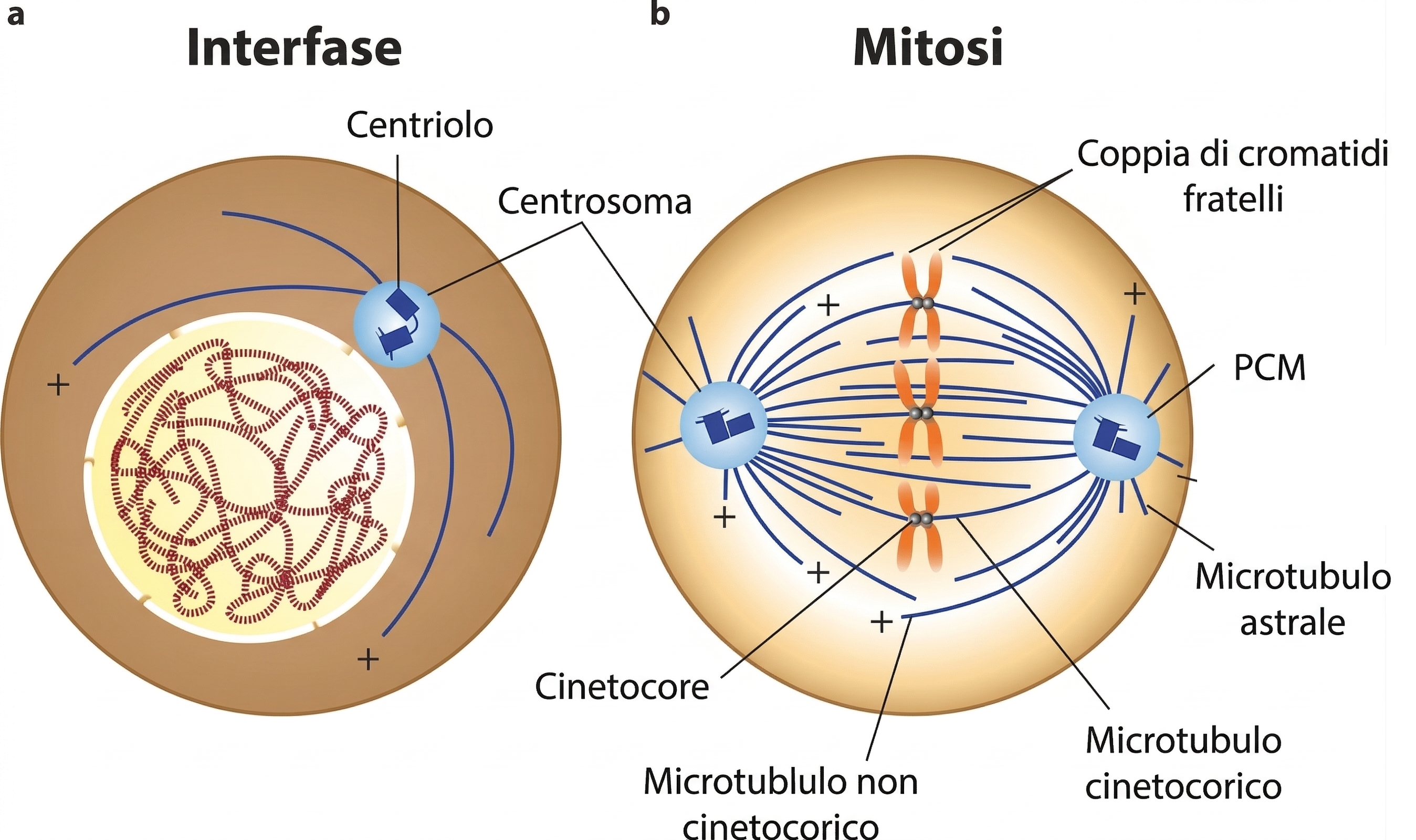
Dentro le cellule, l’avvio e l’orientamento dei microtubuli sono controllati da centri organizzatori che stabiliscono numero, posizione e direzione dei polimeri. Nelle cellule animali, il centrosoma, situato in prossimità del nucleo in interfase, produce un reticolo radiale di microtubuli che si estende in tutto il citoplasma (Figura 05.28-01). Strutturalmente, il centrosoma comprende una matrice proteica pericentriolare che circonda una coppia di centrioli. All’interno della matrice sono presenti numerosi complessi ad anello contenenti tubulina γ (γ-tubulina), che costituiscono i principali siti di nucleazione (Figura 05.28-03). L’orientamento con cui gli eterodimeri αβ si inseriscono su questi anelli fa sì che l’estremità meno del microtubulo resti ancorata al centrosoma, mentre l’estremità più sporge verso il citoplasma, dove avviene l’allungamento (Figura 05.28-03). I centrioli, disposti come cilindri di brevi microtubuli organizzati in corona (Figura 05.28-03), non sono necessari per la nucleazione dal centrosoma: gli anelli di tubulina γ, di per sé, sono sufficienti ad avviare la polimerizzazione. Sebbene la loro funzione in interfase rimanga in parte elusiva, i centrioli sono strutturalmente affini, se non coincidenti, con i corpuscoli basali che fanno da centri organizzatori per le ciglia e i flagelli (Figura 05.28-01). È rilevante inoltre che molte piante superiori siano prive di centrioli, a riprova che la nucleazione può essere realizzata da matrici proteiche alternative. Dal punto di vista energetico e cinetico, i siti di nucleazione abbassano la barriera iniziale alla formazione del polimero. L’assemblaggio “de novo” del primo anello di eterodimeri αβ è sfavorito, mentre l’aggiunta successiva a una struttura preformata è più agevole. In vitro, tubulina purificata può polimerizzare spontaneamente a concentrazioni elevate; in vivo, invece, la concentrazione libera di αβ-tubulina è mantenuta al di sotto della soglia necessaria per la nucleazione spontanea, permettendo alla cellula di confinare la nascita dei microtubuli ai complessi con tubulina γ:
- controllo spaziale: il posizionamento del centrosoma determina l’orientamento dei microtubuli e, di riflesso, la polarità cellulare e la disposizione di Golgi e reticolo endoplasmatico;
- regolazione numerica: la quantità di siti di nucleazione nella matrice pericentriolare modula la densità del reticolo microtubulare;
- ancora per l’estremità meno: l’ancoraggio stabilizza i microtubuli prossimi al centrosoma, lasciando dinamiche le estremità più distali;
- collegamento con strutture specializzate: i centrioli fungono da precursori dei corpuscoli basali nelle cellule ciliari e flagellate.
Questa organizzazione centralizzata rende conto dell’assetto radiale dei microtubuli in interfase e della loro rapida riconfigurazione in fuso mitotico quando la cellula entra in divisione.
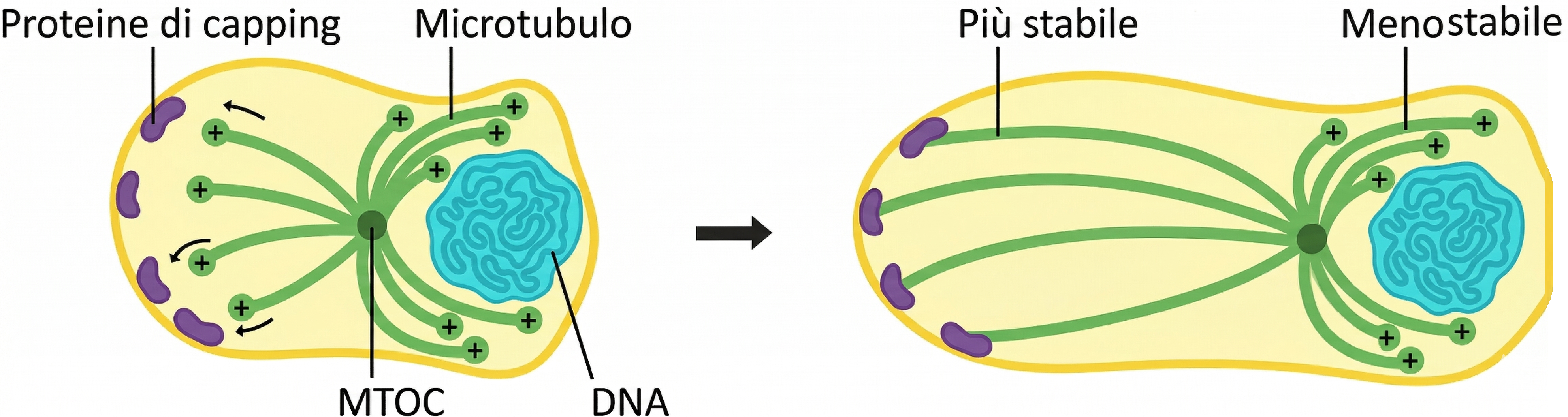
Dopo la nucleazione su complessi ad anello di tubulina γ (γ-TuRC) localizzati nei centri di organizzazione dei microtubuli, l’estremità più (plus-end) di un microtubulo tende a crescere per minuti, estendendosi verso la periferia per l’aggiunta sequenziale di dimeri di tubulina αβ. Questa fase può interrompersi bruscamente con una transizione stocastica a rapido accorciamento, seguita, talvolta, da un recupero dell’allungamento o dalla scomparsa completa del polimero e dalla sua sostituzione tramite una nuova nucleazione sullo stesso sito di γ-tubulina (Figura 05.28-04). La combinazione di crescita, perdita e riformazione definisce l’“instabilità dinamica”, proprietà che consente ai microtubuli di rimodellarsi con grande rapidità nello spazio cellulare. Nei citoplasmi eucariotici, il centrosoma e altri centri organizzatori proiettano costantemente microtubuli in molte direzioni, ritraendoli se non incontrano strutture stabilizzanti. Quando il plus-end si ancora a componenti cellulari distali — per esempio complessi corticali, membrane organellari o cinetocori — l’estremità risulta stabilizzata, inibendo la depolimerizzazione e creando un collegamento relativamente duraturo tra la regione bersaglio e il centrosoma (Figura 05.28-05). Questa modalità, spesso descritta come “ricerca casuale e cattura selettiva”, permette di stabilire architetture di microtubuli direzionate, utili a posizionare organelli e a conferire polarità alla cellula. La dinamica dei microtubuli alterna quattro stati fondamentali: crescita, catastrofe (inizio dell’accorciamento), accorciamento rapido e salvataggio (ripresa della crescita). Parametri quantitativi come velocità di crescita e accorciamento, frequenze di catastrofe e salvataggio, e distribuzione delle lunghezze determinano l’organizzazione globale della rete. In molte cellule, proteine associate all’estremità più (+TIPs) come EB1/EB3 favoriscono la stabilità del plus-end e coordinano l’interazione con membrane e motori; al contrario, fattori depolimerizzanti come kinesina-13 o stathmin aumentano la probabilità di catastrofe, accentuando il comportamento esplorativo.
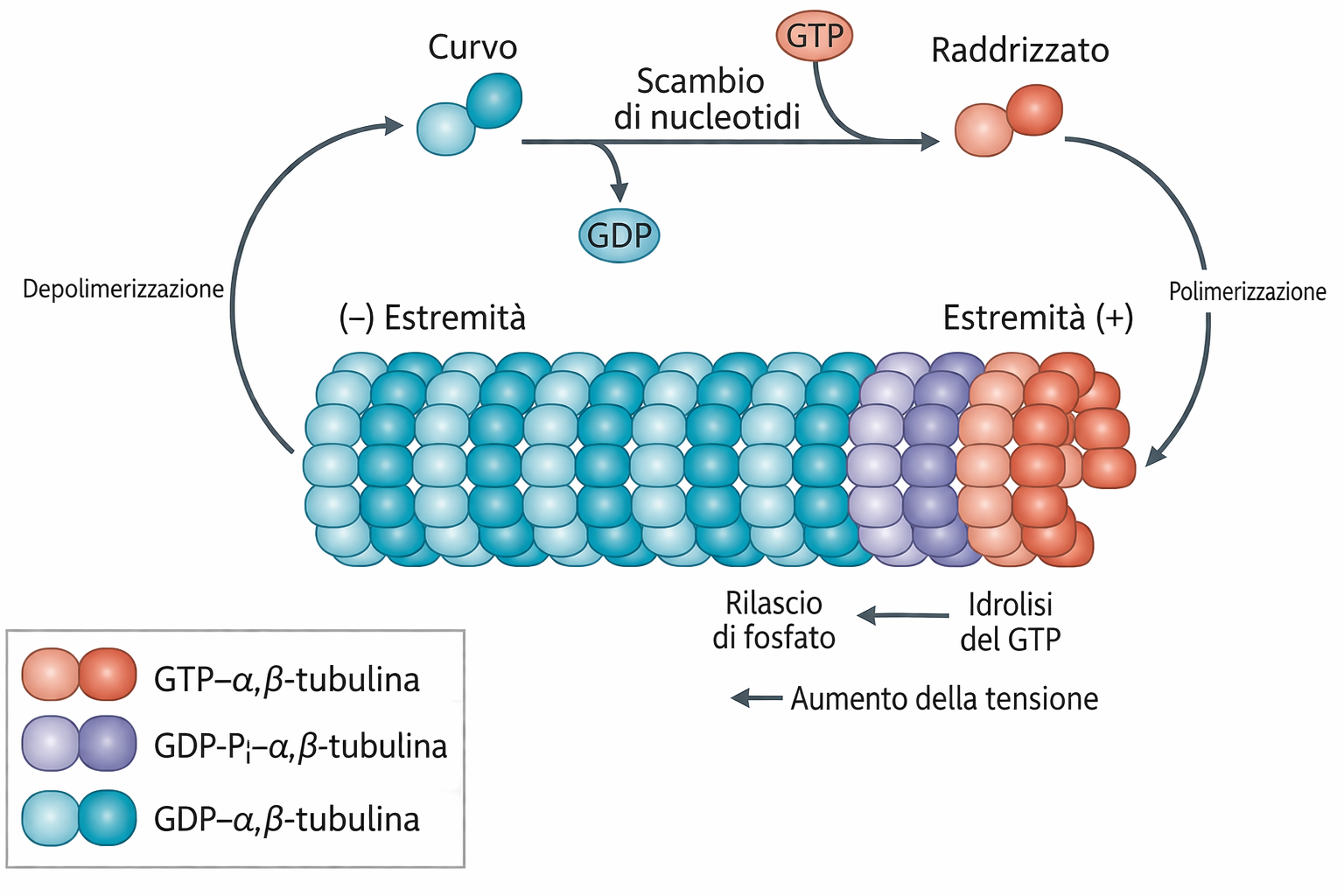
La base molecolare dell’instabilità dinamica risiede nella capacità dei dimeri di tubulina di legare e idrolizzare GTP. Le subunità libere sono cariche di GTP sulla tubulina β; dopo l’incorporazione nella parete del microtubulo, il GTP viene idrolizzato a GDP e fosfato inorganico. La forma GTP promuove un assetto più compatto e lineare dei protofilamenti, mentre la forma GDP favorisce una curvatura intrinseca che indebolisce le interazioni laterali e longitudinali nel reticolo. Quando l’inserzione di nuove subunità al plus-end è più rapida dell’idrolisi, si mantiene un “cappuccio a GTP”, una regione terminale stabilizzante costituita da tubulina-GTP o da intermedi strutturalmente simili. In tali condizioni il microtubulo continua ad allungarsi. Se invece l’idrolisi supera l’apporto di nuove subunità, il cappuccio si esaurisce; l’estremità esposta, composta da tubulina-GDP meno coesa, diventa instabile e tende a disassemblarsi, innescando la catastrofe (Figura 05.28-06). Una formulazione semplice del bilancio cinetico al plus-end è: crescita se \(k_{\mathrm{on}}[T] > k_{\mathrm{hyd}}\); catastrofe probabile se \(k_{\mathrm{on}}[T] \leq k_{\mathrm{hyd}}\), dove \(k_{\mathrm{on}}\) è la costante di associazione per la tubulina libera \([T]\) e \(k_{\mathrm{hyd}}\) la velocità effettiva di idrolisi/consumo del cappuccio. La depolimerizzazione, una volta iniziata, procede rapidamente perché la maggior parte del cilindro è composta da tubulina-GDP; l’accorciamento può arrestarsi se un evento di salvataggio ristabilisce un cappuccio a GTP, ad esempio grazie all’arrivo di nuove subunità o all’azione di proteine che promuovono l’aggiunta (come XMAP215). Le subunità rilasciate durante l’accorciamento rientrano nel pool citosolico, dove il GDP viene scambiato con GTP, ripristinando la competenza alla polimerizzazione. In molti fibroblasti una frazione consistente della tubulina — tipicamente attorno al 40–60% — è presente in forma solubile, costituendo una riserva pronta all’uso, mentre la parte restante è incorporata nei polimeri. Proteine che riconoscono lo stato strutturale del reticolo, come le EB, marcano il cappuccio e coordinano l’assemblaggio con altre componenti cellulari, integrando il controllo chimico (idrolisi del GTP) con regolazioni proteiche.
Piccole molecole che interferiscono con l’assemblaggio o il disassemblaggio della tubulina ridisegnano in pochi minuti l’architettura del citoscheletro con profonde conseguenze funzionali. Il fuso mitotico, reticolo specializzato di microtubuli che cattura e separa i cromosomi (Figura 05.28-01), dipende da un turnover continuo di subunità. Se tale flusso è bloccato in uno dei due sensi, l’apparato fusale collassa o diventa rigidamente immobile, impedendo la corretta segregazione cromosomica. Alcuni esempi indicativi includono:
- colchicina e composti correlati (p.es. colcemide): si legano ai dimeri di tubulina liberi, sequestrandoli e inibendone l’incorporazione; il risultato è la progressiva depolimerizzazione fino alla scomparsa del fuso, con arresto in mitosi;
- nocodazolo: riduce la polimerizzazione destabilizzando le interazioni tubulina-tubulina, con effetti simili alla colchicina sul fuso;
- alcaloidi della vinca (p.es. vinblastina, vincristina): si associano alla tubulina e ai terminali polimerici inducendo curvature e difetti del reticolo che favoriscono la depolimerizzazione;
- taxolo (paclitaxel) e altri taxani: stabilizzano i microtubuli già formati, impedendo la perdita di subunità; i polimeri possono ancora crescere, ma non accorciarsi, rendendo il fuso incapace di riorganizzarsi.
Pur agendo in modo opposto a livello molecolare, stabilizzanti e destabilizzanti convergono su un identico esito cellulare: bloccano la dinamica necessaria per la funzione del fuso e determinano l’arresto mitotico. L’inattivazione prolungata del fuso porta spesso a morte cellulare, un principio sfruttato in oncologia. Farmaci antimitotici che modulano i microtubuli, come taxani e alcaloidi della vinca, sono impiegati nel trattamento di diversi tumori solidi ed ematologici (Tabella 05.28-01). L’efficacia è controbilanciata da effetti avversi attribuibili all’interferenza con microtubuli non mitotici, ad esempio in neuroni e cellule endoteliali, e da fenomeni di resistenza legati a pompe di efflusso o alterazioni delle isoforme di tubulina. Questi aspetti sottolineano come il corretto funzionamento del fuso richieda sia la formazione sia la rimozione dei polimeri, e come la regolazione fine della dinamica sia essenziale per la fisiologia cellulare.
Composti che modulano i microtubuli
| Sostanza | Azione sui microtubuli |
|---|---|
| Taxolo | Si lega ai microtubuli già formati e ne stabilizza la struttura, impedendone la depolimerizzazione |
| Colchicina, Demecolcina | Interagiscono con le subunità di tubulina e bloccano l’assemblaggio dei microtubuli |
| Vinblastina, Vincristina | Si legano alla tubulina inibendo la polimerizzazione e interferendo con la formazione del fuso mitotico |
| Tabella che riassume i principali farmaci e le sostanze naturali in grado di influenzare la dinamica dei microtubuli, alterandone la polimerizzazione e la stabilità. Questi composti sono impiegati sia come strumenti di ricerca sia come agenti chemioterapici, poiché interferiscono con la divisione cellulare e con la motilità intracellulare. | |
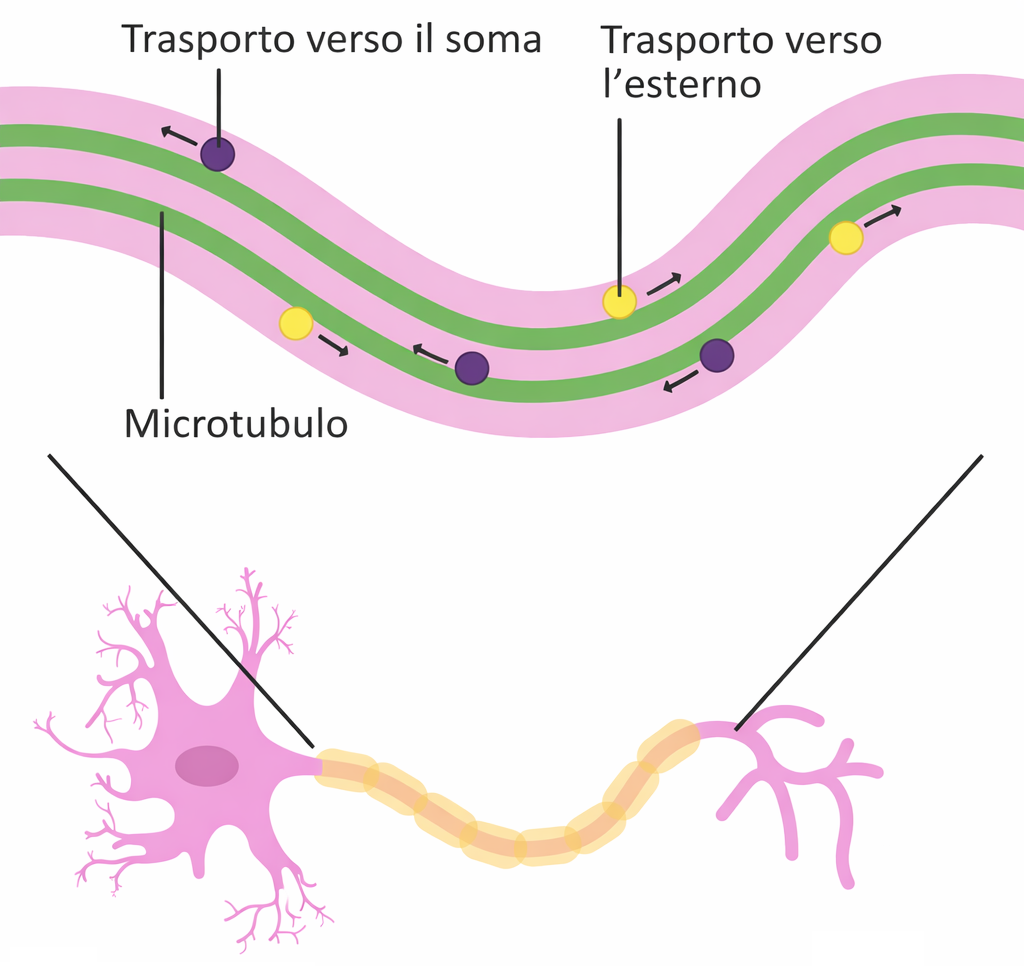
I microtubuli modulano la propria instabilità dinamica per adattarsi allo stato fisiologico della cellula. All’inizio della mitosi, per esempio, aumentano la frequenza di “catastrofi” e riducono i periodi di crescita, così da riorganizzarsi rapidamente nel fuso mitotico. Al contrario, nelle cellule differenziate con morfologia stabile, proteine associate ai microtubuli riducono l’instabilità dinamica legandosi alle estremità o al fianco dei protofilamenti e stabilizzandoli contro la depolimerizzazione. In questo modo i microtubuli stabilizzati contribuiscono a preservare l’architettura intracellulare. Le cellule animali differenziate presentano tipicamente una marcata polarità morfofunzionale. Nelle cellule nervose, ad esempio, l’assone emerge da un lato mentre i dendriti si ramificano dall’altro; nelle cellule secretorie, l’apparato di Golgi occupa una regione interna vicina al centrosoma, spesso orientata verso il sito di secrezione. Questa polarità riflette un sistema microtubulare organizzato che posiziona gli organuli e traccia “corsie preferenziali” per il traffico intracellulare. Nell’assone, i microtubuli sono allineati con i poli coerenti e le estremità più orientate distalmente (Figura 05.28-07), consentendo trasporto anterogrado e retrogrado di organuli, vescicole e complessi macromolecolari lungo piste polarizzate. I carichi assonali possono avanzare con velocità elevate: un valore tipico è circa 1 µm/s, pari a ~8,6 cm al giorno. Il confronto con la diffusione è istruttivo: il tempo di diffusione scala con il quadrato della distanza, secondo \( t \approx \frac{L^{2}}{2D} \). Per una proteina con coefficiente di diffusione citoplasmatico dell’ordine di 10^{-7} cm^{2}/s, coprire distanze centimetriche richiederebbe tempi dell’ordine degli anni, a riprova di quanto il trasporto su microtubuli sia più rapido ed efficiente. I microtubuli non agiscono isolatamente. Proteine accessorie regolano nucleazione, stabilità e interazioni con altri componenti cellulari: alcune contrastano la depolimerizzazione, altre collegano i microtubuli ad organuli o ad altri filamenti del citoscheletro. Cruciali sono anche le proteine motrici, che sfruttano l’energia dell’ATP per trasportare selettivamente i carichi lungo i microtubuli.
Nel citoplasma in vivo, vescicole e organuli compiono spostamenti saltatori, caratterizzati da fasi di moto rapido intervallate da pause, nettamente diversi dal moto browniano casuale. Tali spostamenti orientati sono generati da proteine motrici che percorrono filamenti polari: microtubuli e, in molte situazioni, filamenti di actina. In entrambi i casi, cicli ripetuti di idrolisi di ATP alimentano passi direzionali lungo il polimero. Sui microtubuli operano principalmente due famiglie di motori: le chinesine, che in genere avanzano verso l’estremità più (lontano dal centrosoma e dal corpo cellulare) (Figura 05.28-07), e le dineine, dirette verso l’estremità meno (verso il centro della cellula) (Figura 05.28-07). Molte chinesine e dineine sono dimeri con due teste globulari ATPasiche e una coda unica (Figura 05.28-08); una sottoclasse specializzata, le dineine ciliari, presenta caratteristiche strutturali proprie. Le teste interagiscono con il reticolo di legame dei microtubuli in modo stereospecifico, determinando l’orientamento e la direzione del passo; le code, spesso tramite adattatori, si connettono a carichi specifici, come vescicole o organuli, definendo la “carta d’imbarco” del motore. Il ciclo meccanochimico prevede l’alternanza di legame, idrolisi dell’ATP, rilascio dei prodotti e cambi conformazionali coordinati tra le due teste, che producono un avanzamento processivo lungo il microtubulo (Figura 05.28-08). Le chinesine compiono tipicamente passi di ~8 nm, pari alla periodicità dei dimeri di tubulina, mentre le dineine, assistite da complessi accessori, mostrano passi di ampiezza più variabile. L’efficienza e la direzionalità del trasporto risultano così dalla combinazione di polarità del polimero, ciclo dell’ATP e specificità delle interazioni motore–carico.
La disposizione degli organuli membranosi nelle cellule eucariote dipende in larga misura da microtubuli e proteine motrici. In molte cellule animali il reticolo endoplasmatico (RE) si estende fino alla periferia, mentre l’apparato di Golgi si raccoglie in prossimità del centrosoma (Figura 05.28-09). Le membrane del RE, continue con l’involucro nucleare, si proiettano verso la periferia seguendo i microtubuli che irradianno dal centrosoma. Chinesine associate alla superficie citosolica del RE, attraverso specifici recettori, trascinano queste membrane verso le estremità più, distendendo e mantenendo la rete tubulare (Figura 05.28-09). In parallelo, dineine citoplasmatiche collegate alle membrane del Golgi lo trainano verso le estremità meno dei microtubuli, posizionandolo nella regione perinucleare (Figura 05.28-09). Questa cooperazione direzionale crea e stabilizza differenze regionali tra compartimenti di membrana, essenziali per il funzionamento cellulare. Se i microtubuli vengono depolimerizzati con agenti come la colchicina, la rete del RE, ancorata all’involucro nucleare, collassa verso il centro, mentre il Golgi, privo di connessioni fisiche stabili con altri organuli, si frammenta in vescicole che si disperdono nel citoplasma. Una volta rimosso l’inibitore, la ricostituzione del reticolo microtubulare consente alle proteine motrici di ripristinare la localizzazione originaria di entrambi i compartimenti.
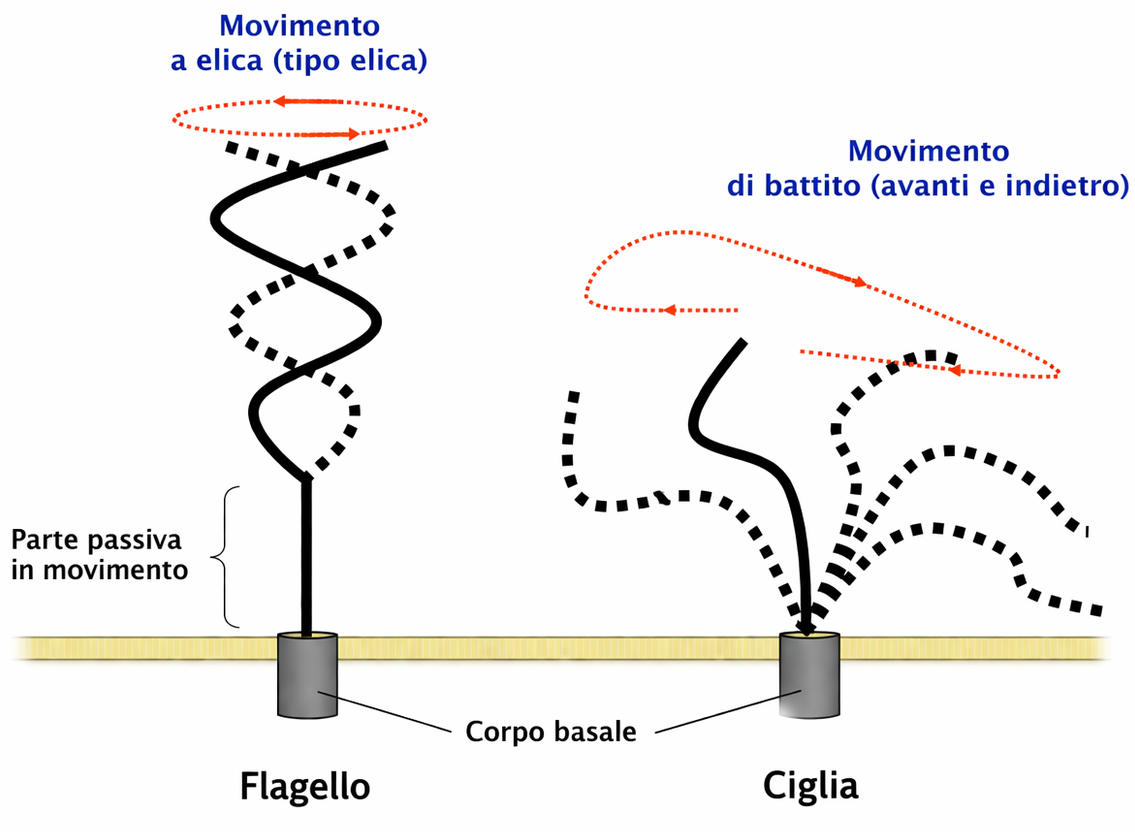
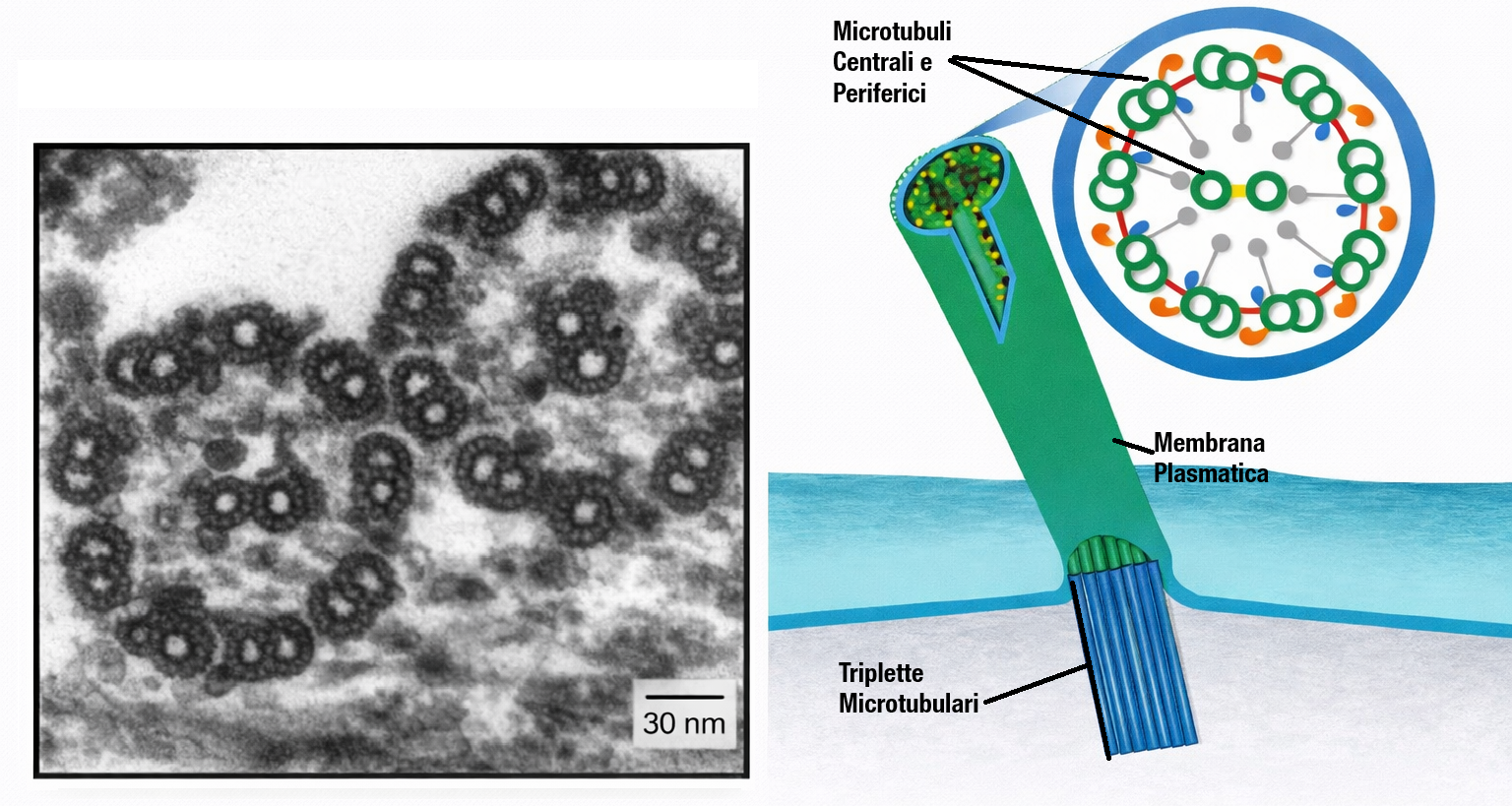
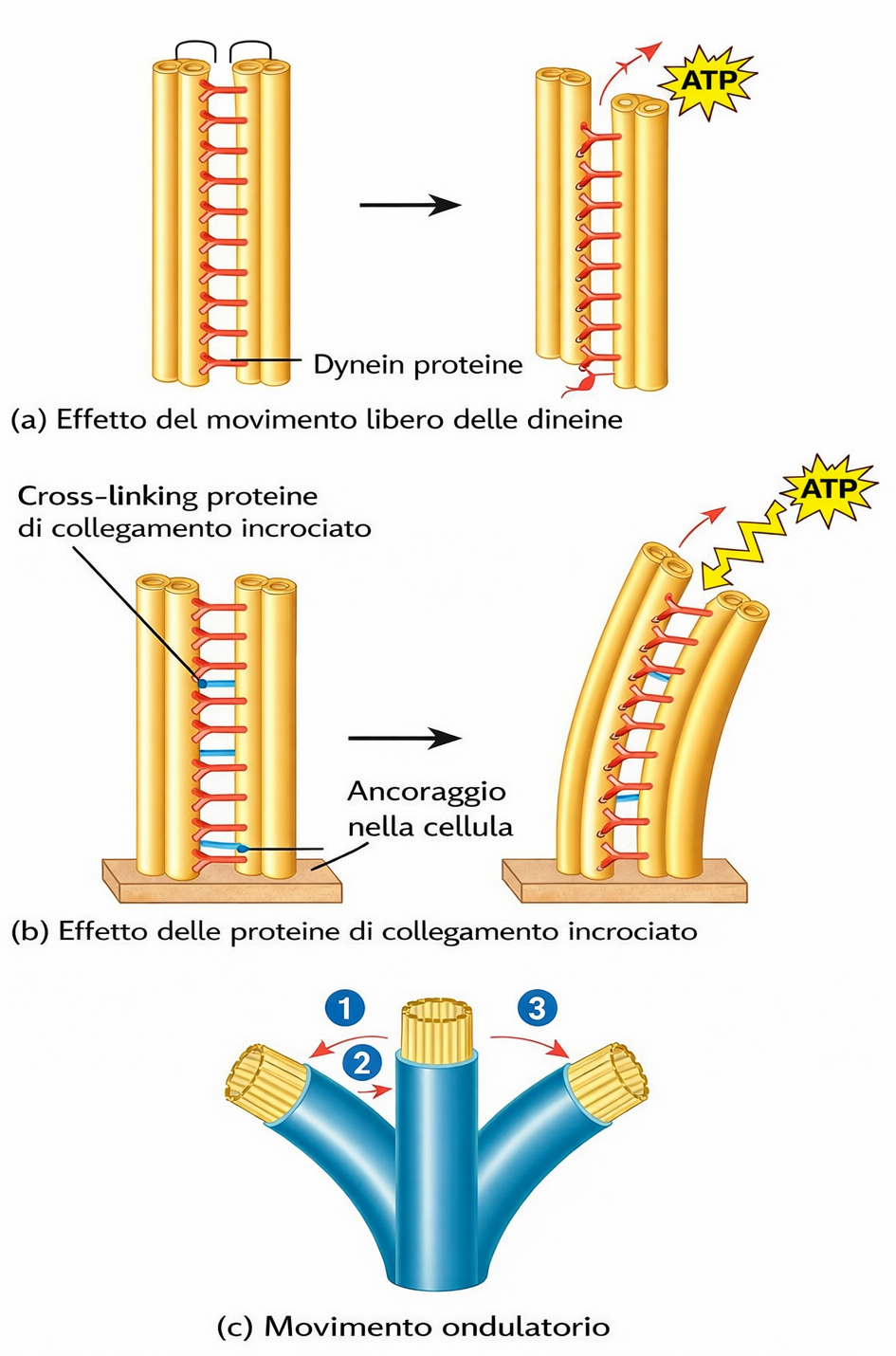
Numerose strutture polari sfruttano microtubuli stabilizzati come elementi portanti. Tra queste spiccano ciglia e flagelli, appendici rivestite da membrana che emergono dalla superficie di diverse cellule eucariote. Ogni ciglio, del diametro di ~0,25 µm, contiene un fusto centrale di microtubuli stabili organizzati in fascio; esso si allunga da un corpuscolo basale situato nel citoplasma, che funge da centro organizzatore (Figura 05.28-01). Le ciglia eseguono una sequenza di colpo efficace e colpo di recupero che muove il liquido adiacente o sposta l’intera cellula. Alcuni protozoi sfruttano le ciglia per convogliare particelle nutritive o per la locomozione. Nell’epitelio respiratorio umano (Figura 05.28-10), un numero elevatissimo di ciglia — oltre un miliardo per centimetro quadrato — spinge verso la faringe il muco che intrappola polveri e cellule desquamate; il materiale viene poi deglutito ed eliminato. In modo analogo, le ciglia dell’ovidotto generano flussi che favoriscono il transito degli ovociti verso l’utero. Ogni ciglio si comporta come un minuscolo remo che, con un ciclo asimmetrico, determina correnti di fluido sulla superficie cellulare (Figura 05.28-11). I flagelli, tipicamente più lunghi, azionano la propulsione di spermatozoi e numerosi protozoi. A differenza delle ciglia, invece di generare correnti locali, trasmettono lungo l’asse un’onda di flessione che avanza la cellula nel mezzo liquido (Figura 05.28-12). L’ultrastruttura dei microtubuli assonemali differisce da quella citoplasmatica. In sezione trasversale si osservano nove doppi microtubuli periferici disposti a corona attorno a una coppia centrale: la classica architettura “9 + 2” (Figura 05.28-13), conservata nella maggior parte di ciglia e flagelli eucariotici. I microtubuli sono corredati da proteine accessorie disposte periodicamente: collegamenti elastici tra doppi (come i ponti nexin) e strutture radiali verso la coppia centrale contribuiscono a mantenere l’integrità del fascio, mentre bracci di dineina generano la forza motile (Figura 05.28-13). La dineina ciliare, ancorata con la coda al microtubulo “A” di un doppietto e con le teste che interagiscono con il microtubulo “B” adiacente, trasforma l’energia dell’ATP in scorrimento relativo tra doppietti. Poiché i doppietti sono interconnessi da legami elastici, lo scorrimento viene convertito in flessione coordinata del fusto, producendo l’onda di battito o la frustata (Figura 05.28-14). L’azione combinata di bracci di dineina esterni e interni regola ampiezza, frequenza e forma dell’oscillazione. Nell’uomo, difetti congeniti della dineina ciliare o di altri componenti assonemali causano la dischinesia ciliare primaria (sindrome di Kartagener). Gli spermatozoi risultano ipomobili o immobili con conseguente infertilità maschile; l’alterato trasporto mucociliare favorisce infezioni respiratorie ricorrenti; in molti casi si osserva situs inversus per compromissione della motilità ciliare embrionale. Molte cellule animali prive di ciglia battenti possiedono un singolo ciglio primario immobile, più corto e con organizzazione “9 + 0”. Questa appendice funziona come antenna sensoriale per segnali extracellulari e stimoli meccanici, contribuendo all’integrazione delle vie di segnalazione che regolano crescita e differenziamento:
- stabilizzazione microtubulare: proteine leganti estremità o fianco del polimero limitano la depolimerizzazione e mantengono la polarità cellulare;
- direzionalità del trasporto: chinesine verso l’estremità più, dineine verso l’estremità meno, con selettività di carico determinata da complessi adattatori;
- organizzazione degli organuli: kinesine estendono il RE verso la periferia, dineine concentrano il Golgi in regione pericentrosomiale (Figura 05.28-09);
- motilità assonemale: architettura “9 + 2” e dineina ciliare convertono scorrimento in flessione coordinata di ciglia e flagelli.