L’ereditarietà mendeliana ha le proprie basi fisiche nel comportamento dei cromosomi
Definizione
La richiesta di energia libera ha modellato in modo decisivo l’evoluzione biologica. Strutture cellulari, funzioni fisiologiche e traiettorie evolutive degli organismi sono profondamente intrecciate con le modalità con cui l’energia viene acquisita, trasformata e immagazzinata. In un ambiente primordiale povero di ossigeno, le prime cellule verosimilmente sintetizzavano ATP per fosforilazione a livello del substrato, sfruttando reazioni fermentative nel citosol a partire da molecole organiche generate da processi geochimici. Nelle cellule attuali, le vie fermentative rimangono attive nel citosol e forniscono ATP ossidando parzialmente nutrienti ricchi di energia.
Ben presto, nella storia della vita, si affermò un meccanismo molto più efficiente, fondato sul trasferimento di elettroni accoppiato a trasporto di protoni attraverso membrane biologiche. A distanza di miliardi di anni, questo principio è diventato centrale per quasi ogni forma di vita e rappresenta la base della produzione di ATP in mitocondri e cloroplasti. I sistemi di trasporto elettronico di membrana sono nati nei batteri oltre tre miliardi di anni fa; i loro discendenti popolano oggi ambienti estremi e nicchie comuni, mentre tracce di tale eredità persistono negli eucarioti come organuli specializzati: mitocondri e cloroplasti.
Qui vengono esposti i fondamenti molecolari che consentono ai sistemi di trasporto di elettroni di generare energia utile alla cellula. Il cardine è l’uso di una membrana per convertire l’energia redox degli elettroni in un gradiente protonico, che a sua volta alimenta la sintesi di ATP. Saranno richiamati i principi chimico-fisici che rendono esergonico il trasferimento di elettroni e, in chiusura, i tratti evolutivi che hanno fissato nel tempo questo meccanismo.
L’adenosina trifosfato (ATP) costituisce la principale valuta energetica cellulare. Nelle cellule eucariotiche, una quota modesta di ATP è prodotta nel citosol durante la glicolisi; la porzione preponderante deriva dalla fosforilazione ossidativa. A differenza della glicolisi, che è solubile, la fosforilazione ossidativa è un processo intrinsecamente membranoso: nei mitocondri essa dipende da catene di trasporto di elettroni inserite nella membrana mitocondriale interna, le quali pompano protoni (H⁺) creando un gradiente elettrochimico. Un meccanismo concettualmente analogo opera nella fotosintesi di piante, alghe e batteri fotosintetici, dove le membrane tilacoidali sostengono la conversione fotochimica dell’energia (Figura 05.11-01).
La produzione di ATP basata su membrana si articola in due fasi intimamente accoppiate: la generazione di un gradiente protonico e il suo utilizzo per la sintesi dell’ATP. Entrambe le fasi sono mediate da complessi proteici transmembrana altamente conservati.
- Nella fase 1, elettroni ad alta energia, provenienti dall’ossidazione di nutrienti, dall’assorbimento di luce o da altre sorgenti redox, fluiscono lungo una catena di trasporto elettronico costituita da trasportatori organizzati nella membrana. L’energia rilasciata a ogni tappa del trasferimento viene impiegata per spostare protoni attraverso la membrana, tipicamente prelevandoli dall’acqua ubiquitaria nei compartimenti cellulari. Ne risulta un gradiente elettrochimico di protoni (o forza proton-motrice) attraverso la membrana stessa (Figura 05.11-02). La forza proton-motrice può essere formalizzata come: \[ \Delta p \;=\; \Delta \psi \;-\; \frac{2,303\,R\,T}{F}\,\Delta \mathrm{pH}, \] dove \(\Delta \psi\) è il potenziale di membrana, \(\Delta \mathrm{pH}\) la differenza di pH tra i lati della membrana, \(R\) la costante dei gas, \(T\) la temperatura e \(F\) la costante di Faraday. Questo gradiente rappresenta una riserva di energia potenziale capace di compiere lavoro quando ai protoni è consentito il ritorno secondo gradiente;
- Nella fase 2, detta fosforilazione ossidativa, i protoni rifluiscono attraverso l’ATP sintasi, un complesso enzimatico rotazionale che catalizza la reazione endoergonica \( \mathrm{ADP} + \mathrm{P_i} \rightarrow \mathrm{ATP} + \mathrm{H_2O} \). L’enzima, spesso indicato come F\(_1\)F\(_\mathrm{o}\)-ATP sintasi, opera come una turbina molecolare che converte l’energia di \(\Delta p\) in legame fosfoanidro dell’ATP (Figura 05.11-02). In condizioni fisiologiche, sono necessari tipicamente ~3–4 H⁺ per sintetizzare una molecola di ATP, valore che dipende dalla struttura del rotore e dal valore di \(\Delta p\).
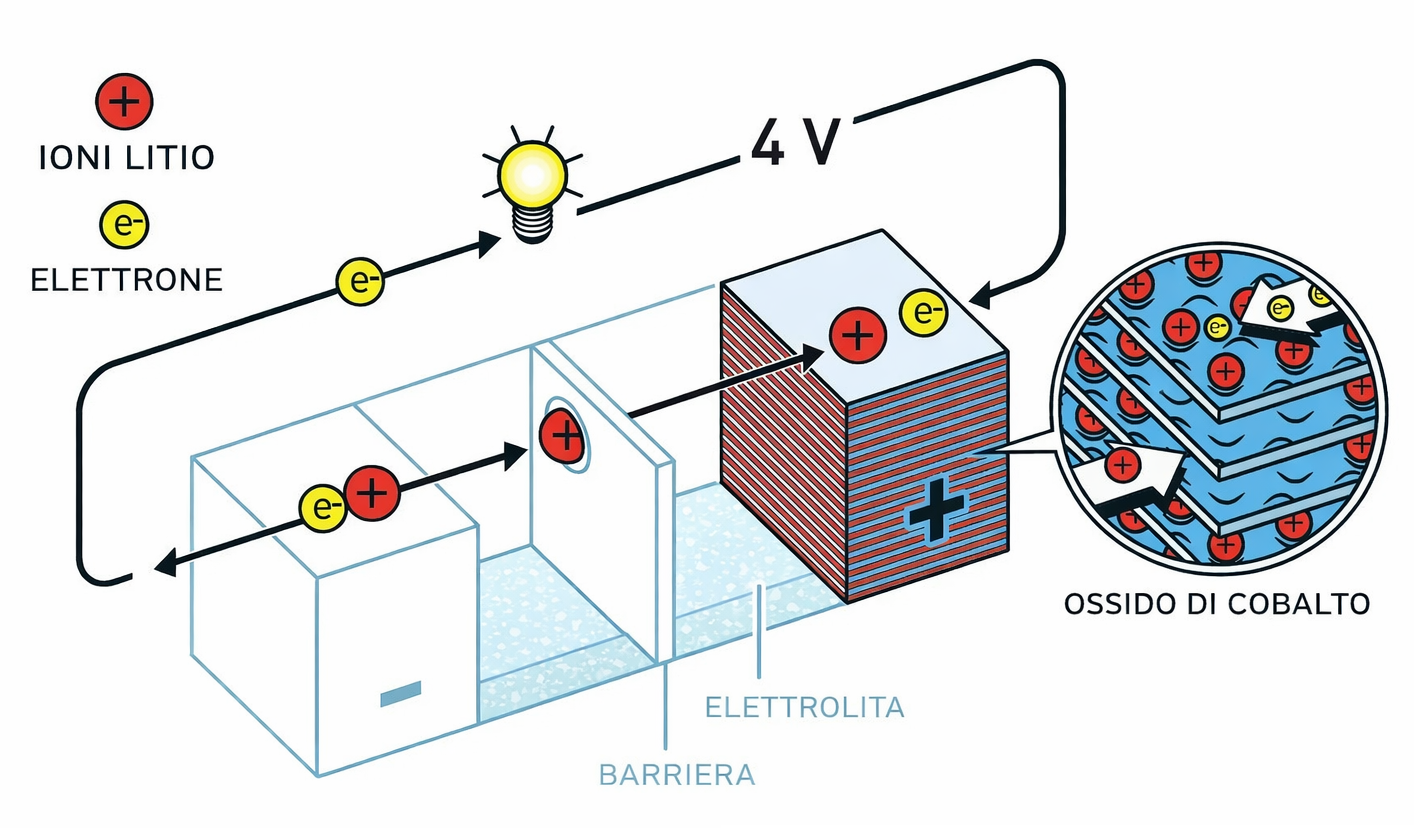
La cornice teorica di questo meccanismo, formulata negli anni ’60 e conosciuta come ipotesi chemiosmotica, ha chiarito il nesso tra reazioni redox e trasporto di ioni attraverso membrane. Per mezzo dell’accoppiamento chemiosmotico, l’energia del flusso di elettroni viene sfruttata in modo analogo a come una batteria alimenta un carico elettrico (Figura 05.11-03).
Nei mitocondri, gli elettroni provengono principalmente da NADH e FADH\(_2\) generati dal metabolismo ossidativo, e l’accettore finale è l’ossigeno molecolare, ridotto a acqua. Nei cloroplasti, l’energia luminosa separa le cariche nei fotosistemi; l’acqua è la fonte di elettroni e di protoni, e l’ossigeno è rilasciato come sottoprodotto. L’orientamento dei gradienti è opposto nei due organuli: nei mitocondri i protoni sono pompati dalla matrice verso lo spazio intermembrana, mentre nei cloroplasti vengono accumulati nel lume tilacoidale a partire dallo stroma.
La forza proton-motrice alimenta anche altri processi, oltre la sintesi di ATP:
- trasporto attivo secondario di metaboliti e ioni tramite simporti e antiporti H⁺-dipendenti;
- movimento rotazionale di motori proteici, come il flagello batterico, che utilizza \(\Delta p\) per la locomozione;
- regolazione dell’omeostasi del pH nei diversi compartimenti cellulari.
Il meccanismo chemiosmotico di sintesi dell’ATP è un’innovazione antichissima che ha preceduto di molto l’atmosfera ossigenata. Batteri e archei moderni utilizzano ancora oggi catene di trasporto di elettroni nella membrana plasmatica, a dimostrazione della robustezza e dell’efficienza del principio. Questa persistenza riflette anche l’origine endosimbiotica degli organuli energetici eucariotici: mitocondri e cloroplasti derivano da antichi batteri inglobati da cellule ancestrali, stabilendo relazioni stabili e vantaggiose per entrambe le parti.
Numerosi indizi supportano tale discendenza batterica. Mitocondri e cloroplasti:
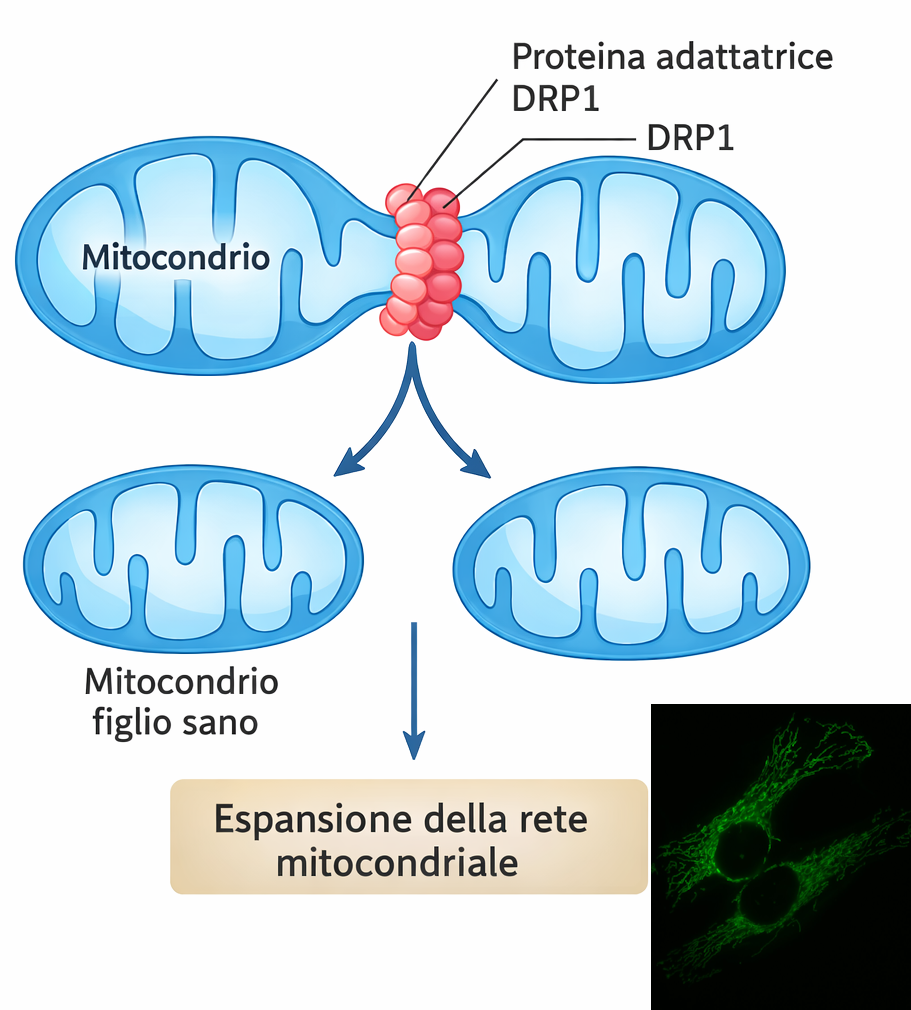
- si dividono per scissione binaria, con dinamiche simili alla proliferazione procariotica (Figura 05.11-04);
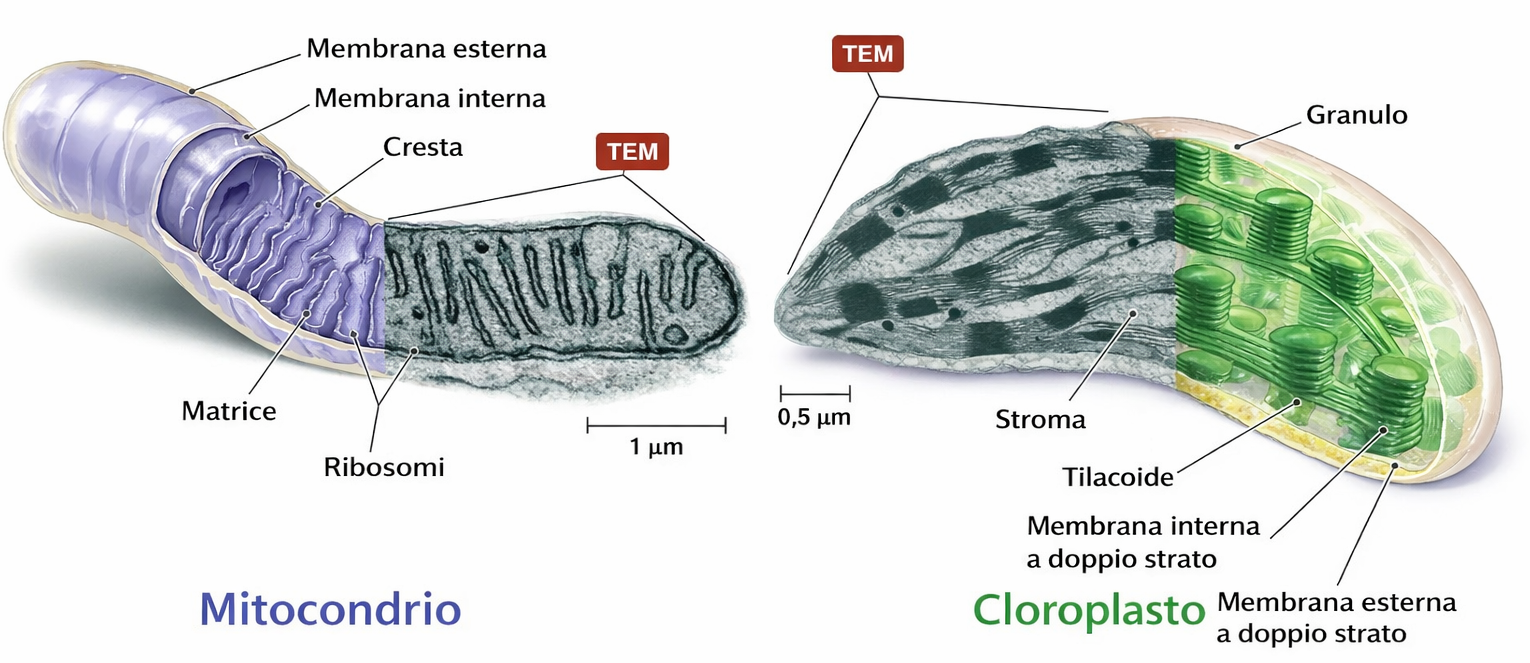
- possiedono un proprio genoma circolare e apparati di trascrizione e traduzione di impronta batterica, incluse ribosomi di tipo 70S, con organizzazione genetica compatibile con l’ipotesi endosimbiotica (Figura 05.11-05);
- mantengono vie metaboliche e catene respiratorie/fotosintetiche che ricordano quelle dei loro progenitori procarioti.
Nonostante ciò, nel corso della coevoluzione gran parte dei geni necessari alla vita autonoma è stata persa o trasferita al nucleo dell’ospite. Questo trasferimento genico ha comportato la dipendenza degli organuli dall’importazione di proteine codificate nel nucleo e sintetizzate nel citosol. Sequenze segnale specifiche e complessi di traslocazione dedicati guidano tale traffico proteico attraverso le doppie membrane, assicurando l’assemblaggio dei complessi respiratori e fotosintetici e la funzionalità dell’ATP sintasi. Nei cloroplasti, molti geni residui mostrano affinità con quelli dei cianobatteri, coerentemente con la loro origine da batteri fotosintetici.
La conservazione dei principi dell’accoppiamento chemiosmotico in domini della vita tra loro distanti, unita all’adattabilità a differenti accettori elettronici e fonti di energia (luminoso, chimico, inorganico), spiega l’ampia diffusione del meccanismo e il suo ruolo centrale nella bioenergetica contemporanea.