La variabilità genetica prodotta dai cicli vitali sessuati contribuisce all’evoluzione
Definizione
Un modo efficace per consentire a piccole molecole idrofile di superare la barriera lipidica è fornire un passaggio acquoso attraverso la membrana. Le proteine canale, o semplicemente canali, assolvono a questa funzione creando pori transmembrana che permettono il movimento passivo di soluti idrosolubili tra citoplasma e ambiente extracellulare, o tra compartimenti intracellulari. Alcuni canali formano condotti relativamente ampi e poco selettivi: ne sono esempi le giunzioni comunicanti fra cellule adiacenti (gap junction), costituite da connessoni, e le porine presenti nella membrana esterna dei mitocondri e nell’involucro esterno di molti batteri Gram-negativi. Se pori così larghi mettessero direttamente in continuità il citosol con lo spazio extracellulare, la cellula perderebbe rapidamente il controllo della propria omeostasi; per questo, nella membrana plasmatica prevalgono canali con lume ristretto e marcata selettività. Le acquaporine, già menzionate, rappresentano un caso paradigmatico: favoriscono un flusso rapido di acqua in numerosi tessuti di procarioti ed eucarioti, consentendo il passaggio di molecole d’acqua elettricamente neutre e, al contempo, escludendo gli ioni, incluso il protone H⁺. Elementi strutturali del poro, come il restringimento centrale e specifici residui polari (ad esempio asparagine) che riorientano le molecole d’acqua, impediscono il trasferimento protonico per meccanismo di Grotthuss. Il panorama complessivo dei canali di membrana comprende inoltre proteine specializzate per il transito di ioni inorganici; su questi canali ionici si concentra l’analisi che segue.
I canali ionici non sono semplici “fori” nella membrana, ma dispositivi molecolari dotati di due caratteristiche chiave. La prima è la selettività ionica: consentono il passaggio ad alcuni ioni mentre ne escludono altri. Tale selettività dipende da più fattori integrati: diametro e geometria del poro, campo elettrico locale generato da residui carichi o polari, e organizzazione del filtro di selettività nella regione più stretta del canale (Figura 05.06-01). Poiché in soluzione gli ioni sono circondati da un guscio di idratazione, l’accesso al filtro richiede la parziale rimozione di molecole d’acqua; interazioni precise fra gli ioni e i gruppi funzionali del filtro (ad esempio ossigeni carbonilici) compensano il costo energetico di disidratazione. Solo specie ioniche con raggio ionico e carica adeguati possono soddisfare queste interazioni e procedere in colonna attraverso il poro. La seconda proprietà è il gating, ossia la capacità di transitare reversibilmente fra stati chiusi e aperti. Un’apertura indiscriminata di migliaia di canali di membrana priverebbe la cellula del controllo sul flusso ionico; per contro, i canali alternano brevi eventi di apertura a periodi di chiusura (Figura 05.06-01), innescati da specifici stimoli e supportati da cambiamenti conformazionali. Le principali modalità di controllo includono:
- dipendenza dal potenziale di membrana (canali voltaggio-dipendenti) il cui stato aperto varia con \(V_m\);
- legame di ligandi extracellulari o intracellulari (canali ligando-dipendenti, ad esempio attivati da neurotrasmettitori o da messaggeri come Ca²⁺ e cAMP);
- stimoli meccanici o tensionali (meccanosensibili, ad esempio nei recettori tattili);
- altri stimoli fisici o chimici specializzati, come temperatura o luce in proteine fotosensibili.
Quando un canale ionico è aperto, il passaggio degli ioni non richiede una riorganizzazione proteica ad ogni evento di trasporto; per questo la conduzione è estremamente rapida, con flussi che possono superare 10⁶ ioni al secondo, nell’ordine di tre grandezze più veloci dei trasportatori medi. Tuttavia, i canali non compiono trasporto attivo: non accoppiano il flusso a sorgenti energetiche e mediano esclusivamente diffusione facilitata. La loro funzione principale è rendere la membrana temporaneamente permeabile a specifici ioni inorganici, in particolare Na⁺, K⁺, Ca²⁺ e Cl⁻. Poiché pompe e cotrasportatori mantengono concentrazioni ioniche lontane dall’equilibrio sui due lati della membrana, l’apertura di un canale determina un flusso rapido governato dal gradiente elettrochimico. Tale forza motrice può essere espressa come: \[ \Delta \mu_i = RT \ln\!\left(\frac{[i]_{\mathrm{in}}}{[i]_{\mathrm{out}}}\right) + z_i F \bigl(V_m - E_i\bigr), \] dove \(E_i = \tfrac{RT}{z_i F}\ln\!\left(\tfrac{[i]_{\mathrm{out}}}{[i]_{\mathrm{in}}}\right)\) è il potenziale di Nernst per lo ione \(i\). L’apertura di canali selettivi modifica il potenziale di membrana \(V_m\) in tempi brevi, perché il flusso di carica altera la distribuzione di potenziali e, quindi, la dinamica elettrica della cellula. La selettività, il gating e la conduttanza di singolo canale si combinano nel definire la permeabilità di membrana istantanea e la probabilità di apertura. Tecniche elettrofisiologiche ad alta risoluzione, come il patch-clamp, hanno permesso di correlare gli stati conformazionali dei canali con le correnti misurate, chiarendo i principi che collegano struttura e funzione nei diversi sottotipi canale.
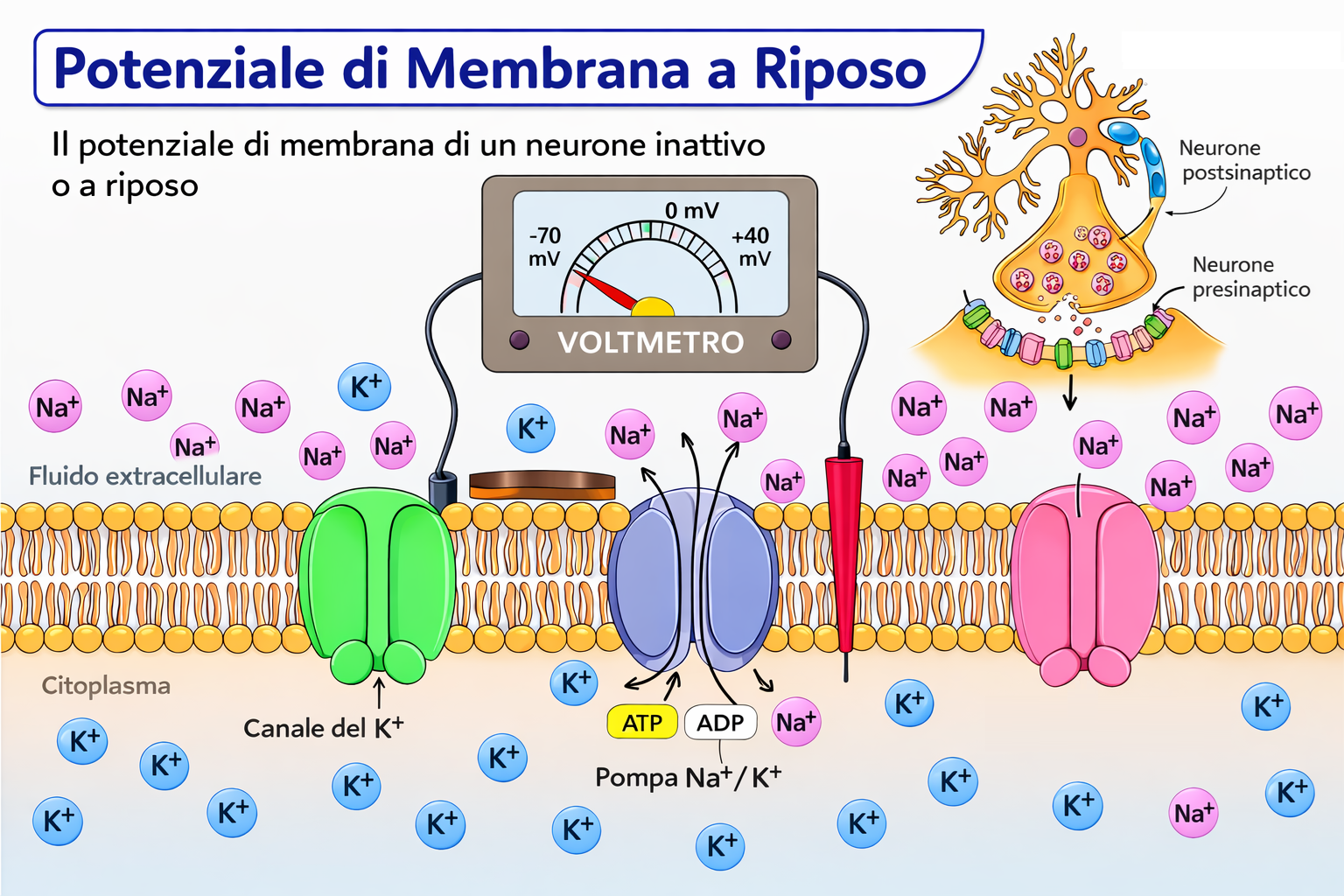
Le variazioni del potenziale di membrana costituiscono il substrato della segnalazione elettrica in molte cellule animali e vegetali, dalle cellule nervose e muscolari fino alle cellule tattili delle piante carnivore (Figura 05.06-02). Tali variazioni emergono da modifiche rapide della permeabilità della membrana a specifici ioni. In condizioni di riposo, nelle cellule animali le cariche negative associate a macromolecole intracellulari sono in larga misura controbilanciate dal K⁺, lo ione monovalente più abbondante nel citoplasma. La Na⁺/K⁺-ATPasi trasferisce continuamente K⁺ all’interno e Na⁺ all’esterno, stabilendo e mantenendo un marcato gradiente transmembrana di K⁺. Poiché la membrana a riposo ospita prevalentemente canali di fuga per il K⁺ (leak K⁺ channels), il potassio diffonde verso l’esterno secondo il proprio gradiente di concentrazione: tale efflusso di cariche positive lascia il citoplasma più negativo rispetto all’ambiente esterno e genera un differenziale di potenziale, il potenziale di membrana (Figura 05.06-03). Il campo elettrico che si sviluppa si oppone all’ulteriore fuoriuscita di K⁺; quando la forza elettrica che trattiene K⁺ all’interno e la forza chimica che ne promuove l’uscita si eguagliano, il gradiente elettrochimico di K⁺ si annulla e si raggiunge un equilibrio dinamico, pur in presenza di una concentrazione intracellulare di K⁺ molto più elevata di quella extracellulare (Figura 05.06-04). Il potenziale a cui si verifica questo bilanciamento è descritto dall’equazione di Nernst, che lega il potenziale di equilibrio di uno ione al rapporto tra le sue concentrazioni ai due lati della membrana:
\( E_{\mathrm{ion}} = \dfrac{RT}{zF} \ln \left( \dfrac{[\mathrm{ion}]_{\mathrm{out}}}{[\mathrm{ion}]_{\mathrm{in}}} \right) \)
Il potenziale di membrana a riposo, condizione stazionaria in cui il flusso netto di cariche attraverso la membrana è nullo, nelle cellule animali risulta in genere compreso tra −20 e −200 mV e riflette in prima approssimazione l’equilibrio del K⁺, data l’elevata permeabilità al K⁺ nella membrana a riposo. Un esempio numerico: assumendo 37 °C, \( [\mathrm{K}^+]_{\mathrm{in}} = 140 \) mM e \( [\mathrm{K}^+]_{\mathrm{out}} = 5 \) mM, si ottiene \( E_{\mathrm{K}} \approx -89 \) mV. In condizioni fisiologiche reali, anche Na⁺ e Cl⁻ contribuiscono al valore di riposo, e una formulazione più generale è data dall’equazione di Goldman-Hodgkin-Katz:
\( V_m = \dfrac{RT}{F} \ln \left( \dfrac{P_{\mathrm{K}}[\mathrm{K}^+]_{\mathrm{out}} + P_{\mathrm{Na}}[\mathrm{Na}^+]_{\mathrm{out}} + P_{\mathrm{Cl}}[\mathrm{Cl}^-]_{\mathrm{in}}}{P_{\mathrm{K}}[\mathrm{K}^+]_{\mathrm{in}} + P_{\mathrm{Na}}[\mathrm{Na}^+]_{\mathrm{in}} + P_{\mathrm{Cl}}[\mathrm{Cl}^-]_{\mathrm{out}}} \right) \)
dove \(P_i\) rappresenta la permeabilità relativa a ciascuno ione. Cambiamenti rapidi del potenziale non richiedono variazioni massicce delle concentrazioni globali: è sufficiente il trasferimento di una piccola frazione di ioni verso/da un sottile strato vicino alla membrana, grazie alla bassa capacità elettrica della membrana stessa. Nella segnalazione elettrica, pertanto, l’elemento decisivo è la rapida modulazione della permeabilità tramite l’apertura e la chiusura di canali ionici, evento che avviene nell’ordine dei millisecondi, più che lente alterazioni delle concentrazioni complessive (Figura 05.06-05):
- determinanti del potenziale di membrana: gradienti di concentrazione stabiliti da pompe e trasportatori attivi;
- permeabilità selettiva dovuta al repertorio di canali ionici aperti a riposo;
- interdipendenza tra voltaggio e stato dei canali, che genera circuiti di feedback elettrici;
- contributo di più ioni, pesato dalle rispettive permeabilità, descritto dalla relazione di Goldman-Hodgkin-Katz.
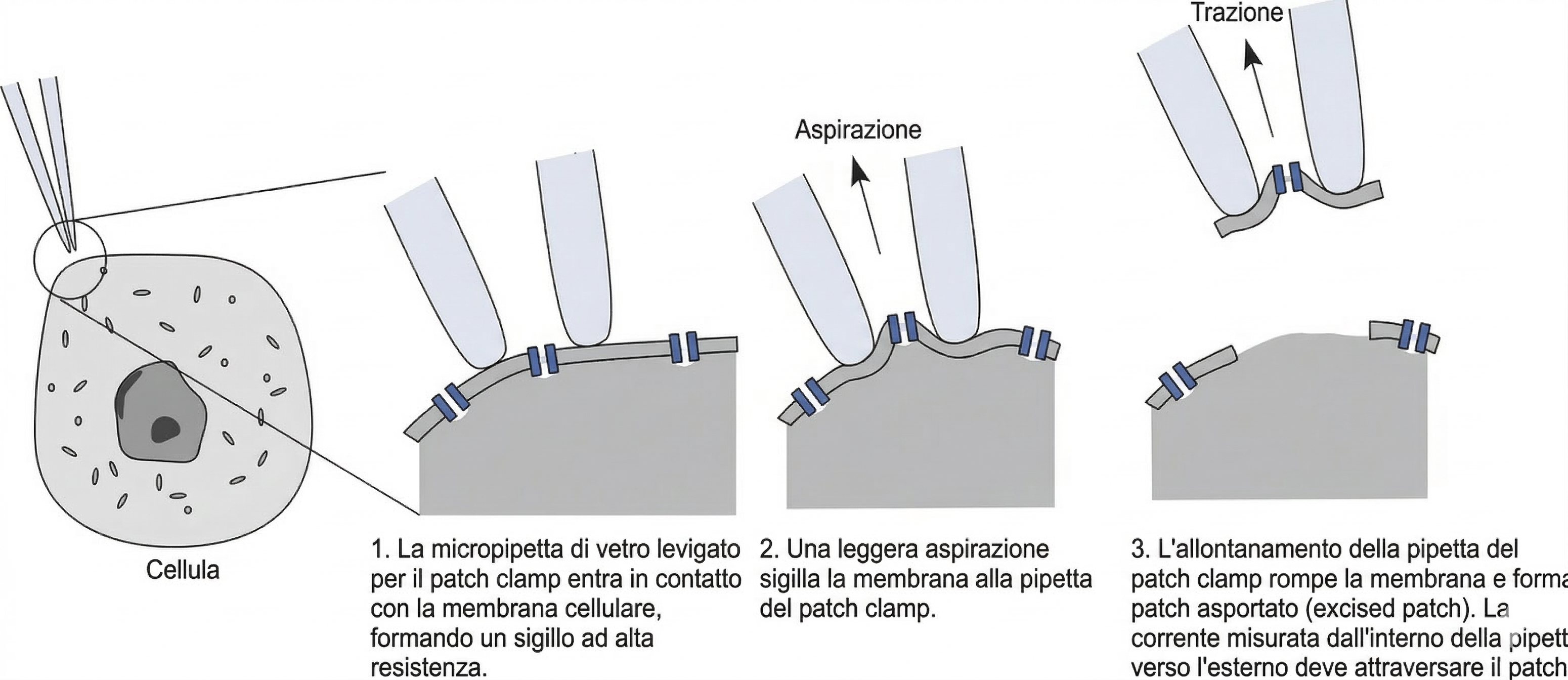
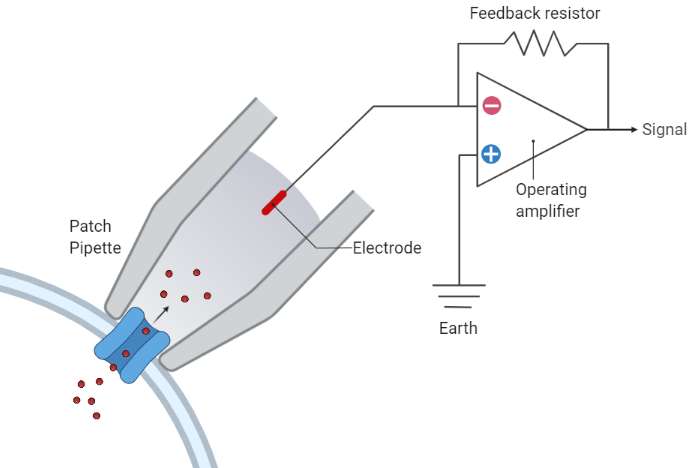
Lo studio diretto dei canali ionici nelle cellule vive si fonda sulla misura di correnti estremamente piccole. La tecnica del patch clamp consente di registrare la corrente che attraversa una minuscola porzione di membrana (patch o areola) grazie a un microelettrodo di vetro che sigilla ermeticamente sulla superficie cellulare e stabilisce un contatto elettrico ad alta resistenza (Figura 05.06-06). Un’areola di dimensioni adeguate può contenere un singolo canale, la cui apertura produce correnti dell’ordine del picoampere (10⁻¹² A), rilevabili come scatti discreti nel tracciato di corrente. Le registrazioni rivelano un comportamento sorprendente: i canali passano bruscamente da uno stato chiuso a uno aperto e viceversa, anche mantenendo costanti le condizioni sperimentali (Figura 05.06-07). Questa dinamica “a scatti” indica l’esistenza di domini proteici mobili che transitano tra conformazioni alternative in seguito a fluttuazioni termiche casuali. L’ampiezza di corrente di un canale aperto è sostanzialmente fissa (“tutto o nulla”), mentre variano la durata e la frequenza degli episodi di apertura. Cambiando le condizioni (per esempio il voltaggio o la presenza di un ligando), non si elimina la natura stocastica del fenomeno, ma si modifica la probabilità di occupare lo stato aperto: aumenta il tempo medio trascorso aperto quando lo stimolo favorisce l’attivazione, e diminuisce quando lo sfavorisce (Figura 05.06-07). La metodologia patch clamp, sviluppata per lo studio di singole molecole canale, ha fornito prove dirette dei passaggi conformazionali proteici e ha rivoluzionato l’elettrofisiologia quantitativa.
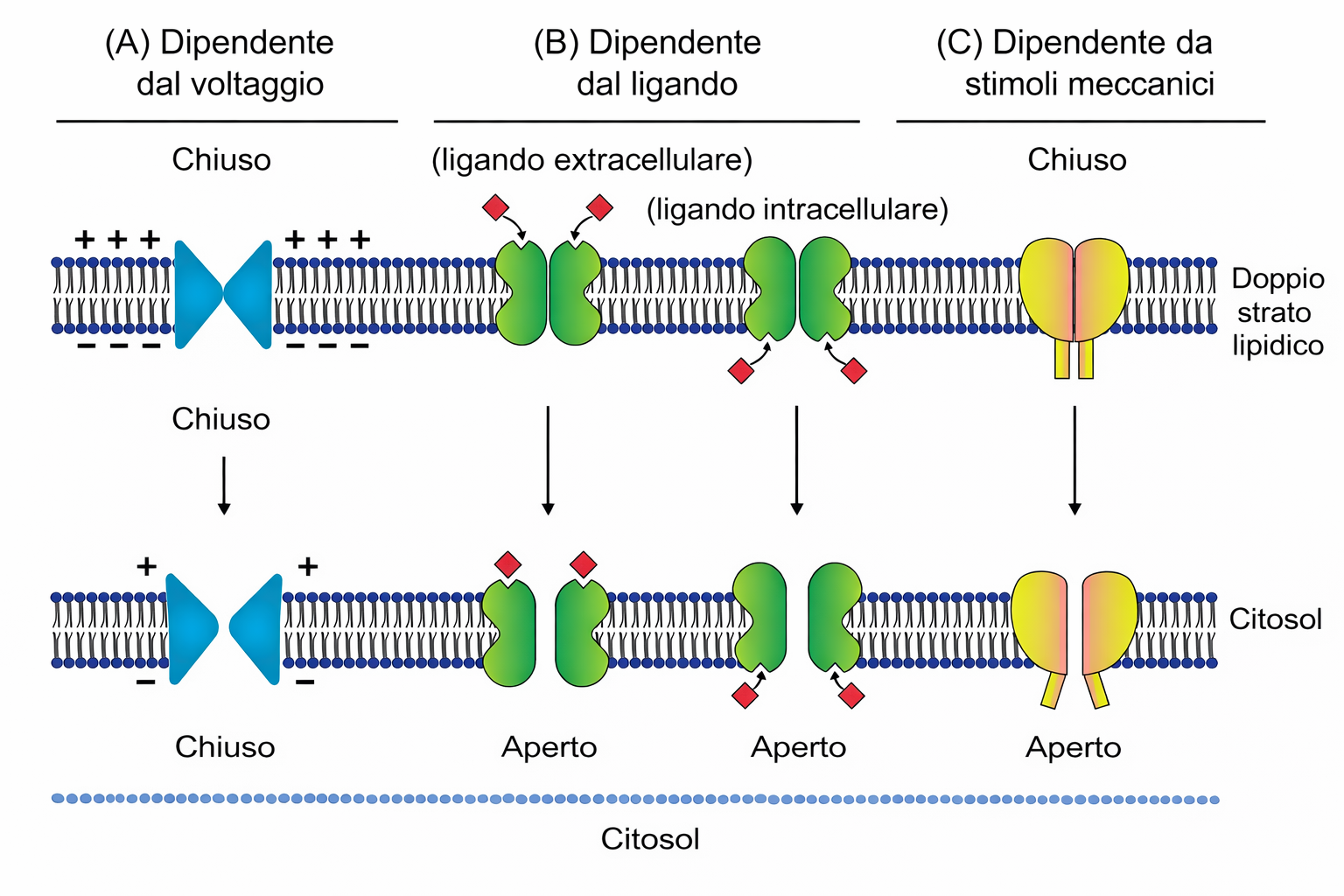
Negli organismi viventi esistono centinaia di canali ionici, anche in specie semplici; nel genoma umano, ad esempio, sono codificati numerosi sottotipi di canali per il K⁺ tra loro imparentati ma funzionalmente distinti. Le principali differenze tra canali riguardano due proprietà: la selettività (quali ioni attraversano il poro) e il meccanismo di gating (quali segnali ne promuovono l’apertura o la chiusura). Si riconoscono tre categorie funzionali principali (Figura 05.06-08):
- canali voltaggio-dipendenti, in cui la probabilità di apertura varia con il potenziale di membrana;
- canali ligando-dipendenti, la cui apertura è controllata dall’interazione con un ligando, che può legarsi al versante extracellulare (p.es., neurotrasmettitori) o intracellulare (p.es., Ca²⁺, cAMP, cGMP);
- canali meccanosensibili, che si aprono in risposta a tensioni o forze applicate alla membrana o al citoscheletro.
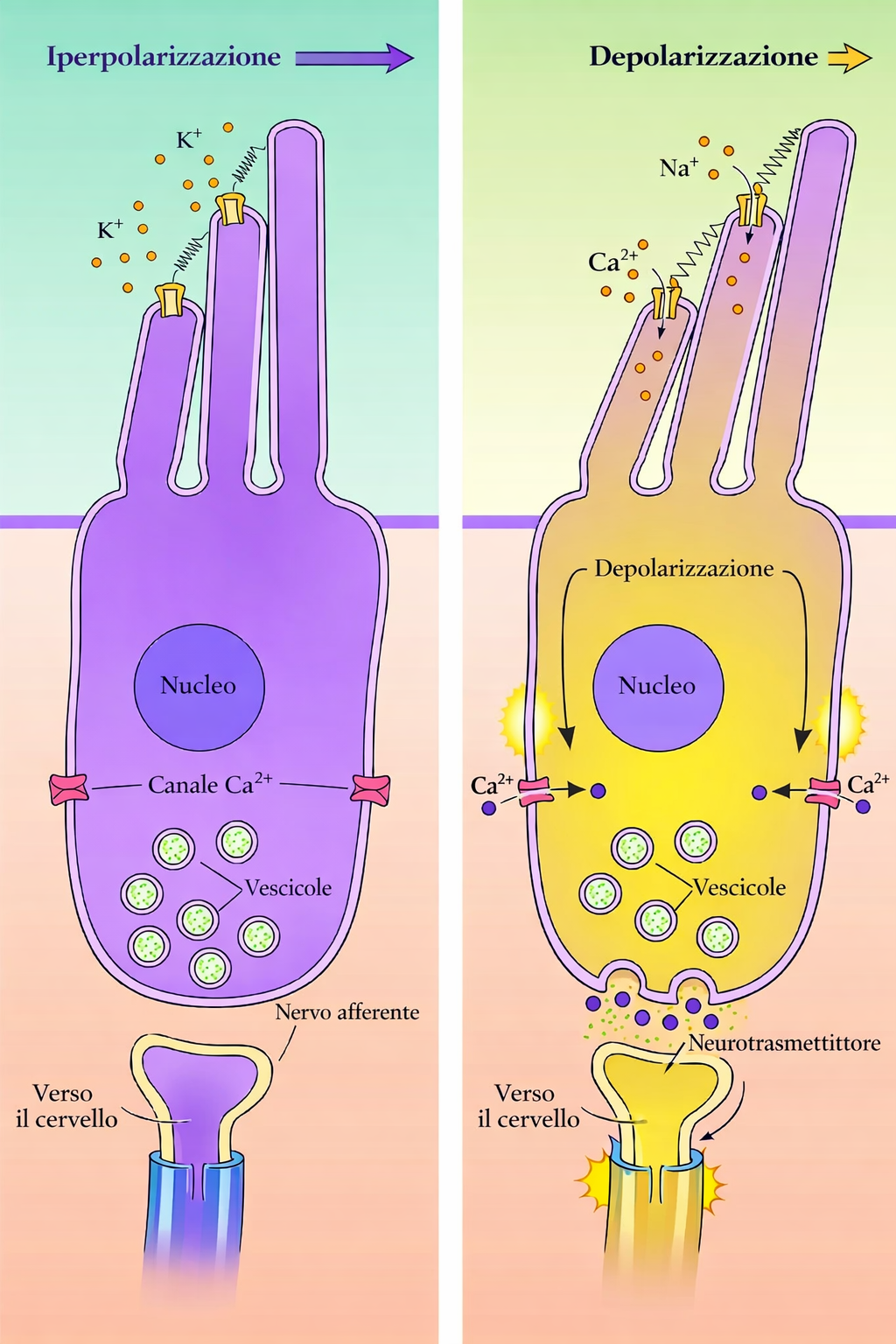
Un caso paradigmatico di meccanoeletrotrasduzione è fornito dalle cellule capellute dell’orecchio interno: le vibrazioni sonore deflettono i microvilli apicali, mettendo in tensione collegamenti proteici che trasmettono la forza ai canali, inducendone l’apertura. L’ingresso di ioni depolarizza la cellula capelluta e avvia un segnale elettrico che, attraverso le sinapsi con le fibre del nervo acustico, raggiunge le strutture encefaliche deputate all’udito (Figura 05.06-09).
I canali controllati dal voltaggio orchestrano la propagazione dei segnali elettrici nelle cellule eccitabili. Nelle cellule nervose, ad esempio, essi consentono la conduzione rapida di segnali su lunghe distanze, come nella via discendente che dal sistema nervoso centrale raggiunge i muscoli distali degli arti inferiori. Canali voltaggio‑dipendenti si ritrovano anche nelle fibre muscolari, nelle cellule uovo, in vari protisti e nelle piante, dove partecipano a risposte rapide quali la chiusura delle foglioline di Mimosa pudica in seguito a stimoli tattili (Figura 05.06-10). Questi canali contengono sensori di voltaggio, domini proteici carichi (spesso arricchiti in residui positivi) che rispondono a modifiche del campo elettrico transmembrana. Quando il potenziale supera una certa soglia, la forza elettrica esercitata sui sensori innesca un passaggio conformazionale che apre il poro; invertendo il segno o l’ampiezza della variazione, il canale tende a richiudersi (Figura 05.06-08). Le variazioni del potenziale non determinano “mezze aperture”: alterano, piuttosto, la probabilità istantanea che un canale sia nello stato aperto. In una patch contenente molte copie della stessa proteina canale, si può quindi osservare che, a un dato voltaggio, è aperta in media una certa frazione di canali (p.es., 10%), che aumenta o diminuisce al variare del potenziale (p.es., fino al 90%). L’apertura di un insieme di canali modifica il potenziale di membrana, che a sua volta può attivare o disattivare altri canali voltaggio‑dipendenti. Questo circuito di retroazione, canali ionici → potenziale di membrana → canali ionici, è il principio cardine della segnalazione elettrica. A tale circuito si aggiungono meccanismi intrinseci come l’inattivazione dipendente dal tempo o dal voltaggio, che modulano la durata della risposta e garantiscono l’affidabilità della codifica del segnale.