La trascrizione è la sintesi dell’RNA dettata dal DNA: uno sguardo da vicino
Definizione
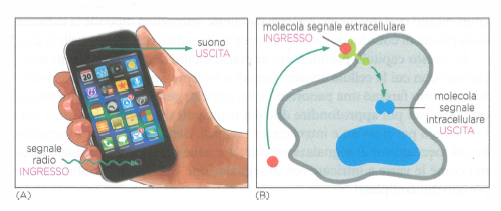
L’informazione biologica può presentarsi in molteplici forme e, per essere efficace, spesso richiede una conversione da un tipo di segnale a un altro. Un esempio quotidiano è l’ascolto di musica in streaming: pacchetti di dati vengono trasformati in variazioni elettriche e poi in onde acustiche percepibili. Questa trasformazione è un caso di trasduzione del segnale (Figura 05.23-01). Nelle cellule, la logica di base è analoga ma più essenziale: una cellula emittente rilascia una specifica molecola segnale nell’ambiente extracellulare, mentre una cellula bersaglio, dotata di recettori appropriati, riconosce quel segnale e attiva una risposta mirata.
La trasduzione del segnale inizia quando il recettore della cellula bersaglio lega il ligando extracellulare e lo “traduce” in variazioni intracellulari, quali modifiche conformazionali di proteine, attivazione di chinasi e fosfatasi, generazione di secondi messaggeri (per esempio cAMP, Ca2+, IP3) e rimodellamento trascrizionale. L’intero processo, che include ricezione, elaborazione, integrazione e risposta, è indicato come segnalazione cellulare. La specificità dipende dall’espressione recettoriale e dal contesto intracellulare: cellule con recettori diversi, o con reti di segnalazione differenti, possono reagire in modo divergente alla stessa molecola segnale. Dal punto di vista fisico-chimico, i ligandi idrofili interagiscono tipicamente con recettori di superficie, mentre segnali idrofobici, come steroidi e ormoni tiroidei, attraversano la membrana e si legano a recettori intracellulari o nucleari, modulando direttamente l’espressione genica.
La trasduzione è inoltre caratterizzata da amplificazione (un singolo evento di legame può innescare l’attivazione di molte molecole effettrici), integrazione di segnali multipli e meccanismi di adattamento o desensitizzazione, che impediscono risposte eccessive o prolungate. Queste proprietà conferiscono alle reti di segnalazione un comportamento dinamico, capace di codificare informazioni in termini di intensità, durata o frequenza degli impulsi. Nelle sezioni seguenti vengono richiamate le principali modalità con cui i segnali extracellulari sono veicolati tra cellule in organismi pluricellulari.
Le cellule degli organismi pluricellulari impiegano numerose classi di molecole segnale extracellulari, tra cui:
- proteine e peptidi, come fattori di crescita e citochine;
- amminoacidi e loro derivati, inclusi diversi neurotrasmettitori;
- nucleotidi e nucleosidi, quali ATP e adenosina;
- steroidi e ormoni tiroidei, lipofili e diffusibili attraverso le membrane;
- derivati degli acidi grassi, come eicosanoidi e prostaglandine;
- gas in soluzione, tra cui ossido nitrico (NO) e monossido di carbonio (CO).
Nonostante l’ampia varietà chimica, le vie fondamentali di comunicazione sono poche e si distinguono soprattutto per raggio d’azione, tempi di risposta e specificità del bersaglio.
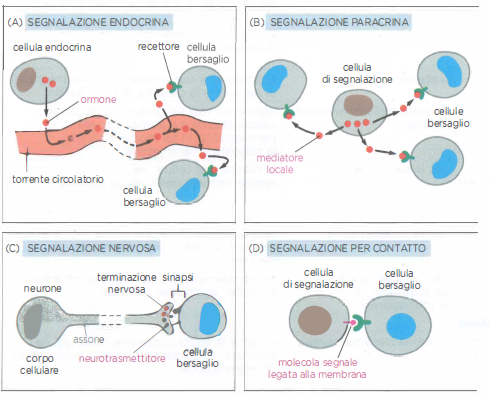
Segnalazione endocrina (a lunga distanza) — Le cellule endocrine rilasciano ormoni nel circolo ematico (o nella linfa delle piante), consentendo al segnale di raggiungere distretti corporei remoti (Figura 05.23-02). La tiroxina, ad esempio, modula il metabolismo in molti tessuti; i glucocorticoidi coordinano risposte allo stress su scala sistemica. L’efficacia dipende da parametri quali emivita, legame a proteine carrier e densità recettoriale nei tessuti bersaglio. Tale via garantisce coerenza di risposta in tutto l’organismo e sincronizzazione fisiologica su tempi che vanno da minuti a ore.
Segnalazione paracrina (locale) e autocrina — Nella comunicazione paracrina, i mediatori locali diffondono nel microambiente extracellulare e agiscono su cellule vicine senza entrare nel circolo ematico (Figura 05.23-02). Fattori di crescita, chemochine e eicosanoidi regolano, per esempio, proliferazione, migrazione e processi infiammatori in tessuti contigui o in una lesione in riparazione. La natura locale è dovuta alla rapida diluizione, degradazione o captazione del segnale e ai limiti imposti dalla diffusione: il tempo di diffusione media su distanza x scala approssimativamente come
\[ t \approx \frac{x^2}{2D}, \]
dove D è il coefficiente di diffusione; all’aumentare della distanza, i tempi crescono rapidamente, limitando l’efficacia oltre brevi range. Nella segnalazione autocrina, la cellula risponde a mediatori da essa stessa secreti; un esempio rilevante è l’autopotenziamento di linfociti T attraverso IL-2, così come l’autostimolazione della crescita in diversi tumori, che sfruttano circuiti autocrini per sostenere proliferazione e sopravvivenza.
Segnalazione sinaptica (neurale) — I neuroni trasmettono segnali su lunghe distanze con alta specificità sfruttando assoni che raggiungono bersagli determinati (Figura 05.23-02). Un potenziale d’azione può propagarsi lungo l’assone con velocità che arrivano a circa 120 m/s, a seconda del calibro e della mielinizzazione. Nella terminazione presinaptica, l’impulso elettrico è convertito in un evento chimico: il rilascio quantico di neurotrasmettitore. Le molecole liberate attraversano rapidamente la fessura sinaptica, tipicamente di 20–30 nm, e attivano recettori postsinaptici in millisecondi. Questa architettura garantisce trasmissione rapida, direzionale e selettiva, riducendo la “dispersione” del segnale che è tipica della diffusione libera.
Segnalazione dipendente dal contatto — La forma più ravvicinata di comunicazione avviene per contatto diretto tra cellule contigue, senza rilascio di ligandi solubili (Figura 05.23-02). In un caso, una cellula esprime sulla membrana un ligando ancorato che attiva un recettore sulla cellula adiacente; vie come Notch/Delta svolgono ruoli chiave nella patterning tissutale durante lo sviluppo, favorendo la diversificazione di cellule inizialmente equivalenti. In altri contesti, le giunzioni comunicanti (gap junctions) permettono il passaggio diretto di ioni e piccoli metaboliti, sincronizzando attività cellulari come la contrazione miocardica. La natura contatto-dipendente assicura una precisione spaziale che nessun’altra via eguaglia.
Per orientare l’intuizione, si può ricorrere a una metafora sociale: la diffusione endocrina somiglia a un annuncio trasmesso su una rete nazionale; la comunicazione paracrina equivale a un avviso affisso nell’atrio di un edificio; la trasmissione sinaptica ricorda un messaggio diretto in una chat privata; la segnalazione da contatto è paragonabile a un sussurro all’orecchio; l’autocrina somiglia a un promemoria annotato sul proprio calendario. La (Tabella 05.23-01) riporta esempi rappresentativi di ormoni, mediatori locali, neurotrasmettitori e segnali ancorati alla membrana, con i relativi recettori e funzioni.
Indipendentemente dalla via, due principi ricorrono. Primo, la cellula è spesso sia emittente sia ricevente: molte popolazioni cellulari scambiano continuamente messaggi con l’ambiente e con se stesse, bilanciando feedback positivi e negativi. Secondo, la risposta dipende tanto dalla natura del segnale quanto dallo stato della rete intracellulare: concentrazione del ligando, durata dell’esposizione, numero di recettori, affinità di legame e organizzazione delle piattaforme di segnalazione determinano che cosa la cellula “decodifica” e come modifica il proprio comportamento.
| Molecola segnale | Origine | Natura chimica | Effetti principali |
|---|---|---|---|
| Adrenalina | Ghiandole surrenali | Derivato della tirosina | Aumenta pressione sanguigna, frequenza cardiaca e metabolismo |
| Cortisolo | Corticale surrenale | Steroide (colesterolo) | Regola metabolismo di carboidrati e proteine, risposta allo stress |
| Estradiolo | Ovaie | Steroide (colesterolo) | Stimola sviluppo dei caratteri sessuali femminili |
| Insulina | Cellule β pancreatiche | Proteina | Promuove ingresso di glucosio e sintesi di glicogeno e lipidi |
| Testosterone | Testicoli | Steroide (colesterolo) | Sviluppo caratteri sessuali maschili |
| Tiroxina | Tiroide | Derivato della tirosina | Regola metabolismo e differenziamento cellulare |
| Fattore di crescita dell’epidermide (EGF) | Varie cellule | Proteina | Stimola crescita e proliferazione cellulare |
| Fattore di crescita piastrinico (PDGF) | Piastrine e cellule varie | Proteina | Promuove divisione cellulare e cicatrizzazione |
| Fattore di crescita nervoso (NGF) | Tessuti nervosi | Proteina | Favorisce sopravvivenza e crescita di neuroni |
| Istamina | Mastociti | Derivato dell’istidina | Vasodilatazione e aumento permeabilità capillare |
| Ossido nitrico (NO) | Neuroni, cellule endoteliali | Gas | Rilassa muscolatura liscia e regola flusso sanguigno |
| Acetilcolina | Terminali nervosi | Derivato della colina | Neurotrasmettitore eccitatorio in sinapsi e giunzioni neuromuscolari |
| GABA | Neuroni | Derivato dell’acido glutammico | Neurotrasmettitore inibitorio |
| Delta (segnale contatto-dipendente) | Cellule in sviluppo | Proteina transmembrana | Controlla differenziamento cellulare in fase embrionale |
Molecole segnale e loro effetti biologici
Le molecole segnale regolano comunicazioni complesse tra cellule e tessuti. Possono essere ormoni, mediatori locali, neurotrasmettitori o segnali contatto-dipendenti. Questi composti modulano funzioni vitali come metabolismo, crescita, differenziamento e attività neuronale, garantendo la coordinazione dei processi fisiologici nell’organismo.
Negli organismi pluricellulari, ogni cellula è immersa in un ambiente extracellulare ricco di molecole segnale eterogenee, presenti in forma solubile nei fluidi, incorporate nella matrice extracellulare o esposte sulla superficie di cellule adiacenti. Da questa molteplicità di input, la cellula seleziona quelli rilevanti, ignorandone altri, in funzione della propria identità e del proprio stato fisiologico. La possibilità stessa di percepire uno specifico segnale è anzitutto legata all’espressione di un recettore appropriato: in assenza del recettore cognato, il segnale resta “invisibile” e non si produce alcuna risposta. In generale, ciascun recettore presenta alta specificità per il proprio ligando e, reciprocamente, un ligando attiva un numero limitato di recettori correlati.
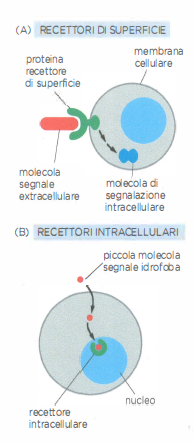
Le molecole segnale extracellulari si possono raggruppare in due grandi categorie, definite dal modo in cui superano la barriera della membrana plasmatica della cellula bersaglio. Il gruppo più numeroso comprende molecole di dimensioni elevate o fortemente idrofile, incapaci di diffondere attraverso il doppio strato lipidico: esse si legano a recettori transmembrana e trasmettono l’informazione oltre la membrana mediante cambiamenti conformazionali e catene di trasduzione intracellulari (Figura 05.23-03). Una seconda classe è costituita da ligandi sufficientemente piccoli o idrofobici da attraversare la membrana e raggiungere il citosol o il nucleo, dove interagiscono con recettori intracellulari, spesso fattori di trascrizione ligandodipendenti (Figura 05.23-03). In questa sede l’attenzione è rivolta prevalentemente alla segnalazione mediata da recettori di superficie;
Poiché una cellula esprime solo un sottoinsieme del vasto repertorio potenziale di recettori, essa limita deliberatamente la gamma di messaggi che può decodificare. Ciononostante, anche un numero relativamente esiguo di segnali è in grado di rimodellare profondamente il comportamento cellulare. Le conseguenze funzionali includono, tra le altre, modificazioni di:
- morfologia e adesione, con riorganizzazione del citoscheletro e dei contatti con la matrice;
- motilità, mediante modulazione di protrusioni e contrazioni cellulari;
- metabolismo, per riconfigurazione dei flussi catabolici e anabolici;
- espressione genica, tramite attivazione o repressione di programmi trascrizionali;
- ciclicità proliferativa, differenziamento o entrata in quiescenza.
Il segnale raccolto alla superficie viene propagato verso l’interno da una rete di intermedi, quali secondi messaggeri (per esempio Ca2+, AMP ciclico, diacilglicerolo), chinasi e fosfatasi, GTPasi della famiglia Ras e proteine adattatrici. Questo flusso informativo culmina nell’attivazione di proteine effettrici che esercitano un’azione diretta sui processi cellulari. Struttura e composizione di tali reti di trasduzione non sono universali: differiscono tra tipi cellulari e stati fisiologici, con la conseguenza che lo stesso segnale extracellulare può generare esiti distinti in cellule differenti. Un esempio istruttivo è fornito dal TGF-β: il medesimo ligando, legandosi ai recettori TGF-β di tipo I e II, può indurre arresto del ciclo cellulare in cellule epiteliali e, al contempo, stimolare la deposizione di matrice extracellulare in fibroblasti; la diversità delle risposte dipende dall’integrazione dei complessi SMAD con cofattori e paesaggi cromatinici specifici di cellula.
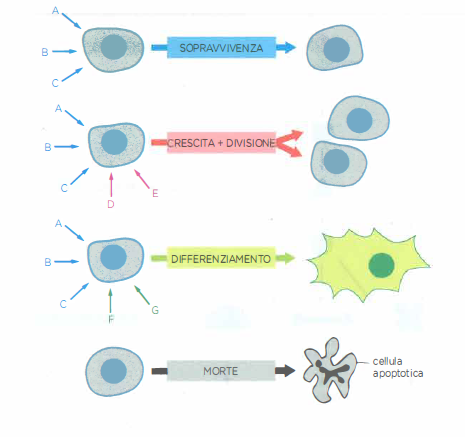
La molecola segnale extracellulare, dunque, non esaurisce il contenuto informativo dell’evento: il significato biologico del messaggio scaturisce dall’interpretazione contestuale operata dalla cellula. Tipicamente, una singola cellula esprime molti tipi di recettori, ciascuno in numerose copie. Tale multirecettorialità consente di percepire simultaneamente più segnali e, soprattutto, di combinarli secondo “codici” integrativi. Le interazioni tra vie di segnalazione — per convergenza su nodi comuni, retroazioni e modulazioni reciproche — fanno sì che combinazioni di ligandi producano risposte non semplicemente addittive. Ne derivano scenari in cui:
- un set di segnali sostiene la sopravvivenza cellulare, mantenendo attive vie antiapoptotiche;
- un diverso insieme promuove differenziamento, con ristrutturazione stabile dei profili trascrizionali;
- altri pattern innescano crescita e divisione, coordinando metabolismo, biosintesi e ciclo cellulare.
Importante, molte cellule animali sono programmate a eliminarsi quando mancano input trofici o segnali di ancoraggio: l’assenza di tali stimoli attiva vie pro-apoptotiche e porta alla morte cellulare programmata (Figura 05.23-05). L’architettura della matrice extracellulare, le connessioni con cellule vicine e la storia recente di esposizione a segnali modulano, inoltre, soglie di risposta e “memorie” intracellulari, influenzando la selettività futura.
Per completezza, si ricorda che le principali famiglie di recettori di superficie includono recettori accoppiati a proteine G, recettori tirosin-chinasici e canali ionici attivati da ligando; i recettori intracellulari comprendono i recettori nucleari per ormoni steroidei e tiroidei, nonché sensori citosolici per gas come NO. Sebbene condividano temi ricorrenti — riconoscimento del ligando, trasduzione e risposta — ciascuna famiglia impiega strategie molecolari distinte e integra segnali in modo specifico per tipo cellulare.
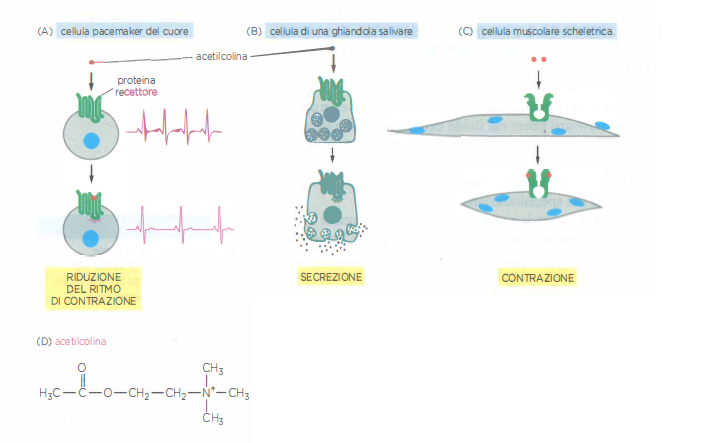
La (Figura 05.23-04) illustra come cambiamenti nei moduli di trasduzione e negli effettori determinino la varietà degli esiti. Per esempio, catecolamine come adrenalina, a seconda del tessuto, inducono aumento della frequenza di contrazione nei cardiomiociti, rilassamento del muscolo liscio bronchiale o mobilizzazione del glicogeno negli epatociti; la risposta finale riflette sia i sottotipi recettoriali espressi sia l’assetto delle vie intracellulari e degli effettori disponibili.
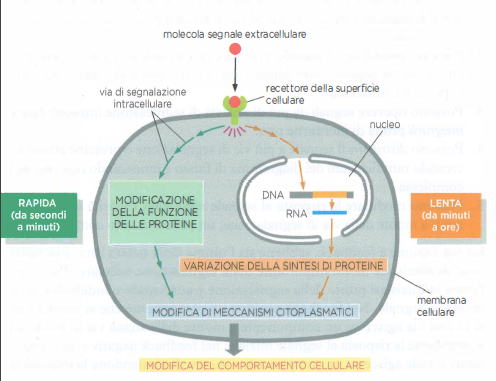
La cinetica con cui una cellula risponde a un segnale extracellulare dipende dagli eventi molecolari necessari a trasformare l’input in un effetto. Alcune risposte sono estremamente rapide perché modulano proteine preesistenti senza necessità di nuova sintesi: l’apertura di canali ionici attivati da ligando altera il potenziale di membrana in millisecondi; l’azione del monossido di azoto sulla guanilato ciclasi solubile nel muscolo liscio vascolare incrementa GMP ciclico e rilassa la parete in pochi secondi. Analogamente, l’attivazione di una cascata di fosforilazioni può riconfigurare velocemente enzimi metabolici o motori del citoscheletro, con esiti percepibili in tempi dell’ordine di secondi o minuti.
Altre risposte richiedono invece tempi lunghi, poiché comportano rimodellamento trascrizionale e traduzione di nuove proteine. L’ingresso in ciclo cellulare e la progressione alla divisione, una volta ricevuti segnali mitogenici appropriati, si sviluppano nell’arco di ore e implicano l’induzione di cicline, la replicazione del DNA e il rimaneggiamento della cromatina (Figura 05.23-06). Similmente, ormoni steroidei che attivano recettori nucleari regolano programmi genici di differenziamento e metabolismo con latenza da decine di minuti a molte ore, coerentemente con i tempi della sintesi proteica e dell’assemblaggio di nuovi complessi funzionali.
In sintesi, la latenza della risposta è funzione di tre fattori principali:
- livello al quale agisce il segnale, post-traduzionale su proteine preformate versus regolazione dell’espressione genica;
- numero e complessità dei passaggi nella catena di trasduzione, inclusi feedback e feedforward che possono accelerare o rallentare la dinamica;
- disponibilità di risorse cellulari (per esempio, pool di secondi messaggeri, aminoacidi, nucleotidi) e stato del ciclo cellulare al momento della stimolazione.
La capacità di alternare risposte rapide, utili all’adattamento immediato, con risposte lente, responsabili di modificazioni stabili, conferisce alle cellule un controllo fine e multilivello del proprio comportamento, integrando segnali ambientali con la propria storia funzionale.
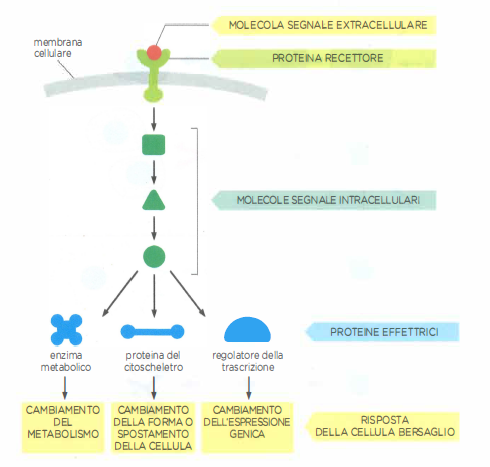
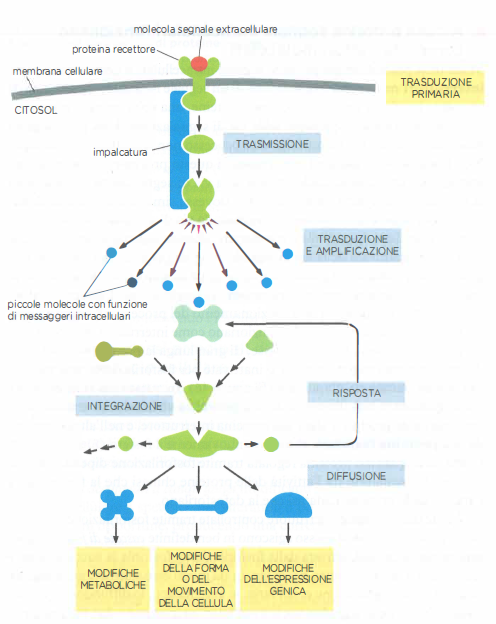
La maggior parte dei mediatori extracellulari è costituita da proteine, peptidi e piccole molecole idrofile che, non potendo attraversare liberamente il doppio strato lipidico, si legano a recettori proteici esposti sulla superficie della cellula (Figura 05.23-03). Questi recettori transmembrana percepiscono l’informazione ambientale e la trasformano in segnali endocellulari di nuova natura, avviando il processo di trasduzione (Figura 05.23-03). L’informazione viaggia poi lungo catene di molecole segnale intracellulari, organizzate in una staffetta biochimica in cui ciascun componente attivato promuove l’attivazione del successivo, fino a coinvolgere proteine effettrici: enzimi metabolici, regolatori del citoscheletro o fattori che modulano l’espressione genica. L’esito integrato di tali modificazioni costituisce la risposta cellulare (Figura 05.23-07). I moduli che compongono queste vie svolgono funzioni riconducibili alle categorie di base illustrate in (Figura 05.23-08).
- Trasferimento del segnale al livello successivo della via, garantendo la propagazione ordinata dell’informazione;
- Amplificazione del segnale, così che anche un ridotto numero di molecole extracellulari possa indurre una risposta intracellulare robusta;
- Integrazione di input multipli, con convergenza di segnali provenienti da vie diverse prima della loro riconsegna a valle;
- Distribuzione verso più rami o verso differenti proteine effettrici, generando risposte composite e contestuali;
- Modulazione retroattiva della via mediante feedback, regolando componenti a monte per aumentare o attenuare la risposta.
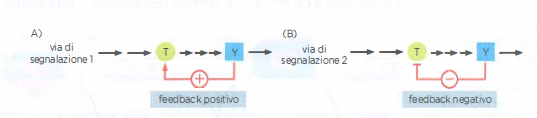
La regolazione a feedback è una proprietà cardine dei sistemi di segnalazione. Può intervenire a molteplici livelli e in qualsiasi fase, rafforzando o smorzando il segnale iniziale. Nel feedback positivo, un componente a valle potenzia un nodo a monte, rendendo la risposta più decisa e talora bistabile; nel feedback negativo, un elemento a valle inibisce un passaggio precedente, stabilizzando l’uscita o generando oscillazioni temporali (Figura 05.23-09). Circuiti a feedback positivo possono produrre risposte di tipo “interruttore” (tutto-o-nulla), mentre feedback negativi, soprattutto se con ritardi temporali, possono indurre andamenti oscillatori. In termini semplificati, la pendenza della risposta può essere descritta da funzioni ultrasensibili, ad esempio con cooperatività effettiva elevata, mentre la stabilità dipende dal bilancio tra guadagni positivi e negativi all’interno dell’anello di controllo.
Numerose proteine di segnalazione intracellulari funzionano come interruttori che commutano tra stati inattivo e attivo. Una volta attivate da un evento a monte, attivano a loro volta altri elementi della via, fino a coinvolgere le proteine effettrici. Affinché il sistema resti modulabile e pronto a rispondere a nuovi stimoli, l’attivazione deve essere transitoria e reversibile: ogni passaggio di attivazione richiede un meccanismo di spegnimento dedicato. Senza questo “ripristino” periodico, una via che, per esempio, incrementa il tono contrattile vascolare rimarrebbe cronicamente attiva, con esiti maladattativi. In termini generali, l’efficienza della trasduzione dipende tanto dai processi di accensione quanto da quelli di disattivazione.
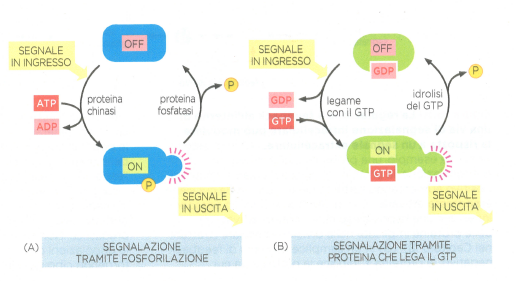
Due classi principali di switch molecolari sono particolarmente diffuse. La prima, la più numerosa, comprende proteine regolate dalla fosforilazione. Una proteina chinasi trasferisce un gruppo fosfato a specifici residui della proteina bersaglio, mentre una proteina fosfatasi rimuove il fosfato, invertendo lo stato (Figura 05.23-10). Il livello di attività di una proteina fosforilabile riflette il bilancio dinamico tra le attività delle chinasi e delle fosfatasi che la controllano. In modo schematico, indicando con P la forma non fosforilata e con P* la forma fosforilata:
\[ \frac{d[P^*]}{dt} = k_{\mathrm{on}}[\text{chinasi}]\,[P] - k_{\mathrm{off}}[\text{fosfatasi}]\,[P^*], \]
dove l’equilibrio tra i due termini determina la frazione di proteina nello stato attivo. Molte proteine regolabili per fosforilazione sono esse stesse chinasi, organizzate in vere e proprie cascate: la fosforilazione di una chinasi a monte attiva una chinasi a valle, e così via, con amplificazione del segnale e possibilità di ramificazione e modulazione fine. Due grandi famiglie sono particolarmente rappresentate nelle vie intracellulari: le serina/treonina chinasi, che modificano residui di serina o treonina, e le tirosina chinasi, che agiscono sui residui di tirosina.
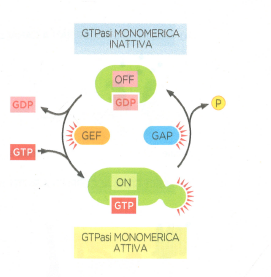
La seconda classe di interruttori è costituita dalle proteine leganti nucleotidi guaninici, che alternano automaticamente stati attivi (GTP-legato) e inattivi (GDP-legato), sfruttando l’attività GTPasica intrinseca per auto-disattivarsi dopo l’attivazione (Figura 05.23-10). Due famiglie operative coesistono: le grandi proteine G trimeriche, che mediano la segnalazione dei recettori accoppiati a proteine G, e le piccole GTPasi monomeriche (ad esempio delle famiglie Ras, Rho, Rab), che instradano molteplici processi intracellulari, dalla proliferazione alla dinamica del traffico vescicolare. Le GTPasi monomeriche sono controllate da due gruppi di regolatori: i fattori di scambio del nucleotide guanina (GEF), che favoriscono la sostituzione del GDP con GTP promuovendo l’attivazione, e le proteine attivanti la GTPasi (GAP), che accelerano l’idrolisi del GTP e quindi la disattivazione (Figura 05.23-11). La combinazione locale di GEF e GAP modula sia l’intensità sia la durata del segnale, consentendo risposte spazialmente circoscritte.
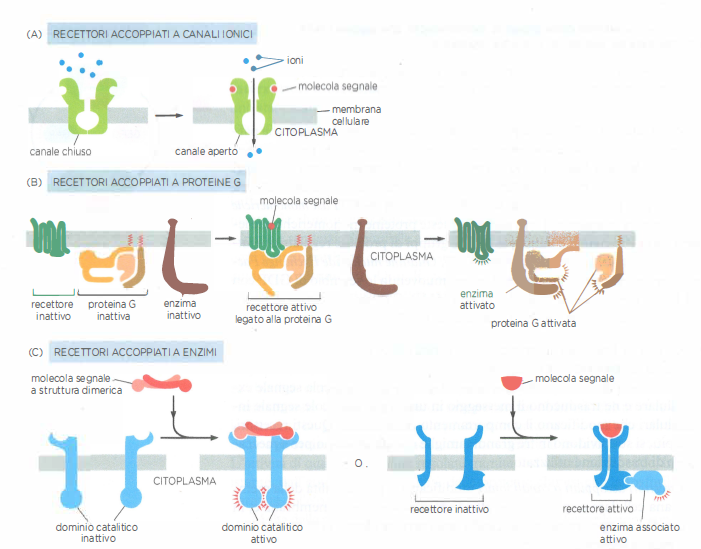
I recettori di membrana riconoscono una molecola segnale extracellulare e la traducono in uno o più segnali intracellulari capaci di modificare il comportamento della cellula. Sulla base del meccanismo di trasduzione, si distinguono tre grandi categorie.
- Recettori accoppiati a canali ionici: alterano la permeabilità della membrana a ioni specifici, modificando il potenziale di membrana e, quando appropriato, generando correnti elettriche misurabili (Figura 05.23-12);
- Recettori accoppiati a proteine G: attivano proteine G trimeriche associate alla membrana, che a loro volta modulano enzimi o canali ionici e avviano cascate di segnalazione intracellulare (Figura 05.23-12);
- Recettori accoppiati a enzimi: possiedono attività enzimatica intrinseca o reclutano enzimi sul versante citosolico della membrana plasmatica, attivando reti di segnalazione a valle (Figura 05.23-12).
Ognuna di queste famiglie include molteplici sottotipi recettoriali. Una stessa molecola segnale può essere riconosciuta da differenti recettori, anche appartenenti a classi diverse, generando segnali intracellulari distinti e risposte fisiologiche differenziate. Un esempio classico è l’acetilcolina, che nel muscolo scheletrico agisce tramite un recettore-canale cationico, mentre nel miocardio opera attraverso un recettore accoppiato a proteina G, con esiti funzionali opposti: contrazione potenziata nelle fibre scheletriche e riduzione di frequenza e forza nel tessuto cardiaco (Figura 05.23-04).
La molteplicità dei recettori di superficie li rende anche bersagli di numerose sostanze esogene capaci di interferire con i circuiti fisiologici: farmaci, tossine, ma anche composti naturali come capsaicina, nicotina o oppioidi. Questi ligandi possono comportarsi da agonisti o antagonisti, rispettivamente attivando o bloccando la funzione recettoriale (Tabella 05.23-02). La farmacologia recettoriale mira a identificare molecole con elevata selettività, in grado di modulare in modo prevedibile un preciso recettore di membrana.
| Sostanza estranea | Molecola segnale imitata | Azione sul recettore | Effetto sull’organismo |
|---|---|---|---|
| Barbiturici e benzodiazepine | GABA | Attivano recettori associati a canali ionici GABA-sensibili | Sedazione e riduzione dell’ansia |
| Nicotina | Acetilcolina | Stimola recettori nicotinici per l’acetilcolina | Vasocostrizione, aumento della pressione arteriosa |
| Morfina ed eroina | Endorfine / encefaline | Legano recettori oppioidi accoppiati a proteine G | Analgesia ed euforia |
| Curaro | Acetilcolina | Blocca recettori nicotinici della giunzione neuromuscolare | Paralisi muscolare per inibizione della trasmissione |
| stricnina | Glicina | Inibisce recettori ionotropici della glicina | Convulsioni per blocco dell’inibizione sinaptica |
| Capsaicina | Stimolo termico (calore) | Attiva recettori sensibili al calore | Sensazione di bruciore e, a lungo termine, analgesia |
| Mentolo | Stimolo termico (freddo) | Attiva recettori sensibili al freddo | Sensazione di freschezza; alte dosi provocano bruciore |
Effetti di sostanze estranee su recettori cellulari
Numerose sostanze di origine naturale o sintetica interagiscono con recettori di superficie, imitando o bloccando molecole segnale fisiologiche. Questi composti possono alterare la trasmissione nervosa, la percezione sensoriale o l’attività muscolare, determinando effetti che vanno dalla sedazione e analgesia fino a convulsioni o paralisi.
Tra i recettori di superficie, i recettori accoppiati a canali ionici (o canali controllati da ligando) sono i più diretti nel meccanismo d’azione. Nel sistema nervoso, consentono una trasmissione rapida attraverso le sinapsi: il legame del neurotrasmettitore sul versante esterno del recettore induce un cambiamento conformazionale che apre o chiude il poro ionico, permettendo il flusso selettivo di ioni come Na⁺, K⁺ e Ca²⁺ (Figura 05.23-12). L’apertura del canale produce una corrente che, in prima approssimazione, può descriversi come
\[ I_{\text{ion}} = g_{\text{ion}}\,(V_m - E_{\text{ion}}), \]
dove \(g_{\text{ion}}\) è la conduttanza del canale per quello ione, \(V_m\) il potenziale di membrana ed \(E_{\text{ion}}\) il potenziale di equilibrio dell’ione, determinabile con l’equazione di Nernst. La variazione di \(V_m\), in genere nell’ordine dei millisecondi, può generare un potenziale d’azione o modulare la probabilità che altri stimoli lo inneschino. L’ingresso di Ca²⁺ riveste inoltre un ruolo di secondo messaggero, regolando proteine sensibili al calcio e collegando il segnale elettrico a risposte biochimiche diffuse.
Sebbene tipici delle cellule eccitabili, come neuroni e fibre muscolari, i recettori-canale sono presenti anche in altri contesti in cui è cruciale una trasduzione rapida e quantizzata del segnale. Per contro, i recettori accoppiati a proteine G e quelli a enzimi sono ampiamente utilizzati dalla maggioranza dei tipi cellulari e orchestrano risposte che si estendono su scale temporali più ampie, dal secondo alle ore, integrando informazione con notevole plasticità.