La traduzione è la sintesi di un polipeptide dettata dall’RNA: uno sguardo da vicino
Definizione
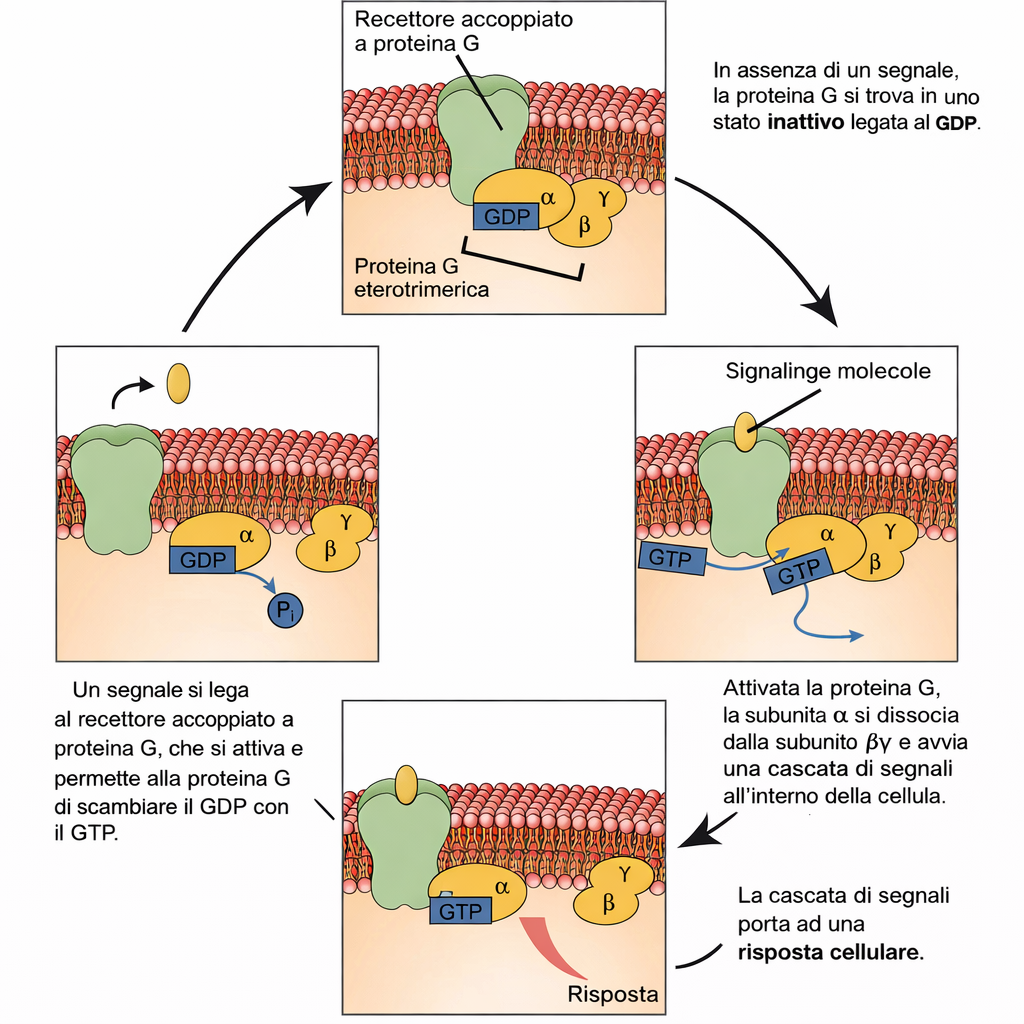
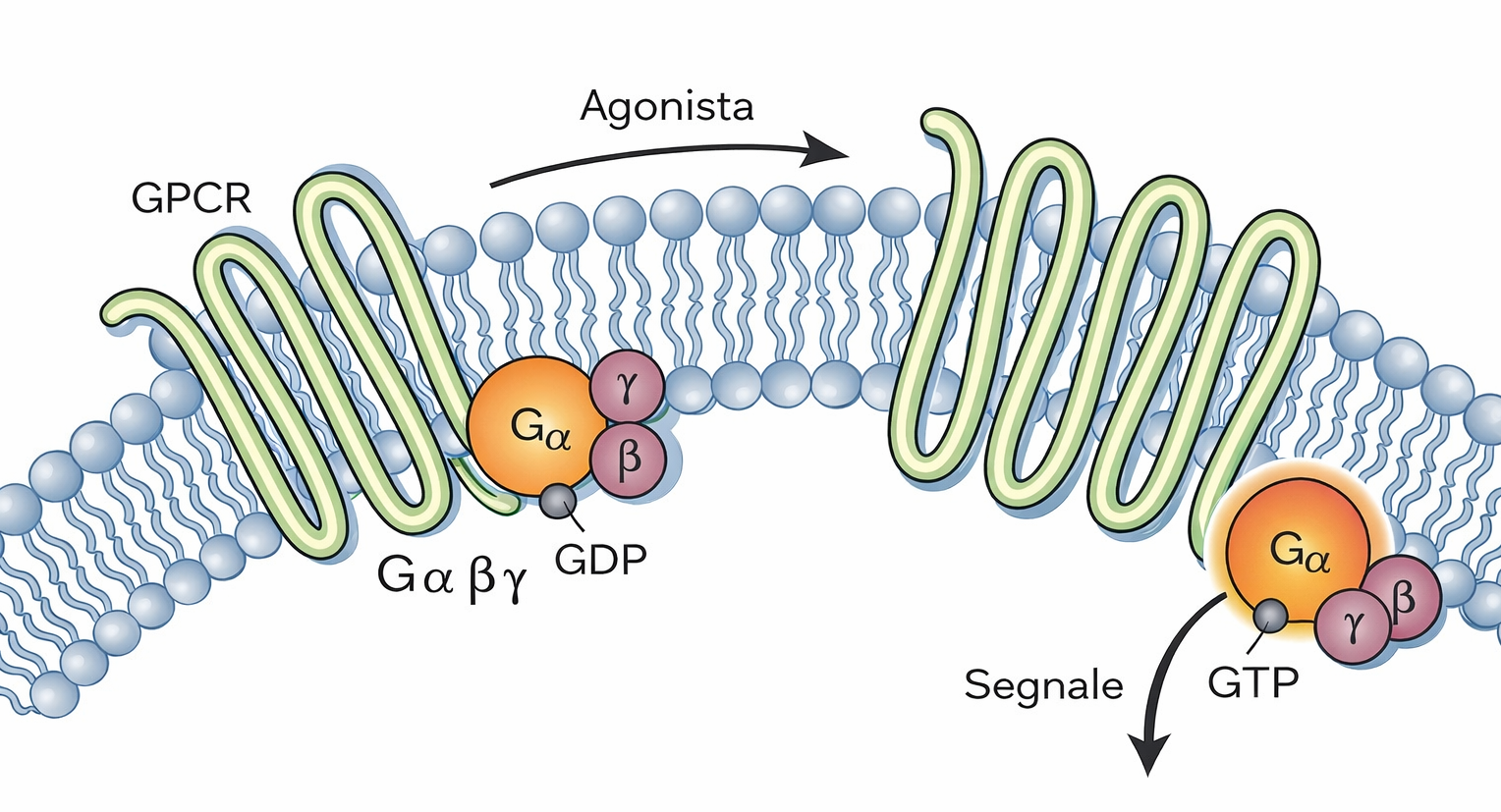
Il legame di un ligando extracellulare a un recettore accoppiato a proteine G (GPCR) induce una transizione conformazionale del recettore che, sulla faccia citosolica della membrana, abilita l’interazione con una proteina G eterotrimerica. Per comprendere come il segnale venga propagato, è utile richiamare l’architettura e la dinamica funzionale di queste proteine. Le proteine G appartengono a famiglie diverse, ognuna selettiva per specifici GPCR e per particolari effettori di membrana (enzimi o canali ionici), ma condividono un disegno modulare: una subunità α (Gα) e un dimero Gβγ. Due componenti del complesso sono ancorati al foglietto citosolico della membrana grazie a code lipidiche (ad esempio, miristoilazione/palmitoilazione su Gα e prenilazione su Gγ), che favoriscono il corretto posizionamento e l’efficienza di accoppiamento. Nello stato basale, Gα lega GDP ed è inattiva (Figura 05.24-02). L’interazione con un GPCR stimolato conferisce al recettore attività di fattore di scambio dei nucleotidi guaninici (GEF), riducendo l’affinità di Gα per il GDP e consentendo la sua sostituzione con GTP, favorito dall’elevato rapporto citosolico GTP/GDP. L’evento di scambio può portare alla separazione di Gα-GTP dal dimero Gβγ, oppure a una loro riorganizzazione pur mantenendo un contatto transitorio; in entrambi i casi, sia Gα-GTP sia Gβγ acquisiscono la capacità di legare direttamente effettori di membrana e di modulare la trasduzione del segnale (Figura 05.24-02). L’intensità e la durata della risposta dipendono dal tempo in cui le subunità attive restano associate ai loro bersagli. Questo intervallo è determinato dalla GTPasi intrinseca di Gα, spesso accelerata da proteine regolatrici della segnalazione delle G (RGS), che catalizzano l’idrolisi del GTP: \( \mathrm{G\alpha{\text -}GTP} \rightarrow \mathrm{G\alpha{\text -}GDP} + \mathrm{P_i} \). Una volta idrolizzato il GTP, Gα-GDP si riaccoppia a Gβγ, riformando il complesso inattivo. Tale ciclo, che avviene tipicamente nell’arco di pochi secondi, consente un controllo fine dello spegnimento del segnale e prepara la proteina G a eventuali successive riattivazioni da parte di GPCR ancora occupati dal ligando. In molte cellule, la portata complessiva della risposta risulta inoltre modulata dai meccanismi di desensibilizzazione del recettore (fosforilazione mediata da GRK e legame di arrestine), che limitano la capacità del GPCR di funzionare come GEF.
Il comportamento a interruttore delle proteine G illustra un principio cardine della segnalazione cellulare: l’accensione del segnale è inscindibile dai meccanismi che ne garantiscono l’arresto controllato. Proprio questi dispositivi di spegnimento rappresentano punti di vulnerabilità. Nel colera, il batterio intestinale Vibrio cholerae secerne la tossina colerica, che entra negli enterociti e ADP-ribosila la Gαs, compromettendo la sua attività GTPasica. Gαs resta bloccata nello stato GTP-legato e continua a stimolare l’adenilato ciclasi, con produzione persistente di AMP ciclico (cAMP). L’aumento di cAMP attiva la proteina chinasi A e potenzia la conduttanza al cloruro del canale CFTR, provocando un robusto efflusso di Cl⁻ nel lume, seguito osmoticamente da Na⁺ e acqua; ne risultano diarrea acquosa profusa e disidratazione potenzialmente letale se non si ripristinano prontamente acqua ed elettroliti. Un meccanismo concettualmente affine, ma con esito molecolare opposto su Gα, caratterizza la pertosse. Bordetella pertussis produce una tossina che ADP-ribosila Gαi vicino all’estremità carbossiterminale, impedendole di interagire con il GPCR e di scambiare GDP con GTP. Gαi rimane così intrappolata nello stato GDP-legato inattivo e non può inibire l’adenilato ciclasi. Anche in questo caso l’effetto finale è un incremento inappropriato e prolungato del cAMP, che, a livello delle vie aeree, contribuisce a un’alterata regolazione dell’epitelio e alla tosse parossistica, facilitando la diffusione del patogeno. In sintesi, colera e pertosse colpiscono snodi distinti dello stesso circuito (Gαs vs Gαi), ma convergono sull’iperattivazione dell’adenilato ciclasi e dei suoi effetti a valle.
Nei mammiferi sono state identificate numerose proteine G eterotrimeriche, ciascuna deputata a uno spettro definito di effettori. Oltre a enzimi di membrana, importanti bersagli sono i canali ionici. Un esempio emblematico riguarda il controllo parasimpatico della frequenza cardiaca: le terminazioni vagali rilasciano acetilcolina, che si lega a recettori muscarinici M2 (GPCR) sulla superficie delle cellule pacemaker del nodo senoatriale. L’attivazione del recettore accoppia una proteina Gi; in questo contesto, il dimero Gβγ è l’elemento operativo principale, poiché si lega ai canali potassici GIRK (Kir3.x) sulla faccia citosolica, stabilizzandone lo stato aperto (Figura 05.24-03). L’aumento della permeabilità al K⁺ induce un’uscita di carica positiva, iperpolarizza la membrana e riduce la probabilità di innesco dei potenziali d’azione, con conseguente rallentamento della frequenza cardiaca. Il canale si richiude quando Gα idrolizza il GTP, il complesso eterotrimerico si riforma e l’input di Gβγ al canale cessa (Figura 05.24-03). Questa modalità di controllo, rapida e localizzata, opera su scale temporali di millisecondi–secondi e si riscontra anche in altri tessuti eccitabili: ad esempio, Gβγ può inibire transitoriamente i canali del Ca²⁺ voltaggio-dipendenti di tipo N e P/Q nei neuroni, modulando il rilascio di neurotrasmettitori:
- stimolo iniziale: legame del ligando al GPCR e attivazione di Gi/Go;
- segnale effettore: rilascio/riorganizzazione del dimero Gβγ e legame diretto al canale ionico bersaglio;
- risposta cellulare: modifica della conduttanza (apertura di canali per K⁺ o inibizione di canali per Ca²⁺), con effetti immediati sull’eccitabilità elettrica;
- terminazione: idrolisi del GTP da parte di Gα, riassemblaggio dell’eterotrimero e chiusura/inversione dell’effetto sul canale.
Quando le proteine G agiscono su enzimi di membrana, l’esito è la formazione di piccole molecole segnale intracellulari, i cosiddetti secondi messaggeri, che diffondono e amplificano l’informazione iniziale. Due vie ricorrenti coinvolgono: 1) l’adenilato ciclasi, che sintetizza AMP ciclico (cAMP); 2) la fosfolipasi Cβ (PLCβ), che scinde un fosfoinositide di membrana generando inositolo 1,4,5-trifosfato (IP₃) e diacilglicerolo (DAG). IP₃ promuove il rilascio di Ca²⁺ dai depositi intracellulari, mentre DAG rimane nella membrana e coopera con Ca²⁺ nell’attivazione della proteina chinasi C (PKC). In molti sistemi, Ca²⁺ agisce esso stesso come secondo messaggero, associandosi a proteine sensori come la calmodulina. Le subfamiglie di Gα presidiano l’instradamento verso effettori distinti: Gαs stimola l’adenilato ciclasi, Gαi la inibisce, Gαq/11 attiva PLCβ; altre vie, come quelle mediate da Gα12/13, dialogano con RhoGEF e con circuiti citoscheletrici. La capacità dei secondi messaggeri di diffondere dal sito di produzione consente un’amplificazione sostanziale dell’output rispetto all’evento di legame recettoriale. In termini funzionali, cAMP può modulare PKA, EPAC e canali ciclico-nucleotidici; IP₃ e Ca²⁺ orchestrano risposte coordinate del reticolo endoplasmatico e del citosol; DAG stabilizza l’attivazione di PKC e di altre proteine sensibili ai lipidi. L’omeostasi del segnale richiede vie di spegnimento altrettanto efficienti: fosfodiesterasi degradano cAMP; le fosfatasi dell’inositolo e le chinasi lipidiche rimodellano IP₃ e DAG; pompe e scambiatori rimuovono il Ca²⁺ dal citosol. Insieme al ciclo di idrolisi del GTP su Gα, tali meccanismi garantiscono che la risposta sia proporzionata nel tempo e nello spazio all’entità dello stimolo.
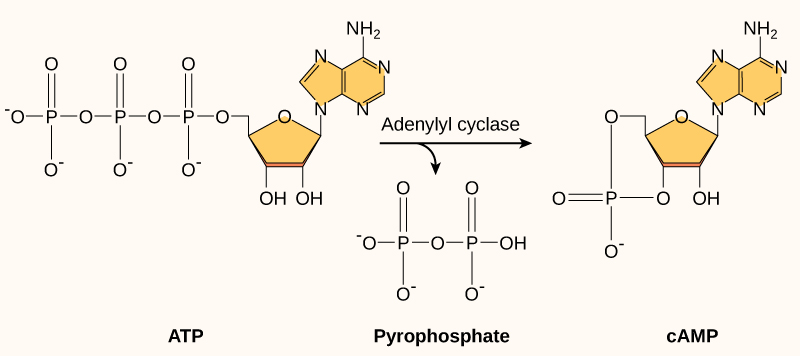
Numerosi segnali extracellulari che agiscono tramite recettori accoppiati a proteine G (GPCR) modulano l’adenilato ciclasi, alterando la concentrazione intracellulare di AMP ciclico (cAMP), un secondo messaggero idrosolubile. Nello scenario più comune, la subunità α di una proteina G di tipo Gs attiva l’adenilato ciclasi, con un brusco incremento della produzione di cAMP a partire dall’ATP, sempre disponibile nella cellula. La reazione catalizzata può essere schematizzata come \( \mathrm{ATP} \rightarrow \mathrm{cAMP} + \mathrm{PP_i} \), seguita dalla rapida idrolisi del pirofosfato a ortofosfato, che rende termodinamicamente favorevole il flusso di reazione. La terminazione del segnale è affidata principalmente alla cAMP-fosfodiesterasi, la quale converte il cAMP in 5′-AMP secondo \( \mathrm{cAMP} + \mathrm{H_2O} \rightarrow 5'\text{-}\mathrm{AMP} \) (Figura 05.24-04). Sostanze di uso comune come la caffeina agiscono bloccando selettivamente la fosfodiesterasi in alcuni distretti del sistema nervoso, rallentando così la degradazione del cAMP e prolungandone l’azione. Poiché la fosfodiesterasi è costitutivamente attiva, la concentrazione di cAMP è altamente dinamica e può variare in pochi secondi di un ordine di grandezza in risposta alla stimolazione recettoriale (Figura 05.24-05). Il cAMP, data la sua solubilità, può muoversi dal punto di sintesi presso la membrana plasmatica al citosol e al nucleo, raggiungendo proteine bersaglio in compartimenti distinti. Tuttavia, nelle cellule reali il segnale è spesso confinato in microdomini grazie a proteine di ancoraggio (AKAP) che organizzano complessi locali con l’adenilato ciclasi, la proteina chinasi A (PKA), le fosfatasi e le fosfodiesterasi, permettendo una trasduzione spazialmente precisa. Il principale effettore del cAMP è la PKA, una serina/treonina chinasi che in condizioni basali è presente come oloenzima inattivo (tipicamente R2C2, con due subunità regolatorie R e due catalitiche C). Il legame del cAMP ai siti allosterici delle subunità R induce una transizione conformazionale che libera le subunità C attive, le quali fosforilano residui di serina o treonina su specifiche proteine. La selettività della risposta dipende dall’insieme di substrati disponibili in ciascun tipo cellulare e dalla loro colocalizzazione con PKA. La (Tabella 05.24-01) riassume una serie di risposte cellulari pilotate dal cAMP, evidenziando l’eterogeneità dei bersagli e degli esiti funzionali:
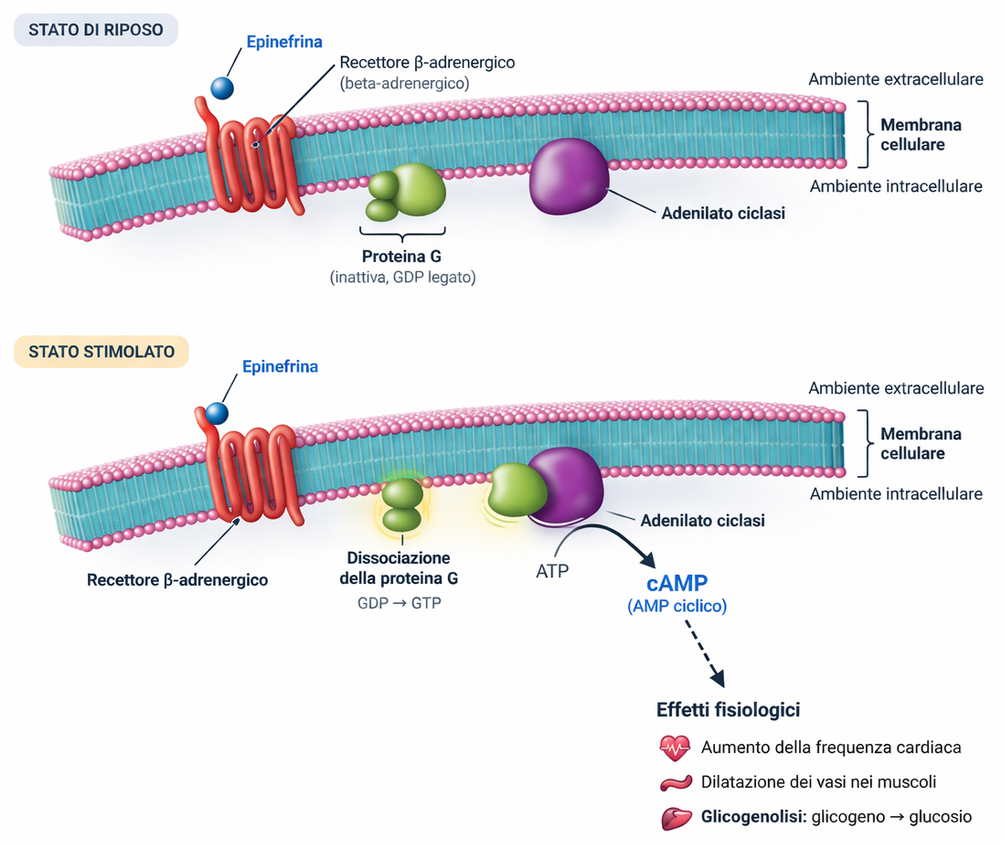
- muscolo scheletrico: l’adrenalina che si lega ai recettori adrenergici β (Figura 05.24-01) eleva il cAMP, attiva PKA e favorisce la demolizione del glicogeno tramite fosforilazione della fosforilasi chinasi con conseguente attivazione della glicogeno fosforilasi, mentre inibisce la glicogeno sintasi mediante fosforilazione inibitoria;
- tessuto adiposo: l’incremento di cAMP promuove la lipolisi attraverso la fosforilazione delle perilipine e dell’ormone-sensibile lipasi (HSL), liberando acidi grassi come combustibile ossidabile;
- miocardio: PKA fosforila canali del Ca²⁺ di tipo L e proteine regolatorie del reticolo sarcoplasmatico (ad esempio fosfolambano), aumentando ingresso e riciclo di Ca²⁺, con potenziamento dell’inotropismo e, tramite modulazione di correnti pacemaker, della frequenza cardiaca.
Molte di queste risposte sono rapide: nel muscolo scheletrico, l’aumento del cAMP indotto dall’adrenalina si traduce in attivazioni enzimatiche osservabili entro pochi secondi (Figura 05.24-06). Altre azioni sono invece tardive e implicano rimodellamenti dell’espressione genica. In tali casi, le subunità catalitiche della PKA raggiungono il nucleo e fosforilano regolatori trascrizionali, tra cui CREB (cAMP response element-binding protein) su Ser133; il complesso CREB–CBP/p300 recluta la macchina trascrizionale su promotori contenenti elementi CRE, aumentando la sintesi di specifici mRNA. In neuroni selezionati, l’impennata di cAMP modula l’espressione di proteine legate alla plasticità sinaptica e ai processi di memoria. La fine della risposta non dipende soltanto dalla fosfodiesterasi (Figura 05.24-04), ma anche da meccanismi di desensibilizzazione recettoriale: fosforilazione dei GPCR da parte di GRK, legame di β–arrestina, internalizzazione del recettore e, a monte, idrolisi del GTP sulla subunità Gα. Inoltre, GPCR accoppiati a proteine Gi possono ridurre l’attività dell’adenilato ciclasi, opponendosi ai segnali Gs. L’insieme di questi dispositivi garantisce che la variazione di cAMP sia transiente e proporzionata allo stimolo (Figura 05.24-05). Le vie a cAMP illustrano come uno stesso secondo messaggero coordini risposte multiple, da adattamenti metabolici acuti fino a cambiamenti trascrizionali durevoli. Passiamo ora all’altra grande rotta di trasduzione a valle dei GPCR, incentrata sull’attivazione della fosfolipasi C e sulla generazione di diacilglicerolo, inositolo trifosfato e Ca²⁺.
Risposte cellulari indotte dall’AMP ciclico
| Molecola segnale | Tessuto bersaglio | Risposta cellulare |
|---|---|---|
| Adrenalina | Miocardio | Aumento della frequenza e della forza contrattile |
| Adrenalina | Muscolo scheletrico | Attivazione della demolizione del glicogeno |
| Adrenalina, Glucagone | Tessuto adiposo | Stimolazione della lipolisi con demolizione dei grassi |
| Ormone adrenocorticotropo (ACTH) | Corticale surrenale | Induzione della secrezione di cortisolo |
| Tabella che illustra come molti ormoni e mediatori extracellulari trasmettano i loro effetti tramite l’AMP ciclico (cAMP), secondo messaggero intracellulare capace di amplificare rapidamente il segnale e di indurre risposte specifiche come la regolazione del metabolismo energetico, la mobilizzazione dei depositi lipidici e la modulazione dell’attività cardiaca. | ||
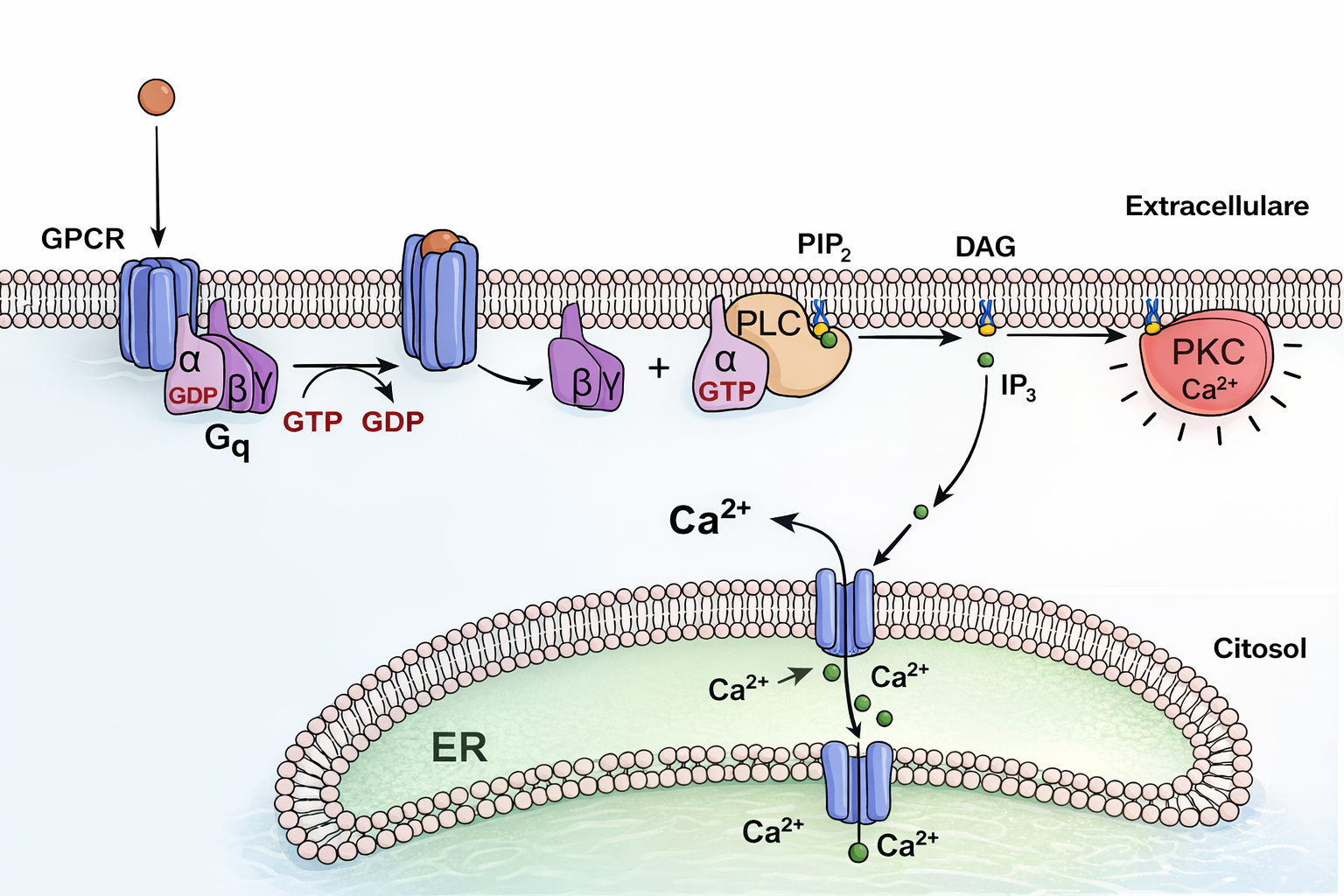
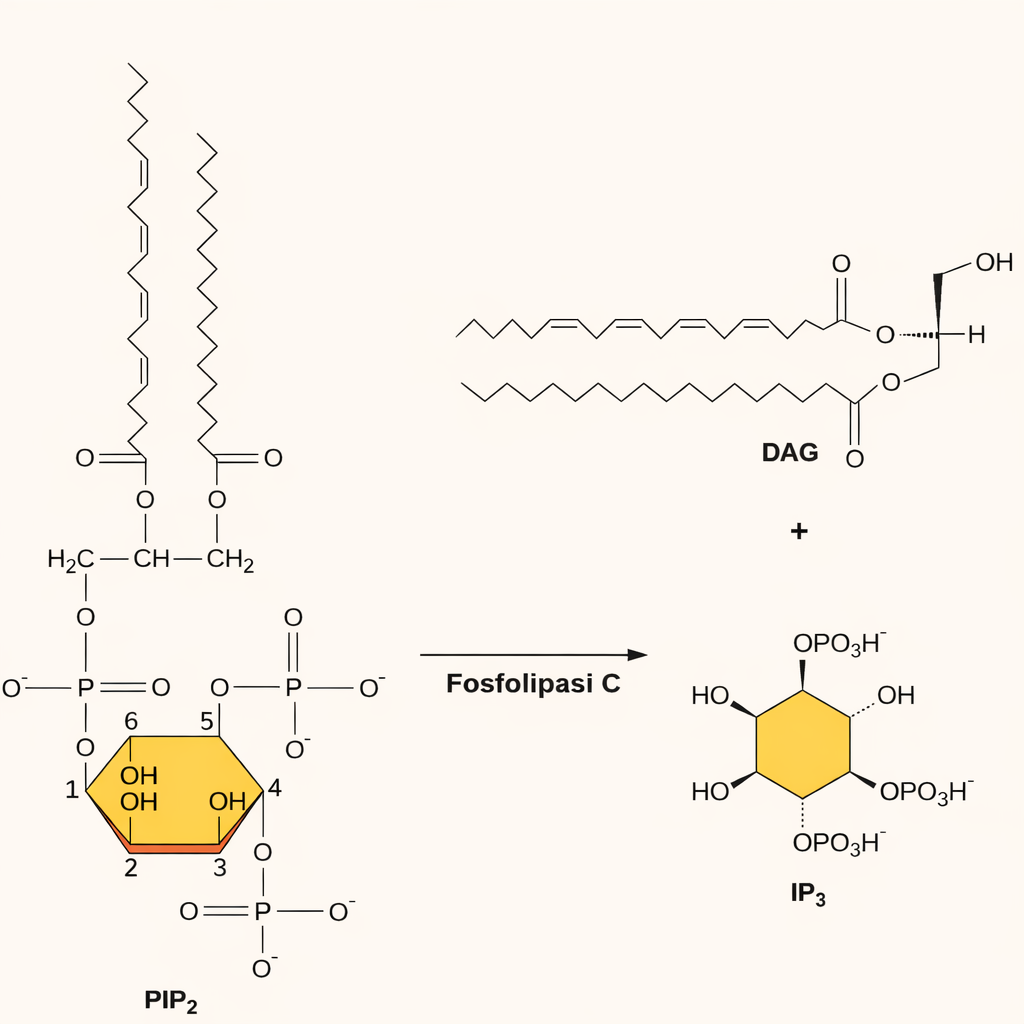
Un distinto gruppo di GPCR segnala attraverso proteine G di classe Gq, che attivano la fosfolipasi Cβ (PLCβ) di membrana invece dell’adenilato ciclasi. La (Tabella 05.24-02) elenca ligandi tipici di questa via. Una volta attivata, PLCβ idrolizza un fosfoinositide presente nel foglietto citosolico della membrana plasmatica, il fosfatidilinositolo 4,5-bisfosfato (PIP₂), producendo due secondi messaggeri: inositolo 1,4,5-trifosfato (IP₃) e diacilglicerolo (DAG), secondo \( \mathrm{PIP_2} \rightarrow \mathrm{IP_3} + \mathrm{DAG} \) (Figura 05.24-07). Questa cascata è spesso denominata “via del fosfoinositide” e opera in quasi tutte le cellule eucariote, regolando bersagli molteplici. L’IP₃ è solubile e diffonde nel citosol fino a raggiungere i recettori-canale per il Ca²⁺ (IP₃R) del reticolo endoplasmatico; il loro apertura consente il rilascio di Ca²⁺ dai depositi interni, aumentando rapidamente la concentrazione citosolica dello ione a partire da un livello basale molto basso. Il Ca²⁺ così liberato si lega a proteine sensibili allo ione, tra cui la calmodulina, che a sua volta attiva chinasi e fosfatasi Ca²⁺/calmodulina-dipendenti (ad esempio CaMKII e la fosfatasi calcineurina), modulando contrazione, secrezione ed espressione genica a seconda del contesto. Il DAG rimane inserito nella membrana e coopera con il Ca²⁺ nel reclutare e attivare la proteina chinasi C (PKC), che trasloca dal citosol alla membrana plasmatica (Figura 05.24-07). Le isoforme convenzionali di PKC richiedono sia Ca²⁺ sia DAG, quelle “novel” necessitano soltanto di DAG, mentre le “atypical” non dipendono da entrambi ma da altri fosfolipidi di segnalazione. Una volta attivata, PKC fosforila un’ampia gamma di substrati, con effetti che variano profondamente tra i diversi tipi cellulari. Il DAG, oltre ad agire su PKC, può essere metabolizzato lungo vie lipidiche che generano ulteriori mediatori:
- formazione e rimodellamento del segnale Ca²⁺: pompe SERCA ricatturano Ca²⁺ nel reticolo endoplasmatico, mentre PMCA e lo scambiatore Na⁺/Ca²⁺ lo estrudono verso l’esterno, riportando rapidamente i livelli basali;
- compartimentalizzazione: l’ingresso di Ca²⁺ nel mitocondrio tramite il uniporter mitocondriale nei microdomini ad alta concentrazione contribuisce sia al tamponamento sia alla regolazione del metabolismo ossidativo;
- rifornimento dei depositi: la deplezione del Ca²⁺ nel reticolo endoplasmatico attiva l’ingresso capacitivo (SOCE) mediato dal sensore STIM1 e dal canale Orai1, garantendo la sostenibilità del segnale e il ripristino delle riserve;
- codifica del segnale: oscillazioni in ampiezza e frequenza del Ca²⁺ citosolico trasmettono informazione ai diversi effettori, permettendo risposte specifiche e dosate allo stimolo.
Esempi fisiologicamente rilevanti includono: nelle fibrocellule muscolari lisce, agonisti α1-adrenergici attivano PLCβ, l’IP₃ libera Ca²⁺ e l’aumento dello ione attiva la chinasi della catena leggera della miosina via calmodulina, promuovendo la contrazione; negli epatociti, vasopressina e altri ormoni accoppiati a Gq favoriscono la glicogenolisi mediante attivazione Ca²⁺-dipendente della fosforilasi chinasi; nelle cellule esocrine, transitori di Ca²⁺ sincronizzati innescano l’esocitosi di granuli secretori. In tutti questi scenari, l’attivazione concomitante di PKC da parte del DAG modula in parallelo canali ionici, trasportatori e complessi enzimatici, integrando il segnale. La via del fosfoinositide, generando IP₃, DAG e Ca²⁺, costituisce quindi un sistema versatile per trasformare un singolo evento recettoriale in risposte coordinate che vanno dall’attivazione enzimatica immediata fino a modulazioni trascrizionali più lente. La sua interazione con la segnalazione a cAMP, attraverso substrati condivisi e regolazioni incrociate di chinasi e fosfatasi, consente un controllo fine del destino cellulare in funzione del tipo di cellula e del contesto fisiologico.
Risposte cellulari attivate dalla fosfolipasi C
| Molecola segnale | Tessuto bersaglio | Risposta |
|---|---|---|
| Vasopressina | Fegato | Attivazione della glicogenolisi |
| Acetilcolina | Pancreas | Secrezione di amilasi e altri enzimi digestivi |
| Acetilcolina | Muscolatura liscia | Induzione della contrazione |
| Trombina | Piastrine | Aggregazione piastrinica |
| Tabella che descrive l’azione della fosfolipasi C nella scissione dei fosfolipidi di membrana e nella produzione di messaggeri intracellulari capaci di modulare processi specifici, attraverso cui ormoni e neurotrasmettitori come vasopressina e acetilcolina inducono risposte metaboliche e contrattili, mentre proteine come la trombina regolano l’attività piastrinica durante la coagulazione. | ||
Lo ione calcio è uno dei principali mediatori intracellulari dei metazoi e degli eucarioti unicellulari, con un raggio d’azione che abbraccia processi elettrici, meccanici e biochimici. Incrementi transitori della concentrazione citosolica di Ca²⁺ libero si osservano in risposta a una varietà di stimoli, non limitati ai recettori accoppiati a proteine G (GPCR). Tra gli esempi classici rientrano: l’onda di Ca²⁺ che segue la fecondazione e avvia lo sviluppo embrionale (Figura 05.24-08); l’aumento di Ca²⁺ nelle fibrocellule muscolari scheletriche che accoppia l’impulso nervoso alla contrazione; l’esocitosi regolata in cellule endocrine, esocrine e neuronali, in cui lo ione funge da “trigger” della secrezione:
- un singolo segnale può mobilizzare Ca²⁺ da serbatoi intracellulari, soprattutto dal reticolo endoplasmatico, oppure favorirne l’ingresso dall’ambiente esterno attraverso canali di membrana voltaggio- o ligando-dipendenti;
- il Ca²⁺ modula l’attività di proteine bersaglio sensibili allo ione, innescando risposte coordinate a livello della cellula e del tessuto;
- l’elevata versatilità del segnale è conferita dalla durata, dall’ampiezza e dalla compartimentazione spaziale dei transitori di Ca²⁺.
In condizioni basali, la concentrazione di Ca²⁺ libero nel citosol è mantenuta estremamente bassa, \( [Ca^{2+}]_{citosol} \approx 10^{-7}\,\mathrm{M} \), mentre il compartimento extracellulare e il lume del reticolo endoplasmatico raggiungono valori nell’ordine di \(10^{-3}\,\mathrm{M}\). Tale differenza, di circa \(10^{4}\)–\(10^{5}\) volte, è sostenuta da pompe e scambiatori che rimuovono continuamente lo ione dal citosol: tra questi, la Ca²⁺-ATPasi del reticolo endoplasmatico (SERCA), la Ca²⁺-ATPasi della membrana plasmatica (PMCA) e lo scambiatore Na⁺/Ca²⁺ (NCX). La presenza di proteine leganti Ca²⁺ (per esempio, calreticulina e calsequestrina nei lumi intracellulari) contribuisce alla capacità di accumulo e alla pronta mobilizzazione. Quando canali per il Ca²⁺ si aprono transitoriamente, il marcato gradiente elettrochimico consente un rapido ingresso o rilascio dello ione, attivando proteine citosoliche sensibili al Ca²⁺; la successiva azione di pompe e scambiatori riconduce la concentrazione ai livelli di quiete, terminando la risposta e predisponendo la cellula a un nuovo ciclo di segnalazione. Gli effetti del Ca²⁺ sono in gran parte mediati da proteine citosoliche o membranarie che ne rilevano l’aumento. La calmodulina, ubiquitaria nelle cellule eucariotiche, rappresenta il sensore più diffuso: legando Ca²⁺ in siti EF-hand, subisce un cambiamento conformazionale che le consente di avvolgere e modulare numerose proteine bersaglio (Figura 05.24-09). Tra queste spiccano le chinasi Ca²⁺/calmodulina-dipendenti (CaM chinasi), che fosforilano substrati specifici e coordinano risposte come metabolismo, traffico vescicolare e plasticità sinaptica. Una forma sinaptica abbondante, la CaMKII, organizza complessi oligomerici ad alta efficienza catalitica e, grazie all’autofosforilazione, può mantenere uno stato di attività persistente in risposta a brevi picchi di Ca²⁺, contribuendo a fenomeni di potenziamento a lungo termine nelle reti neuronali. Modelli murini con alterazioni della CaMKII mostrano deficit selettivi in compiti di memoria spaziale, evidenziando il ruolo funzionale della via calmodulina/CaM chinasi nel sistema nervoso.
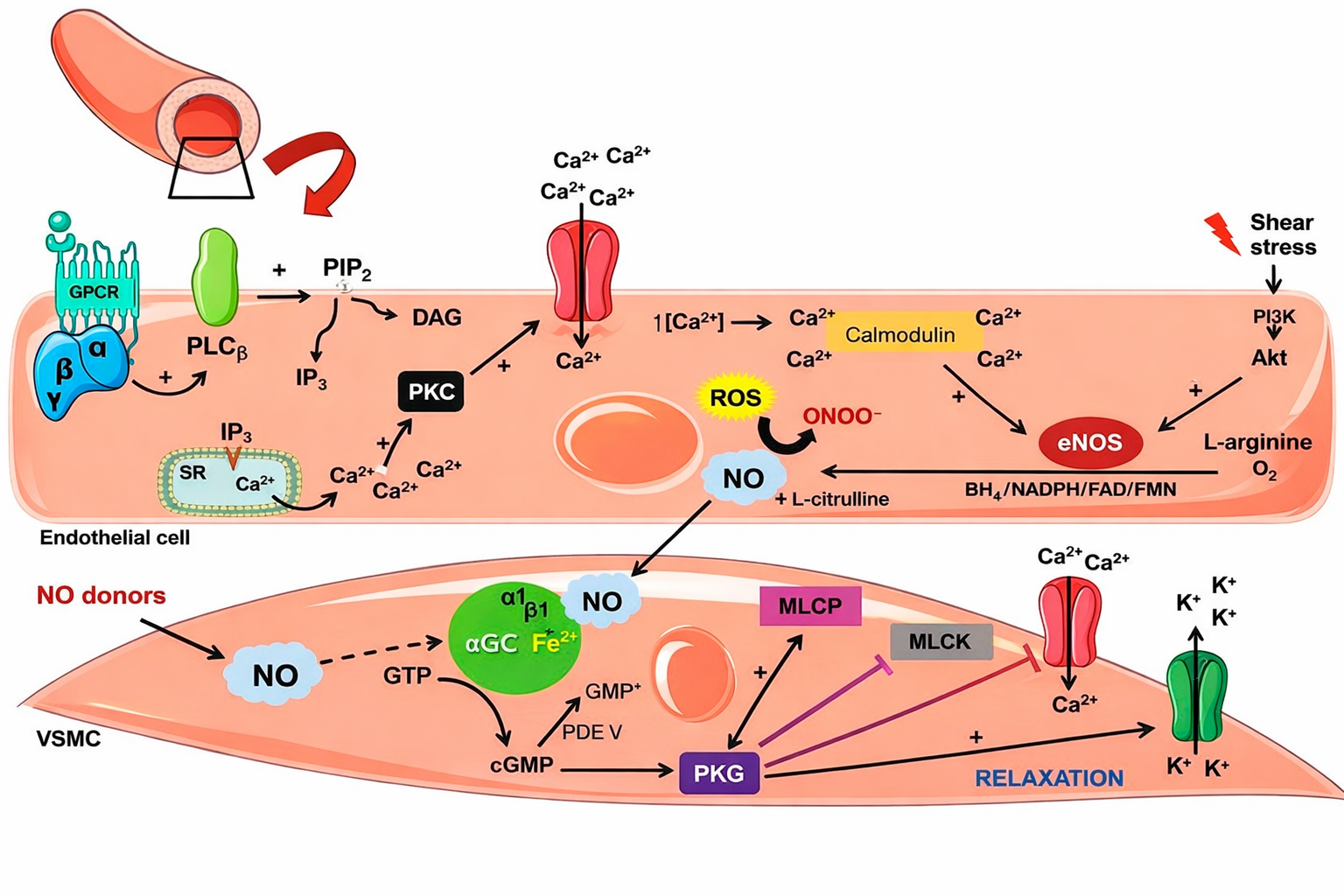
Molti secondi messaggeri idrofili, come AMP ciclico e Ca²⁺, rimangono confinati nella cellula che li produce. Esistono tuttavia segnali di piccole dimensioni o sufficientemente lipofili da attraversare le membrane e agire per diffusione su cellule contigue. Un esempio centrale è l’ossido nitrico (NO), un gas reattivo con emivita di pochi secondi che, dopo la sintesi, diffonde rapidamente dallo spazio intracellulare all’ambiente circostante, dove viene inattivato tramite reazioni con ossigeno e acqua, formando nitriti e nitrati. Nell’endotelio vascolare, l’acetilcolina rilasciata da terminazioni parasimpatiche lega GPCR di tipo muscarinico, attivando Gq e la fosfolipasi C-β, con produzione di inositolo 1,4,5-trifosfato (IP₃) e aumento del Ca²⁺ citosolico (Figura 05.24-07). Il Ca²⁺, attraverso la calmodulina, stimola la NO sintasi endoteliale (eNOS), che converte l’arginina in citrullina e NO. Il gas così generato permea le cellule muscolari lisce adiacenti, dove si lega alla guanilato ciclasi solubile (sGC) e ne attiva il gruppo eme, incrementando la formazione di GMP ciclico (Figura 05.24-10). Il cGMP attiva la proteina chinasi G (PKG), che riduce il tono contrattile attraverso più bersagli, inclusa la modulazione della sensibilità dei filamenti di miosina al Ca²⁺ e l’attivazione della fosfatasi della catena leggera della miosina; il risultato è il rilasciamento della muscolatura liscia e la vasodilatazione (Figura 05.24-10). Questo circuito chiarisce l’efficacia clinica dei donatori di NO, come la nitroglicerina, nella riduzione del carico emodinamico del cuore in pazienti con angina: il rilascio controllato di NO dilata i vasi e facilita il flusso ematico. Analogamente, in ambito neurovascolare periferico, neuroni nitrergici rilasciano NO nel tessuto erettile, determinando vasodilatazione locale. La durata del segnale è regolata da fosfodiesterasi specifiche per il cGMP; il sildenafil inibisce la fosfodiesterasi di tipo 5 (PDE5), prolungando la disponibilità di cGMP e l’effetto vasodilatatore. L’interferenza farmacologica con più componenti della via (per esempio, PDE5-inibitori e nitrati) può causare ipotensione marcata, a sottolineare la potenza dell’asse NO–cGMP.
Le vie a cascata innescate da GPCR possono essere estremamente veloci, pur coinvolgendo numerosi passaggi biochimici. La tachicardia evocata da adrenalina, la salivazione indotta da acetilcolina e la trasduzione olfattiva mediata da recettori GPCR nella mucosa nasale sono esempi di risposte che insorgono in tempi di secondi o meno. Tra le più rapide in assoluto vi è la fototrasduzione nei coni retinici, la cui risposta elettrica a un lampo luminoso può emergere in circa 20 millisecondi, a testimonianza dell’elevata efficienza con cui le cellule trasformano un segnale esterno in variazioni di potenziale di membrana. Le cellule fotorecettrici retiniche mostrano in modo paradigmatico sia l’amplificazione del segnale sia l’adattamento su un ampio intervallo dinamico (Figura 05.24-11). Nei bastoncelli, la rodopsina (un GPCR sensibile alla luce) assorbe fotoni e attiva la proteina G trasducina; la subunità α-GTP attiva quindi una fosfodiesterasi (PDE6) che abbassa il livello di cGMP. La diminuzione di cGMP provoca la chiusura dei canali cationici CNG permeabili a Na⁺ e Ca²⁺, riducendo la corrente al buio e iperpolarizzando la cellula. Il cambiamento del potenziale di membrana modula il rilascio del neurotrasmettitore verso i neuroni bipolari, generando l’informazione visiva diretta all’encefalo. L’amplificazione è notevole: una singola rodopsina attivata può stimolare molte molecole di trasducina, ciascuna delle quali può attivare PDE6 a idrolizzare numerosissime molecole di cGMP. In condizioni di scarsa luminosità, pochi fotoni (anche meno di una ventina, distribuiti su diverse cellule) possono generare un segnale rilevabile; alla luce intensa, l’intera cascata riduce l’amplificazione di oltre 10 000 volte, prevenendo la saturazione e preservando la capacità di discriminare ulteriori variazioni di intensità. Questo adattamento dipende da feedback negativi innescati dal Ca²⁺: la diminuzione del Ca²⁺ intracellulare durante la chiusura dei canali CNG modula proteine regolatrici come le GCAPs, aumentando l’attività della guanilato ciclasi e ripristinando il cGMP; parallelamente, sistemi come la chinasi della rodopsina e l’arrestina limitano la durata dello stato attivo del fotorecettore. Anche proteine come recoverina e calmodulina partecipano a questi anelli di retroazione Ca²⁺-dipendenti. La capacità di adattarsi non è esclusiva della fototrasduzione: molte vie di segnalazione attivate da molecole extracellulari integrano circuiti di feedback positivi e negativi, consentendo risposte proporzionate alle variazioni relative del segnale più che al suo valore assoluto. Tale architettura di controllo rende possibile la rilevazione affidabile di stimoli molto deboli come di segnali intensi, senza compromettere l’omeostasi cellulare. Anche gusto e olfatto utilizzano ampi repertori di GPCR, un retaggio evolutivo che sottolinea l’importanza di recettori capaci di decodificare rapidamente segnali ambientali complessi. I GPCR non esauriscono, tuttavia, le strategie di trasduzione: altre classi recettoriali accoppiate a enzimi coordinano crescita, differenziamento e motilità cellulare negli organismi pluricellulari.