La tecnologia del DNA consente lo studio dell’espressione e della funzione di un gene
Definizione
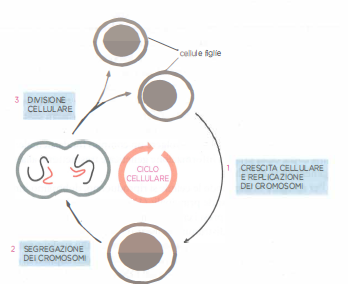
Il ciclo cellulare assicura due compiti essenziali: la duplicazione accurata dell’intero patrimonio genetico contenuto nei cromosomi e la ripartizione equa delle copie in due cellule figlie, in modo che ciascuna erediti un genoma completo e integro (Figura 07.02-01). In parallelo, la maggior parte delle cellule raddoppia la propria massa, le scorte di macromolecole e gli organuli, così da mantenere dimensioni stabili dopo la divisione. Senza una crescita coordinata, cicli successivi produrrebbero cellule progressivamente più piccole. Pertanto, l’aumento di massa e la divisione devono essere strettamente sincronizzati.
La durata del ciclo varia marcatamente in base al tipo cellulare e allo stato fisiologico (Tabella 07.02-01). In organismi pluricellulari, ad esempio, i fibroblasti in coltura possono completare un ciclo in 20–30 ore, mentre i cardiomiociti adulti raramente si dividono. In tessuti ad alto turnover, come l’epitelio intestinale, cellule staminali e progenitori possono rinnovarsi nell’arco di 1–2 giorni. Tale variabilità riflette un controllo fine che integra fattori intrinseci ed estrinseci.
Una rappresentazione quantitativa utile è il tempo di raddoppio, legato al tasso di crescita specifico \(\mu\):
\[ T_d = \frac{\ln 2}{\mu}. \]
In termini volumetrici, se la divisione avvenisse senza crescita, il volume medio dopo \(n\) divisioni seguirebbe \(V_n = V_0 / 2^n\), evidenziando la necessità biologica del coordinamento tra biosintesi e mitosi.
| Tipo di cellula | Durata del ciclo cellulare |
|---|---|
| Cellule embrionali precoci di rana | ~30 minuti |
| Cellule di lievito | ~1,5 ore |
| Cellule epiteliali intestinali di mammifero | ~12 ore |
| Fibroblasti di mammifero in coltura | ~20 ore |
Durata del ciclo cellulare in diversi tipi cellulari
Il tempo necessario a completare un ciclo cellulare varia notevolmente tra organismi e tessuti. Le cellule embrionali mostrano divisioni estremamente rapide per sostenere lo sviluppo iniziale, mentre cellule differenziate, come i fibroblasti, possiedono cicli più lunghi, riflettendo esigenze funzionali e regolative differenti.
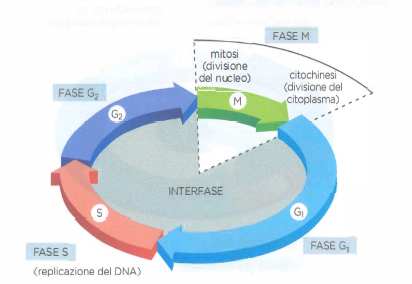
Gli eventi morfologicamente più appariscenti sono la divisione del nucleo (mitosi) e la separazione della cellula madre in due cellule figlie (citochinesi). Insieme costituiscono la fase M, che in molte cellule di mammifero occupa circa 1 ora, una piccola frazione dell’intero ciclo (Tabella 07.02-01). L’intervallo tra due fasi M consecutive è definito interfase e, contrariamente a quanto suggerisca l’osservazione al microscopio, è un periodo di intensa attività biosintetica e di controllo.
L’interfase comprende tre fasi funzionali: G1, S e G2. Nella fase S (“sintesi”) avviene la replicazione del DNA nucleare, prerequisito per una segregazione fedele dei cromosomi. Le fasi G1 e G2 (dall’inglese gap) sono periodi in cui la cellula cresce, sintetizza proteine, duplica la maggior parte degli organuli e verifica lo stato interno ed esterno prima di impegnarsi in eventi irreversibili come la replicazione del genoma o l’ingresso in mitosi (Figura 07.02-02). In momenti chiave di G1 e G2, la cellula valuta se procedere o attendere, assicurandosi che i preparativi siano completi.
Le fasi G, nel complesso, forniscono il tempo necessario a raddoppiare la massa citoplasmatica prima della divisione. Quando i cicli sono estremamente rapidi, le fasi G possono essere ridotte o assenti; nelle prime divisioni dell’embrione di Drosophila, ad esempio, nuclei multipli si replicano e si separano in rapida successione senza accrescimento citoplasmatico, con cicli sincronizzati e compatti (Tabella 07.02-01). In tali condizioni la crescita è disaccoppiata dalla divisione, con impatto sulle dimensioni cellulari e sulla dinamica tissutale.
| Tipo di cellula | Durata del ciclo cellulare |
|---|---|
| Cellule embrionali precoci di rana | ~30 minuti |
| Cellule di lievito | ~1,5 ore |
| Cellule epiteliali intestinali di mammifero | ~12 ore |
| Fibroblasti di mammifero in coltura | ~20 ore |
Durata del ciclo cellulare in diversi tipi cellulari
Il tempo necessario a completare un ciclo cellulare varia notevolmente tra organismi e tessuti. Le cellule embrionali mostrano divisioni estremamente rapide per sostenere lo sviluppo iniziale, mentre cellule differenziate, come i fibroblasti, possiedono cicli più lunghi, riflettendo esigenze funzionali e regolative differenti.
| Tipo di cellula | Durata del ciclo cellulare |
|---|---|
| Cellule embrionali precoci di rana | ~30 minuti |
| Cellule di lievito | ~1,5 ore |
| Cellule epiteliali intestinali di mammifero | ~12 ore |
| Fibroblasti di mammifero in coltura | ~20 ore |
Durata del ciclo cellulare in diversi tipi cellulari
Il tempo necessario a completare un ciclo cellulare varia notevolmente tra organismi e tessuti. Le cellule embrionali mostrano divisioni estremamente rapide per sostenere lo sviluppo iniziale, mentre cellule differenziate, come i fibroblasti, possiedono cicli più lunghi, riflettendo esigenze funzionali e regolative differenti.
Nelle cellule eucariotiche un sofisticato sistema di controllo, costituito da reti di chinasi ciclina-dipendenti (CDK), cicline, inibitori, e complessi ubiquitina–ligasi, orchestra l’ordine e la tempistica degli eventi del ciclo. Questo apparato garantisce che ogni processo (licensing e replicazione del DNA, condensazione cromosomica, assemblaggio del fuso, segregazione dei cromatidi, citochinesi) si attivi soltanto quando il precedente è completato, integrando segnali di feedback e meccanismi di arresto temporaneo.
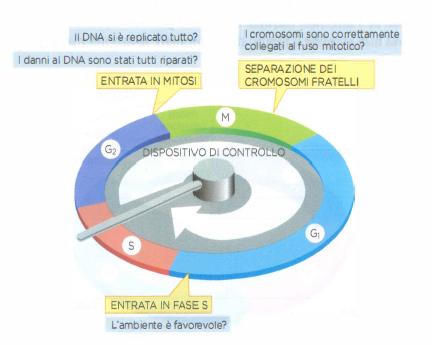
Se la replicazione del DNA procede lentamente o si arresta, l’ingresso in mitosi viene rimandato; se il DNA risulta danneggiato, il ciclo viene bloccato in G1, S o G2 per consentire le riparazioni. Questi arresti avvengono in corrispondenza di punti di controllo (checkpoints), attivati da sensori molecolari che convergono su effettori del ciclo. La (Figura 07.02-03) riassume tre nodi regolatori principali:
- Transizione G1–S (punto di restrizione/Start): verifica che l’ambiente extracellulare sia favorevole, con nutrienti e fattori di crescita adeguati, e che non vi siano danni al DNA prima dell’impegno irreversibile nella replicazione; negli animali, segnali paracrini e ormonali modulano fortemente questa decisione e, in condizioni sfavorevoli, le cellule possono rallentare in G1 o entrare in quiescenza reversibile (G0);
- Transizione G2–M: impedisce l’ingresso in mitosi finché la replicazione non è completa e le lesioni del DNA non siano state riparate, coordinando l’attivazione delle CDK mitotiche con i circuiti di risposta al danno;
- Punto di controllo del fuso (SAC): durante la mitosi assicura che tutti i cromosomi siano correttamente attaccati ai microtubuli del fuso mitotico attraverso i cinetocori prima dell’anafase, bloccando la separazione dei cromatidi in caso di attacchi errati.
Dal punto di vista molecolare, l’uscita dal SAC e l’avvio dell’anafase richiedono l’attivazione dell’APC/C (Anaphase-Promoting Complex/Cyclosome), che promuove la degradazione delle cicline mitotiche e di securina, liberando separasi per scindere la coesina. Nella fase S, la “licenza” alla replicazione è controllata dal caricamento dei complessi MCM agli ori, regolato da fattori come Cdc6 e Cdt1; la riaccensione indesiderata degli ori nella stessa fase è impedita da meccanismi che dipendono dall’attività CDK e da inibitori specifici.
Nei vertebrati, il punto di controllo G1–S è particolarmente sensibile a segnali extracellulari: fattori di crescita, citochine e contatti cellula–cellula modulano l’espressione di cicline, CDK e inibitori (ad esempio, p21, p27), contribuendo a stabilire l’equilibrio tra proliferazione, quiescenza e differenziamento. Deregolazioni persistenti di questi circuiti possono favorire iperproliferazione e tumorigenesi.
Sebbene la durata delle singole fasi e la sensibilità ai segnali variino tra tipi cellulari e organismi, l’architettura del sistema di controllo è ampiamente conservata in tutti gli eucarioti. Le proteine regolatrici del ciclo cellulare sono emerse più di un miliardo di anni fa e hanno mantenuto funzioni intercambiabili: componenti umani possono sostituire l’omologo in lieviti, evidenziando una profonda omologia funzionale. Questa conservazione ha permesso approcci complementari in più modelli sperimentali.
Nei lieviti, screening genetici per mutanti condizionali (mutanti cdc) hanno identificato nodi critici del controllo del ciclo; in estratti ovocitari di anfibi si sono ricostruiti in vitro eventi mitotici e meiotici ad alta risoluzione temporale; in embrioni di Drosophila si è studiata la regolazione di cicli rapidi e sincronizzati; in colture di cellule di mammifero si sono chiarite interazioni tra segnali extracellulari e punti di controllo. L’integrazione di questi sistemi ha delineato un quadro unitario nel quale cicline, CDK, complessi SCF e APC/C, coesina, condensina e checkpoint del danno al DNA collaborano per garantire ordine, fedeltà e adattabilità del ciclo cellulare.
Complessivamente, la somiglianza dei meccanismi e la loro modulazione da parte dell’ambiente spiegano perché i principi esposti siano applicabili, con adattamenti quantitativi, a cellule e tessuti molto diversi, dai microrganismi eucariotici alle cellule somatiche umane.