Il cambiamento di energia libera di una reazione indica se la reazione avviene spontaneamente o meno
Definizione
Solo nella seconda metà del Novecento si è affermata l’idea, oggi centrale in biologia molecolare, che i geni possano essere regolati in modo dinamico, venendo attivati o silenziati in risposta a segnali interni ed esterni. Una conferma decisiva è emersa dagli studi su Escherichia coli, nei quali si è osservata la capacità del batterio di modulare l’espressione genica in funzione della composizione del terreno di coltura. Molti principi scoperti nei procarioti sono validi anche per le cellule eucariotiche; tuttavia, la presenza del nucleo, l’organizzazione del DNA in cromatina e l’azione di più livelli di controllo rendono la regolazione genica negli eucarioti particolarmente articolata e ricca di possibilità di integrazione dei segnali. In questa sede si considerano innanzitutto i regolatori della trascrizione (fattori trascrizionali), proteine in grado di riconoscere specifiche sequenze di DNA e modulare il flusso informativo a livello trascrizionale.
La maggior parte dei geni, tanto nei procarioti quanto negli eucarioti, è affiancata da regioni di DNA che ne guidano la trascrizione. Il promotore è la sede di assemblaggio dell’RNA polimerasi e dei cofattori necessari a posizionare l’enzima sul sito di inizio della trascrizione. Nei batteri, tale posizionamento è mediato dal fattore sigma, mentre negli eucarioti avviene tramite fattori generali della trascrizione che formano il complesso di pre-inizio; in quest’ultimo caso, proteine come TFIID, TFIIB, TFIIE, TFIIF e TFIIH cooperano per fondere localmente il DNA e avviare la sintesi dell’RNA. Oltre al promotore, i geni ospitano elementi regolativi di natura e posizione variabili. Questi moduli fungono da piattaforme di lettura dei segnali e trasformano input molecolari in frequenze di inizio trascrizionale. In batteri e archei, brevi sequenze di poche decine di nucleotidi possono comportarsi da interruttori semplici in grado di rispondere a un unico segnale. Negli eucarioti, elementi distali come intensificatori (enhancer) e silenziatori possono estendersi per oltre 10 000 coppie di basi e agire a distanza attraverso il ripiegamento tridimensionale della cromatina, coordinando più segnali e integrandoli in un’unica istruzione di output. Per chiarezza, alcuni elementi ricorrenti possono essere ricondotti alle categorie seguenti:
- promotori, sequenze prossimali che ospitano il sito di inizio e i determinanti per il reclutamento dell’RNA polimerasi;
- operatori o siti di legame per regolatori, tipici dei procarioti, che modulano l’accesso dell’RNA polimerasi;
- enhancer e silencer, elementi eucariotici spesso distali che aumentano o riducono la probabilità di inizio trascrizionale;
- isolatori e boundary elements, sequenze che delimitano i domini regolativi impedendo interferenze tra unità adiacenti.
Gli elementi regolativi funzionano solo se riconosciuti da proteine specifiche, i regolatori della trascrizione. È l’accoppiata sequenza-proteina a costituire l’unità funzionale dell’interruttore trascrizionale. Anche il più semplice batterio codifica centinaia di tali regolatori, ciascuno dei quali riconosce motivi nucleotidici distinti e governa insiemi dedicati di geni. Negli esseri umani si contano almeno 2 000 fattori trascrizionali, in linea con l’elevato fabbisogno di controllo di un organismo complesso. Il riconoscimento del DNA avviene sfruttando la complementarità di forma e chimica tra la superficie della proteina e il profilo del solco maggiore della doppia elica. La disposizione di donatori e accettori di legami idrogeno, cariche e gruppi metilici, che costituisce la “firma” chimica di ciascuna coppia di basi, varia con la sequenza; in tal modo, domini proteici distinti (per esempio elica-giro-elica, dita di zinco, leucine zipper, homeodomini) discriminano motivi nucleotidici differenti (Figura 03.10-01). I contatti individuali tra residui amminoacidici e basi, se presi singolarmente, sono deboli; tuttavia, 10–20 interazioni coordinate generano una specificità elevata e un’affinità complessiva notevole. Molti regolatori si associano al DNA come dimeri, spesso riconoscendo sequenze palindrome o ripetute: la dimerizzazione raddoppia la superficie di contatto, aumenta l’affinità e consente cooperatività allosterica tra i monomeri (Figura 03.10-02). La probabilità che un sito sia occupato da un regolatore a concentrazione libera [TF] può essere approssimata, in condizioni semplici, da \( P_{\mathrm{bound}} \approx \frac{[\mathrm{TF}]}{[\mathrm{TF}] + K_d} \), dove \( K_d \) è la costante di dissociazione. In presenza di cooperatività tra più subunità o siti adiacenti, il comportamento segue frequentemente una dipendenza di tipo hilliano con esponente \( n \gt 1 \), che acuisce la transizione tra stati “spento” e “acceso”. Negli eucarioti, oltre al riconoscimento di sequenza, intervengono vincoli fisici imposti dai nucleosomi e dallo stato della cromatina. Rimodellatori ATP-dipendenti e modificazioni istoniche (per esempio acetilazioni e metilazioni) modulano l’accessibilità dei siti, mentre complessi di coattivazione e il Mediator connettono gli enhancer ai promotori operando a lungo raggio. Questi livelli aggiuntivi non sostituiscono, ma amplificano, la logica di base fondata dall’interazione fattore–DNA.
La regolazione nei batteri rappresenta un modello particolarmente nitido. Il genoma di E. coli è costituito da una singola molecola circolare di circa 4,6 × 10⁶ paia di basi e codifica all’incirca 4 300 proteine. Non tutte vengono prodotte simultaneamente: la cellula modula l’espressione in relazione alle risorse disponibili e alle necessità metaboliche. Un caratteristico schema procariotico è l’operone, ovvero un cluster di geni contigui trascritti come unico mRNA policistronico a partire da un singolo promotore (Figura 03.10-03). Negli eucarioti, tale architettura è rara e l’unità di regolazione è in genere il singolo gene. L’operone del triptofano (trp) in E. coli fornisce un esempio classico di controllo a feedback negativo. Quando la disponibilità cellulare di triptofano è bassa, l’operone è trascritto e tradotto, producendo gli enzimi necessari alla biosintesi dell’amminoacido. Se, al contrario, il triptofano è abbondante, per esempio nell’intestino tenue umano dopo l’assorbimento di prodotti proteici, la cellula importa l’amminoacido dall’esterno e la sintesi endogena non è più richiesta.
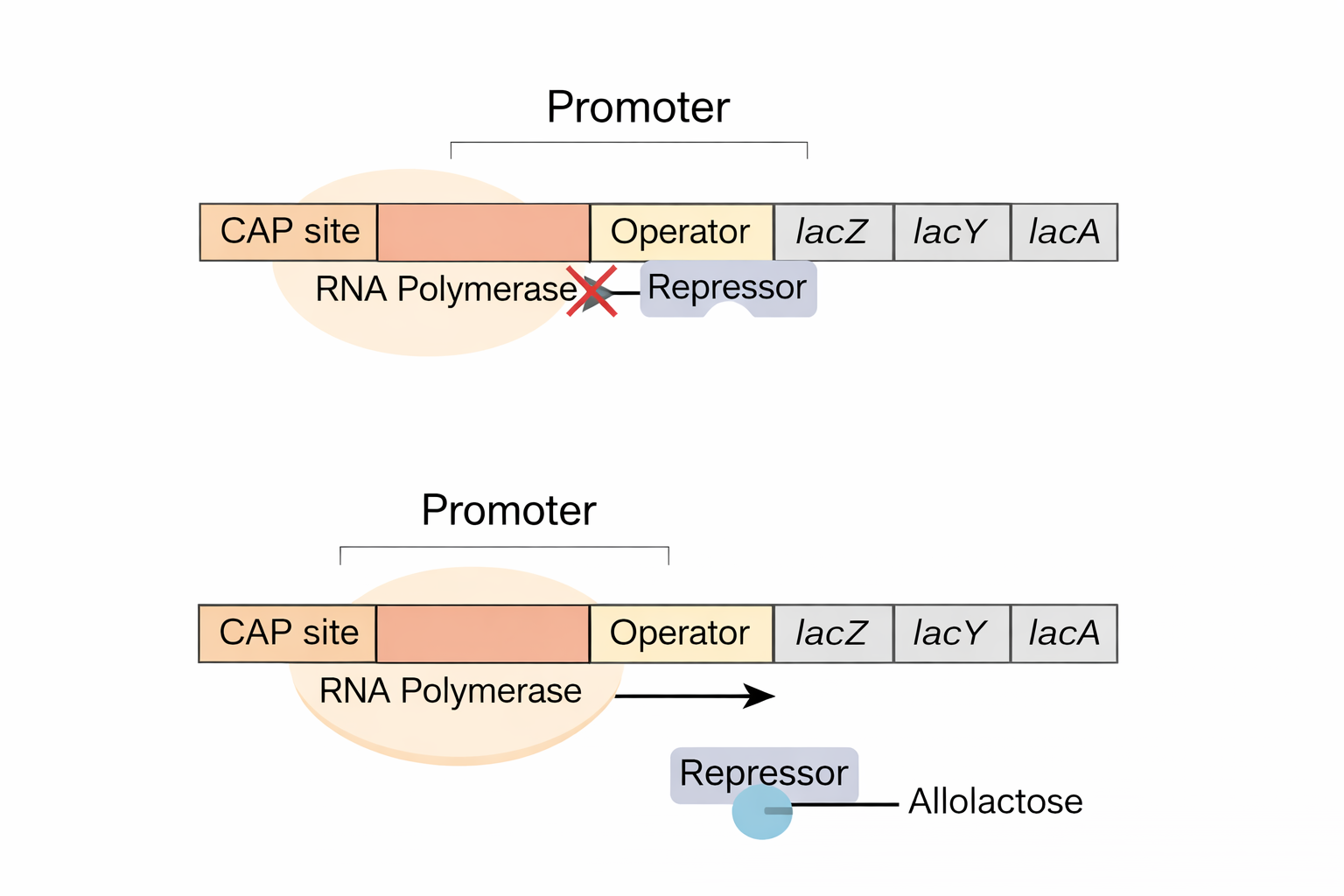
Il meccanismo molecolare di repressione del trp è ben definito. All’interno del promotore è presente una breve sequenza chiamata operatore, riconosciuta da un regolatore specifico. Quando tale proteina è legata all’operatore, l’RNA polimerasi non può impegnare correttamente il promotore e l’inizio trascrizionale è inibito (Figura 03.10-03). Il regolatore, noto come repressore del triptofano, è una proteina allosterica: può legare il DNA solo quando è associata a molecole di L-triptofano che ne stabilizzano la conformazione ad alta affinità per l’operatore (Figura 03.10-04). Il processo può essere schematizzato come \[ \mathrm{R} + n\,\mathrm{Trp} \;\rightleftharpoons\; \mathrm{R}\!\cdot\!(\mathrm{Trp})_n \;\xrightleftharpoons[\;]{\text{DNA}}\; \mathrm{R}\!\cdot\!(\mathrm{Trp})_n\!:\!\mathrm{Operatore}, \] con \( n \) che riflette il numero di siti di legame per il ligando nel dimero attivo. All’aumentare di [Trp], l’equilibrio si sposta verso la forma attiva legante il DNA, determinando la repressione; quando [Trp] diminuisce, il repressore perde il ligando, cambia conformazione e si dissocia dall’operatore, consentendo la trascrizione. Il circuito realizza una logica “soglia” efficiente:
- a triptofano basso, l’operatore è libero, l’RNA polimerasi inizia la trascrizione e gli enzimi biosintetici sono prodotti;
- a triptofano alto, il complesso repressore–ligando occupa l’operatore e blocca l’inizio, evitando sprechi energetici;
- il gene del repressore è espresso costitutivamente a basso livello, garantendo una prontezza di risposta a rapide variazioni di [Trp].
Questo schema di controllo negativo convive, in molti sistemi batterici, con meccanismi di attivazione positiva, in cui un attivatore favorisce il reclutamento dell’RNA polimerasi; l’integrazione di segnali multipli su promotori e operatori distinti consente di implementare comportamenti logici complessi. Sebbene gli eucarioti difficilmente raggruppino geni in operoni, utilizzano un principio analogo di combinatorialità: più fattori trascrizionali, coattivatori o corepressori e lo stato della cromatina convergono su promotori e enhancer per determinare, con elevata specificità spazio-temporale, la probabilità di avvio della trascrizione. Nel complesso, gli interruttori trascrizionali costituiscono l’interfaccia tra segnale e genoma: traducendo la concentrazione di metaboliti, ormoni o fattori di crescita in stati di occupazione dei siti regolativi, orchestrano l’adattamento cellulare e mantengono l’omeostasi in ambienti dinamici.
Il repressore del triptofano è un classico esempio di regolatore negativo della trascrizione: in presenza del suo corepressore, il triptofano, assume la conformazione capace di legare l’operatore e inibire l’avvio trascrizionale. In contrasto, numerosi fattori batterici agiscono come attivatori, cioè incrementano l’espressione genica. Questi ultimi operano tipicamente su promotori intrinsecamente deboli, incapaci da soli di reclutare in modo efficiente l’RNA polimerasi; l’attivatore, legandosi a una sequenza adiacente, stabilisce contatti cooperativi con la polimerasi e ne facilita il posizionamento corretto sul sito d’inizio (Figura 03.10-05). In molti batteri, l’interazione diretta avviene con i domini C-terminali della subunità α dell’RNA polimerasi o con fattori sigma, stabilizzando il complesso di pre-inizio. Come il repressore del triptofano richiede il metabolita cognato per attivarsi, anche diversi attivatori necessitano di un piccolo ligando. Un caso paradigmatico è la CAP (Catabolite Activator Protein), detta anche CRP, che lega il DNA solo in complesso con l’AMP ciclico (cAMP). L’aumento del cAMP segnala scarsità di glucosio e orienta il metabolismo verso fonti alternative: CAP–cAMP attiva così gruppi di geni coinvolti nell’assorbimento e nella degradazione di zuccheri diversi dal glucosio, amplificando la risposta globale al catabolismo preferenziale.
Il promotore dell’operone lac in Escherichia coli è un punto di integrazione tra segnali metabolici distinti: l’attivatore CAP e il repressore LacI vi esercitano un controllo combinatorio. L’operone codifica proteine deputate all’importazione e all’utilizzo del lattosio. Quando il glucosio è scarso, l’aumento di cAMP consente a CAP di attivare la trascrizione dei geni per l’uso di fonti carboniose alternative, tra cui il lattosio. Tuttavia, in assenza di lattosio sarebbe inutile sintetizzare tali enzimi: per questo LacI si lega all’operatore e sopprime l’operone fino a quando un induttore (allolattosio o analoghi) non ne riduce l’affinità per il DNA. La regione regolativa dell’operone lac implementa quindi una logica booleana, in cui l’espressione massimale si verifica solo quando coesistono due condizioni: lattosio presente e glucosio assente. In forma schematica: \( \text{lac ON} = \text{Lattosio} \land \neg \text{Glucosio} \) (Figura 03.10-06):
- glucosio assente, lattosio presente: CAP–cAMP occupa il suo sito, LacI è inattivato dall’induttore, la trascrizione è elevata;
- glucosio assente, lattosio assente: CAP–cAMP è attivo ma LacI resta legato all’operatore, la trascrizione è repressa;
- glucosio presente, lattosio presente: LacI è inattivato, ma CAP non è attivo per bassi livelli di cAMP, si osserva espressione basale;
- glucosio presente, lattosio assente: repressione forte per effetto combinato di LacI e assenza di attivazione.
Questa architettura regolativa, chiarita da studi classici di genetica e biochimica, ha costituito un modello per comprendere come reti di regolatori traducano stati metabolici in programmi di espressione genica coordinati. Nei sistemi eucariotici, principi analoghi sono implementati su scala più ampia e con maggiore complessità, fino a sostenere programmi di differenziamento e sviluppo.
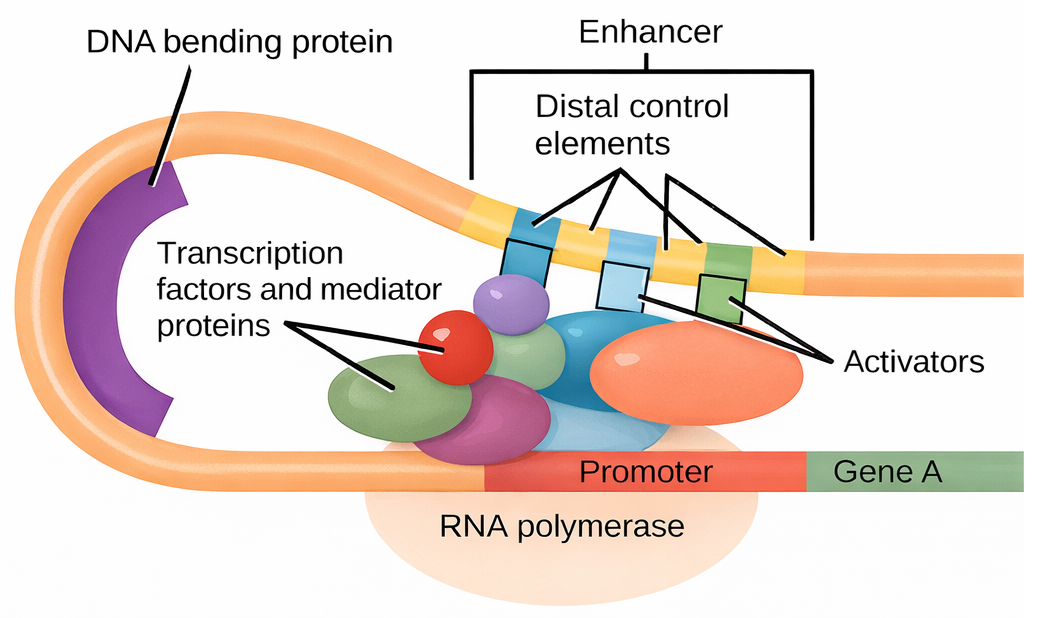
Nelle cellule eucariote, attivatori e repressori controllano la trascrizione con modalità spazialmente flessibili. I siti di legame degli attivatori sono detti intensificatori (enhancer) perché aumentano drasticamente la frequenza d’inizio trascrizionale. Sorprendentemente, un enhancer può agire quando si trova centinaia o migliaia di coppie di basi a monte o a valle del promotore, talvolta all’interno di introni o oltre il gene bersaglio. Ciò solleva il problema del “contatto a distanza” tra elementi regolatori e macchinario trascrizionale. Il modello oggi più generale invoca il ripiegamento del DNA in anse che avvicinano fisicamente l’enhancer al promotore (Figura 03.10-07). In questo contesto, coattivatori multiproteici, in primis il complesso Mediatore, fungono da ponte tra attivatori legati agli enhancer e i fattori generali di trascrizione (TFIID, TFIIA, TFIIB, ecc.) e l’RNA polimerasi II, promuovendo la formazione del complesso di inizio. I repressori eucariotici, al contrario, possono impedire questi contatti, competere per i siti di legame o reclutare corepressori che ostacolano l’assemblaggio del complesso pre-inizio, con conseguente riduzione della trascrizione.
La cromatina rappresenta un livello ulteriore di controllo: il DNA avvolto in nucleosomi e organizzato in strutture di ordine superiore può ostacolare l’accesso del macchinario trascrizionale. Nucleosomi posizionati su promotori o su regioni regolatrici possono sopprimere l’inizio trascrizionale, limitando il legame di TFIID e della polimerasi II. Non a caso, la regolazione eucariotica sfrutta meccanismi che rimodellano o modificano la cromatina per rendere accessibili, o al contrario schermare, sequenze specifiche. Gli attivatori reclutano spesso:
- complessi di rimodellamento della cromatina ATP-dipendenti (ad esempio famiglie SWI/SNF, ISWI), che traslocano o espellono nucleosomi per “scoprire” il DNA;
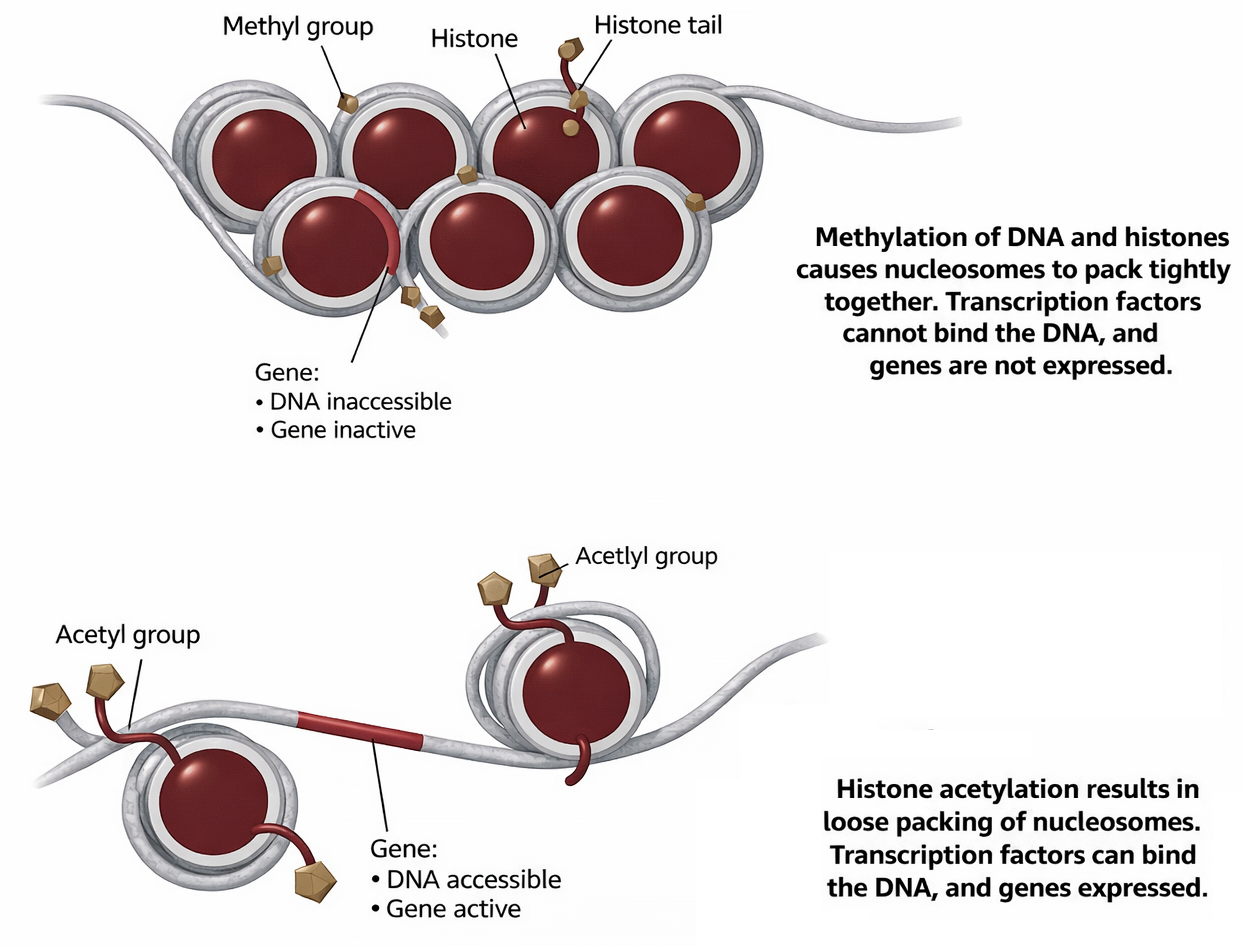
- enzimi che apportano modifiche covalenti alle code istoniche, quali le acetiltransferasi (HAT) che acetilano lisine su istoni H3/H4, creando siti per proteine con bromodomini e favorendo il legame dei fattori generali di trascrizione (Figura 03.10-08).
Questi interventi cooperano per aumentare la probabilità di avvio trascrizionale. Altre modifiche, come la trimetilazione di H3K4 ai promotori attivi, contribuiscono a stabilire stati permissivi. I repressori, per contro, possono:
- reclutare deacetilasi istoniche (HDAC) che rimuovono i gruppi acetilici, riducendo l’accessibilità del DNA;
- favorire marchi repressive quali H3K27me3 (complessi Polycomb) o H3K9me3, associate a compattazione ed eterocromatina;
- stabilizzare il posizionamento dei nucleosomi sui promotori, scoraggiando l’assemblaggio del complesso di inizio.
A scala più ampia, interi domini cromatinici possono essere resi inattivi, come nell’eterocromatina interfasica o nell’inattivazione del cromosoma X mediata da RNA non codificanti e complessi rimodellatori.
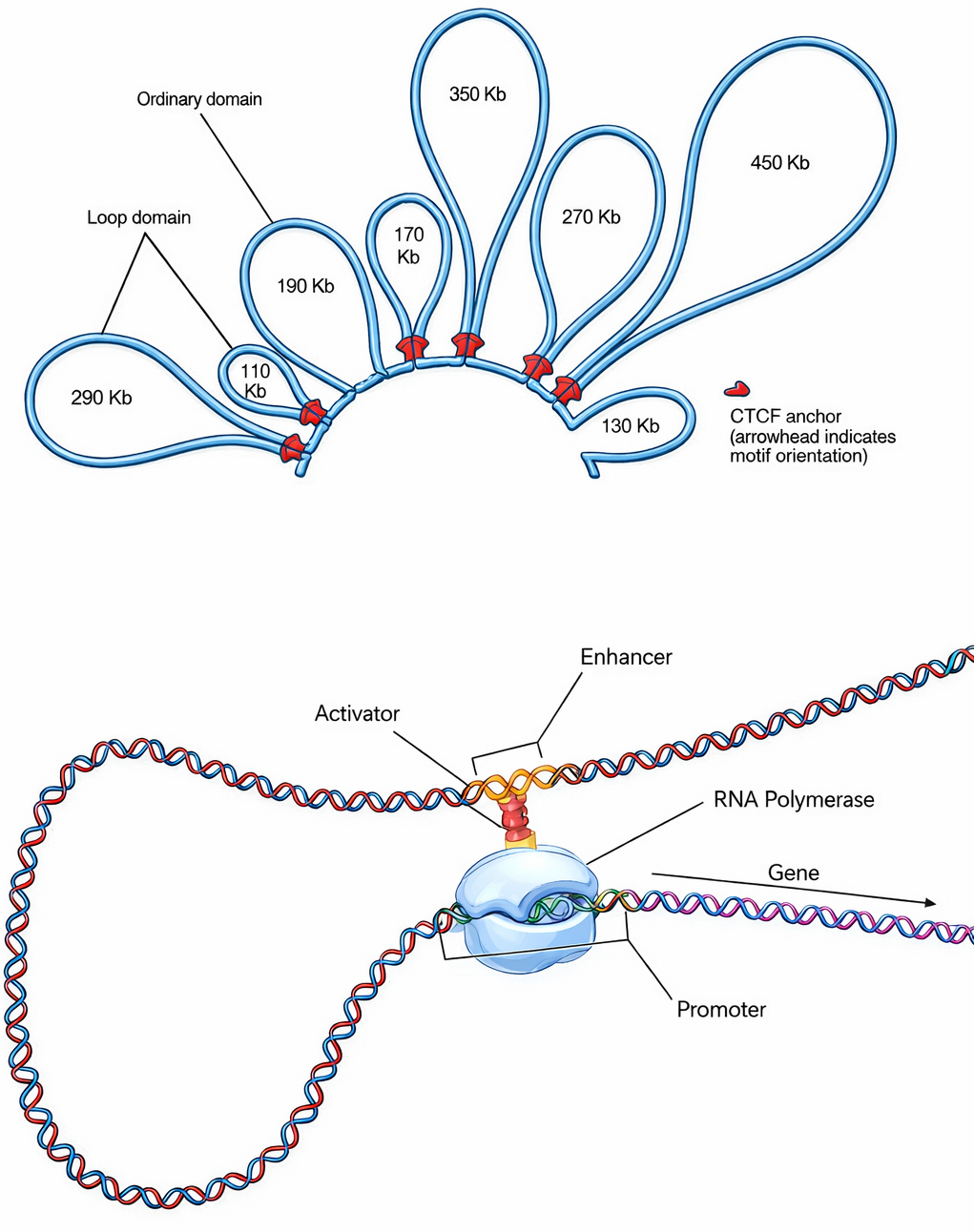
Poiché gli enhancer possono influenzare promotori lontani, sorge la necessità di confinare la loro azione ai geni appropriati. Nelle cellule animali e vegetali, il genoma è organizzato in domini tridimensionali ad ansa che mantengono in prossimità fisica ciascun gene e le sue regioni di controllo, riducendo il rischio che un enhancer “sbagli bersaglio”. Proteine architetturali si legano a coppie di sequenze specifiche e, tramite complessi di coesione e fattori barriera, accoppiano i siti formando la base dell’ansa (Figura 03.10-09). Questi domini, spesso identificati come TAD (Topologically Associating Domains), delimitano il raggio d’azione degli enhancer e fungono da isolatori funzionali. La rilevanza biologica di tale organizzazione emerge quando i confini di dominio sono alterati: riarrangiamenti cromosomici o mutazioni nei fattori architetturali possono consentire a un enhancer di attivare geni vicini in modo inappropriato, con esiti patologici. Espressione ectopica o temporizzata in modo scorretto è stata osservata in diverse neoplasie e in malattie congenite, confermando che l’integrità dei circuiti ad ansa è cruciale per la regolazione genica precisa.