Idrocarburi aromatici
Definizione
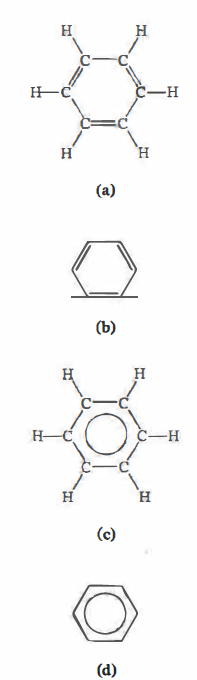
All’inizio del XIX secolo i chimici individuarono una classe di composti costituiti esclusivamente da carbonio e idrogeno che, pur essendo idrocarburi, mostravano comportamenti chimici insoliti rispetto a alcani, alcheni e alchini. Poiché molti di questi composti vennero estratti da resine e balsami dall’odore intenso, furono denominati “aromatici”. Le loro formule empiriche, caratterizzate da un rapporto carbonio/idrogeno indicativo di marcata insaturazione, lasciavano presagire una spiccata tendenza alle reazioni di addizione tipiche dei doppi e tripli legami; al contrario, tali sostanze risultarono notevolmente meno reattive verso l’addizione di quanto previsto. Oggi il termine “idrocarburi aromatici” non rimanda all’odore, bensì a un peculiare surplus di stabilità termodinamica e a una reattività selettiva, entrambe connesse alla delocalizzazione elettronica nell’anello π. L’architettura più rappresentativa è il nucleo benzenico esagonale, al quale si ispirano un’enorme varietà di composti monociclici e policiclici. Le differenti modalità convenzionali di raffigurazione del benzene sono illustrate in (Figura 06.11-01).
Il benzene, C6H6, è un esagono planare in cui i sei atomi di carbonio occupano i vertici e ciascuno è legato a un idrogeno. La prima proposta strutturale organica coerente con questa formula fu avanzata da Friedrich Kekulé (1865), che postulò un sistema ciclico con alternanza di legami singoli e doppi. Per conciliare tale schema con l’osservazione che il benzene non decolora il bromo in condizioni blande, Kekulé ipotizzò un’interconversione estremamente rapida tra due strutture limite, spesso richiamate come le due forme “a scambio” del benzene. In notazione moderna, queste due strutture contribuiscono all’ibrido di risonanza, e sono comunemente rappresentate come in (Figura 06.11-01).
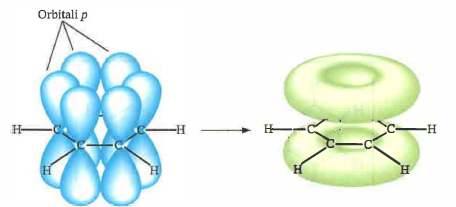
La comprensione attuale si fonda sul modello degli orbitali molecolari: ogni carbonio è ibridato \(sp^2\) e impiega tre orbitali \(sp^2\) coplanari (angoli di circa 120°) per formare tre legami σ, due con i carboni adiacenti e uno con l’idrogeno. Il quarto elettrone di valenza occupa un orbitale p perpendicolare al piano dell’anello. La sovrapposizione laterale dei sei orbitali p genera un sistema π delocalizzato, continuo e circolare, che si estende sopra e sotto il piano dell’anello (Figura 06.11-02). Questa delocalizzazione porta a lunghezze di legame C–C equivalenti (circa 1,39 Å), intermedie tra un singolo e un doppio legame, e a un’energia di stabilizzazione (energia di risonanza) sostanziale. Per sottolineare l’equivalenza dei legami e la natura circolare della densità elettronica π, si usa spesso il simbolo con il cerchio all’interno dell’esagono, come in (Figura 06.11-01).
La stabilità e la reattività del benzene si spiegano con i criteri di aromaticità, che richiedono:
- struttura ciclica e completamente coniugata, con orbitali p contigui su ogni atomo dell’anello;
- planarità, in modo che gli orbitali p siano allineati e possano sovrapporsi efficacemente;
- un numero di elettroni π pari a \(4n+2\), con \(n\) intero non negativo; nel benzene gli elettroni π sono 6, quindi \(n=1\).
Queste condizioni conferiscono un’eccezionale stabilità al sistema π e modificano la reattività: invece di subire addizioni elettrofile distruttive dell’anello π (come avviene negli alcheni), il benzene privilegia reazioni di sostituzione elettrofila aromatica, che preservano l’aromaticità del nucleo. Solo in presenza di catalizzatori o condizioni drastiche si osservano reazioni di addizione. La natura circolare della densità elettronica π è coerente, tra l’altro, con la corrente di anello indotta da un campo magnetico esterno, fenomeno che si riflette nelle caratteristiche anisotrope osservate, ad esempio, nella spettroscopia NMR.
In sintesi, il benzene è descritto in modo efficace come ibrido di risonanza delle due strutture di Kekulé (Figura 06.11-01), ma trova la sua spiegazione più profonda nel quadro degli orbitali molecolari e della delocalizzazione π continua, opportunamente resa dal simbolo con il cerchio (Figura 06.11-01) e dalla rappresentazione degli orbitali p sovrapposti (Figura 06.11-02).
Nella denominazione dei composti aromatici più semplici, l’anello benzenico rappresenta il riferimento strutturale: la molecola è descritta come benzene sostituito oppure mediante il tema “benz-” inserito nel nome del sistema. In pratica, si antepone al termine “-benzene” il nome dei sostituenti oppure si impiega il termine “benz-” all’interno del nome del composto, come mostrano gli esempi nelle figure seguenti;
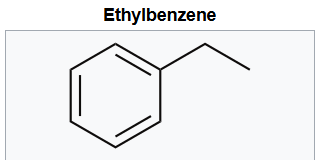 |
| Struttura dell’etilbenzene. |
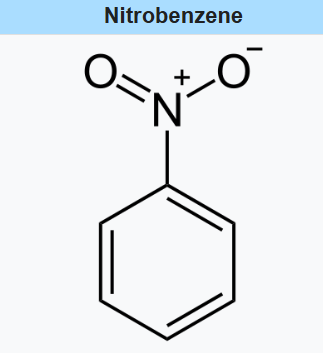 |
| Struttura del nitrobenzene. |
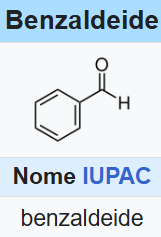 |
| Struttura della benzaldeide. |
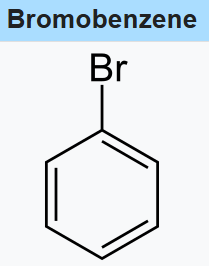 |
| Struttura del bromobenzene. |
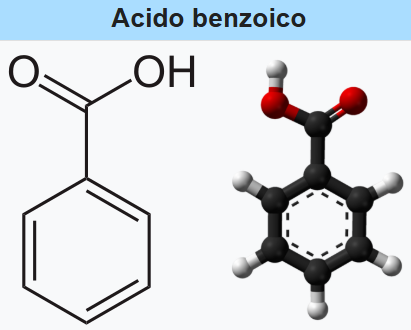 |
| Struttura dell’acido benzoico. |
Accanto ai nomi sistematici IUPAC rimangono d’uso corrente alcuni nomi tradizionali (triviali), riportati in letteratura e ancora accettati nella pratica comune, per esempio;
| Derivati del benzene. |
Tra i più diffusi si ricordano “xilene”, che indica i tre isomeri dimetilbenzene, e “cresolo”, che designa i tre isomeri metilfenolo. Nel caso di due sostituenti sull’anello, la posizione relativa è cruciale e si esprime sia con la nomenclatura comune sia con quella IUPAC:
- ortho- (o-) corrisponde a 1,2-, cioè i due sostituenti su carboni adiacenti;
- meta- (m-) corrisponde a 1,3-, cioè i sostituenti separati da un carbonio;
- para- (p-) corrisponde a 1,4-, cioè i sostituenti separati da due carboni.
La Figura seguente riassume i pattern di sostituzione sull’anello benzenico;
 |
| Posizioni orto, meta e para nel benzene. |
Le strutture dei tre isomeri degli xileni e dei cresoli sono riportate di seguito;
 |
| Isomeri orto, meta e para dello xylene. |
 |
| Direttori orto/para e meta nella sostituzione aromatica. |
Con tre o più sostituenti, si numerano gli atomi dell’anello per assegnare il set di locanti più basso possibile e si elencano i sostituenti in ordine alfabetico come prefissi, preceduti dai loro numeri di posizione; i prefissi moltiplicativi (di-, tri-, ecc.) non influiscono sull’ordine alfabetico.
Nella terminologia IUPAC, l’unità –C6H5 è il gruppo fenile: quando un anello aromatico è legato a una catena alifatica “lunga” (almeno tre atomi di carbonio), il nome principale è quello dell’idrocarburo alifatico e il fenile compare come sostituente. Esempi illustrativi sono riportati nelle figure seguenti;
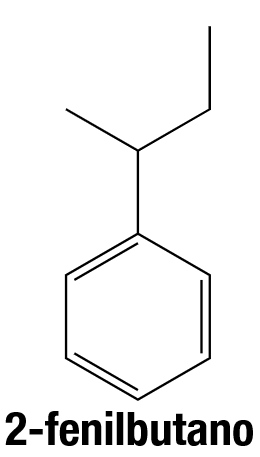 |
| Struttura del propilbenzene. |
Un altro termine di uso comune è “benzilico” (benzile), che indica il carbonio immediatamente adiacente all’anello fenilico, spesso rappresentato come –CH2–C6H5. La particolare stabilizzazione dei centri reattivi in posizione benzilica (carbocationi, radicali e anioni) spiega la reattività caratteristica di molti derivati;
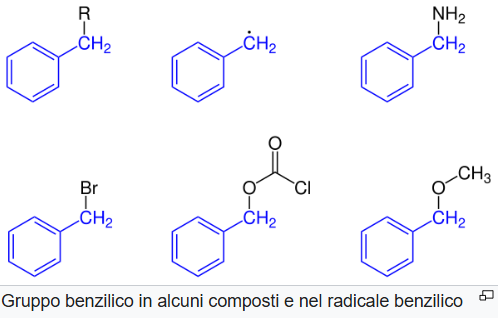 |
| Gruppo benzilico e suoi derivati. |
L’impiego del termine “benzilico” è mostrato nei seguenti esempi;
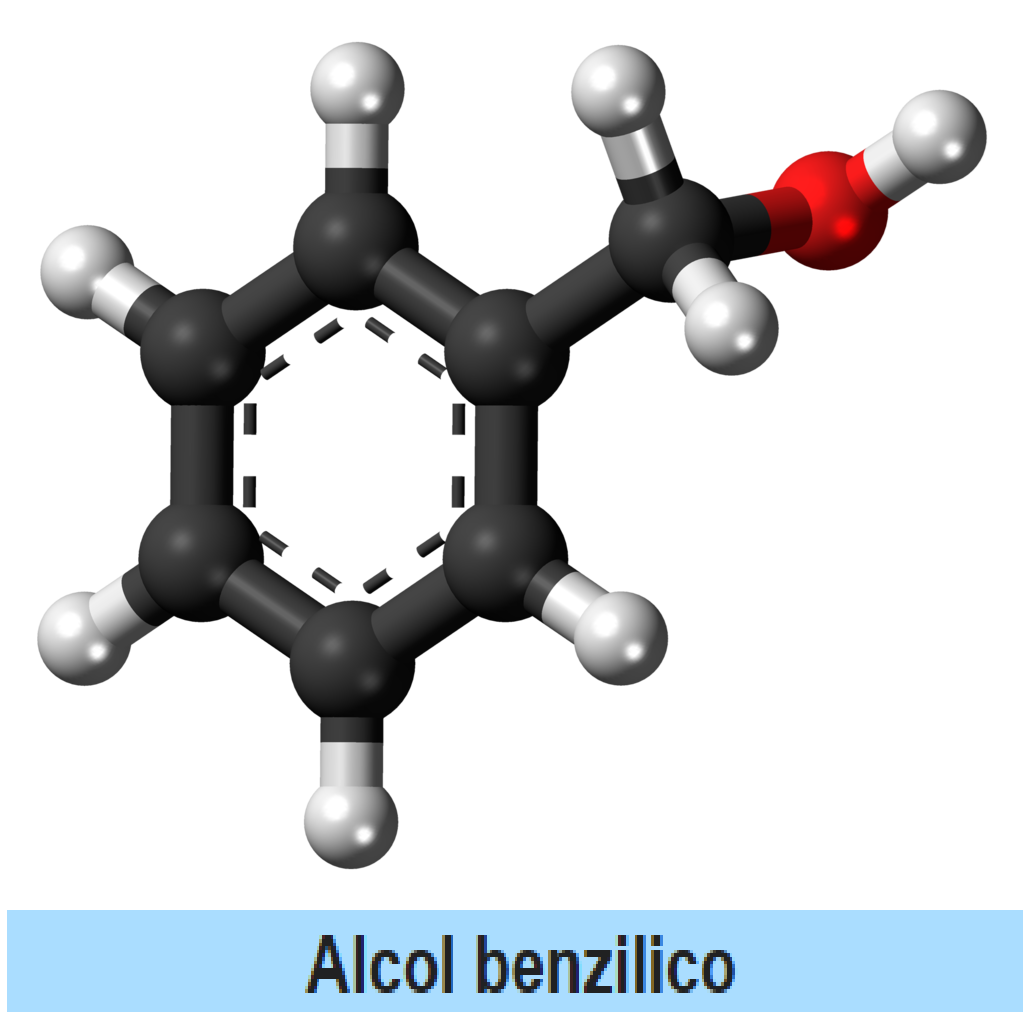 |
| Alcol benzilico. |
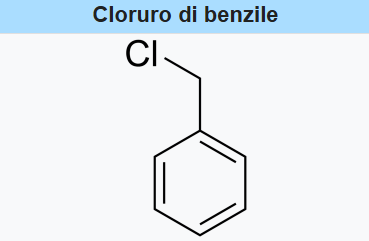 |
| Cloruro di benzile. |
Gli idrocarburi policiclici aromatici (IPA, o PAH) sono sistemi in cui due o più anelli benzenici condividono lati (anelli “condensati”), preservando un’estesa coniugazione elettronica. Esempi classici includono naftalene, antracene, fenantrene, pirene e benzo[a]pirene;
 |
| Idrocarburi aromatici policiclici. |
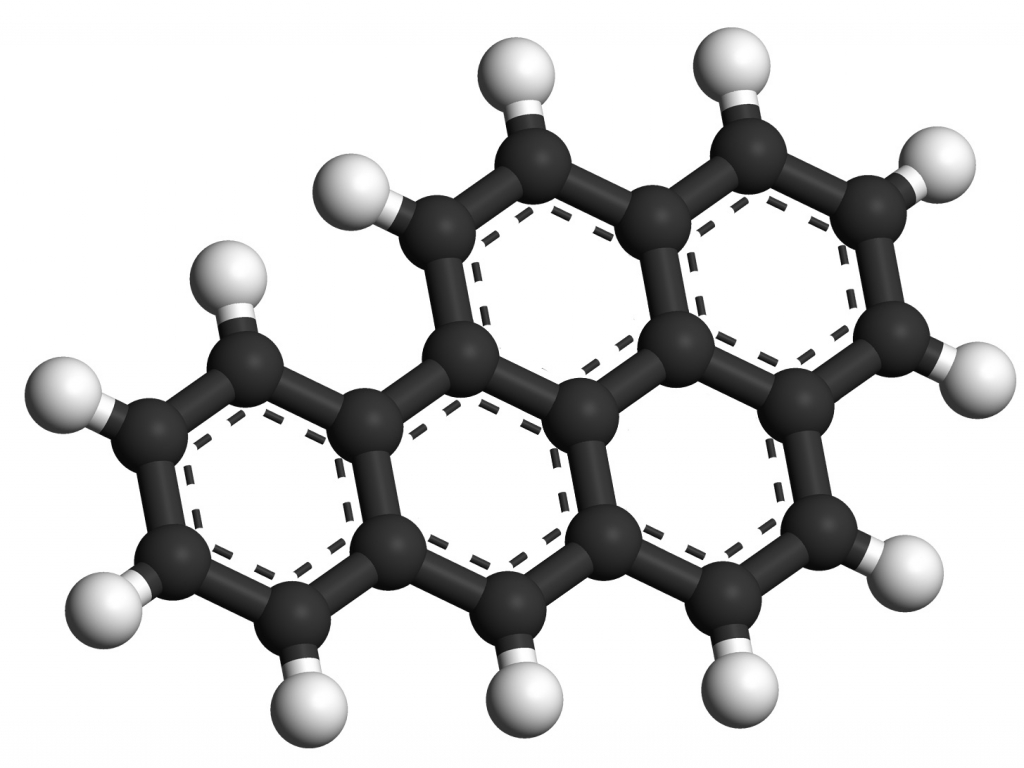 |
| Modello 3D del fenantrene. |
Il naftalene, storicamente impiegato nelle palline antitarme, è oggi soggetto a restrizioni per motivi sanitari: può causare anemia emolitica, specialmente nei soggetti con deficit di G6PD; riguardo alla cancerogenicità, la sua classificazione internazionale è “possibilmente cancerogeno per l’uomo” (IARC, Gruppo 2B). L’antracene (tre anelli in linea) è un derivato del catrame, precursore di numerosi pigmenti; il fenantrene (isomero angolato dell’antracene) è tipico dei prodotti di combustione incompleta di biomasse e combustibili fossili; entrambi non sono classificati come cancerogeni certi per l’uomo (in genere Gruppo 3, non classificabile). Di particolare rilievo tossicologico è il benzo[a]pirene, presente nel fumo di tabacco, nella carne fortemente affumicata o grigliata e nei gas di scarico: è classificato cancerogeno per l’uomo (IARC, Gruppo 1). Si noti che la reattività degli IPA può differire da quella del benzene: per esempio, l’antracene è relativamente più reattivo in addizione al doppio legame 9,10, mentre il naftalene tende alla sostituzione elettrofila con preferenza per la posizione α (C-1).
La stabilità peculiare degli anelli aromatici non è spiegata unicamente ricorrendo alle forme limite di Kekulé: un ruolo centrale è svolto dal numero di elettroni π e dalla delocalizzazione su una struttura planare coniugata. Molecole cicliche con 4 o 8 elettroni π (per esempio sistemi a 4 o 8 atomi con doppi legami coniugati) tendono a essere instabili o a evitare la planarità per sfuggire a uno stato antiaromatico, mentre sistemi con 6, 10, 14 elettroni π risultano insolitamente stabili e poco reattivi verso addizione. In termini formali, per attribuire carattere aromatico a un sistema organico devono valere le seguenti condizioni:
- ciclicità: la struttura deve costituire un circuito chiuso di orbitali p sovrapposti;
- planarità e coniugazione: tutti gli atomi dell’anello devono essere ibridi sp2 (o possedere un orbitale p disponibile) e disposti in modo da consentire la sovrapposizione laterale continua;
- conteggio degli elettroni π che soddisfi la regola di Hückel: \(N_{\pi} = 4n + 2\), con \(n \in \mathbb{Z}_{\ge 0}\).
Per molecole monocicliche, tali criteri sono diagnostici: il benzene ha 6 elettroni π (\(n = 1\)) ed è aromatico; il ciclobutadiene ne ha 4 (\(n = 1\) nella forma \(4n\)) ed è antiaromatico; il cicloottatetraene, con 8 elettroni π, adotta una geometria a “vasca” non planare per evitare l’antiaromaticità. Per sistemi policiclici condensati, l’applicazione della sola regola \(4n + 2\) al numero totale di elettroni π può essere fuorviante: l’analisi più accurata considera circuiti di periferia e il concetto di sestetto aromatico di Clar; in molti benzenoidi lineari (naftalene, antracene, fenantrene) il totale di elettroni π rientra comunque in sequenze \(4n+2\) (10, 14, 14 rispettivamente), ma la semplice uguaglianza “n = numero di anelli” non è generale.
Non solo specie neutre possono essere aromatiche: ioni che rispettino i criteri suddetti mostrano stabilizzazione analoga. Il ciclopentadiene, non aromatico perché uno dei cinque atomi è sp3 e il sistema ha solo 4 elettroni π, può deprotonarsi a dare lo ione ciclopentadienile, \(\mathrm{C_5H_5^-}\): la coppia elettronica risultante occupa un orbitale p, rendendo tutti i cinque centri sp2 e fornendo 6 elettroni π (\(n = 1\)), con aromaticità marcatamente osservata sperimentalmente. Altri esempi sono lo ione ciclopropenilico \(\mathrm{C_3H_3^+}\) (2 elettroni π) e il catione tropilio \(\mathrm{C_7H_7^+}\) (7 elettroni π), entrambi aromatici.
La trasformazione caratteristica degli idrocarburi aromatici è la sostituzione elettrofila aromatica (SEA), in cui un atomo di idrogeno dell’anello viene rimpiazzato da un elettrofilo, conservando l’aromaticità complessiva. Il meccanismo procede in tre tappe: generazione dell’elettrofilo forte (E+), attacco all’anello con formazione del complesso σ (intermedio arenio), e deprotonazione per ristabilire la delocalizzazione.
In assenza di catalizzatori appropriati, il benzene non subisce addizione al bromo o al cloro. In presenza di ferro o alogenuri ferrosi/ferrici (Fe, FeCl3, FeBr3), avviene invece la bromurazione/clorurazione per sostituzione;
 |
| Clorurazione elettrofila del benzene. |
| Bromurazione elettrofila del benzene. |
La sostituzione di un secondo idrogeno può generare tre isomeri (orto, meta, para). L’orientazione è influenzata dalla natura del primo sostituente: gruppi donatori di elettroni (per esempio –CH3, –OH, –NH2) sono tipicamente attivanti e orto/para-orientanti, mentre gruppi fortemente attrattori (–NO2, –SO3H, –CF3, –COH, –CO2R) deattivano l’anello e orientano in meta.
Il benzene reagisce con triossido di zolfo in ambiente acido dando l’acido benzensolfonico (solfonazione), reazione reversibile in condizioni idonee;
 |
| Meccanismo della solfonazione elettrofila del benzene. |
La nitrazione richiede acido nitrico concentrato in presenza di acido solforico, che genera l’elettrofilo nitronio \(\mathrm{NO_2^+}\);
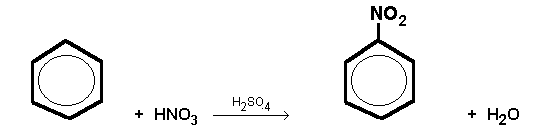 |
| Nitrificazione del benzene. |
Tra le SEA più utilizzate figurano inoltre le alchilazioni e acilazioni di Friedel–Crafts, catalizzate da \(\mathrm{AlCl_3}\) o analoghi: l’acilazione (con cloruri acilici o anidridi) introduce un gruppo acilico e, rispetto all’alchilazione, evita polialchilazioni e dà prodotti più prevedibili. Condizioni fortemente deattivanti (es. presenza di –NO2) o la presenza di gruppi basici coordinanti possono inibire queste trasformazioni.