I meccanismi dell’ereditarietà si presentano spesso più complessi di quanto previsto dalla genetica mendeliana
Definizione
La cellula può essere descritta come un sistema chimico altamente integrato, nel quale centinaia di vie metaboliche interagiscono in modo dinamico e coordinato (Figura 05.10-01). In questa prospettiva, la descrizione di glicolisi e ciclo dell’acido citrico rappresenta solo una porzione del quadro complessivo: in ogni istante coesistono, nello stesso volume cellulare, molteplici sequenze enzimatiche che condividono intermedi, cofattori e fonti energetiche. Perché l’insieme rimanga funzionale, la cellula deve selezionare con precisione la destinazione di ciascun metabolita a ogni snodo, sincronizzando le decisioni locali con lo stato energetico globale e con i segnali ambientali. Il mantenimento dell’omeostasi energetica richiede una ricostituzione continua delle riserve di ATP mediante l’ossidazione di carboidrati e lipidi. Tuttavia, la disponibilità di nutrienti ed energia non è costante: gli animali si alimentano a intervalli, mentre le piante attraversano fasi di buio nelle quali la fotosintesi è assente. Per far fronte a tali cicli, organismi vegetali e animali hanno evoluto strategie di immagazzinamento e mobilizzazione delle risorse, come la sintesi di glicogeno e triacilgliceroli negli animali o di amido nei cloroplasti delle piante, accumulati quando le risorse abbondano e consumati quando scarseggiano. Ne consegue che, in base alle condizioni, una cellula deve bilanciare l’impiego degli intermedi metabolici tra processi anabolici, orientati alla biosintesi e alla crescita, e processi catabolici, finalizzati a produrre energia chimica immediatamente utilizzabile. In ciò risiede la logica di regolazione che sostiene tanto le esigenze contingenti quanto l’adattamento a lungo termine.
Le reazioni sintetiche e degradative richiamate nella (Figura 05.10-01) si svolgono in una cellula con dimensioni inferiori a 0,1 mm, e ciascuna tappa è catalizzata da un enzima distinto. La complessità aumenta perché uno stesso intermedio può partecipare a vie differenti e concorrenti. Il piruvato ne è un esempio paradigmatico: è convertito in acetil-CoA dal complesso piruvato deidrogenasi, ridotto a lattato dalla lattato deidrogenasi durante la fermentazione, carbossilato a ossalacetato da un’enzima anaplerotico, oppure transaminato ad alanina. Queste rotte competono per lo stesso substrato, e analoghe competizioni interessano innumerevoli altre piccole molecole all’interno della cellula. Per distribuire in modo coerente i flussi metabolici e adattarsi a variazioni di nutrienti, richiesta energetica e stress, agisce una rete multilivello di meccanismi regolatori che modulano l’attività degli enzimi e la disponibilità dei metaboliti. Tra i principi più rilevanti si annoverano:
- allosteria e feedback: metaboliti a valle o cofattori (per esempio ATP, ADP, AMP, citrato, NADH) si legano agli enzimi chiave modulandone l’attività; fenomeni di feedback inibitorio e feed-forward favoriscono la stabilità dei flussi;
- modificazioni covalenti: fosforilazioni e defosforilazioni reversibili, nonché acetilazioni o uridilazioni, ricalibrano rapidamente la velocità enzimatica tramite chinasi e fosfatasi;
- controllo dell’espressione genica: l’abbondanza di specifici enzimi varia nel tempo attraverso regolazione trascrizionale e traduzione selettiva, con impatto sulle capacità di flusso a medio-lungo termine;
- compartimentazione e trasporto: la separazione spaziale tra citosol, mitocondri, perossisomi e plastidi, e i sistemi di trasporto di metaboliti, evitano cicli futili e indirizzano i substrati verso la destinazione richiesta;
- stato energetico e redox: la “carica energetica” della cellula, spesso stimata come \( \mathrm{EC} = \frac{[\mathrm{ATP}] + 0{,}5[\mathrm{ADP}]}{[\mathrm{ATP}] + [\mathrm{ADP}] + [\mathrm{AMP}]} \), e il rapporto NADH/NAD\(^+\) o FADH\(_2\)/FAD orientano l’accensione o lo spegnimento di vie ossidative e biosintetiche;
- segnalazione ormonale e ambientale: negli animali, ormoni come insulina, glucagone e adrenalina coordinano il metabolismo di glucosio e lipidi in tessuti distinti; nelle piante, luce/buio e segnali circadiani modulano l’alternanza tra fissazione del carbonio e utilizzo delle riserve;
- reciprocità delle vie: coppie anaboliche e cataboliche (ad esempio glicolisi e gluconeogenesi) sono regolate in modo antitetico per evitare sprechi energetici e garantire la direzionalità del flusso.
In termini operativi, la cellula integra segnali locali e sistemici per decidere se convogliare il piruvato verso ossidazione nel ciclo dell’acido citrico, fermentazione, rifornimento anaplerotico o sintesi di amminoacidi. Scelte analoghe riguardano altri nodi centrali, come glucosio-6-fosfato, acetil-CoA e ossalacetato. La regolazione può essere potenziante o inibente e agisce su enzimi chiave di sintesi e degradazione del glucosio, come sarà approfondito più avanti. Grazie a questo coordinamento, le cellule mantengono l’equilibrio tra produzione di ATP, generazione di equivalenti riducenti e sintesi di componenti strutturali, preservando la funzionalità anche in condizioni di apporto energetico intermittente o di fluttuazioni ambientali.
Negli animali il rifornimento di glucosio deve essere continuo: il muscolo in attività lo ossida per sostenere la contrazione e il tessuto nervoso ne dipende quasi esclusivamente per la respirazione cellulare. Nelle fasi di digiuno o durante sforzi prolungati, le riserve circolanti si esauriscono più rapidamente di quanto possano essere ripristinate con l’alimentazione. In tali condizioni, il glucosio può essere rigenerato a partire da precursori non carboidratici, soprattutto dal piruvato, attraverso la gluconeogenesi. Questa via, pur condividendo diversi intermedi ed enzimi con la glicolisi, opera con direzione opposta e impiega reazioni alternative per scavalcare i passaggi irreversibili della glicolisi. Gli stadi 1, 3 e 10 della glicolisi sono fortemente esoergonici e indirizzano il flusso verso la degradazione del glucosio. La gluconeogenesi utilizza quindi “bypass” enzimatici: la glucosio 6-fosfatasi sostituisce l’esochinasi/glucochinasi (stadio 1), la fruttosio 1,6-bisfosfatasi sostituisce la fosfofruttochinasi-1 (stadio 3), mentre la coppia piruvato carbossilasi e fosfoenolpiruvato carbossichinasi (PEPCK) elude la reazione della piruvato chinasi (stadio 10). Un esempio è illustrato in (Figura 05.10-02): l’intermedio fruttosio 1,6-bisfosfato, invece di essere prodotto per fosforilazione, viene defosforilato dalla fruttosio 1,6-bisfosfatasi per formare fruttosio 6-fosfato. La decisione di una cellula se ossidare o sintetizzare glucosio dipende in larga misura da meccanismi di regolazione allosterica e ormonale che agiscono su questi nodi irreversibili. La fosfofruttochinasi-1 (PFK-1) funge da valvola di controllo per la glicolisi ed è modulata da metaboliti che riflettono lo stato energetico:
- attivatori: AMP, ADP e fosfato inorganico, segnali di carenza energetica che promuovono la glicolisi;
- inibitori: ATP e citrato, indicatori di abbondanza energetica e di precursori biosintetici;
- regolatore chiave: fruttosio 2,6-bisfosfato, potente attivatore di PFK-1 e, simultaneamente, inibitore della fruttosio 1,6-bisfosfatasi.
Il fruttosio 2,6-bisfosfato è controllato dall’enzima bifunzionale PFK-2/FBPasi-2, bersaglio della segnalazione ormonale: il glucagone e l’adrenalina ne riducono i livelli nei tessuti appropriati inibendo la glicolisi e favorendo la gluconeogenesi, mentre l’insulina ha l’effetto opposto. Questa regolazione reciproca garantisce che glicolisi e gluconeogenesi non procedano simultaneamente alla massima velocità, prevenendo cicli futili. Le reazioni di deviazione della gluconeogenesi hanno un costo notevole: l’elusione dello stadio 10 richiede, per ogni molecola di piruvato, 1 ATP (piruvato carbossilasi) e 1 GTP (PEPCK). Nel complesso, per sintetizzare una molecola di glucosio a partire da due piruvati sono necessari 4 ATP, 2 GTP e 2 NADH, con consumo di acqua e rilascio di fosfato inorganico. La stechiometria globale può essere riassunta come:
\[2\,\text{piruvato} + 4\,\text{ATP} + 2\,\text{GTP} + 2\,\text{NADH} + 6\,\text{H}_2\text{O} \rightarrow \text{glucosio} + 4\,\text{ADP} + 2\,\text{GDP} + 6\,\text{P}_i + 2\,\text{NAD}^+ + 2\,\text{H}^+.\]
Data l’elevata spesa energetica, l’attivazione concomitante di glicolisi e gluconeogenesi genererebbe un “ciclo futile” con migrazione pendolare degli intermedi e dissipazione di energia sotto forma di calore. Per evitarlo, l’inibizione di PFK-1 si accompagna all’attivazione della fruttosio 1,6-bisfosfatasi e viceversa (Figura 05.10-02). Nei mammiferi, la gluconeogenesi è localizzata prevalentemente in fegato e corteccia renale, con tappe che coinvolgono mitocondri, citosol e, per l’idrolisi del glucosio 6-fosfato, il lume del reticolo endoplasmatico.
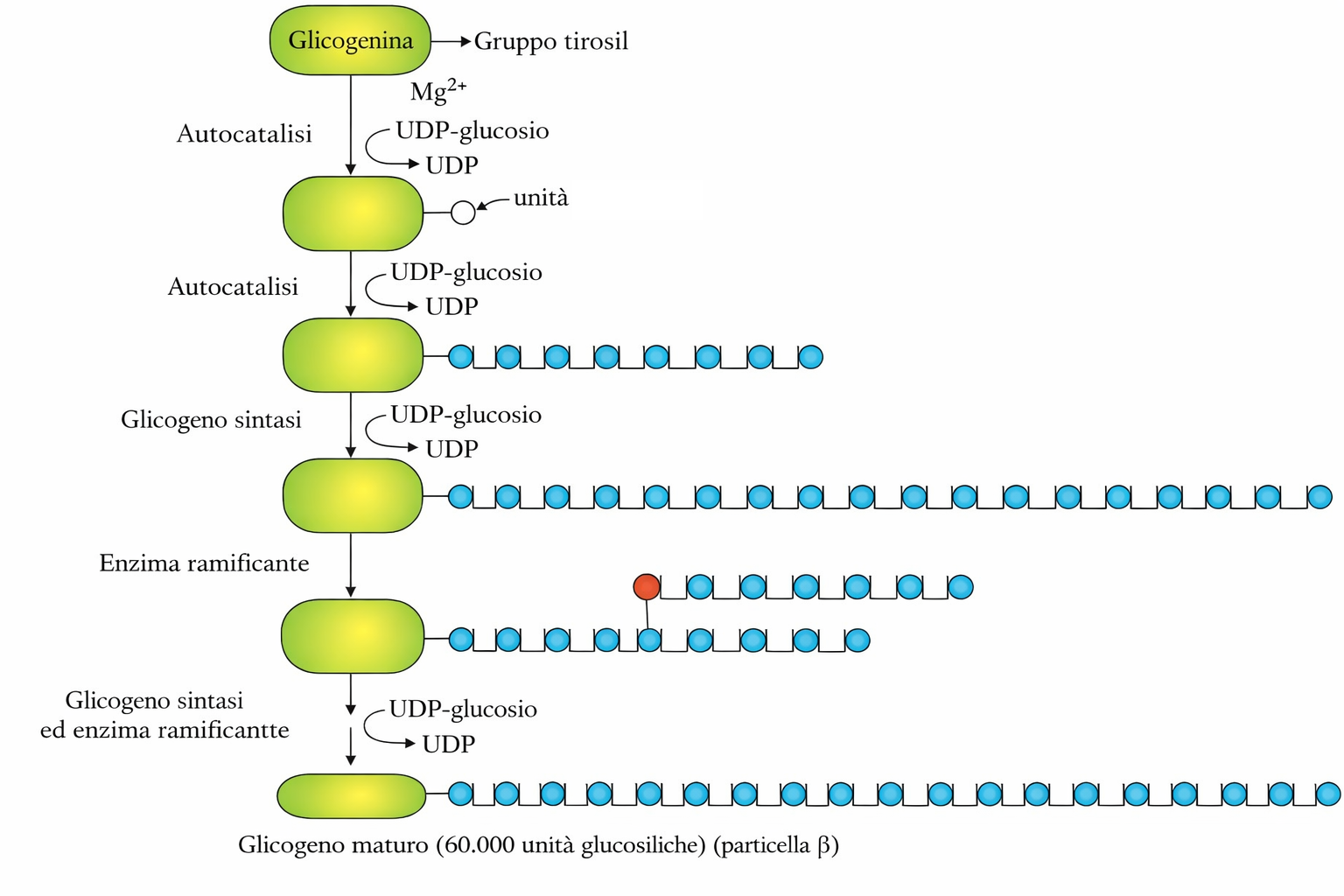
Poiché la gluconeogenesi richiede un ampio investimento di ATP e GTP, quando esistono riserve pronte all’uso la cellula preferisce mobilizzarle. Il glucosio è stoccato come glicogeno, un polimero ramificato di residui di glucosio uniti da legami α-1,4 con ramificazioni α-1,6 (Figura 05.10-03). Granuli di glicogeno sono abbondanti nel citoplasma degli epatociti e delle fibre muscolari (Figura 05.10-03). La degradazione del glicogeno è catalizzata dalla glicogeno fosforilasi, che libera glucosio 1-fosfato; la fosfoglucomutasi lo converte in glucosio 6-fosfato, pronto per entrare nella glicolisi o per essere defosforilato a glucosio libero nel fegato (Figura 05.10-03). La sintesi procede attraverso l’attivazione del glucosio a UDP-glucosio, l’azione della glicogeno sintetasi e dell’enzima ramificante. La regolazione assicura una risposta rapida e coordinata alle richieste energetiche:
- controllo allosterico: il glucosio 6-fosfato attiva la glicogeno sintetasi e inibisce la glicogeno fosforilasi; nel muscolo, l’AMP attiva la fosforilasi durante sforzo, mentre l’ATP la inibisce;
- controllo covalente mediato da segnali ormonali: l’adrenalina (muscolo) e il glucagone (fegato) attivano la proteina chinasi A, che favorisce la fosforilazione e l’attivazione della fosforilasi e inibisce la sintetasi; l’insulina promuove la defosforilazione tramite fosfatasi come PP1, stimolando la sintesi;
- integrazione con il calcio nel muscolo: il Ca2+ attiva la fosforilasi chinasi via calmodulina, sincronizzando contrazione e disponibilità di glucosio 6-fosfato.
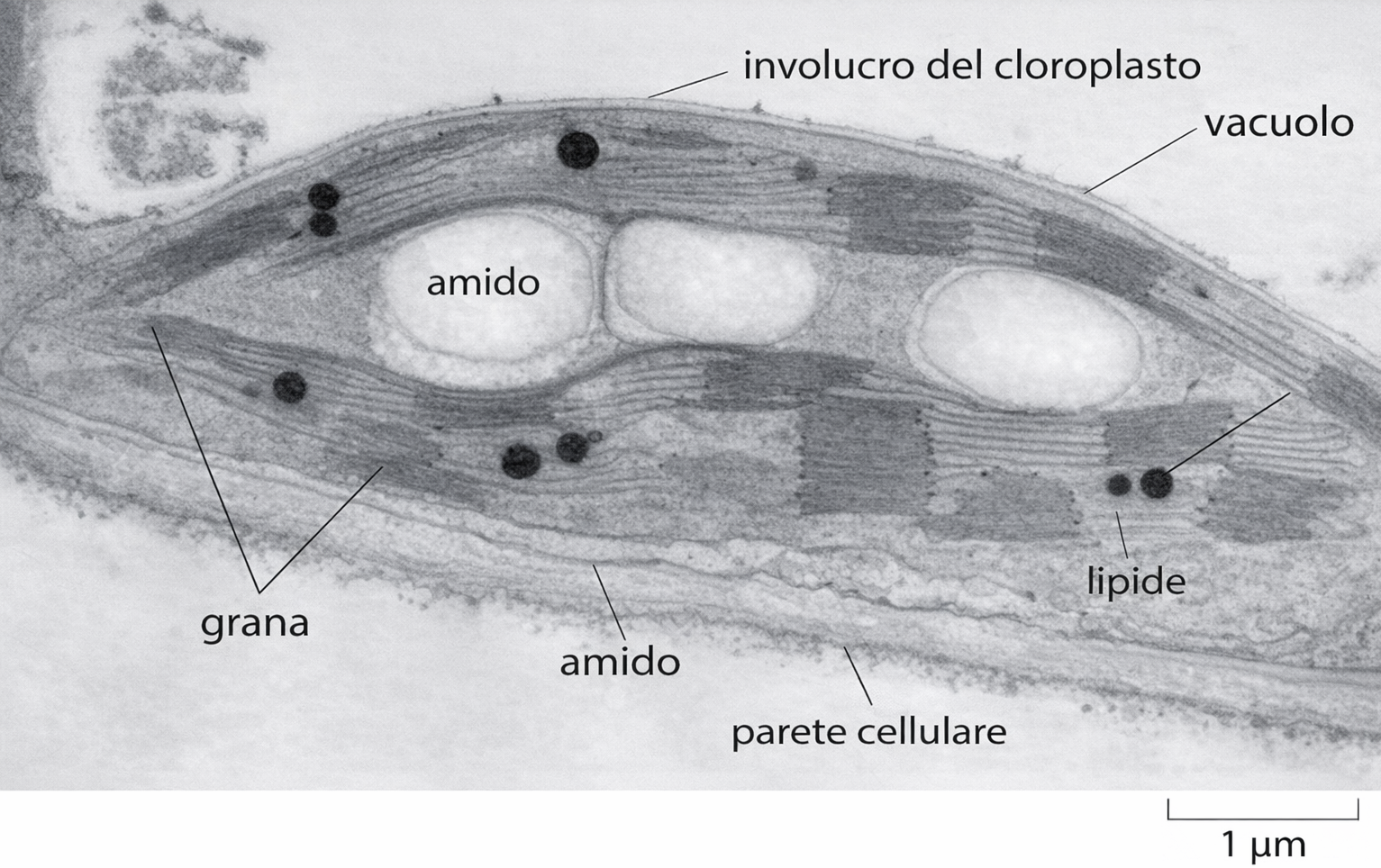
Su scala quantitativa, i lipidi rappresentano la riserva energetica predominante. L’ossidazione di 1 g di triacilglicerolo libera circa il doppio dell’energia rispetto a 1 g di glicogeno, e il glicogeno, idrofilo, trattiene acqua in proporzioni elevate, aumentando il volume occupato di circa sei volte rispetto a un deposito lipidico energeticamente equivalente. Una persona adulta possiede tipicamente glicogeno sufficiente per circa 24 ore di attività moderata, mentre le scorte lipidiche possono sostenere il metabolismo per settimane. La maggior parte dei trigliceridi è accumulata in goccioline lipidiche idrofobiche negli adipociti (Figura 05.10-04). In risposta a ormoni lipolitici, gli acidi grassi sono rilasciati nel circolo e ossidati nei tessuti che ne hanno necessità. Già dopo una normale notte di digiuno, l’acetil-CoA che alimenta il ciclo dell’acido citrico proviene in misura considerevole dall’ossidazione degli acidi grassi; dopo un pasto, invece, prevale l’ossidazione del glucosio e l’eccesso di carboidrati viene convertito in glicogeno e in acidi grassi per il deposito. Le cellule animali non realizzano una conversione netta dei lipidi in glucosio, poiché l’acetil-CoA non può essere riconvertito a piruvato e il ciclo citrico disperde carbonio come CO2; fanno eccezione contributi minori da acidi grassi a catena dispari via propionil-CoA e succinil-CoA, che non sostengono però una gluconeogenesi significativa. Nelle piante, parte degli zuccheri prodotti con la fotosintesi è stoccata come amido, un polimero del glucosio strutturalmente affine al glicogeno, e come triacilgliceroli (Figura 05.10-05). I semi, che devono sostenere l’embrione fino all’autonomia fotosintetica, accumulano grandi quantità di oli e amido. Durante la germinazione, i depositi lipidici sono mobilizzati in corpi oleosi e, attraverso il ciclo del gliossilato, convertiti in carboidrati; gli amidi e i grassi si accumulano nei cloroplasti delle cellule fotosintetiche e in plastidi specializzati, e vengono utilizzati per generare ATP nei mitocondri durante i periodi di scarsa disponibilità di nutrienti (Figura 05.10-06). Queste riserve, tanto negli animali quanto nelle piante, costituiscono fonti fondamentali di energia e materia prima anche per l’alimentazione umana, grazie all’elevato contenuto di amido e lipidi dei tessuti di deposito.