I geni legati al sesso mostrano quadri ereditari unici
Definizione
I mitocondri sono organelli ubiquitari nelle cellule eucariotiche e rappresentano il principale sito di sintesi dell’ATP tramite fosforilazione ossidativa. In assenza della loro attività, la cellula dovrebbe affidarsi quasi esclusivamente alla glicolisi citosolica, processo che, convertendo il glucosio in piruvato, fornisce un guadagno netto di due ATP per molecola di glucosio, una frazione modesta dell’energia libera potenzialmente estraibile dall’ossidazione completa degli zuccheri. Quando l’ossidazione prosegue nei mitocondri, il bilancio energetico sale fino a circa 30–32 molecole di ATP per glucosio, grazie al trasferimento di elettroni a una catena respiratoria membranosa e all’accoppiamento chemiosmotico con la sintesi di ATP.
Su scala evolutiva, la comparsa dei mitocondri è interpretata nell’ambito della teoria endosimbiotica: un’antica associazione con progenitori batterici avrebbe consentito alle cellule eucariotiche di sfruttare con efficienza l’ossidazione di substrati energetici, facilitando l’emergere di organismi complessi. La rilevanza funzionale dei mitocondri è testimoniata dall’impatto clinico dei difetti mitocondriali. Nella MERRF (Myoclonic Epilepsy with Ragged Red Fibers), per esempio, mutazioni del DNA mitocondriale compromettono la sintesi di componenti necessari al trasporto elettronico, con conseguente deficit di ATP. Tessuti ad alta richiesta energetica, come muscolo e sistema nervoso, manifestano tipicamente debolezza, cardiomiopatie, epilessia e deterioramento cognitivo. Poiché il DNA mitocondriale è ereditato per via materna, le varianti patogene si trasmettono attraverso l’ovocita (Figura 05.12-14). Per evitare la propagazione di mutazioni gravi, sono state sviluppate procedure di sostituzione mitocondriale che prevedono il trasferimento del materiale genetico nucleare materno in un ovocita donatore con mitocondri funzionali; una nascita con questa tecnica è stata riportata nel 2016. Rimangono, tuttavia, questioni aperte etiche e regolatorie legate alla presenza di materiale genetico di tre soggetti (madre, padre e donatrice mitocondriale).
Alla base della conversione energetica mitocondriale vi è la creazione di una forza proton-motrice accoppiata alla sintesi di ATP. In termini termodinamici, il gradiente elettrochimico dei protoni si esprime come: \[ \Delta p = \Delta \psi - \frac{2,303\,RT}{F}\,\Delta \text{pH}, \] dove \(\Delta \psi\) è il potenziale di membrana, \(R\) la costante dei gas, \(T\) la temperatura assoluta e \(F\) la costante di Faraday.
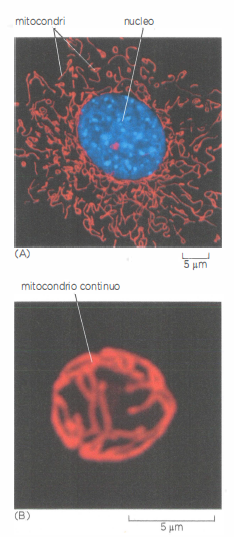
Pur derivando da antenati batterici, i mitocondri hanno acquisito una notevole adattabilità, riorganizzandosi in risposta allo stato metabolico cellulare. Possono muoversi lungo i microtubuli, ancorarsi dove il fabbisogno energetico è elevato e modulare il proprio numero tramite biogenesi e mitofagia. In cellule contrattile-intense, come i cardiomiociti, si dispongono in prossimità dell’apparato sarcomerico per fornire ATP a pochi nanometri dalla richiesta meccanica; negli spermatozoi circondano l’assonema del flagello per sostenere la motilità (Figura 05.12-01). In altri contesti, formano reti tubulari estese e altamente dinamiche che attraversano il citoplasma (Figura 05.12-02), sottoposte a continui eventi di scissione e fusione (Figura 05.12-15), processi mediati da GTPasi come DRP1 (fissione) e MFN1/2 e OPA1 (fusione).
Il contenuto mitocondriale varia con la funzione del tessuto e con gli stimoli ambientali. L’allenamento di resistenza o l’adattamento all’ipossia, per esempio, incrementano la densità mitocondriale nei muscoli scheletrici tramite l’attivazione di programmi di biogenesi regolati da PGC‑1α e NRF. In un atleta di endurance, il volume mitocondriale del muscolo può aumentare in modo sostanziale rispetto a quello di soggetti sedentari, con ricadute misurabili su capacità ossidativa e resistenza alla fatica. Analogamente, in neuroni con lunghi assoni i mitocondri si concentrano nei terminali sinaptici per tamponare flussi di Ca²⁺ e sostenere l’esocitosi; negli adipociti bruni, proteine disaccoppianti come UCP1 deviano la forza proton-motrice verso la termogenesi, rendendo questi mitocondri particolarmente abbondanti e specializzati.
Nonostante la variabilità in forma e organizzazione, l’architettura interna dei mitocondri è condivisa e finalizzata a massimizzare la produzione di ATP, come illustrato in seguito.
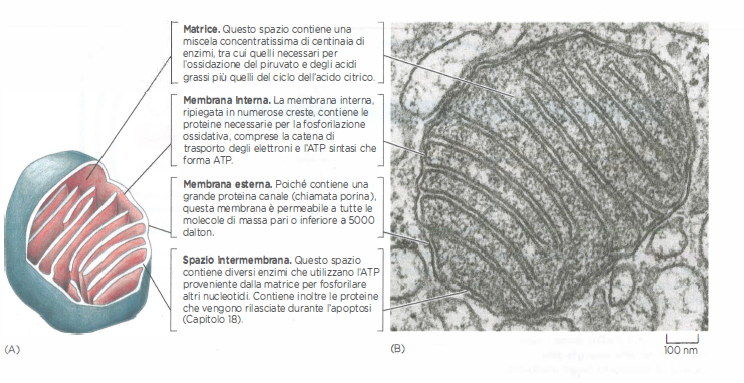
Il mitocondrio è delimitato da due membrane concentriche, esterna e interna, che definiscono due spazi: la matrice e lo spazio intermembrana (Figura 05.12-03). Ciascun compartimento ospita insiemi specifici di proteine e metaboliti, con una compartimentazione fine essenziale per la funzione.
La membrana esterna contiene canali porinici (VDAC) che consentono il passaggio di soluti idrofilici fino a circa 5 kDa, rendendo lo spazio intermembrana simile al citosol per la composizione delle piccole molecole e degli ioni. Sono inoltre presenti complessi d’importazione proteica (TOM), che collaborano con i complessi della membrana interna (TIM) per trasferire proteine nucleari nella matrice o nelle membrane mitocondriali.
La membrana interna è altamente selettiva e ricca di cardiolipina; è impermeabile alla maggior parte degli ioni e dei metaboliti, che la attraversano solo tramite trasportatori specifici (famiglia SLC25), tra cui il trasportatore ADP/ATP e il carrier del fosfato. In essa sono organizzati i complessi della catena di trasporto degli elettroni, le pompe protoniche e l’ATP sintasi, che sfruttano la superficie amplificata dalle creste per aumentare la capacità di fosforilazione ossidativa. In cellule metabolicamente attive, come gli epatociti, la superficie complessiva della membrana interna può rappresentare una frazione importante dell’intero patrimonio membranoso cellulare.
La matrice contiene enzimi per il ciclo dell’acido citrico, la β‑ossidazione e la replicazione/trascrizione del DNA mitocondriale, oltre a ribosomi mitocondriali. La composizione distinta della matrice riflette la selettività della membrana interna e la presenza di gradienti di pH e potenziale elettrico che alimentano i processi energetici:
- Membrana esterna: porine (VDAC), enzimi per il metabolismo lipidico, complesso TOM;
- Spazio intermembrana: ambiente simile al citosol per piccoli soluti, fattori coinvolti nell’apoptosi;
- Membrana interna: complessi respiratori I–IV, ATP sintasi, trasportatori specializzati;
- Matrice: enzimi del ciclo citrico e della β‑ossidazione, mtDNA, ribosomi, complesso piruvato deidrogenasi.
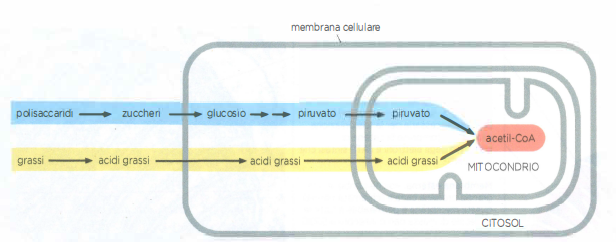
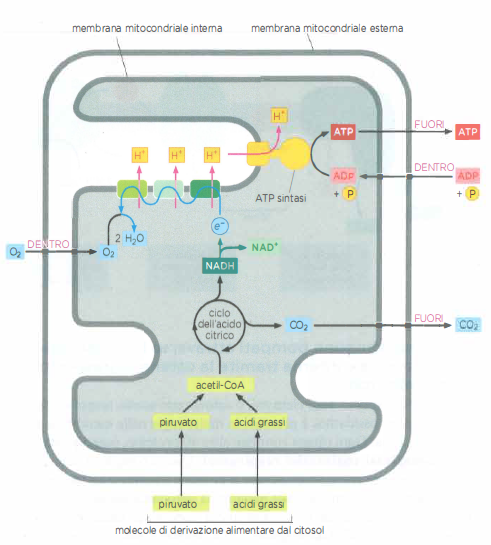
Il flusso elettronico che guida la produzione di ATP origina dall’ossidazione di carboidrati, lipidi e altri substrati. Il piruvato, prodotto dalla glicolisi citosolica, attraversa la membrana esterna tramite porine e raggiunge la matrice attraverso il carrier specifico del piruvato; qui il complesso piruvato deidrogenasi lo converte in acetil‑CoA, liberando CO₂ e generando NADH (Figura 05.12-04). Analogamente, gli acidi grassi entrano nei mitocondri e, dopo attivazione e trasporto tramite la carnitina, sono degradati per β‑ossidazione a unità di acetil‑CoA, con produzione concomitante di NADH e FADH₂.
L’acetil‑CoA alimenta il ciclo dell’acido citrico, nel quale il gruppo acetile è completamente ossidato a CO₂. Per ogni giro del ciclo, per molecola di acetil‑CoA si formano: \[ 3\,\text{NADH} + 1\,\text{FADH}_{2} + 1\,\text{GTP (o ATP)}. \] Gli equivalenti riducenti NADH e FADH₂ trasferiscono gli elettroni alla catena respiratoria nella membrana interna, con pompaggio di protoni e generazione della forza proton-motrice necessaria all’ATP sintasi (Figura 05.12-05).
In termini di resa energetica, l’ossidazione completa di una molecola di glucosio comporta: \[ \text{Glicolisi: } 2\,\text{ATP} + 2\,\text{NADH};\quad \text{PDH: } 2\,\text{NADH};\quad \text{Ciclo citrico: } 2\,\text{GTP} + 6\,\text{NADH} + 2\,\text{FADH}_{2}. \] La successiva fosforilazione ossidativa converte l’energia di NADH e FADH₂ in ATP, portando la resa complessiva a circa 30–32 ATP per molecola di glucosio, a seconda del sistema navetta degli equivalenti riducenti impiegato e dell’efficienza del trasporto mitocondriale.
Un esempio numerico alternativo riguarda un acido grasso saturo a 16 atomi di carbonio: la sua β‑ossidazione e successiva ossidazione nel ciclo citrico generano un numero molto elevato di equivalenti riducenti, che si traduce in una resa in ATP sensibilmente superiore a quella del glucosio, evidenziando perché i lipidi costituiscano una riserva energetica densa e a lungo termine.
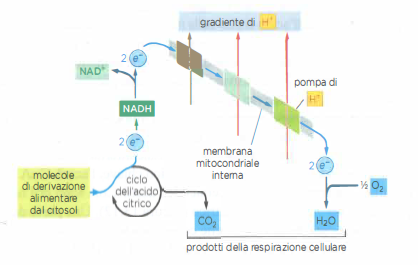
La conversione chemiosmotica dell’energia prende avvio quando i coenzimi ridotti NADH e FADH₂ cedono elettroni ad alto contenuto energetico alla catena di trasporto degli elettroni localizzata nella membrana mitocondriale interna, venendo ossidati rispettivamente a NAD⁺ e FAD (Figura 05.12-05). Gli elettroni transitano rapidamente tra trasportatori con crescenti potenziali di riduzione fino all’ossigeno molecolare (O₂), che agisce come accettore terminale formando acqua (H₂O). L’energia libera rilasciata lungo questo percorso viene utilizzata per spostare protoni (H⁺) dalla matrice verso lo spazio intermembrana, costruendo un gradiente elettrochimico (Figura 05.12-06) che, a sua volta, fornisce la forza motrice per la sintesi di ATP. La sequenza delle trasformazioni è illustrata nella (Figura 05.12-07).
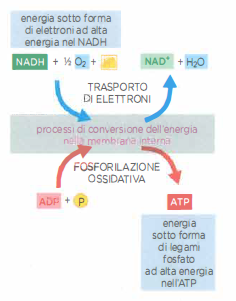
La membrana mitocondriale interna, pertanto, agisce da trasduttore: converte l’energia degli elettroni provenienti da NADH e FADH₂ nell’energia del legame fosfato dell’ATP (Figura 05.12-08). Questo processo, definito fosforilazione ossidativa, comprende simultaneamente l’utilizzo di O₂ e la fosforilazione dell’ADP a ATP. In molte cellule animali si ottengono in media circa 2,5 molecole di ATP per ogni NADH ossidato e circa 1,5 per ogni FADH₂, valori che possono variare in funzione delle condizioni fisiologiche e dell’assetto della catena respiratoria.
Le sorgenti di elettroni ad alta energia differiscono tra organismi e metabolismi: nella respirazione mitocondriale e batterica aerobica derivano in prevalenza dall’ossidazione di carboidrati e acidi grassi; nella fotosintesi sono trasferiti dalla clorofilla eccitata dalla luce; in numerosi archei e batteri chemioautotrofi provengono da substrati inorganici, come H₂, Fe²⁺ o composti ridotti dello zolfo. A prescindere dall’origine degli elettroni, l’impiego di un meccanismo chemiosmotico per generare ATP è ampiamente conservato negli esseri viventi.
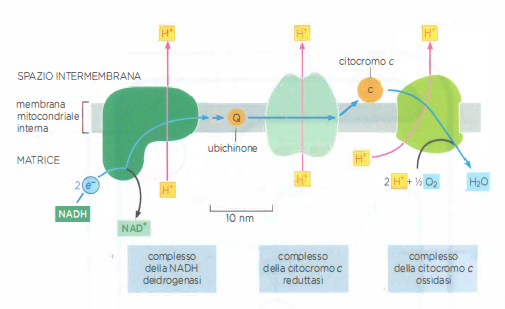
La catena di trasporto degli elettroni (o catena respiratoria), responsabile della fosforilazione ossidativa, è presente in numerose copie nella membrana mitocondriale interna ed è formata da oltre 40 subunità proteiche organizzate in tre grandi complessi proton-pumping, integrati nella membrana, coadiuvati da trasportatori mobili lipidici e proteici (Figura 05.12-09). I tre complessi che pompano protoni, nell’ordine di ricezione degli elettroni, sono:
- Complesso della NADH deidrogenasi (Complesso I), che riceve gli elettroni da NADH e li convoglia all’ubichinone;
- Complesso della citocromo c reduttasi (Complesso III), che trasferisce elettroni dall’ubichinolo al citocromo c mediante il ciclo della Q;
- Complesso della citocromo c ossidasi (Complesso IV), che accetta elettroni dal citocromo c e riduce l’O₂ ad H₂O.
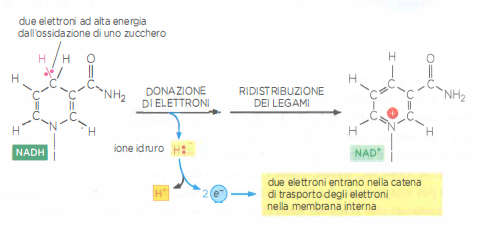
Ogni complesso ospita cofattori redox, tra cui gruppi Fe–S, FMN o FAD, eme dei citocromi e centri rame, che facilitano il passaggio sequenziale degli elettroni. La NADH deidrogenasi estrae dal NADH uno ione idruro, che viene convertito secondo \( \mathrm{H^- \rightarrow H^+ + 2\,e^-} \), e utilizza l’energia di trasferimento per pompare protoni nella direzione matrice → spazio intermembrana. Gli elettroni proseguono poi verso il complesso III e quindi al complesso IV tramite due vettori mobili: l’ubichinone (coenzima Q), un trasportatore liposolubile diffondente nel doppio strato, e il citocromo c, una piccola proteina periferica dello spazio intermembrana (Figura 05.12-09).
Oltre all’ingresso degli elettroni tramite NADH, esiste un secondo punto di accesso attraverso la succinato deidrogenasi (Complesso II), che ossida FADH₂ prodotto, ad esempio, nel ciclo dell’acido citrico. Il Complesso II trasferisce elettroni al coenzima Q ma, a differenza dei tre complessi principali, non pompa protoni; di conseguenza, gli elettroni provenienti da FADH₂ generano un gradiente protonico leggermente inferiore rispetto a quelli provenienti da NADH.
Il flusso elettronico lungo la catena è termodinamicamente favorito: gli elettroni passano da trasportatori con minore affinità verso accettori con maggiore affinità, fino alla riduzione dell’ossigeno. Il consumo di O₂ ha luogo quasi esclusivamente al livello del complesso IV, che catalizza la reazione terminale e impiega, oltre agli elettroni, protoni della matrice per la formazione di H₂O. Questo stadio costituisce la fase della respirazione cellulare dipendente dall’ossigeno e rappresenta la principale destinazione dell’O₂ inspirato.
Sebbene la stechiometria possa variare con le condizioni, per ogni coppia di elettroni trasferita a O₂ il pompaggio tipico è di circa 4 H⁺ al Complesso I, 4 H⁺ al Complesso III e 2 H⁺ al Complesso IV; ulteriori protoni della matrice sono consumati “chimicamente” per la formazione di acqua. L’insieme di questi processi costruisce la forza motrice protonica necessaria all’ATP sintasi.
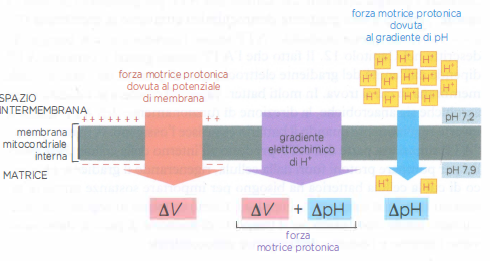
In assenza di un meccanismo di cattura, l’energia libera liberata dal trasferimento complessivo di elettroni da NADH a O₂ verrebbe dissipata come calore. I complessi respiratori sfruttano invece tale energia per espellere attivamente H⁺ nella direzione della membrana esterna (Figura 05.12-09), determinando due componenti del gradiente elettrochimico:
- un gradiente di concentrazione di protoni, ovvero un gradiente di pH, per cui la matrice risulta più alcalina dello spazio intermembrana;
- un gradiente di potenziale elettrico attraverso la membrana (potenziale di membrana), con la matrice caricata negativamente e il lato citosolico positivamente.
Valori tipici suggeriscono una differenza di pH nell’ordine di 0,5–1,0 unità; ad esempio, una matrice con pH circa 7,9 e uno spazio intermembrana vicino a pH 7,2, simile al citosol. Il potenziale di membrana contribuisce in modo rilevante alla forza totale, spesso nell’intervallo di 150–180 mV, rendendo energeticamente favorito il rientro dei protoni nella matrice attraverso vie specifiche.
La forza motrice protonica può essere descritta da: \[ \Delta p \;=\; \Delta \psi \;-\; \frac{2{,}303\,RT}{F}\,\Delta \mathrm{pH}, \] dove \( \Delta \psi \) è la differenza di potenziale attraverso la membrana, \( R \) la costante dei gas, \( T \) la temperatura assoluta e \( F \) la costante di Faraday. A 37 °C, una unità di pH corrisponde a circa 60 mV. Poiché i protoni portano carica positiva, il loro movimento passivo è favorito sia da un eccesso di carica negativa nella matrice sia da una minore concentrazione di H⁺ in tale compartimento. Le due componenti cooperano dunque per costruire un ripido gradiente elettrochimico che immagazzina energia (Figura 05.12-10) e guida processi dipendenti dai protoni, in primis la sintesi di ATP a opera dell’ATP sintasi.
Il mantenimento del gradiente richiede l’integrità della membrana interna, altamente impermeabile agli ioni. Eventuali vie di corto circuito per H⁺, naturali (proteine disaccoppianti) o indotte da agenti ionofori, dissipano \( \Delta p \) sotto forma di calore, riducendo la resa di ATP e mettendo in evidenza il ruolo centrale della forza motrice protonica nell’efficienza bioenergetica della cellula.
Se i protoni accumulati nello spazio intermembrana rientrassero liberamente nella matrice, l’energia del gradiente elettrochimico verrebbe dissipata come calore. In alcuni tessuti, tale dissipazione è intenzionale: nelle specie con adiposo bruno, una proteina disaccoppiante (UCP1) consente il riflusso dei protoni producendo termogenesi, fenomeno utile per l’ibernazione e la termoregolazione. Nella gran parte delle cellule, tuttavia, il gradiente di protoni attraverso la membrana mitocondriale interna viene sfruttato per la fosforilazione dell’ADP a ATP.
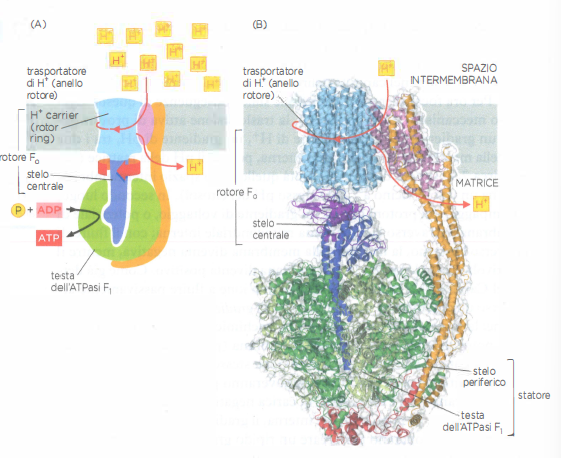
L’enzima responsabile, l’ATP sintasi, è un complesso multiproteico conservato lungo l’evoluzione e presente in mitocondri, cloroplasti e batteri. La porzione catalitica F1, simile a una “testa” che sporge nella matrice, è collegata tramite uno stelo centrale al motore di membrana Fo, un traslocatore di H⁺ che attraversa il doppio strato lipidico (Figura 05.12-11). Il passaggio dei protoni attraverso Fo induce la rotazione del suo anello c e dello stelo γ, i quali a loro volta determinano cambiamenti conformazionali ciclici nelle subunità β della testa F1. Secondo il meccanismo del “cambio conformazionale” proposto da P. Boyer, tali variazioni guidano in sequenza il legame dell’ADP e del Pᵢ, la sintesi dell’ATP e il rilascio del prodotto. In condizioni fisiologiche, la macchina catalitica compie cicli estremamente rapidi, con frequenze di turnover dell’ordine di decine–centinaia al secondo; una rotazione completa del rotore corrisponde tipicamente alla formazione di tre molecole di ATP.
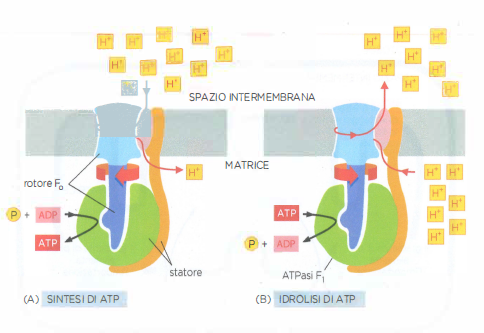
La resa protoni/ATP dipende dal numero di subunità dell’anello c: nei mammiferi, valori prossimi a otto subunità implicano circa 8 protoni per giro e quindi ~2,7 H⁺ per ATP per la sola catalisi; il fabbisogno effettivo per ATP netto risulta maggiore quando si considerano i costi di trasporto di ADP, ATP e Pᵢ. La conversione energia meccanica → energia chimica operata dall’ATP sintasi è reversibile: se il gradiente protonico si riduce, il complesso può idrolizzare ATP e funzionare come pompa H⁺ che ricostituisce il gradiente (Figura 05.12-12). In molti batteri facoltativi, quando l’ossigeno scarseggia e la catena di trasporto elettronico rallenta, l’enzima inverte regolarmente la direzione: l’ATP derivato dalla glicolisi alimenta l’estrusione di protoni per mantenere il potenziale di membrana necessario al trasporto accoppiato di nutrienti. Meccanismi analoghi di accoppiamento energetico governano l’ingresso e l’uscita di piccoli soluti anche attraverso le membrane mitocondriali, come discusso in seguito.
Il gradiente elettrochimico dei protoni, o forza proton-motrice, non alimenta solo la sintesi di ATP. Esso sostiene una varietà di trasporti accoppiati che spostano selettivamente metaboliti e ioni attraverso la membrana mitocondriale interna. La forza proton-motrice si esprime come Δp, somma delle componenti elettrica e chimica: \[ \Delta p = \Delta \psi - \frac{2{,}303\,RT}{F}\,\Delta \mathrm{pH}, \] dove Δψ è il potenziale di membrana e ΔpH il gradiente di pH. Il lato matriciale è più negativo e più alcalino rispetto allo spazio intermembrana (Figura 05.12-10).
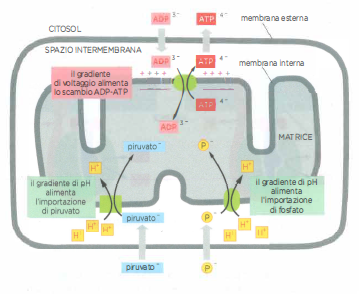
Diversi trasportatori sfruttano direttamente una o entrambe le componenti di Δp. Alcuni esempi rilevanti includono:
- Simtrasporto H⁺/piruvato e H⁺/fosfato inorganico (Pᵢ), che utilizza lo scorrimento favorevole dei protoni per importare nella matrice le molecole necessarie alla produzione di acetil-CoA e all’ossidazione fosforilativa;
- Translocasi degli adeninnucleotidi (antiporto ADP/ATP), elettrogenica: l’uscita di ATP⁴⁻ in cambio di ADP³⁻ sfrutta Δψ, promuovendo un rapido rifornimento citosolico di ATP e l’ingresso di ADP per la ricarica (Figura 05.12-13);
- Traslocazione di proteine precursori: l’importo post-traduzionale attraverso il complesso TIM richiede il potenziale di membrana per guidare la sequenza preposta (presequence) e l’idrolisi di ATP da parte di chaperoni matriciali per completare il tiraggio del polipeptide.
In ambito batterico, lo stesso gradiente sulla membrana plasmatica alimenta la sintesi di ATP e il trasporto di soluti; inoltre, costituisce una fonte di energia meccanica direttamente utilizzabile, come dimostra la rotazione rapida del flagello batterico azionata dal flusso protonico.
L’antiporto ADP/ATP descritto nella (Figura 05.12-13) assicura un ciclo continuo: l’ADP generato dall’idrolisi dell’ATP nel citosol entra prontamente nella matrice per essere riconvertito, mentre l’ATP neoformato viene esportato verso i distretti dove è richiesto. I mitocondri consumano una frazione dell’ATP che producono per le proprie esigenze (replicazione del DNA mitocondriale, sintesi proteica, mantenimento ionico), ma la maggior parte alimenta processi citosolici. In condizioni fisiologiche, ciascuna molecola di ATP può essere riutilizzata molte volte in tempi brevi, riflettendo un turnover cellula-specifico estremamente elevato.
Perché le reazioni biosintetiche e di trasduzione energetica procedano, il rapporto [ATP]/[ADP] nel citosol è mantenuto alto, tipicamente di un ordine di grandezza. Oltre alla fosforilazione ossidativa, sistemi tampone come la creatina chinasi e l’adenilato chinasi contribuiscono alla gestione locale dell’energia, trasferendo equivalenti fosforici tra compartimenti e modulando la “charge” adenilica. Un arresto della funzione mitocondriale farebbe collassare il potenziale di membrana e ridurrebbe rapidamente i livelli di ATP: inibitori della catena respiratoria, come il cianuro che blocca la citocromo c ossidasi, conducono così a un’immediata crisi energetica incompatibile con la sopravvivenza cellulare.
La progressiva ossidazione dei nutrienti non è una complicazione superflua, ma una strategia per catturare in modo controllato l’energia libera. La scomposizione del flusso di elettroni in molte tappe consente di immagazzinare frazioni di energia in trasportatori ridotti come NADH e FADH₂, che successivamente alimentano la catena di trasporto degli elettroni. Gli elettroni del NADH, generati nella matrice dal ciclo dell’acido citrico, entrano al complesso I (NADH deidrogenasi), innescando il pompaggio di protoni a ogni passaggio tra complessi. Il bilancio medio corrisponde a circa 2,5 ATP per NADH. Gli elettroni del FADH₂, prodotti tra l’altro dalla succinato deidrogenasi, by-passano il complesso I e sono trasferiti all’ubichinone (Figura 05.12-09); entrando più “a valle”, promuovono il pompaggio di meno protoni e rendono circa 1,5 ATP per FADH₂. La resa complessiva dell’ossidazione completa del glucosio è riassunta nella (Tabella 05.12-01) e dipende, tra l’altro, dal percorso con cui gli equivalenti riducenti citosolici raggiungono la catena respiratoria (navette malato-aspartato o glicerolo-3-fosfato) e dalla stechiometria della c-ring della Fo-ATP sintasi, nonché da eventuali perdite protoniche.
Nonostante la complessità, la respirazione cellulare raggiunge un’efficienza notevole: all’incirca il 50% dell’energia teoricamente liberabile dalla combustione di carboidrati e lipidi viene immagazzinata nei legami fosfato dell’ATP, mentre il resto si disperde come calore. Questa prestazione supera ampiamente quella di molte macchine non biologiche per la conversione dell’energia, come motori elettrici e a combustione interna, spesso limitati al 10–20% di efficienza. Un’efficienza più bassa richiederebbe un apporto alimentare sproporzionato e impegni termoregolatori gravosi; la straordinaria efficacia della fosforilazione ossidativa ha quindi rappresentato una leva evolutiva cruciale per lo sviluppo di organismi complessi.
| Processo | Prodotti diretti | Resa finale in ATP per molecola di glucosio |
|---|---|---|
| Glicolisi | 2 ATP, 2 NADH (citoplasma) | ~5 |
| Ossidazione del piruvato ad acetil-CoA (per 2 molecole di piruvato) | 2 NADH (matrice mitocondriale) | 5 |
| Ossidazione completa dell’acetil-CoA nel ciclo di Krebs (per 2 molecole di acetil-CoA) | 6 NADH, 2 FADH₂, 2 GTP (matrice mitocondriale) | 20 |
| Totale | — | ~30 |
Bilancio energetico dell’ossidazione del glucosio
L’ossidazione completa di una molecola di glucosio attraverso glicolisi, conversione del piruvato e ciclo di Krebs, seguita dalla fosforilazione ossidativa, porta a una resa energetica di circa 30 ATP. Questa produzione varia leggermente in base all’efficienza dei sistemi di trasporto degli equivalenti riducenti dal citoplasma ai mitocondri, ma rappresenta la principale fonte di energia per le cellule eucariotiche.