Gli scienziati nello studio della natura fanno osservazioni e formulano e verificano ipotesi
Definizione
La comprensione dell’organizzazione e del funzionamento delle cellule dipende in modo cruciale dalle tecnologie di osservazione. La biologia cellulare nacque ben prima dell’era delle sonde fluorescenti, dei rilevatori digitali e dell’elaborazione numerica delle immagini: agli inizi, i ricercatori potevano solo esaminare campioni di tessuto con semplici lenti, sezionandoli in strati sottili nel tentativo di intuire come fossero strutturati all’interno. L’immagine che ne emergeva era sconcertante: minuscole entità appena distinguibili, la cui relazione con le proprietà della materia vivente non era affatto evidente. Eppure fu proprio l’osservazione diretta a gettare le fondamenta della biologia cellulare e continua ancora oggi a esserne una colonna portante. Le cellule divennero accessibili soltanto nel XVII secolo, con l’invenzione del microscopio. Per oltre due secoli, il perfezionamento degli strumenti ottici ha guidato una lunga sequenza di scoperte, pur entro i limiti imposti dalla fisica della luce. La svolta successiva, negli anni 1930, fu l’introduzione della microscopia elettronica, che impiega fasci di elettroni al posto della luce visibile e amplia grandemente la risoluzione, fino a distinguere dettagli nanometrici e, in alcuni casi, singole macromolecole. In quanto segue, verranno sintetizzate le principali tipologie di microscopi ottici ed elettronici, che, insieme ad altre forme di microscopia avanzata, restano strumenti fondamentali nei laboratori di biologia cellulare per rivelare aspetti inattesi della costruzione e della dinamica delle cellule.
Nel Seicento, il miglioramento delle lenti consentì di superare i limiti dell’occhio nudo. Nel 1665, Robert Hooke osservò con un microscopio un sottile frammento di sughero e descrisse alla Royal Society di Londra una trama di piccole cavità, che battezzò “cellule”, evocando le austere stanzette dei monasteri. Quelle strutture erano in realtà pareti cellulari di cellule vegetali morte. Poco dopo, Hooke e il suo contemporaneo olandese Antoni van Leeuwenhoek documentarono l’esistenza di cellule viventi e di un pullulare di microrganismi in movimento, fino ad allora ignoto.
Per gran parte dei due secoli successivi, i microscopi rimasero strumenti relativamente rari, appannaggio di laboratori e collezionisti facoltosi. Nell’Ottocento, la loro adozione divenne più ampia e sistematica, favorendo lo sviluppo della biologia cellulare come disciplina autonoma. Due lavori sono tradizionalmente indicati come fondativi: il botanico Matthias Schleiden (1838) e lo zoologo Theodor Schwann (1839) mostrarono, su base comparativa, che i tessuti animali e vegetali sono assemblati a partire da unità elementari, le cellule. L’insieme di queste osservazioni confluisce nella cosiddetta teoria cellulare, poi estesa all’idea che le cellule provengono esclusivamente dalla crescita e dalla divisione di cellule preesistenti (Figura 01.03-01). Questa conclusione, che esclude la generazione spontanea, incontrò inizialmente resistenze ma fu consolidata, intorno al 1860, dagli esperimenti di Louis Pasteur.
L’asserzione “ogni cellula da una cellula” implica che i processi biologici contemporanei siano l’esito di una storia continua di discendenze cellulari. Comprendere il comportamento delle cellule odierne richiede, quindi, di ricostruirne l’origine e l’evoluzione. La teoria dell’evoluzione di Charles Darwin (1859) fornisce la cornice concettuale: variazione casuale e selezione naturale, applicate a progenitori comuni, hanno generato la diversità degli organismi. Integrata con la teoria cellulare, questa prospettiva collega la biologia attuale a una filogenesi di cellule che si estende dalle prime forme di vita fino al presente e illumina molte delle domande affrontate in questo volume.
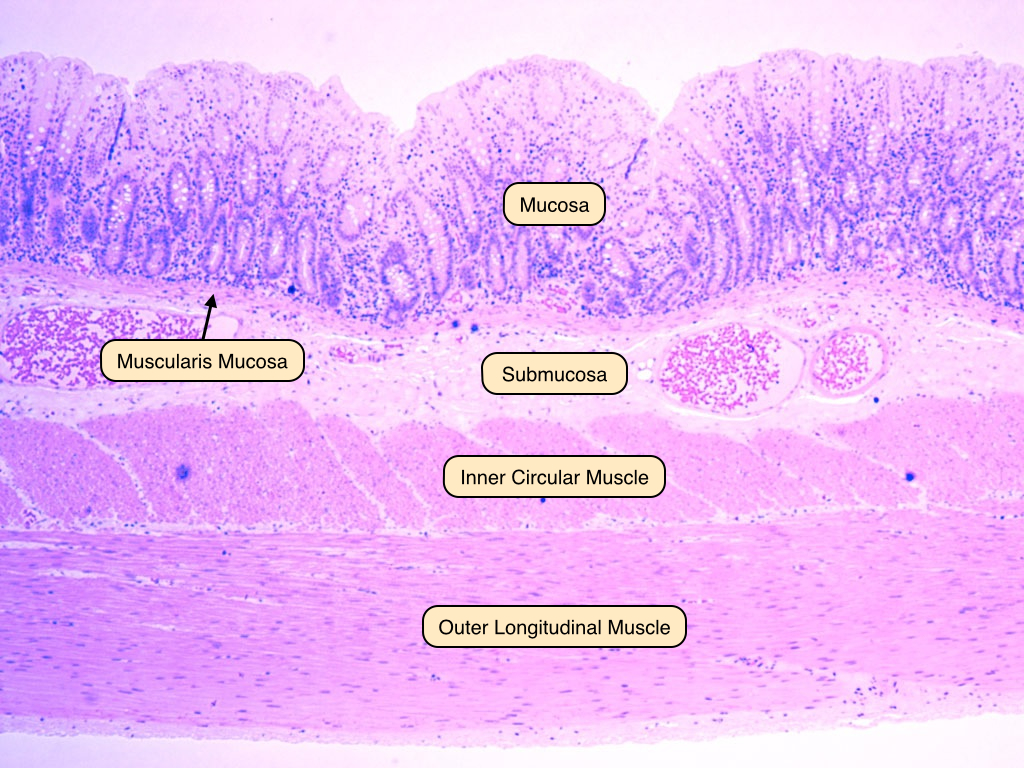
Una sezione sottile di tessuto vegetale o animale mostra, al microscopio ottico, che la materia vivente è organizzata in un mosaico di cellule. In certi tessuti, esse risultano fitte e contigue; in altri, sono immerse in una matrice extracellulare ricca di fibre proteiche e polisaccaridi. Le dimensioni lineari delle cellule eucariotiche sono spesso dell’ordine di decine di micrometri, con valori frequenti intorno a 10–30 µm. In condizioni adeguate, campioni vitali consentono di cogliere spostamenti intracellulari e, con sufficiente pazienza, mutamenti di forma e divisioni cellulari (Figura 01.03-01).
Rilevare i dettagli interni è tuttavia impegnativo: molti componenti sono quasi trasparenti e hanno indici di rifrazione simili. Per aumentare il contrasto si possono utilizzare colorazioni specifiche dei diversi costituenti cellulari (Figura 01.03-02) oppure tecniche che sfruttano le minute differenze di indice di rifrazione fra organelli e citosol, convertendole in variazioni d’intensità. Questi approcci ottici, combinati con l’elaborazione digitale dell’immagine, migliorano notevolmente la leggibilità delle strutture (Figura 01.03-03). In immagini di buona qualità, le cellule animali rivelano una fitta architettura: un bordo netto corrispondente alla membrana plasmatica, un nucleo prominente immerso nel citoplasma e una costellazione di organelli.
La risoluzione di un microscopio ottico convenzionale è limitata dalle proprietà ondulatorie della luce. In termini approssimati, la separazione minima distinguibile fra due punti è descritta da \( d \approx \frac{\lambda}{2\,\mathrm{NA}} \), il che pone, per luce visibile e obiettivi ad alta apertura numerica, un limite attorno a 0,2 µm. Strutture più piccole risultano non risolte e appaiono come un’unica entità sfocata. Per superare almeno in parte questo vincolo, la microscopia a fluorescenza impiega fluorocromi e sorgenti di eccitazione selettive, esaltando specifici bersagli molecolari (Figura 01.03-03). Tecniche contemporanee quali confocale, deconvoluzione e le metodiche a super-risoluzione (ad esempio STED, PALM/STORM) riducono la soglia di risoluzione a poche decine di nanometri; alcuni strumenti raggiungono circa 20 nm, comparabili alla dimensione di un ribosoma, complesso macromolecolare deputato alla sintesi proteica. Pur non equiparando la microscopia elettronica, queste soluzioni ottiche offrono il vantaggio dell’imaging in cellule vive e della marcatura selettiva di molecole specifiche:
- microscopia in campo chiaro: evidenzia tessuti e cellule mediante contrasto intrinseco o colorazioni;
- contrasto di fase e interferenza differenziale: trasformano differenze di indice di rifrazione in variazioni di intensità e rilievo apparente;
- fluorescenza (ampio campo, confocale, a super-risoluzione): consente localizzazione e dinamica di bersagli specifici con sensibilità elevata.
Quando occorrono ingrandimenti elevati e risoluzioni nell’ambito dei nanometri, si ricorre alla microscopia elettronica. La preparazione dei campioni è più laboriosa rispetto all’ottica: i tessuti vengono in genere fissati chimicamente, inclusi in resine, tagliati in ultrasezioni (spessore tipico di 50–100 nm) e contrastati con sali di metalli pesanti. Queste procedure, analoghe per certi versi a quelle adottate per la microscopia ottica (Figura 01.03-02), non consentono però l’osservazione di cellule vive.
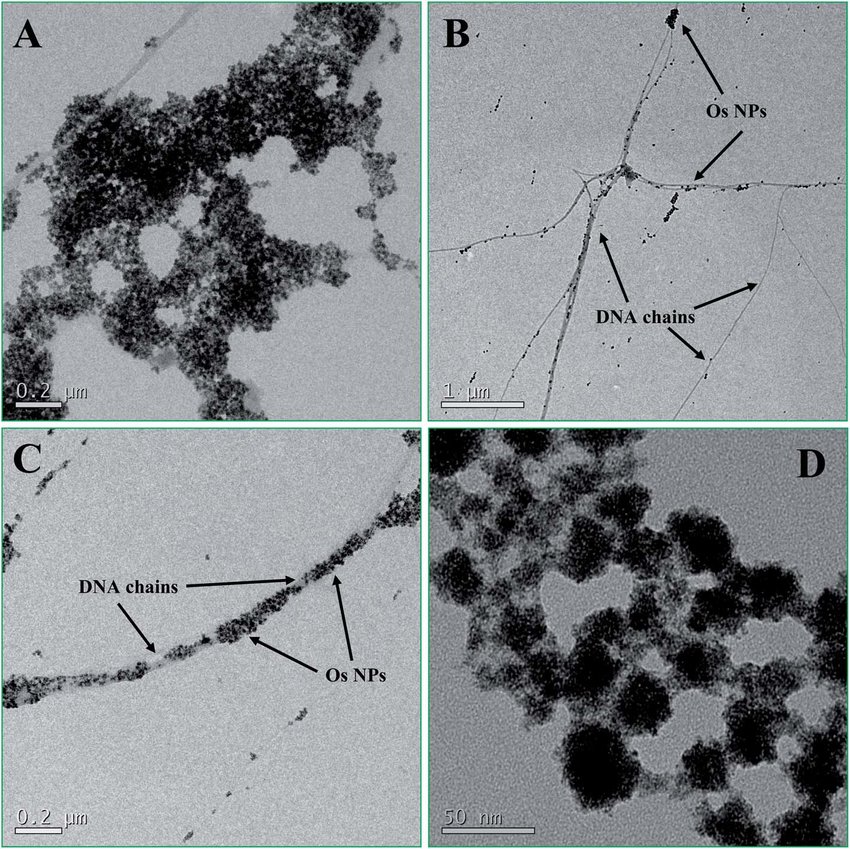
Le sezioni osservate al microscopio elettronico a trasmissione rivelano che ciò che al microscopio ottico appare come un insieme confuso di particelle corrisponde in realtà a organelli distinti, dotati di morfologie e funzioni specifiche. La membrana plasmatica, spessa circa 5 nm, delimita il citoplasma; membrane interne di simile spessore delimitano molti organelli (Figura 01.03-04) e (Figura 01.03-04). Tali membrane sono costituite da un doppio strato lipidico, cioè da due foglietti molecolari contrapposti. Con un’elevata qualità di preparazione, è possibile visualizzare anche macromolecole isolate o complessi su scala nanometrica (Figura 01.03-04).
La microscopia elettronica si presenta in due configurazioni principali, complementari:
- microscopio elettronico a trasmissione (TEM): un fascio di elettroni attraversa il campione, generando immagini dell’interno delle cellule e dei loro organelli;
- microscopio elettronico a scansione (SEM): registra elettroni emessi dalla superficie del campione, fornendo una resa tridimensionale dei rilievi superficiali di cellule e materiali.
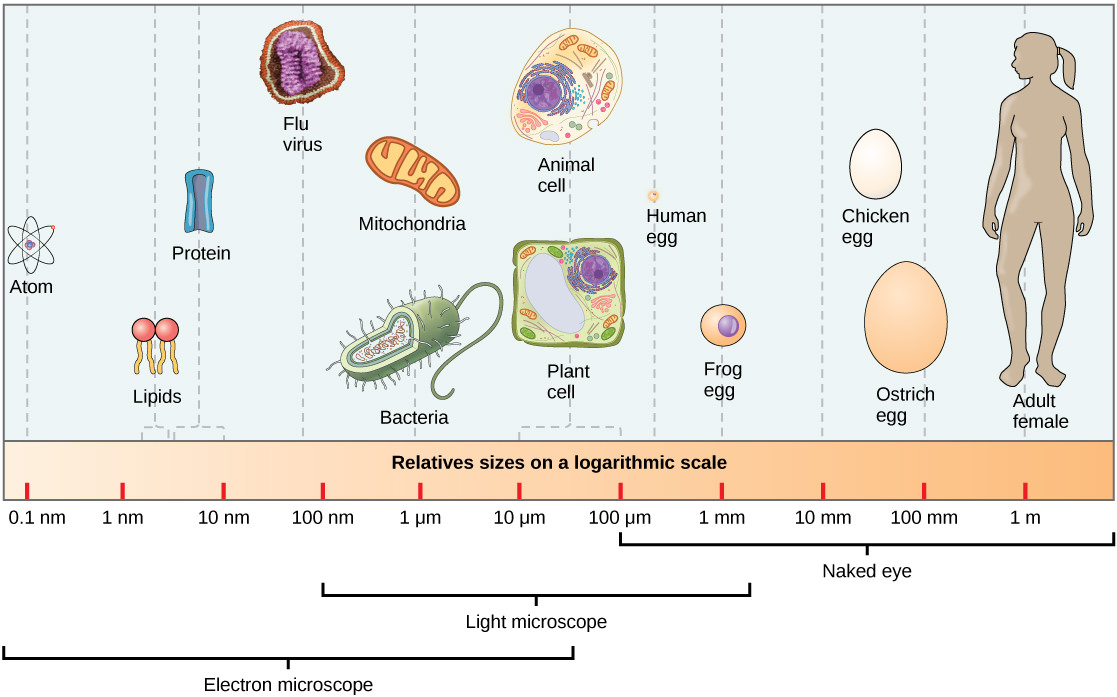
Anche i più potenti microscopi elettronici non risolvono i singoli atomi nelle molecole biologiche in condizioni fisiologiche (Figura 01.03-05). Per portare l’analisi al livello atomico, i biologi strutturali impiegano tecniche dedicate, come la cristallografia a raggi X e la criomicroscopia elettronica in singola particella, che permettono di ricostruire con precisione la struttura tridimensionale di proteine e complessi macromolecolari.
In sintesi, microscopia ottica e elettronica sono strumenti complementari: la prima consente l’osservazione di cellule vive e la marcatura specifica di componenti con risoluzione sub-micrometrica, spinta dalle metodiche a super-risoluzione; la seconda fornisce l’accesso all’ultrastruttura con dettaglio nanometrico, a scapito della vitalità del campione. L’integrazione delle informazioni derivanti da entrambe, insieme alle tecniche di biologia strutturale, continua ad ampliare il nostro sguardo sull’architettura e sulla dinamica della cellula, rivelando connessioni tra forma, organizzazione molecolare e funzione.