Gli organismi clonati e le cellule staminali sono utili per la ricerca e per altre applicazioni
Definizione
La proliferazione cellulare dipende dall’azione coordinata di due grandi insiemi di apparati: da un lato i sistemi biosintetici che accrescono massa e duplicano i componenti, dall’altro i meccanismi meccanico-strutturali che organizzano e ripartiscono cromosomi e organelli nella divisione. Il controllo del ciclo cellulare sincronizza questi apparati attraverso una sequenza ordinata di “interruttori” biochimici in grado di attivare o disattivare intere vie molecolari. Tali interruttori orchestrano gli eventi chiave, tra cui la replicazione del DNA, la condensazione e segregazione dei cromosomi e la citochinesi, in modo che ciascun passaggio avvenga solo quando il precedente è stato completato.
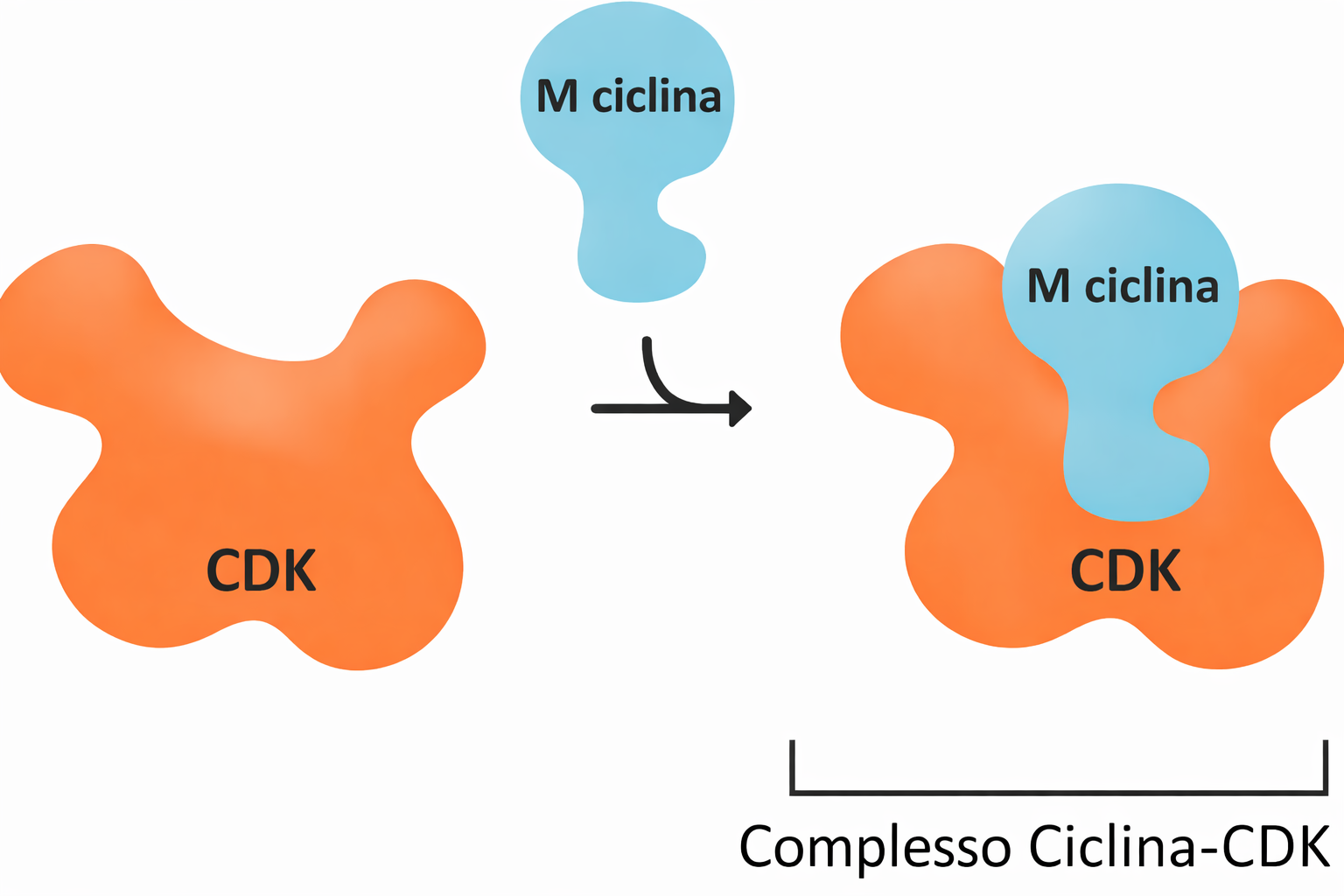
Il sistema di controllo regola la progressione del ciclo attivando e spegnendo ciclicamente proteine e complessi che promuovono l’ingresso in fase S, l’entrata in mitosi e la citochinesi. Il principio operativo è la modulazione dello stato fosforilativo: chinasi e fosfatasi modificano proteine bersaglio determinandone lo stato funzionale. Un gruppo specializzato di chinasi, onnipresente nelle cellule in proliferazione ma attivo solo in finestre temporali definite, costituisce il cuore del sistema. Queste chinasi richiedono l’associazione con subunità regolatorie denominate cicline per acquisire attività catalitica; perciò sono dette proteine chinasi dipendenti da cicline, o Cdk (Cyclin-dependent kinases) (Figura 07.03-01). A differenza delle Cdk, le cicline oscillano di concentrazione durante il ciclo cellulare. L’assemblaggio temporizzato dei complessi ciclina–Cdk e la loro attivazione impulsiva generano onde di fosforilazione che innescano le transizioni principali, come l’ingresso in fase S o in fase M. La rapida disattivazione successiva ristabilisce l’ordine e impedisce regressioni improprie.
Ciclina e Cdk esistono in più varianti che si combinano per attivare stadi distinti del ciclo. La ciclina M, associandosi con la sua Cdk specifica, forma M-Cdk, il complesso che guida la cellula dall’ultima parte della G₂ alla fase M. Le cicline S e G₁/S, legando Cdk appropriate, formano S-Cdk e G₁/S-Cdk, promuovendo rispettivamente l’avvio della replicazione e il superamento delle ultime soglie in G₁. In momenti più precoci, le cicline G₁ si associano a Cdk che sostengono la progressione in G₁ costituendo complessi G₁-Cdk, spesso indotti da segnali mitogenici extracellulari nelle cellule animali. Le corrispondenze tra cicline e Cdk sono riassunte nella (Tabella 07.03-01). Ogni complesso ciclina–Cdk attivo fosforila un repertorio specifico di substrati, provocando effetti funzionali distinti:
- G₁-Cdk fosforila regolatori della trascrizione che sbloccano programmi genici per la biosintesi di nucleotidi e la preparazione alla duplicazione del DNA;
- G₁/S-Cdk e S-Cdk avviano e stabilizzano la replicazione agendo su proteine di “licensing” dei replicatori, prevenendo riavvii multipli nello stesso ciclo;
- M-Cdk promuove condensazione cromosomica e riorganizzazione della cellula per la mitosi, includendo fosforilazioni su componenti del fuso e su proteine del rivestimento nucleare.
L’attivazione di gruppi differenti di bersagli rende ogni complesso responsabile di una transizione specifica e irreversibile.
Complessi ciclina-Cdk nei vertebrati
| Complesso ciclina-Cdk | Ciclina coinvolta | Cdk corrispondente |
|---|---|---|
| G1-Cdk | Ciclina D (D1, D2, D3 nei mammiferi) | Cdk4, Cdk6 |
| G1/S-Cdk | Ciclina E | Cdk2 |
| S-Cdk | Ciclina A | Cdk2 |
| M-Cdk | Ciclina B | Cdk1 |
| Tabella che descrive come il controllo del ciclo cellulare negli eucarioti superiori sia affidato a specifici complessi costituiti da cicline e chinasi ciclina-dipendenti (Cdk); ciascuna fase del ciclo è regolata da una diversa associazione ciclina-Cdk, che assicura la corretta progressione dalla crescita cellulare alla replicazione del DNA fino alla mitosi. | ||
L’abbondanza di ciascuna ciclina è determinata dall’equilibrio tra produzione e degradazione. In prima approssimazione, la dinamica può essere descritta come \( \frac{d[\text{ciclina}]}{dt} = v_{\text{sintesi}} - v_{\text{degradazione}} \), con un incremento graduale legato a programmi trascrizionali specifici, seguito da cadute rapide per proteolisi mirata. La distruzione sincrona delle cicline M e S a metà della fase M dipende da un complesso ubiquitina–ligasi di classe E3, l’APC/C (Anaphase Promoting Complex/Cyclosome), che poliubiquitina queste cicline indirizzandole al proteasoma (Figura 07.03-02). La rimozione della ciclina fa regredire la Cdk allo stato inattivo, favorendo la transizione all’uscita dalla mitosi. Accanto ad APC/C, altre E3 (per esempio il complesso SCF) contribuiscono in fasi precedenti alla rimozione di inibitori o di cicline di G₁, affinando la tempistica della progressione.
Sebbene l’accumulo delle cicline sia graduale, l’attività dei complessi ciclina–Cdk spesso si accende in modo brusco. Ciò dipende da circuiti di fosforilazione/defosforilazione che fungono da interruttori bistabili. Le Cdk sono soggette a:
- fosforilazione attivante nel “T-loop” da parte di chinasi attivanti Cdk (CAK);
- fosforilazioni inibitrici su residui specifici a opera di chinasi come Wee1;
- defosforilazione di tali siti inibitori da parte di fosfatasi, quali Cdc25, che sbloccano l’attività Cdk (Figura 07.03-03).
Circuiti di feedback positivo (per esempio M-Cdk che potenzia Cdc25 e inibisce Wee1) generano risposte ultrasensibili e temporizzano l’ingresso in mitosi come evento collettivo e coordinato.
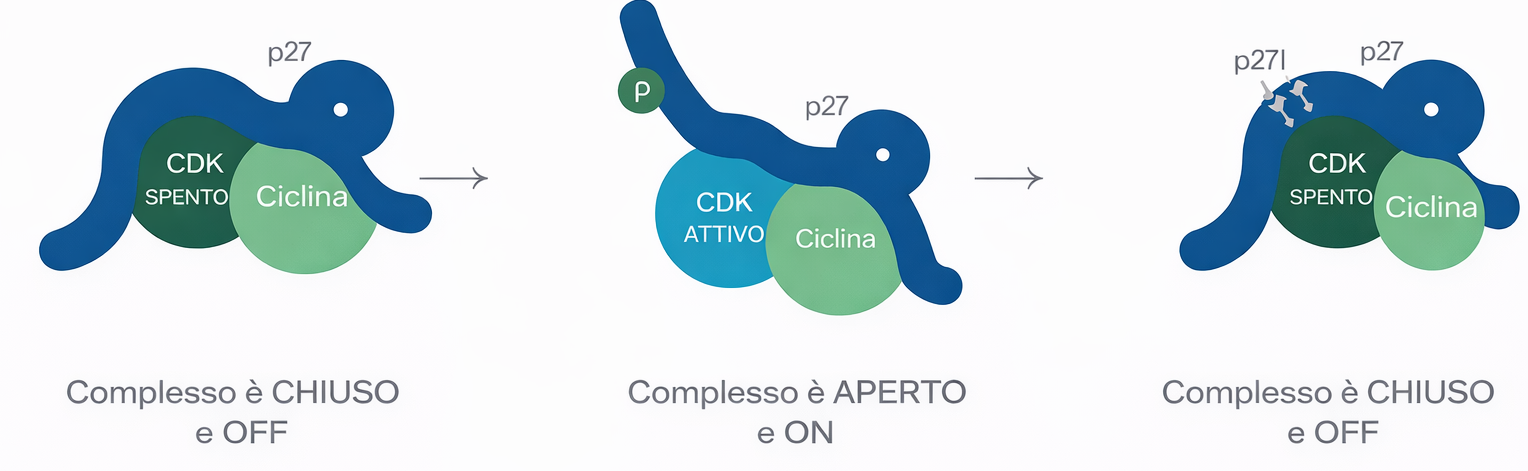
Oltre allo stato fosforilativo, l’attività delle Cdk è modulata da proteine che le inibiscono (CKI). Questi inibitori possono impedire la formazione del complesso o bloccarne il sito catalitico, risultando particolarmente efficaci nella fase G₁, dove dilatano la finestra temporale prima della duplicazione del DNA (Figura 07.03-04). Nelle cellule animali, famiglie di CKI come CIP/KIP (per esempio p21 e p27) e INK4 (per esempio p16) integrano segnali di danno al DNA o condizioni extracellulari sfavorevoli, consentendo arresti reversibili e proteggendo l’integrità del genoma.
Il sistema di controllo interviene in punti-chiave per garantire che gli eventi avvengano in ordine corretto e in presenza di condizioni interne ed esterne adeguate. Alcuni esempi:
- transizione G₁–S: l’ingresso in fase S è impedito quando nutrienti e segnali mitogenici sono insufficienti o in presenza di danno al DNA; l’azione degli inibitori delle Cdk consolida il blocco (Figura 07.03-04);
- transizione G₂–M: l’attivazione di M-Cdk è soppressa inibendo la fosfatasi necessaria alla rimozione delle fosforilazioni inibitrici, prevenendo l’ingresso prematuro in mitosi (Figura 07.03-03);
- fase M: l’assetto del fuso e l’allineamento dei cromosomi sono monitorati da segnali che mantengono l’APC/C inattivo finché i cinetocori non sono tutti correttamente attaccati, ritardando così la degradazione della ciclina M e la progressione verso l’anafase (Figura 07.03-02).
Questi blocchi, consentono decisioni integrate sulla prosecuzione o sul rinvio della divisione. Il risultato è un avanzamento ordinato, robusto e adattabile alle condizioni cellulari ed extracellulari.