Genomica e proteomica hanno trasformato la ricerca in campo biologico e le sue applicazioni
Definizione
In ogni ciclo proliferativo, le cellule duplicano l’intero patrimonio genetico con una precisione e una rapidità straordinarie. La replicazione del DNA procede a velocità che possono raggiungere circa 1000 nucleotidi al secondo, pur mantenendo un tasso di errore estremamente basso. Questo risultato è reso possibile da complessi proteici altamente coordinati, che orchestrano l’apertura della doppia elica e la sintesi fedele dei nuovi filamenti.
La doppia elica di DNA è composta da due filamenti antiparalleli, ciascuno con una sequenza nucleotidica complementare a quella dell’altro. Di conseguenza, ogni filamento può fungere da matrice per la sintesi del proprio complementare. Se si indicano i due filamenti parentali come S e S′, il filamento S guida la formazione del nuovo S′ e viceversa, come illustrato nella (Figura 03.02-01). La separazione temporanea dei due filamenti consente l’appaiamento specifico delle basi azotate, permettendo l’inserimento del nucleotide corretto di fronte a ciascuna base della matrice.
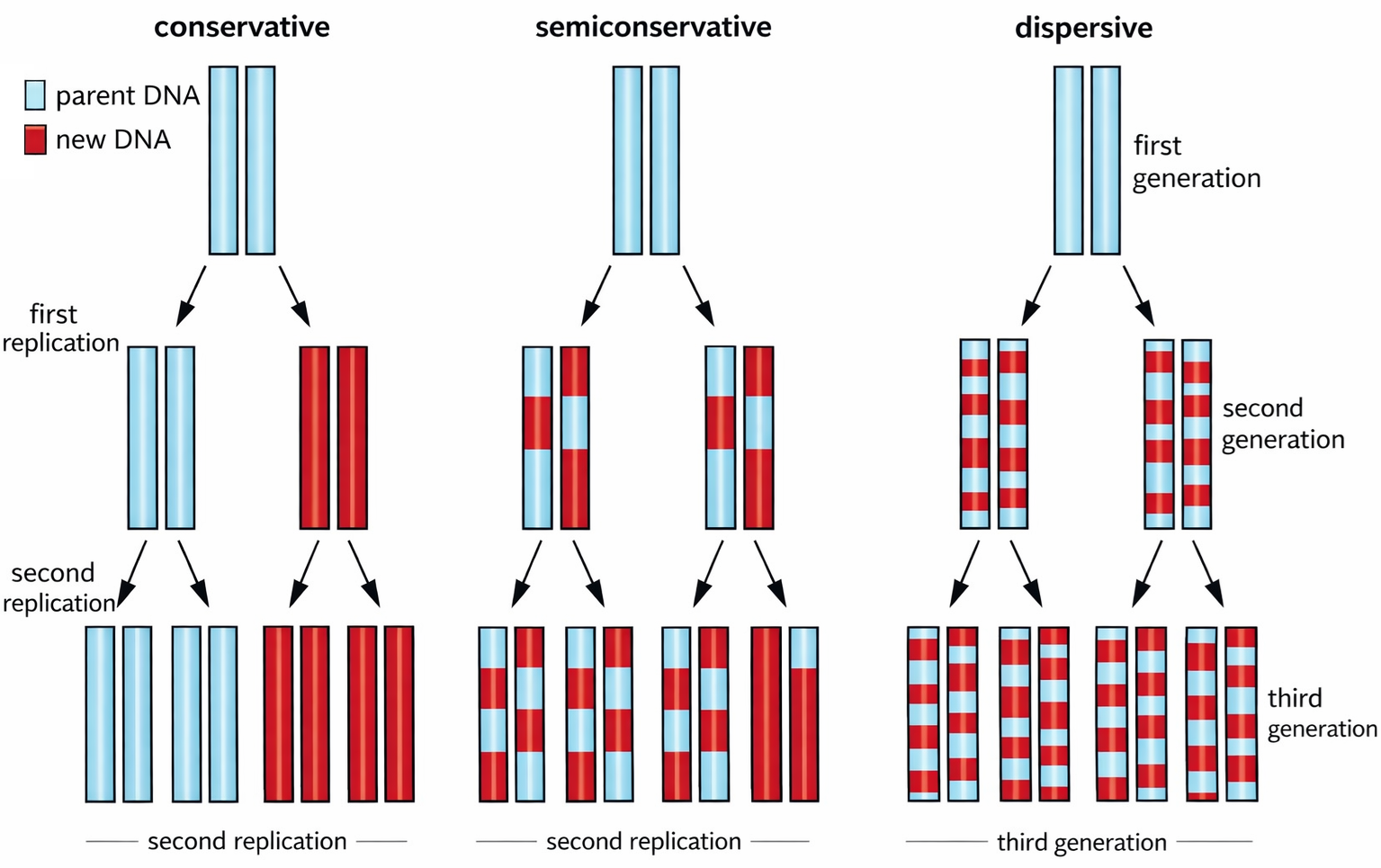
Questo principio garantisce una copia affidabile dell’informazione genetica: dalla molecola iniziale si ottengono due doppie eliche, la cui sequenza è sostanzialmente identica a quella della doppia elica parentale (Figura 03.02-01). Poiché ogni filamento originario rimane associato a un filamento neosintetizzato, il meccanismo prende il nome di replicazione semiconservativa (Figura 03.02-02). L’eleganza del processo risiede nella sua semplicità chimica e nella robustezza informazionale: grazie alla complementarità, il sistema si “autoverifica” ad ogni passo, riducendo la probabilità di errori.
La portata quantitativa dell’operazione è notevole: un genoma eucariotico complesso viene copiato interamente in un intervallo temporale inferiore alla metà di una giornata, ovvero un volume di informazione paragonabile a quello di un’ampia enciclopedia, con solo rarissime imprecisioni residue.
La doppia elica, nel suo insieme, è stabilizzata da numerosi legami a idrogeno tra basi complementari e da interazioni di impilamento, per cui a temperatura fisiologica i filamenti non si separano spontaneamente su lunghi tratti. L’apertura controllata necessaria alla replicazione avviene in siti specifici del genoma, le origini di replicazione, dove proteine iniziatrici riconoscono sequenze determinate e innescano la separazione locale dei filamenti (Figura 03.02-03).
Due aspetti strutturali favoriscono l’avvio:
- la presenza di motivi di legame per le proteine iniziatrici, che reclutano e organizzano il macchinario replicativo;
- regioni ricche in coppie A–T, più agevoli da “sfioccare” perché unite da due, e non tre, legami a idrogeno, con conseguente minore stabilità termodinamica locale.
Nelle cellule procariotiche, come in molti batteri, il cromosoma circolare (lungo milioni di coppie di basi) possiede in genere un’unica origine. Nei genomi eucariotici, molto più estesi, sono presenti migliaia di origini: nell’uomo se ne stimano circa 10 000, con una media di circa 220 per cromosoma. L’attivazione simultanea di numerosi siti riduce drasticamente i tempi complessivi necessari per completare la copia del genoma. Il legame delle proteine iniziatrici all’origine promuove la denaturazione locale della doppia elica e il reclutamento di ulteriori componenti del complesso replicativo. Questi fattori cooperano per stabilizzare i singoli filamenti esposti, prevenire il riappaiamento e predisporre i punti di ingresso della DNA polimerasi.
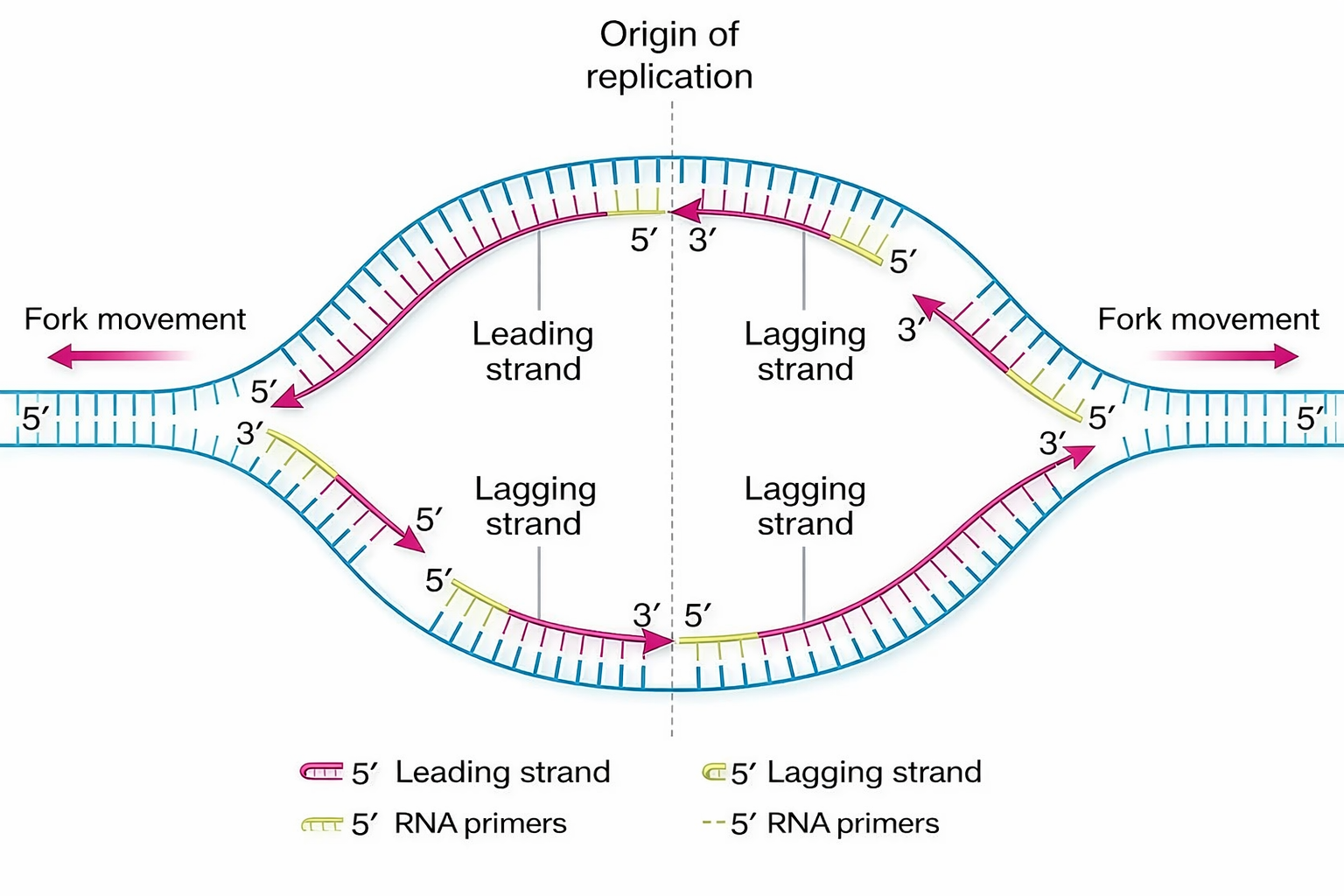
All’aprirsi della doppia elica in corrispondenza di un’origine si formano strutture a Y, dette forcelle replicative, che avanzano in direzioni opposte (Figura 03.02-04). Ciascuna forcella è un sito dinamico dove i filamenti parentali si separano e servono da stampo per la sintesi dei filamenti figli, con un movimento che ricorda l’azione di una cerniera che scorre lungo la molecola (Figura 03.02-05). Il risultato complessivo è una replicazione bidirezionale a partire da ogni origine attiva. Le velocità di avanzamento delle forcelle variano tra domini della vita:
- batteri: circa 1000 coppie di nucleotidi al secondo, grazie a cromosomi compatti e a un’organizzazione del DNA relativamente semplice;
- eucarioti: circa 100 coppie di nucleotidi al secondo nell’uomo, verosimilmente a causa dell’architettura della cromatina e dei complessi processi di regolazione che ne modulano l’accessibilità.
La progressione coordinata delle forcelle richiede un assemblaggio stabile del “replisoma”, nel quale i diversi enzimi lavorano in sincronia per garantire continuità e accuratezza.
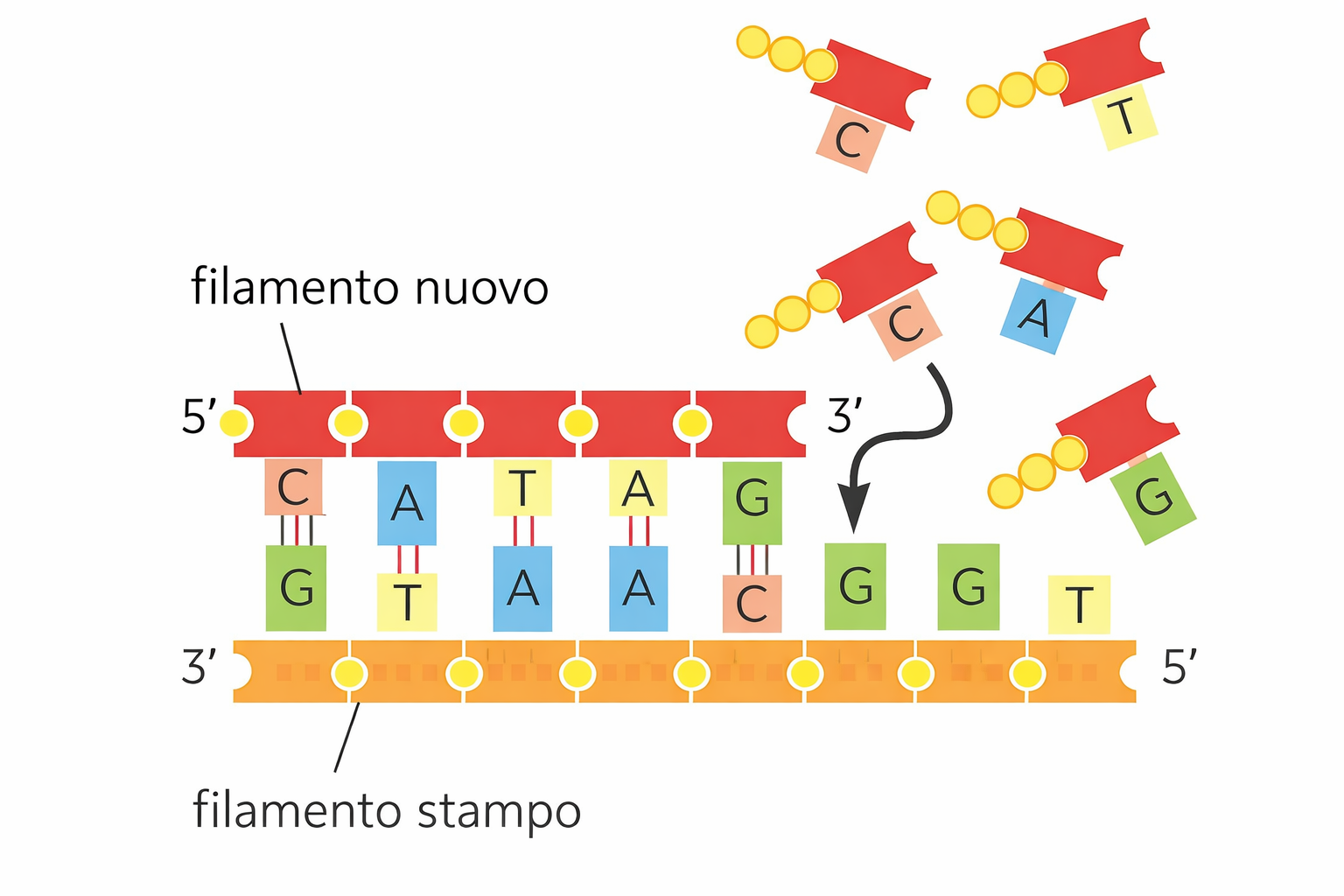
Il fulcro delle reazioni alla forcella di replicazione è la DNA polimerasi, l’enzima che catalizza l’aggiunta sequenziale di deossinucleotidi al capolinea 3′ del filamento in crescita, utilizzando un filamento parentale come matrice (Figura 03.02-06). L’appaiamento corretto tra il nucleotide entrante e la base esposta sullo stampo determina quale tra A, T, G o C venga incorporato in ciascuna posizione. La reazione di polimerizzazione consiste nella formazione di un legame fosfodiesterico tra il gruppo 3′-ossidrile del filamento nascente e il gruppo 5′-fosfato del deossiribonucleoside trifosfato (dNTP) in arrivo. Il trasferimento è energeticamente favorito dall’idrolisi del legame ad alta energia del dNTP, con liberazione di pirofosfato (PPi) che viene successivamente scisso in due fosfati inorganici, spingendo la reazione in avanti in modo praticamente irreversibile (Figura 03.02-07). In forma schematica:
\[ (\text{DNA})_n\text{-3′OH} + \text{dNTP} \rightarrow (\text{DNA})_{n+1}\text{-3′OH} + PP_i \quad\text{e}\quad PP_i \rightarrow 2\,P_i \]
Dal punto di vista meccanicistico, il 3′-OH attacca nucleofilicamente il fosforo α del dNTP, formando il nuovo ponte fosfodiesterico e rilasciando PPi. La selezione del nucleotide corretto è potenziata dalla complementarità delle basi e dalla geometria del sito attivo dell’enzima. La DNA polimerasi è altamente processiva: non si stacca dal DNA dopo ogni singola incorporazione, ma rimane ancorata alla matrice e scorre lungo di essa effettuando numerosi cicli di catalisi consecutivi. Questa proprietà è amplificata dalla presenza di un “anello scorrevole” (sliding clamp), una proteina che circonda la doppia elica e trattiene la polimerasi sul DNA, aumentando drasticamente la velocità e la continuità della sintesi. Un apposito caricatore di clamp, alimentato da nucleotidi, apre e posiziona l’anello sul DNA al momento opportuno. Oltre alla selezione basata sull’appaiamento complementare, molte DNA polimerasi possiedono attività di correzione 3′→5′ (proofreading) che rimuove nucleotidi erroneamente inseriti, contribuendo in modo determinante alla fedeltà complessiva della replicazione. L’insieme di controllo sterico, proofreading e reazioni a valle di riparo consente di mantenere il numero di errori a livelli estremamente bassi, coerenti con le esigenze di stabilità del genoma.
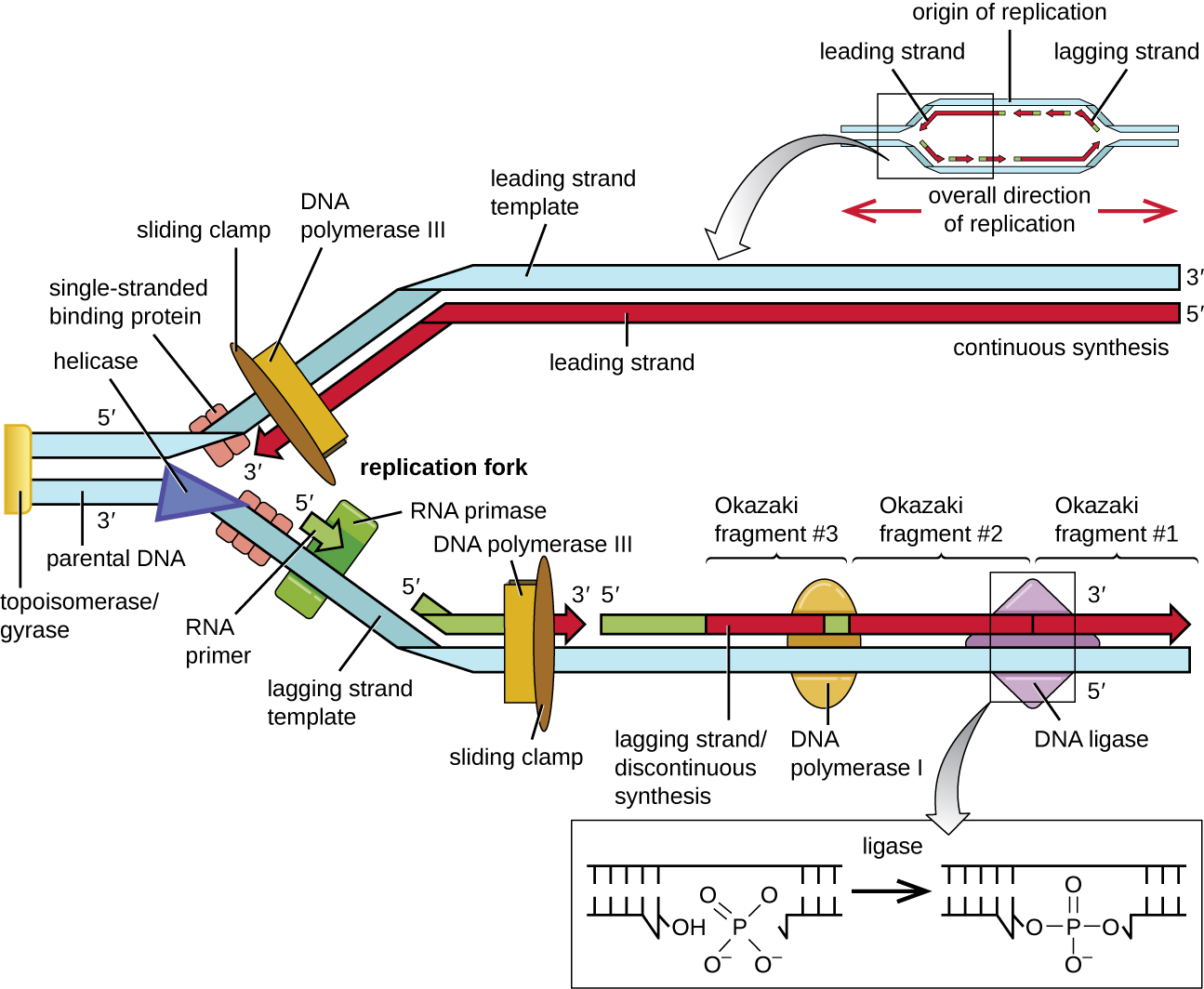
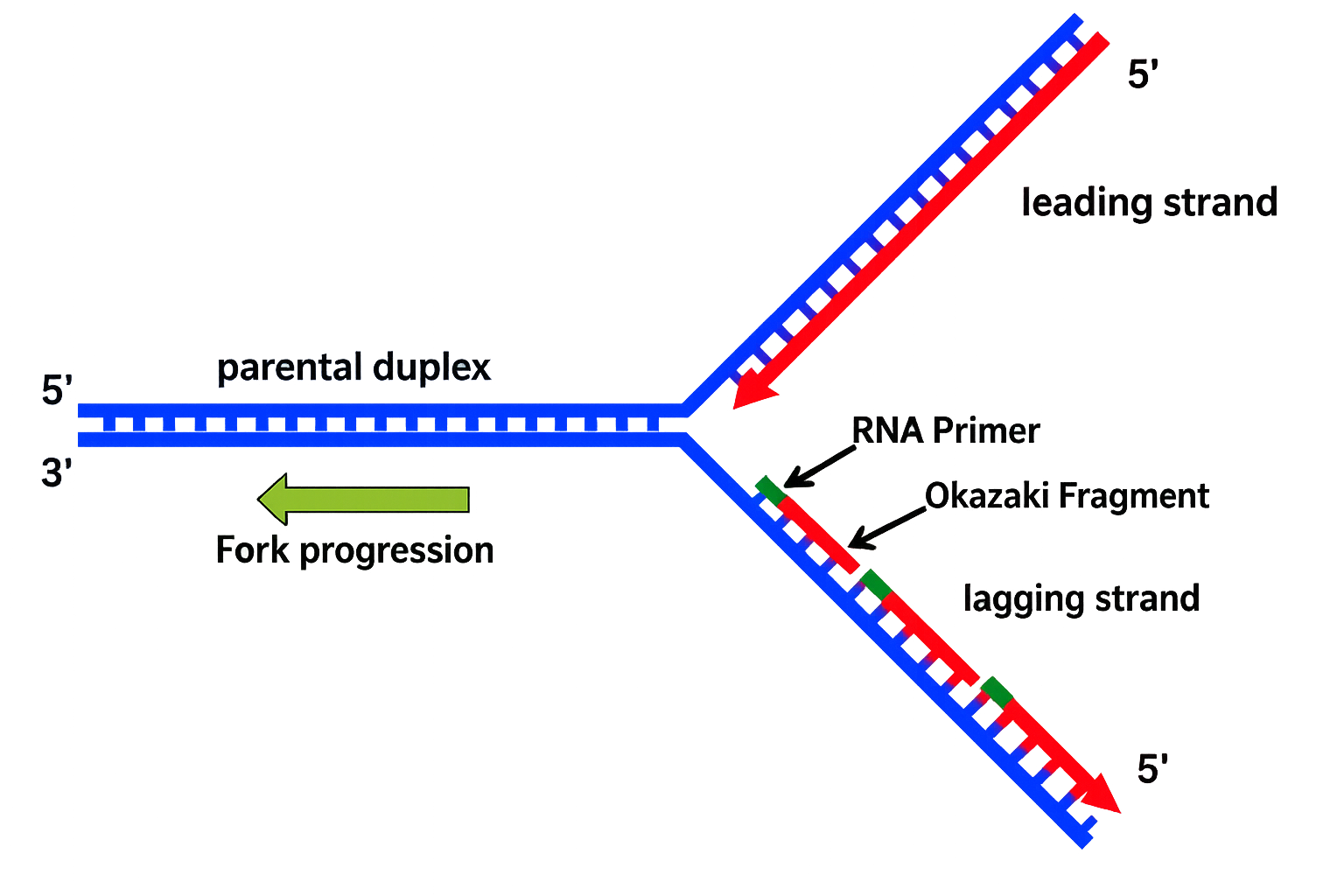
La chimica della polimerizzazione del DNA impone una direzione obbligata: l’allungamento della catena avviene soltanto aggiungendo nuovi deossinucleotidi all’estremità 3′ libera. Questa proprietà discende dalla polarità dell’ossatura zucchero‑fosfato, definita dal legame tra il carbonio 3′ di un desossiribosio e il 5′ del successivo. Nella doppia elica i due filamenti decorrono antiparalleli, per cui, in prossimità di una forcella replicativa, uno stampo è letto in direzione 3′→5′, mentre l’altro procede in verso opposto 5′→3′. Ne deriva un’inevitabile asimmetria strutturale e operativa della forcella (Figura 03.02-07). Un’osservazione ingannevole emerge considerando la (Figura 03.02-05): i due filamenti neosintetizzati sembrano avanzare verso il fronte di apertura, come se entrambi si espandessero nella medesima direzione spaziale. Potrebbe sembrare, dunque, che uno cresca 5′→3′ e l’altro 3′→5′, implicando l’esistenza di due tipi di DNA polimerasi con opposte direzionalità catalitiche. Non è così: tutte le DNA polimerasi conosciute estendono esclusivamente un’estremità 3′‑OH, catalizzando la formazione del legame fosfodiestere mediante l’attacco nucleofilo del 3′‑OH al fosfato α del dNTP in ingresso, con rilascio di pirofosfato (Figura 03.02-07). In simboli, la reazione di allungamento può essere riassunta come: \( \text{(DNA)}_n\text{-3′OH} + \text{dNTP} \rightarrow \text{(DNA)}_{n+1} + \text{PP}_{\mathrm{i}} \). Di conseguenza, la sintesi procede sempre 5′→3′ lungo il filamento nascente. Come si concilia questa costrizione con l’antiparallelismo degli stampi? La soluzione è un’architettura di sintesi differenziata: il filamento guida (leading) viene copiato in modo continuo, mentre il filamento lento (lagging) è generato discontinuitamente tramite una sequenza di brevi tratti, i frammenti di Okazaki, ciascuno dei quali è prodotto comunque 5′→3′ ma in direzione opposta all’avanzamento della forcella. Tali frammenti, denominati in onore del loro scopritore, sono successivamente raccordati in un polimero continuo (Figura 03.02-07). Il risultato apparente è che entrambi i nuovi filamenti si estendono verso la forcella, pur essendo stati sintetizzati con strategie diverse. La sintesi discontinua si compone di passaggi coordinati, ripetuti ciclicamente sul filamento lento:
- inizio con la deposizione di un breve innesco a RNA da parte della primasi, che fornisce l’estremità 3′‑OH necessaria alla polimerasi;
- estensione del primer da parte della DNA polimerasi in direzione 5′→3′, fino a incontrare il frammento precedente;
- rimozione dell’RNA primer (nelle cellule eucariotiche tramite RNasi H e FEN1; nei batteri mediante l’attività 5′→3′ esonucleasica della Pol I);
- riempimento della lacuna con DNA e saldatura finale operata dalla DNA ligasi, che consuma ATP o NAD⁺ a seconda dell’organismo.
Nella maggior parte dei batteri i frammenti di Okazaki hanno dimensioni nell’ordine di 1–2 kb, mentre negli eucarioti risultano più brevi, circa 100–200 nucleotidi, anche per la diversa organizzazione della cromatina. La sincronizzazione tra sintesi continua e discontinua è assicurata dal replisoma, un complesso multiproteico che, oltre alle DNA polimerasi, include elicasi, proteine leganti il singolo filamento (SSB/RPA), una pinza scorrevole e il relativo caricatore. In molti sistemi la polimerasi opera come dimero: una subunità copia il filamento guida, l’altra cicla ripetutamente sui nuovi primer del filamento lento, compiendo la caratteristica “manovra a punto indietro” che rende conto del piccolo ritardo del lagging rispetto al leading. L’universalità di questa asimmetria tra procarioti ed eucarioti riflette la medesima costrizione chimica: l’allungamento è necessariamente 5′→3′, condizione che, come discusso oltre, integra un vantaggio cruciale per la fedeltà della copia.
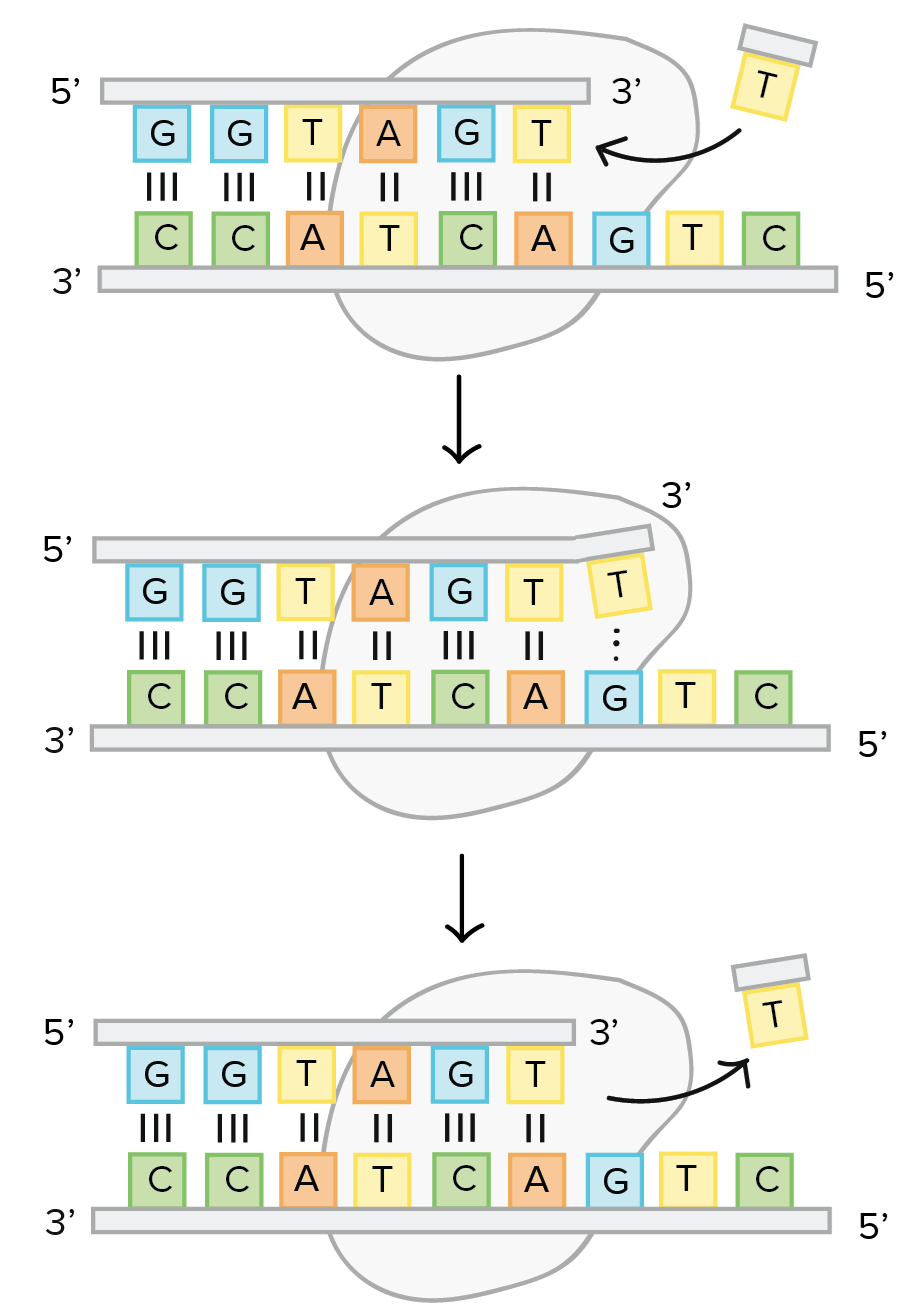
La replicazione è straordinariamente accurata: la DNA polimerasi introduce mediamente un errore ogni \(10^{7}\) coppie di basi copiate. Questo livello di precisione è più elevato di quanto ci si aspetterebbe dalla sola selettività termodinamica dell’appaiamento (A–T e C–G sono le coppie più stabili, ma appaiamenti “wobble” come G–T o C–A possono verificarsi sporadicamente). Due caratteristiche cooperative dell’enzima elevano la fedeltà oltre la selezione di base: il controllo conformazionale dell’inserzione e il proofreading esonucleasico.
In primo luogo, l’enzima verifica la compatibilità geometrica tra il nucleotide in ingresso e la base dello stampo; soltanto un appaiamento corretto induce la chiusura del sito attivo e l’avvio della catalisi. In secondo luogo, qualora avvenga un’inserzione errata, la polimerasi trasferisce l’estremità 3′ del DNA nascente in un distinto sito catalitico con attività esonucleasica 3′→5′, che rimuove il nucleotide mal appaiato, ripristinando un 3′‑OH correttamente appaiato e pronto alla prosecuzione della sintesi (Figura 03.02-08). Le due funzioni — polimerasica ed esonucleasica — risiedono in domini separati ma allostericamente coordinati della stessa proteina o complesso enzimatico (Figura 03.02-07). Grazie a questa integrazione, l’errore complessivo si riduce drasticamente; nei sistemi cellulari, la successiva riparazione delle non‑corrispondenze (mismatch repair) può spingere la fedeltà fino a circa \(10^{-9}\)–\(10^{-10}\) per base replicata.
Il nesso tra proofreading e direzionalità 5′→3′ è sostanziale. Se si ipotizza, per assurdo, una DNA polimerasi che estenda 3′→5′, l’eliminazione di un nucleotide sbagliato renderebbe “cieca” l’estremità della catena, privandola della necessaria energia di attivazione per il passo successivo. Nella sintesi fisiologica 5′→3′, l’energia per formare ciascun legame fosfodiestere proviene dal dNTP in arrivo: anche dopo l’escissione di un errore, un nuovo dNTP può donare il proprio pirofosfato per alimentare la reazione. Al contrario, con una ipotetica polimerizzazione 3′→5′, l’energia sarebbe legata al gruppo trifosfato terminale del filamento nascente; la sua rimozione durante la correzione lascerebbe un’estremità chimicamente inerte, non più prolungabile (Figura 03.02-07). In termini meccanicistici: soltanto il modello 5′→3′ rende compatibili, nello stesso ciclo catalitico, crescita della catena ed eliminazione tempestiva degli inserimenti errati.
Questa interdipendenza spiega perché la cellula “accetti” la complessità operativa del filamento lento. La strategia dell’andare avanti e indietro nella regione lagging non è un ripiego inefficiente, bensì il prezzo — evolutivamente vantaggioso — da pagare per mantenere l’attività autocorrettiva in corso di sintesi e salvaguardare l’integrità del genoma. In pratica, la combinazione di: selezione conformazionale al sito polimerasico; proofreading 3′→5′ in tempo reale; e, successivamente, vie di riparazione post‑replicative, consente di coniugare velocità di duplicazione con un’eccezionale fedeltà. L’asimmetria della forcella (Figura 03.02-07) e l’architettura bifunzionale delle polimerasi (Figura 03.02-08) sono dunque due aspetti complementari della stessa soluzione chimico‑enzimatica, fondata sulla direzione obbligata 5′→3′ dell’allungamento.
L’elevata fedeltà della replicazione dipende in larga misura dalla DNA polimerasi, che controlla l’appaiamento corretto dell’ultima base al 3′-OH prima di incorporare un nuovo deossiribonucleotide. Tuttavia, questa classe di enzimi non è in grado di iniziare de novo una catena: necessita di un’estremità 3′-OH preesistente appaiata allo stampo. Per creare tale punto di partenza interviene la primasi, un’RNA polimerasi specializzata che, usando il DNA come matrice, sintetizza brevi segmenti di RNA (circa 8–12 nucleotidi) capaci di fornire l’estremità 3′-OH appaiata richiesta dalla DNA polimerasi (Figura 03.02-07). L’RNA differisce dal DNA per la presenza del ribosio e della base uracile (U) al posto della timina (T); poiché U si appaia con A, la formazione del primer rispetta le regole dell’appaiamento di basi come per il DNA.
Una volta posizionato il primer, la DNA polimerasi estende la catena in direzione 5′→3′. Sul filamento guida è in genere sufficiente un singolo innesco all’origine di replicazione, dopo il quale l’enzima progredisce in modo continuo. Sul filamento ritardato, invece, la sintesi è discontinua e richiede la formazione ripetuta di nuovi primer a valle della forcella, da cui originano successivi frammenti di Okazaki (Figura 03.02-07). La polimerasi prolunga ciascun primer fino a incontrare l’innesco successivo, producendo una serie di segmenti adiacenti che devono essere processati per ottenere un filamento continuo.
La maturazione dei frammenti sul filamento ritardato coinvolge tre attività enzimatiche principali (Figura 03.02-07):
- una nucleasi che rimuove l’RNA primer appaiato al DNA stampo; nei batteri ciò include spesso l’attività esonucleasica 5′→3′ della DNA polimerasi I, mentre negli eucarioti intervengono RNase H e FEN1 per eliminare l’ibrido RNA/DNA e il “flap” residuo;
- una DNA polimerasi di riparazione che colma la lacuna con deossiribonucleotidi, utilizzando come innesco l’estremità 3′ del frammento di Okazaki adiacente; nei procarioti questa funzione è classicamente svolta dalla DNA polimerasi I, negli eucarioti prevalentemente da DNA polimerasi δ;
- la DNA ligasi, che sigilla l’interruzione fosfodiesterica unendo il gruppo 5′-fosfato al 3′-OH contiguo; l’enzima consuma energia (ATP negli eucarioti; spesso NAD+ nei batteri).
La DNA polimerasi responsabile della maggior parte della sintesi alla forcella nei batteri è indicata come DNA polimerasi III, mentre la DNA polimerasi I partecipa soprattutto alla rimozione dei primer e al riempimento delle lacune. A differenza delle DNA polimerasi replicative, la primasi non esercita correzione di bozze, per cui i primer possono contenere errori; essendo RNA, tali tratti vengono però riconosciuti e sostituiti, ripristinando l’accuratezza complessiva grazie all’attività autocorrettiva delle polimerasi che li rimpiazzano.
La direzione obbligata 5′→3′ discende dalla chimica della reazione: l’attacco nucleofilo dell’ossidrile 3′ sul fosforo α del dNTP genera un nuovo legame fosfodiestere, liberando pirofosfato. La reazione complessiva può essere schematizzata come:
\[ (DNA)_{n} + dNTP \xrightarrow{\text{DNA pol}} (DNA)_{n+1} + PP_i \]
La successiva idrolisi del pirofosfato, \(PP_i \to 2P_i\), rende il processo termodinamicamente favorevole e direzionale.
Nota comparativa: negli eucarioti, l’avvio sul filamento ritardato è spesso mediato dal complesso pol α–primasi, che deposita un breve ibrido RNA/DNA, poi esteso con alta processività da pol δ; nei batteri, la primasi DnaG deposita primer RNA puri, estesi dalla polimerasi III holoenzima.
La duplicazione del genoma richiede l’azione congiunta di numerose proteine organizzate in un complesso multienzimatico, spesso definito replisoma, che opera all’interfaccia della forcella replicativa. Per consentire l’accesso delle polimerasi ai filamenti stampo, la doppia elica deve essere localmente separata. Le DNA elicasi aprono l’elica avanzando lungo il DNA e sfruttando l’energia dell’idrolisi di ATP (Figura 03.02-07). Le regioni di singolo filamento esposte vengono stabilizzate da proteine leganti ssDNA, che impediscono il riappaiamento e l’insorgenza di strutture secondarie: nei batteri la proteina SSB, negli eucarioti il complesso RPA.
Lo svolgimento dell’elica genera tensione torsionale a monte della forcella, con accumulo di superavvolgimenti positivi che ostacolerebbero la progressione enzimatica (Figura 03.02-09). Le DNA topoisomerasi risolvono questo vincolo introducendo tagli transitori nello scheletro zucchero-fosfato: gli enzimi di tipo I rompono una singola elica per rilassare gradualmente la torsione, quelli di tipo II tagliano entrambe le eliche e possono passare un duplex attraverso l’altro, eliminando superavvolgimenti in modo più rapido (Figura 03.02-09). Nei procarioti, la girasi (una topoisomerasi II) introduce anche superavvolgimenti negativi, facilitando ulteriormente la replicazione.
La processività delle DNA polimerasi è assicurata dalla “pinza scorrevole”, un anello proteico che abbraccia il duplex e ancora l’enzima allo stampo, prevenendone il distacco prematuro (Figura 03.02-07). Il caricatore della pinza, un ATPasi specializzata, apre e posiziona l’anello attorno al DNA e ne coordina l’aggancio alla polimerasi; nei batteri questo ruolo è svolto dal complesso γ, negli eucarioti dal fattore RFC. Un singolo evento di caricamento è sufficiente sul filamento guida per ogni ciclo replicativo, mentre sul filamento ritardato la pinza viene ripetutamente sganciata e ricaricata a ogni nuovo frammento di Okazaki; nei batteri ciò avviene con frequenza dell’ordine di una volta al secondo. Nella pratica, i frammenti di Okazaki sono lunghi tipicamente 1–2 kb nei procarioti e 100–200 nt negli eucarioti.
Quasi tutti i componenti della replicazione sono fisicamente e funzionalmente coordinati in un’unità che avanza lungo il DNA, sincronizzando la sintesi continua del filamento guida con quella discontinua del filamento ritardato (Figura 03.02-07). Un modello operativo, spesso descritto come “a trombone”, prevede il looping transitorio del filamento ritardato per permettere alle due polimerasi sorelle di procedere nella stessa direzione spaziale pur sintetizzando catene con polarità opposta. Un elenco delle principali proteine della replicazione è riportato nella (Tabella 03.02-01).
Proteine della replicazione del DNA
| Proteina | Attività |
|---|---|
| DNA polimerasi | Aggiunge nucleotidi al filamento nascente di DNA in direzione 5’→3’, utilizzando come stampo il filamento parentale. |
| DNA elicasi | Consuma ATP per separare i due filamenti di DNA, aprendo la doppia elica alla forcella di replicazione. |
| Proteina legante il DNA a singolo filamento | Si associa ai filamenti singoli mantenendoli distesi e impedendo la ricombinazione prematura delle basi. |
| DNA topoisomerasi | Taglia temporaneamente i filamenti di DNA per alleviare le tensioni generate davanti alla forcella di replicazione. |
| Pinza scorrevole | Tiene la DNA polimerasi ancorata al DNA, permettendole di sintetizzare in maniera continua e stabile. |
| Caricatore della pinza | Utilizza ATP per posizionare la pinza scorrevole sul DNA. |
| Primasi | Sintetizza brevi tratti di RNA che fungono da innesco per la polimerizzazione del DNA sul filamento lento. |
| DNA ligasi | Salda i frammenti di Okazaki sul filamento lento utilizzando l’energia derivata dall’idrolisi di ATP. |
| Tabella che riassume le principali proteine coinvolte nella duplicazione del DNA e le loro funzioni specifiche, dalla separazione e stabilizzazione dei filamenti fino all’avvio e completamento della sintesi, garantendo una replicazione fedele dell’informazione genetica. | |
La sintesi discontinua del filamento ritardato crea un problema alle estremità lineari dei cromosomi: rimosso l’ultimo primer, non resta un 3′-OH disponibile per riempire la regione terminale, con conseguente accorciamento progressivo del DNA a ogni ciclo replicativo (Figura 03.02-10). I procarioti eludono questa difficoltà grazie al DNA cromosomico circolare, privo di estremità. Negli eucarioti, la soluzione è fornita dai telomeri, sequenze ripetute specializzate che reclutano l’enzima telomerasi.
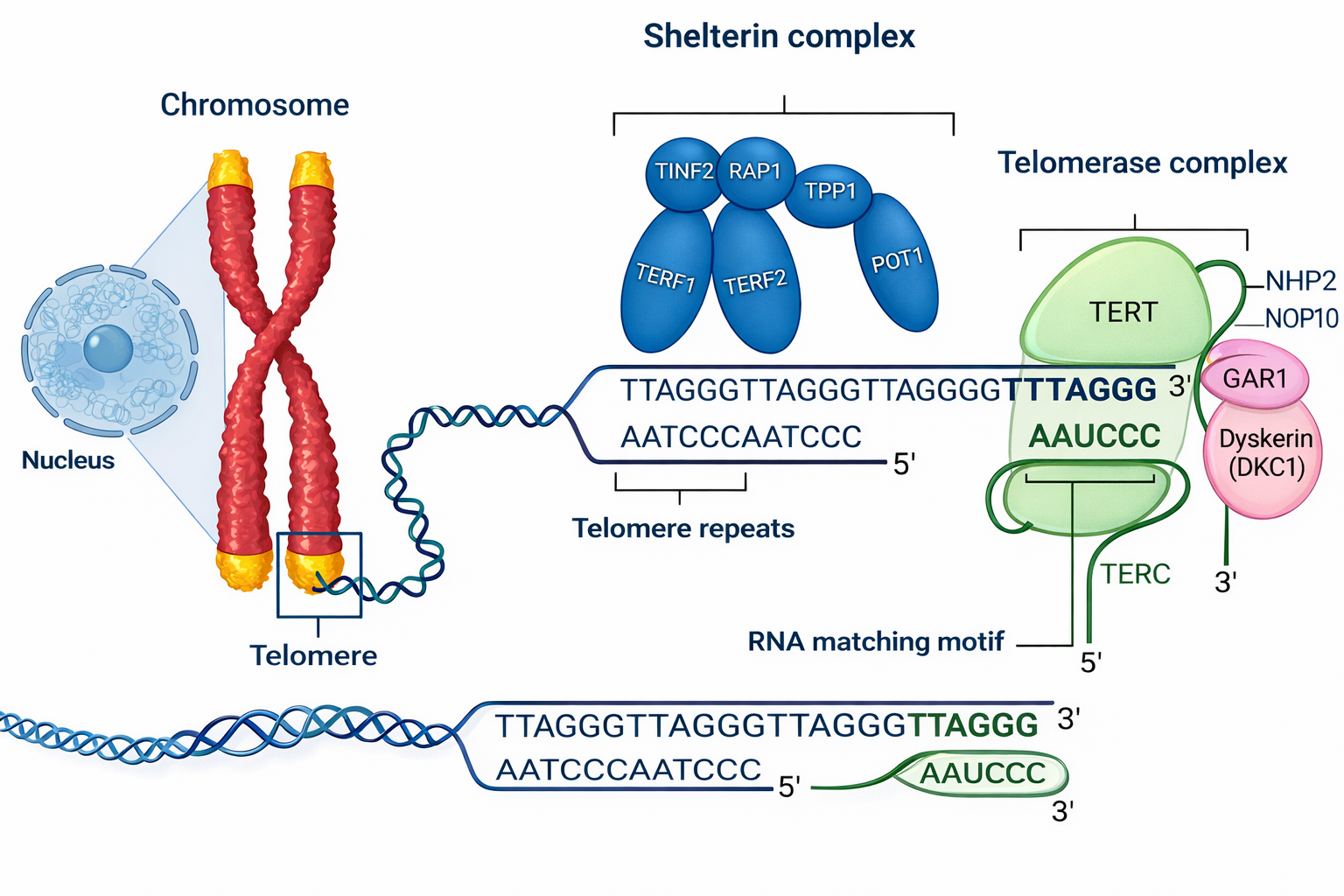
La telomerasi è una trascrittasi inversa a RNA intrinseco: contiene un RNA guida che funge da stampo per estendere il filamento 3′ terminale del cromosoma aggiungendo ripetizioni specifiche per specie. Tale estensione genera una sovrapposizione a 3′ che, a sua volta, permette la deposizione di un primer e il riempimento del filamento complementare da parte della normale macchina replicativa, completando la copia anche del filamento ritardato (Figura 03.02-10). In molte cellule in attiva proliferazione, l’attività telomerasica consente il mantenimento della lunghezza telomerica, evitando la perdita di sequenze codificanti vicine alle estremità.
Oltre alla loro funzione replicativa, i telomeri formano complessi nucleoproteici che “segnano” le vere estremità cromosomiche, distinguendole da rotture accidentali all’interno dei cromosomi che richiederebbero invece risposte di riparazione. Strutture come la T-loop e l’assemblaggio di proteine telomeriche (ad esempio il complesso shelterin negli eucarioti superiori) contribuiscono sia alla protezione fisica delle estremità sia alla regolazione dell’accesso della telomerasi.
Le sequenze ripetute dei telomeri fungono da piattaforma per proteine che modulano sia la stabilità fisica delle estremità sia la loro lunghezza. Tali fattori regolano l’accesso della telomerasi e collegano lo stato strutturale del telomero al ciclo cellulare. In tessuti a rapido turn-over, come epitelio intestinale e compartimenti ematopoietici, l’attività della telomerasi rimane elevata per sostenere la proliferazione. In molte cellule somatiche differenziate, invece, l’espressione o l’attività dell’enzima si riduce nel tempo, con progressivo accorciamento dei telomeri fino a raggiungere una soglia critica che attiva risposte di danno al DNA e arresto proliferativo.
Il controllo della lunghezza telomerica contribuisce a un meccanismo di salvaguardia contro la proliferazione incontrollata. Una volta che i telomeri diventano troppo corti, si attivano vie di sorveglianza (ad esempio mediate da p53/p21) che inducono senescenza replicativa o apoptosi, limitando l’espansione di cloni cellulari potenzialmente pericolosi. Fa eccezione la linea germinale, diverse cellule staminali e le cellule embrionali precoci, nelle quali la telomerasi è attiva per preservare la capacità replicativa a lungo termine. Molti tumori riacquistano attività telomerasica o sfruttano vie alternative di allungamento dei telomeri (ALT), superando questa barriera di controllo.






![1: Electron micrograph showing multiple replication bubbles of Drosophila melanogaster DNA. Arrows indicate the position of replication bubbles, areas on the DNA that have been already duplicated. From [6], courtesy of D. S. Hogness.](https://www.researchgate.net/profile/John-Bechhoefer/publication/6981656/figure/fig1/AS:280587974791168@1443908794289/Electron-micrograph-showing-multiple-replication-bubbles-of-Drosophila-melanogaster-DNA.png)