Fonazione
Definizione
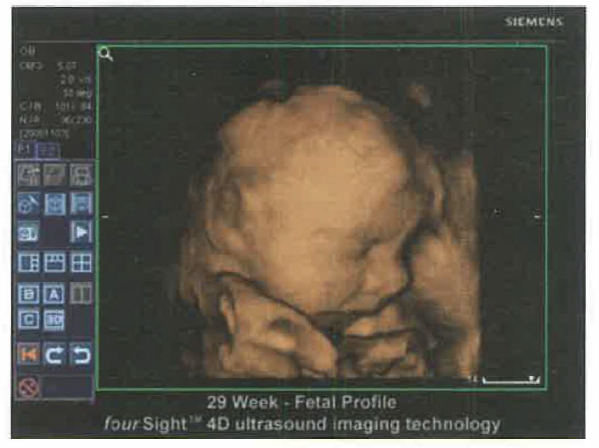
L’impiego degli ultrasuoni in ambito clinico si fonda soprattutto sulla marcata direttività del fascio acustico, sfruttata per ottenere la rappresentazione di strutture interne mediante ecografia bidimensionale e tridimensionale (Figura 04.22-02). I trasduttori piezoelettrici, sottoposti a una tensione alternata, convertono l’energia elettrica in vibrazioni meccaniche alla medesima frequenza; in modo reciproco, vibrazioni incidenti generano un segnale elettrico di uguale frequenza. Lo stesso elemento piezoelettrico, quindi, funge da emettitore e da rivelatore. Le frequenze operative in diagnostica si collocano tipicamente tra 0,5 e 15 MHz, mentre l’intensità acustica varia da 10⁻⁴ W/cm² a ~10 W/cm² a seconda che l’uso sia diagnostico o terapeutico.
Nei tessuti biologici gli effetti primari sono di natura meccanica e termica, con riscaldamento per assorbimento viscoelastico; la cavitazione non controllata, ovvero la crescita e collasso di microbolle, deve essere evitata in ambito clinico. La velocità di propagazione è circa 343 m/s in aria e ~1.450 m/s in acqua (e ~1.540 m/s nei tessuti molli, con dipendenza dalla temperatura). La lunghezza d’onda è \(\lambda = v/\nu\): a 1 MHz vale ~0,34 m in aria e ~1,5 mm in acqua; a 10 MHz, nei tessuti molli, \(\lambda \approx 0,154\) mm. Lunghezze d’onda sub-millimetriche consentono un’elevata risoluzione spaziale e, in combinazione con aperture acustiche idonee, una propagazione altamente collimata (direttività elevata).
L’attenuazione degli ultrasuoni nei mezzi biologici segue una legge esponenziale, con dipendenza dal tipo di tessuto e dalla frequenza. La legge di assorbimento si esprime come:
\[ I(x) = I_o e^{-ax}, \]
con \(I_{0} = I(x=0)\) intensità incidente e \(I(x)\) l’intensità dopo lo spessore \(x\); il coefficiente di assorbimento \(\alpha\) dipende dal materiale attraversato (Tabella 04.22-01) e dalla frequenza.
Nella banda 0,5–15 MHz, per molti tessuti biologici vale approssimativamente la proporzionalità:
\(\alpha \propto \nu\).
Ne consegue che frequenze più alte migliorano la risoluzione ma riducono la profondità di penetrazione. L’acqua presenta un assorbimento molto ridotto e agisce come “finestra” acustica verso i distretti profondi. Per minimizzare le riflessioni dovute al forte disaccoppiamento d’impedenza tra aria e cute, le sonde sono accoppiate alla pelle mediante un gel conduttivo, che elimina l’aria all’interfaccia e riduce la perdita per riflessione, favorendo il trasferimento di energia nel corpo:
- Fasce di frequenza tipiche: 2–5 MHz per distretti profondi (addome, ostetricia); 7–15 MHz per strutture superficiali (tendini, tiroide, cute);
- Compromesso fisico: all’aumentare della frequenza migliorano risoluzione assiale e laterale, ma aumenta l’attenuazione complessiva;
- Direttività del fascio: definita dal rapporto tra apertura acustica e lunghezza d’onda, con focalizzazione elettronica nei trasduttori a schiera (phased/linear array).
In diagnostica sono visualizzati sul display indici di sicurezza internazionalmente adottati, come Thermal Index (TI) e Mechanical Index (MI), per la gestione del rischio termico e meccanico (norme IEC/FDA/AIUM).
| Sostanza / Tessuto | α (cm⁻¹) | Nota |
|---|---|---|
| Acqua | 0.0006 | Riferimento di base, quasi trasparente agli ultrasuoni. |
| Plasma | 0.014 | Valore basso, utile come confronto con il sangue intero. |
| Sangue intero | 0.04 | Assorbimento moderato, importante per applicazioni in diagnostica Doppler. |
| Muscolo scheletrico | 0.4 – 0.5 | Elevato assorbimento, dipende dall’orientamento delle fibre muscolari. |
| Fegato | 0.34 | Caratteristica intermedia, utile per ecografie addominali. |
| Rene | 0.44 | Assorbimento relativamente alto, rilevante nella diagnostica renale. |
| Tessuto adiposo | 0.26 | Proprietà di attenuazione minore rispetto al muscolo, influenza l’imaging in ecografia. |
| Polmone (parenchima) | ~1.0 | Elevata attenuazione per via della presenza di aria. |
| Ossa corticali | 5 – 20 | Estremamente alto, ostacola il passaggio degli ultrasuoni. |
| Midollo osseo | ~2.5 | Valori elevati, ma inferiori alle ossa corticali. |
| Encefalo (materia grigia) | 0.5 – 0.6 | Assorbimento medio, importante nella neurosonologia. |
| Encefalo (materia bianca) | 0.3 – 0.4 | Inferiore alla materia grigia, ma significativo in imaging cerebrale. |
Assorbimento degli ultrasuoni (1 MHz)
Coefficienti di attenuazione a 1 MHz in differenti materiali e tessuti.
L’impiego terapeutico è mirato a specifici distretti con effetti sia meccanici sia termici. La diatermia ultrasonica induce un incremento controllato della temperatura tessutale, utile per modulare il dolore e favorire la vasodilatazione in condizioni come lombalgie, tendinopatie, artrosi e alcune forme reumatiche. Per evitare surriscaldamenti locali, il fascio a bassa intensità viene fatto scorrere sulla regione bersaglio, limitando l’esposizione statica di un singolo punto a pochi secondi.
Impulsi di elevata potenza hanno azione litotrissica e consentono la frammentazione di calcoli in rene o vie urinarie; in ambito odontoiatrico, vibrazioni ultrasoniche di intensità molto inferiore sono impiegate per la rimozione del tartaro e, in endodonzia, per la strumentazione dei canali radicolari. In oculistica, tecniche basate su energia ultrasonica sono utilizzate per emulsificare il cristallino opacizzato e aspirarne i frammenti nella chirurgia della cataratta. In chirurgia vascolare, sistemi miniaturizzati montati su cateteri consentono la caratterizzazione della placca aterosclerotica e, in casi selezionati, la sua distruzione mirata.
L’ablazione ultrasonica ad alta intensità focalizzata (HIFU, High-Intensity Focused Ultrasound) concentra l’energia in un fuoco di pochi millimetri, innalzando rapidamente la temperatura e provocando necrosi coagulativa selettiva, con applicazioni nel trattamento di alcune neoplasie e di lesioni benigne. In chirurgia estetica, la cavitazione controllata e il riscaldamento focalizzato vengono impiegati per la riduzione di adiposità localizzate. Tutti questi impieghi richiedono un controllo accurato dei parametri di esposizione, evitando la cavitazione non desiderata e monitorando gli indici TI e MI visualizzati dal sistema:
- Range d’intensità: da frazioni di mW/cm² in applicazioni sensibili fino a W/cm² per effetti termici terapeutici;
- Modalità d’erogazione: continua per diatermia omogenea; pulsata per ridurre la carica termica mantenendo gli effetti meccanici;
- Focalizzazione: acustica o elettronica per concentrare la dose in volumi ridotti, minimizzando l’esposizione dei tessuti adiacenti;
- Precauzioni: movimento costante della sonda, monitoraggio del feedback termico, attenzione alle interfacce ossee e a sacche gassose.
L’ecografia si basa sulla riflessione del fascio ultrasonico alle interfacce con diversa impedenza acustica. Misurando il tempo di volo degli echi, nota la velocità di propagazione nel tessuto (≈1.540 m/s), si ricostruiscono sezioni bidimensionali (B-mode) e, attraverso acquisizioni volumetriche, immagini tridimensionali (Figura 04.22-02). La notevole direttività del fascio, combinata con focalizzazione e formazione di fascio (beamforming) in trasduttori a schiera, consente elevata risoluzione spaziale.
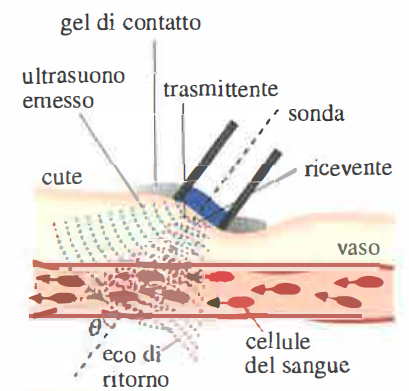
La velocimetria emodinamica non invasiva sfrutta l’effetto Doppler, che fornisce informazioni su velocità e direzione del flusso ematico. Lo schema in (Figura 04.22-01) illustra la geometria: un trasduttore emette a frequenza \(\nu_s\) verso un vaso; gli eritrociti in moto con velocità \(u\) riflettono l’onda, che viene ricevuta e analizzata. Per piccoli angoli \(\theta\) rispetto all’asse del fascio, la frequenza incidente sugli scatter mobili risulta:
\[ \nu_i = \nu_s \left(1 - \frac{u}{v}\right), \]
dove \(v\) è la velocità del suono nel sangue. Considerando la riflessione, gli eritrociti agiscono come sorgenti in allontanamento che riemettono a \(\nu_{i}\). La frequenza ricevuta \(\nu_{r}\) dal trasduttore fisso è:
\[ \nu_t = \nu_i \frac{v}{v+u} = \nu_s \left(\frac{v-u}{v}\right) \left(\frac{v}{v+u}\right) = \nu_s \left(\frac{v-u}{v+u}\right) = \\ = \nu_s \left(\frac{v+u-u-u}{v+u}\right) = \nu_s \left(1 - \frac{2u}{v+u}\right). \]
La differenza di frequenza tra segnale emesso e ricevuto risulta pertanto:
\[ \Delta \nu = \nu_{\mathrm{s}} - \nu_{\mathrm{r}} = \nu_{\mathrm{s}} \left( \frac{2u}{v + u} \right) \]
Tenendo conto dell’angolo \(\theta\) fra fascio e direzione del flusso:
\[ \Delta \nu = \nu_{\mathrm{s}} - \nu_{\mathrm{r}} = \nu_{\mathrm{s}} \left( \frac{2u \cos\theta}{v + u \cos\theta} \right) \]
Poiché nei liquidi fisiologici \(v \gg u\), l’espressione più usata in pratica è:
\[ \Delta \nu = \nu_{\mathrm{s}} - \nu_{\mathrm{r}} = \nu_{\mathrm{s}} \frac{2u \cos\theta}{v} \]
Misurando \(\Delta \nu\) e conoscendo \(\nu_{s}\), \(v\) e \(\theta\), si ottiene la velocità media istantanea del sangue. Se il diametro del vaso è ricavato dagli echi delle pareti (interfaccia tessuto-liquido), la portata volumetrica si calcola come \(Q = \bar{u} \cdot A\). Strumenti opportunamente calibrati forniscono una stima diretta e non invasiva della portata.
Esempio numerico: con \(\nu_{s} = 4\) MHz, \(v = 1.540\) m/s, \(\theta = 60^\circ\) e velocità media \(u = 0,60\) m/s, si ha \(\Delta \nu \approx \nu_{s}\dfrac{2u\cos\theta}{v} = 4\cdot10^{6}\dfrac{2\cdot0{,}60\cdot0{,}5}{1540} \approx 1{,}56\) kHz:
- Doppler continuo (CW): sensibile ad alte velocità ma privo di risoluzione in profondità;
- Doppler pulsato (PW): selettivo in profondità (volume campione), limita l’aliasing entro la frequenza di Nyquist;
- Doppler colore: mappa direzione e modulo medi del flusso sul B-mode, utile per la panoramica emodinamica;
- Doppler power: più sensibile ai flussi lenti, indipendente dalla direzione, meno suscettibile ad aliasing.
Oltre alla valutazione vascolare, le tecniche ultrasonore comprendono la densitometria ossea a ultrasuoni, in cui l’assorbimento e la velocità dell’onda nei segmenti scheletrici periferici forniscono informazioni sulla qualità ossea e sul rischio di osteoporosi. La ricostruzione volumetrica consente, infine, immagini tridimensionali di organi e strutture fetali (Figura 04.22-02).