Flussi elettrochimici
Definizione
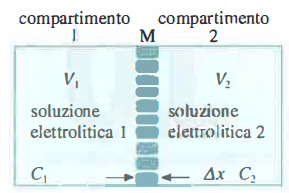
Se due soluzioni elettrolitiche sono separate da una membrana permeabile e presentano un dislivello di potenziale elettrico, V1 ≠ V2, nello spessore della membrana M si stabilisce un campo elettrico uniforme E, approssimativamente pari a \(\displaystyle E = \frac{V_1 - V_2}{\Delta x}\) (Figura 06.10-01). Oltre ai processi di trasporto indotti da gradienti di concentrazione, di pressione idraulica e di pressione osmotica, il campo elettrico esercita una forza sulle specie cariche (ioni), generando un ulteriore contributo di flusso. Indichiamo con \(J_{\text{mol}}\) il flusso molare dell’ione S attraverso la membrana, dovuto esclusivamente al campo elettrico. Per definizione, il prodotto tra \(J_{\text{mol}}\) e la carica trasportata da una mole di ioni è uguale alla densità di corrente elettrica \(j\): \( j = J_{\text{mol}}\,N_A\,Z\,e \). Qui \(J_{\text{mol}}\) è il flusso molare dello ione (mol·cm\(^{-2}\)·s\(^{-1}\)), \(N_A\) è il numero di Avogadro, \(Z\) la valenza dello ione ed \(e\) la carica elementare; ne segue che \(j\) esprime la carica trasportata per unità di superficie e di tempo (C·cm\(^{-2}\)·s\(^{-1}\)).
Assumendo \(E\) uniforme nella membrana e ricordando la relazione ohmica \(j=\sigma E\), si ottiene:
\( J_{\text{mol}}=\dfrac{j}{N_A Z e}=\dfrac{\sigma E}{N_A Z e}=\dfrac{\sigma}{N_A Z e}\,\dfrac{V_1 - V_2}{\Delta x} \).
Per un singolo tipo ionico, la conduttività può essere collegata alla mobilità elettrica e alla concentrazione dello ione \(S\), mostrando che il flusso indotto dal campo si scrive: \( J_{\text{mol}} = \dfrac{Z e N_S \mu_S}{N_A Z e} \dfrac{V_1 - V_2}{\Delta x} = \mu_S (S)\dfrac{V_1 - V_2}{\Delta x} \), dove \(\mu_S\) è la mobilità elettrica dell’ione \(S\). Tale grandezza si esprime in funzione del coefficiente d’attrito \(f\) (o, in alternativa, del coefficiente di diffusione \(D\) attraverso la relazione di Einstein): \( \mu_S = \dfrac{Z e}{f} = \dfrac{Z e N_A D}{R T} \). Dove \(\mu_S\) è la mobilità elettrica dell’ione \(S\). Tale grandezza si esprime in funzione del coefficiente d’attrito \(f\) (o, in alternativa, del coefficiente di diffusione \(D\) attraverso la relazione di Einstein): \(\mu_S = \dfrac{Z e}{f} = \dfrac{Z e N_A D}{R T}\). La concentrazione dello ione \(S\) è indicata con \(C_S\). Introducendo il coefficiente di riflessione della membrana \(\phi\) (0 ≤ \(\phi\) ≤ 1), che quantifica l’ostacolo selettivo al passaggio dell’elettrolita all’interno della membrana, e considerando la concentrazione locale nella membrana \(C_M(x)\), si ottiene: \( J_{\text{mol}} = \mu_S\, C_M(x)\,(1 - \phi)\,\dfrac{V_1 - V_2}{\Delta x} \).
Il contributo J_{\text{mol}} = \mu_s C_M(x) (1-\phi) \frac{V_1 - V_2}{\Delta x}. si somma ai flussi generati dagli altri meccanismi passivi di trasporto attraverso le membrane biologiche esaminati nel Capitolo 14. Esso rappresenta l’effetto del gradiente di potenziale elettrico. Si osservi che il segno di \(J_{\text{mol}}\) è determinato dal prodotto \(Z \, (V_1 - V_2)\): i cationi (Z > 0) migrano, a parità di condizioni, nella direzione del campo, mentre gli anioni (Z < 0) si spostano in verso opposto. La relazione tra flusso ionico e densità di corrente rimane coerente con la forma locale della legge di Ohm \(j = \sigma E\), con \(\sigma = Z^2 (N_0 e)^2 \, \dfrac{D}{R T} \, C_M(x) \, (1-\phi)\) per un singolo specie in assenza di altri contributi.
Esempio numerico. Si consideri una membrana di spessore \(\Delta x = 5\,\mu\text{m}\) con \(\Delta V = 10\,\text{mV}\) e uno ione monovalente (Z = +1) con \(D = 1,3\times 10^{-9}\,\text{m}^2\text{/s}\) a 310 K. Dalla \mu_s = \frac{Z e}{f} = \frac{Z e N_0 D}{R T}, segue \(\mu_s = \dfrac{Z N_0 e D}{R T} \approx 4,87\times 10^{-8}\,\text{m}^2\,\text{V}^{-1}\,\text{s}^{-1}\). Se \(C_M(x) = 50\,\text{mol}\,\text{m}^{-3}\) e \(\phi = 0,2\), allora \(E = \dfrac{\Delta V}{\Delta x} = 2{.}000\,\text{V/m}\) e, dalla J_{\text{mol}} = \mu_s C_M(x) (1-\phi) \frac{V_1 - V_2}{\Delta x}., \(J_{\text{mol}} \approx 3{,}9 \times 10^{-3}\,\text{mol}\,\text{m}^{-2}\,\text{s}^{-1}\) (pari a \(3{,}9 \times 10^{-7}\,\text{mol}\,\text{cm}^{-2}\,\text{s}^{-1}\)).
Nei sistemi biologici isotermi, i meccanismi di trasporto passivo che possono concorrere al movimento di ciascun soluto attraverso una membrana sono i seguenti:
- diffusione, legata ai gradienti di concentrazione e descrivibile dal primo principio di Fick;
- filtrazione, correlata a differenze di pressione idrostatica e alle proprietà idrauliche della membrana;
- osmosi, determinata da gradienti di pressione osmotica e dalla selettività della barriera semipermeabile;
- gradiente di potenziale elettrico, associato all’azione di E sulle specie cariche (ioni).
Il contributo netto di ciascun soluto è dato dalla somma dei corrispondenti flussi i-esimi, ognuno modulato dalle proprietà fisico-chimiche della molecola/ione e dai parametri della membrana; molti soluti coesistono sui due lati della membrana, influenzando la conduzione complessiva secondo le rispettive concentrazioni e valenze.