Fenoli
Definizione
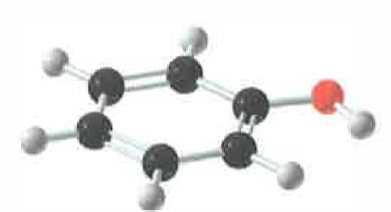
Con il termine fenoli si indicano composti organici nei quali il gruppo ossidrilico è direttamente legato a un sistema aromatico, tipicamente un anello benzenico (Figura 07.07-01). La presenza dell’ossidrile conferisce polarità alla molecola e capacità di formare legami a idrogeno, caratteristiche che rendono i fenoli a basso peso molecolare moderatamente solubili in acqua. Derivati fenolici sono componenti di miscele odorose naturali e sintetiche e trovano impiego come additivi a funzione conservante.
 |
| Struttura del fenolo, capostipite della famiglia dei fenoli. |
Oltre al fenolo, appartengono alla stessa classe numerosi composti sostituiti. Nell’immagine seguente sono illustrati alcuni derivati rappresentativi;
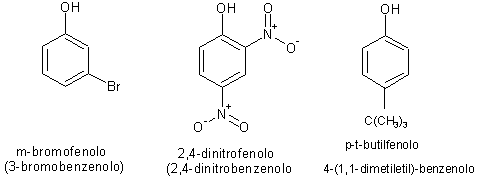 |
| Esempi riportati: m-bromofenolo, 2,4-dinitrofenolo, p-tert-butilfenolo. |
Ulteriori esempi largamente studiati sono o-cresolo (2-metilfenolo), resorcinolo (1,3-diidrossibenzene), catecolo (1,2-diidrossibenzene) e timolo (2-isopropil-5-metilfenolo), i cui comportamenti acido–base e reattività su anello rendono evidente l’effetto dei sostituenti aromatici.
Storicamente, soluzioni diluite di fenolo in acqua (acido carbolico) furono introdotte da Joseph Lister come antisettici per la disinfezione di ferite e strumenti chirurgici, con un impatto determinante sulla riduzione delle infezioni postoperatorie. Tra i derivati fenolici utilizzati come antisettici o disinfettanti si annoverano composti quali esaclorofene, esilresorcinolo e o-fenilfenolo, che sfruttano la capacità del nucleo fenolico di denaturare proteine e destabilizzare membrane.
 |
| Alcuni fenoli di uso frequente e relative denominazioni storiche. |
Come l’acqua e gli alcoli alifatici (R–OH), anche i fenoli sono anfoteri: l’ossigeno, ricco di coppie elettroniche di non legame, può agire da base di Lewis, mentre il legame O–H può scindersi generando \( \mathrm{H^+} \). Negli alcoli, l’influenza del gruppo alchilico sull’elettronegatività dell’ossigeno è limitata e l’acidità risulta dell’ordine di grandezza di quella dell’acqua. In termini termodinamici, a 25 °C si hanno valori comparabili di \( pK_a \) e \( K_a \): per l’acqua \( pK_a \approx 15,7 \) (cioè \( K_a \approx 1,8 \times 10^{-16} \)), mentre per l’etanolo \( pK_a \approx 16 \) (cioè \( K_a \approx 1,3{-}1,6 \times 10^{-16} \)).
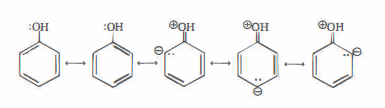
Il quadro cambia in modo sostanziale nel caso dei fenoli: il nucleo aromatico altera la distribuzione elettronica e rende più acido il legame O–H. A 25 °C, per il fenolo si osserva \( pK_a \approx 10,0 \), corrispondente a \( K_a \approx 1,0{-}1,3 \times 10^{-10} \), quindi diverse potenze di dieci superiore rispetto agli alcoli. Questa maggiore acidità si interpreta considerando la delocalizzazione per risonanza della coppia elettronica dell’ossigeno nell’anello aromatico e, soprattutto, la stabilizzazione del coniugato base (fenossido) mediante strutture di risonanza addizionali che implicano separazione di carica e distribuzione della carica negativa sul sistema aromatico (Figura 07.07-02).
Dal punto di vista strutturale, le coppie elettroniche sull’ossigeno sono allineate con il sistema \( \pi \) dell’anello, consentendo un accoppiamento \( p\)-\( \pi \) efficace. Le forme di risonanza con separazione di carica, pur contribuendo in misura non dominante all’ibrido reale, aumentano la densità elettronica sull’anello e lasciano una parziale carica positiva su ossigeno. Ne risulta un incremento della polarizzazione del legame O–H e una più agevole dissociazione in \( \mathrm{H^+} \) e fenossido, spiegando perché i fenoli siano più acidi rispetto agli alcoli alifatici privi di tale delocalizzazione.
La dissociazione acida dei fenoli si rappresenta come segue: \[ \mathrm{ArOH \rightleftharpoons ArO^- + H^+}, \qquad K_a = \frac{[\mathrm{ArO^-}][\mathrm{H^+}]}{[\mathrm{ArOH}]}\,. \] La stabilità del fenossido determina direttamente l’entità di \( K_a \). Ne discende che qualunque fattore capace di stabilizzare il fenossido ne aumenta il contributo all’ibrido di risonanza e accresce l’acidità del fenolo di partenza.
Gli effetti dei sostituenti sul nucleo aromatico seguono regole prevedibili:
- Gruppi elettron-attrattori per effetto induttivo e/o mesomerico negativo (ad esempio –NO2, –CF3, –CN, –SO3H) in posizione orto e para stabilizzano il fenossido per risonanza, elevando marcatamente l’acidità; in meta prevale l’effetto induttivo, con incremento più moderato;
- Gruppi elettron-donatori (+M o +I, come –OCH3, –NH2, alchili) destabilizzano il coniugato base e riducono l’acidità, con effetti più forti nelle posizioni orto e para;
- Interazioni specifiche, come il legame a idrogeno intramolecolare in derivati orto-sostituiti (es., o-nitrofenolo), possono favorire la deprotonazione o modificare la solubilità e la volatilità per formazione di dimeri intramolecolari.
A titolo illustrativo, il p-fluorofenolo è più acido del fenolo per effetto induttivo del fluoro, mentre il p-metossifenolo (idrochinone monometiletere) è meno acido per effetto mesomerico donatore dell’ossigeno metossilico. L’incremento cumulativo di gruppi elettron-attrattori può condurre ad acidità molto elevate: il 2,4,6-trinitrofenolo (acido picrico) è un caso estremo in cui tre gruppi –NO2 in orto/para stabilizzano potentemente il fenossido, portando a un comportamento quasi paragonabile a quello di acidi minerali deboli, con \( K_a \approx 4,2 \times 10^{-1} \) e \( pK_a \approx 0,38 \).
 |
| L’acido picrico (2,4,6-trinitrofenolo) è un esplosivo aromatico ad alta energia; chimicamente è un fenolo fortemente attivato da tre gruppi nitro. |
La maggiore acidità dei fenoli rispetto agli alcoli si accompagna, in genere, a una basicità di Lewis meno pronunciata dell’ossigeno rispetto ai corrispondenti alcoli, proprio perché la delocalizzazione elettronica verso l’anello diminuisce la disponibilità delle coppie di non legame. Questo si riflette, per esempio, nelle costanti di formazione di complessi con acidi di Lewis e nella reattività in alchilazione o acilazione dell’ossigeno.
Oltre alle proprietà acido–base, i fenoli presentano una reattività aromatica peculiare: l’ossidrile attiva l’anello per sostituzione elettrofila in orto e para e guida la regioselettività per effetto +M. Ne derivano velocità elevate di nitrurazione, alogenazione e solfonazione rispetto al benzene, nonché la possibilità di ossidazioni selettive a chinoni; la propensione all’ossidazione aumenta in presenza di basi che generano il fenossido, specie più facilmente ossidabile.
Dal punto di vista applicativo e di sicurezza, il fenolo è caustico e potenzialmente tossico per contatto e inalazione; i suoi derivati richiedono manipolazione in ambiente ventilato e adeguati dispositivi di protezione. Al contempo, l’ampia gamma di attività biologiche dei fenoli, naturali e sintetici, spiega il loro impiego in ambiti che vanno dai disinfettanti ai materiali polimerici, passando per antiossidanti alimentari e farmacofori di numerosi agenti terapeutici.
Le considerazioni precedenti sono coerenti con la terminologia e i principi riportati nelle fonti di riferimento di chimica organica e fisica (IUPAC Gold Book; manuali universitari di chimica organica e di termodinamica chimica), che inquadrano i fenoli come alcoli aromatici caratterizzati da equilibrio acido–base spostato verso la forma deprotonata per effetto della delocalizzazione elettronica nel sistema aromatico.