Equilibrio fisico ed equilibrio chimico
Definizione
Nelle trattazioni introduttive si assume spesso che le trasformazioni fisiche e chimiche procedano fino a esaurire completamente i reagenti. In realtà, un gran numero di processi di rilievo scientifico e tecnologico non raggiunge la completa conversione: quando l’evoluzione macroscopica cessa di essere osservabile, nel sistema coesistono quantità misurabili di reagenti e di prodotti. Tali trasformazioni sono dette reazioni all’equilibrio. Esempi di equilibri, sia fisici sia chimici, sono diffusi in ambiente naturale: la concentrazione di ossigeno disciolto in un lago è regolata dall’equilibrio gas–liquido, con implicazioni fondamentali per gli organismi acquatici; anche l’evoluzione del paesaggio carsico dipende da equilibri multipli e accoppiati. Stalattiti e stalagmiti, costituite da carbonato di calcio solido, si formano e si dissolvono in base a un equilibrio in cui intervengono ioni calcio e bicarbonato, anidride carbonica e acqua:
Ca²⁺(aq) + 2 HCO₃⁻(aq) ⇌ CaCO₃(s) + CO₂(aq) + H₂O(l)
La direzione preferenziale di questo equilibrio dipende, tra l’altro, dalla pressione parziale di CO₂, dalla temperatura e dal pH della soluzione, variabili che modulano solubilità e precipitazione del CaCO₃.
Un equilibrio fisico, come la dissoluzione di un soluto molecolare in un solvente, è tipicamente un processo reversibile e si indica con una doppia freccia. La saturazione di una soluzione di saccarosio in acqua è un esempio classico di equilibrio dinamico. Per equilibrio dinamico si intende una condizione in cui, per una trasformazione reversibile, la velocità del processo diretto e quella del processo inverso sono uguali. Consideriamo il caso dello zucchero in acqua. Se si introduce una piccola quantità di zucchero, ad esempio 1,5 g, in 100 mL di acqua e si agita brevemente, il solido si dissolve completamente: l’intero campione passa in fase acquosa e si ottiene una soluzione omogenea, che possiamo schematizzare come:
zucchero (s) ⇌ zucchero (aq)
Se invece, nello stesso volume d’acqua, si aggiunge un marcato eccesso di zucchero, per esempio 250 g a 25 °C, la dissoluzione procede fino al raggiungimento della saturazione; oltre tale punto permane zucchero non disciolto a contatto con la soluzione. Osservando a scala macroscopica, dopo un certo tempo la quantità di solido residuo non varia più: la concentrazione del soluto in soluzione si è stabilizzata. A livello microscopico, tuttavia, le molecole lasciano continuamente la superficie del solido per entrare in soluzione, mentre un numero uguale di molecole in soluzione ritorna alla fase solida. La condizione di equilibrio è dunque caratterizzata da flussi opposti di uguale intensità:
r_{\text{diss}} = r_{\text{prec}}
La rappresentazione con doppia freccia comunica simultaneamente che:
- il processo può procedere in entrambi i sensi, dal solido alla soluzione e viceversa;
- si è raggiunta una condizione stazionaria di equilibrio tra le due direzioni;
- l’equilibrio è dinamico, poiché gli scambi molecolari continuano pur mantenendo costanti le quantità globali.
Sintesi di NH3 da N2 e H2
Alla temperatura elevata di circa 500 °C, in una miscela di azoto molecolare (N₂) e idrogeno (H₂) si verificano urti efficaci capaci di rompere i legami N≡N e H–H; gli atomi si riarrangiano formando ammoniaca (NH₃):
\( \mathrm{N_2(g) + 3H_2(g) \rightleftharpoons 2NH_3(g)} \)
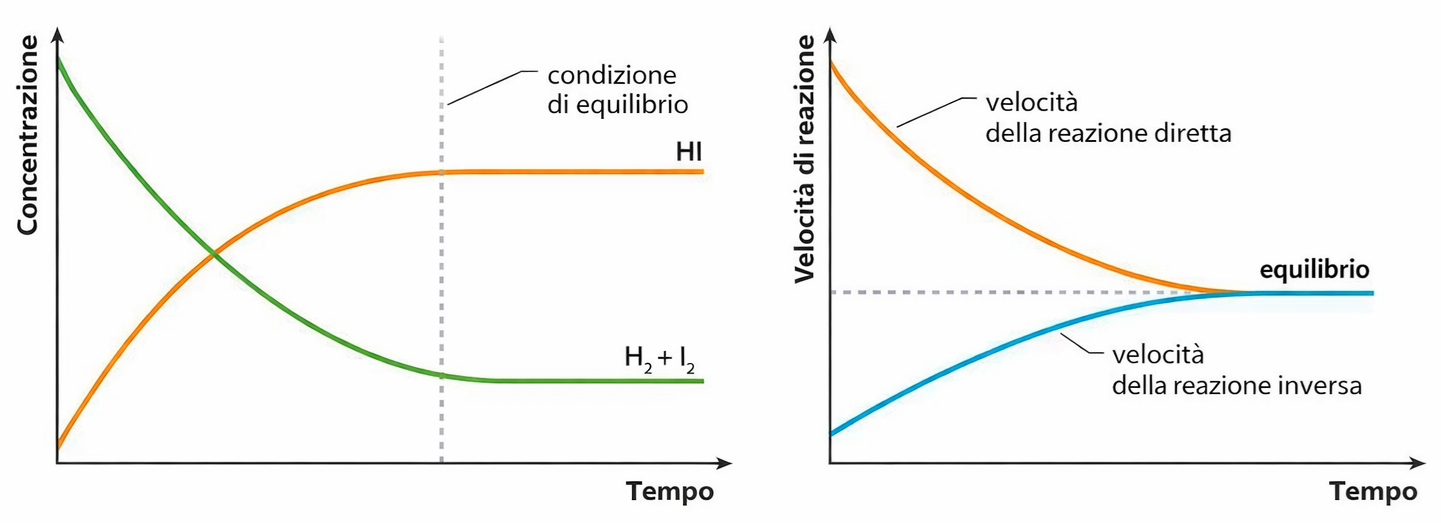
Se si parte da soli reagenti, la velocità della reazione diretta è inizialmente elevata, poiché le concentrazioni di N₂ e H₂ sono alte; con l’avanzare della reazione tali concentrazioni diminuiscono mentre aumenta quella dell’ammoniaca, che rende via via più probabile la reazione inversa di decomposizione. All’equilibrio, le due velocità opposte si eguagliano: la formazione e il consumo di NH₃ procedono alla stessa velocità, e così pure il consumo e la rigenerazione di N₂ e H₂. Le concentrazioni non cambiano nel tempo, pur in presenza di trasformazioni continue, cioè si realizza un equilibrio dinamico. L’andamento temporale delle velocità della reazione diretta e di quella inversa è rappresentato in (Figura 04.09-01). Per sistemi come quello N₂/H₂/NH₃ è utile definire una costante di equilibrio in termini di concentrazioni molari, \( K_c \), che collega le concentrazioni delle specie all’equilibrio:
\[
K_c = \frac{[\mathrm{NH_3}]^2}{[\mathrm{N_2}] \,[\mathrm{H_2}]^3}
\]
Per fasi gassose si impiega spesso la forma in termini di pressioni parziali, \( K_p \). Le due costanti sono legate dalla relazione generale:
\[
K_p = K_c \,(RT)^{\Delta n}
\]
con \( \Delta n = \) moli gassose dei prodotti − moli gassose dei reagenti (per la reazione di sintesi dell’ammoniaca, \( \Delta n = 2 - 4 = -2 \)).
La direzione spontanea dell’evoluzione da uno stato qualunque è diagnosticata dal quoziente di reazione \( Q_c \), definito come per \( K_c \) ma con concentrazioni istantanee: se \( Q_c < K_c \) il sistema evolve verso destra (formazione di NH₃), se \( Q_c > K_c \) evolve verso sinistra (decomposizione di NH₃), mentre \( Q_c = K_c \) identifica la condizione di equilibrio.
Per una reazione chimica generica all’equilibrio, rappresentata da:
aA + bB ⇌ cC + dD
dove A e B sono i reagenti, C e D i prodotti e a, b, c, d i coefficienti stechiometrici dell’equazione bilanciata, la formulazione più rigorosa della costante di equilibrio utilizza le attività:
\[ K = \prod_{i} a_i^{\nu_i} \]
dove \(a_i\) è l’attività del componente i-esimo e \(\nu_i\) è il coefficiente stechiometrico (positivo per i prodotti, negativo per i reagenti). In condizioni in cui le deviazioni dall’idealità sono trascurabili, le attività possono essere approssimate con:
concentrazioni molari per soluti in soluzione ideale, \(a_i \approx \frac{[i]}{c^\circ}\) con \(c^\circ = 1\,\text{mol L}^{-1}\);
pressioni parziali per gas ideali, \(a_i \approx \frac{p_i}{p^\circ}\) con \(p^\circ = 1\,\text{bar}\).
In tali condizioni operative si usano spesso le forme pratiche:
\(K_c = \dfrac{[C]^c [D]^d}{[A]^a [B]^b}\) per concentrazioni molari, e \(K_p = \dfrac{(p_C)^c (p_D)^d}{(p_A)^a (p_B)^b}\) per pressioni parziali. Le espressioni corrette richiedono l’equazione chimica completa e bilanciata, poiché i coefficienti stechiometrici compaiono come esponenti nell’espressione di \(K\). La relazione tra le due forme per sistemi gassosi è:
\[ K_p = K_c (RT)^{\Delta n} \quad \text{con} \quad \Delta n = (\text{moli totali di gas nei prodotti}) - (\text{moli totali di gas nei reagenti}). \]
Per la sintesi dell’ammoniaca, bilanciata come N\(_2\)(g) + 3 H\(_2\)(g) ⇌ 2 NH\(_3\)(g), si ottiene:
\(K_c = \dfrac{[\text{NH}_3]^2}{[\text{N}_2][\text{H}_2]^3}\).
Il valore di \(K\) dipende unicamente dalla temperatura: a composizione iniziale variabile, quando il sistema raggiunge l’equilibrio il rapporto dato dall’espressione di \(K\) risulta invariabile alla temperatura fissata. Per confronto fra reazioni diverse, i valori in letteratura sono spesso riportati a 25 °C. In notazione moderna, la costante di equilibrio è un numero adimensionale perché definita su attività normalizzate rispetto a stati standard; quando si usano molarità o pressioni parziali, l’assenza di unità deriva dalla divisione per gli opportuni standard.
Nell’espressione di \(K\) compaiono solo le specie la cui concentrazione può variare: soluti e gas. I solidi puri e i liquidi puri hanno attività unitaria, dunque sono omessi da \(K\). In molte reazioni in soluzione, il solvente è un liquido puro in grande eccesso: la sua attività rimane approssimativamente 1 e non entra nel calcolo della costante.
Significato della costante di equilibrio
La doppia freccia segnala che, all’equilibrio, reagenti e prodotti coesistono in proporzioni determinate. Il valore numerico di \(K\) fornisce un’indicazione immediata della posizione dell’equilibrio:
- \(K > 1 \times 10^{2}\): l’equilibrio è spostato verso i prodotti, che risultano predominanti;
- \(K < 1 \times 10^{-2}\): l’equilibrio è spostato verso i reagenti, che prevalgono nella miscela;
- \(K\) compreso tra \(1 \times 10^{-2}\) e \(1 \times 10^{2}\): reagenti e prodotti sono presenti in quantità comparabili.
Questa informazione è essenziale nello studio di processi chimici e biochimici, in chimica ambientale e in sintesi industriale, perché consente di prevedere se una data trasformazione, a temperatura fissata, fornirà conversioni apprezzabili.
Determinazione sperimentale della costante di equilibrio
Il valore di \(K\) si ricava da misure sperimentali. Si lascia procedere il sistema fino al raggiungimento di concentrazioni costanti di tutte le specie, quindi si determina la concentrazione molare o la pressione parziale di ciascun componente con metodi analitici appropriati (ad esempio spettrofotometria UV-Vis, gascromatografia, titolazioni). Sostituendo questi valori nell’espressione di \(K\), si ottiene la costante alla temperatura considerata.
Esempio didattico: per l’equilibrio Fe³⁺(aq) + SCN⁻(aq) ⇌ FeSCN²⁺(aq), si prepara una soluzione tampone e si misura l’assorbanza a una lunghezza d’onda in cui assorbe solo il complesso. Dal coefficiente di estinzione molare si ricava [FeSCN²⁺]; per bilancio di massa si stimano le concentrazioni residue di Fe³⁺ e SCN⁻. Inserendo i dati in \(K_c = \frac{[\text{FeSCN}^{2+}]}{[\text{Fe}^{3+}][\text{SCN}^{-}]}\) si calcola \(K_c\).
Conoscendo \(K\), si possono prevedere concentrazioni all'equilibrio a partire da condizioni iniziali diverse. È utile introdurre il quoziente di reazione: \(Q = \dfrac{[C]^c [D]^d}{[A]^a [B]^b}\), che ha la stessa forma di \(K\) ma con concentrazioni istantanee. Se \(Q < K\), la reazione procede in senso diretto; se \(Q > K\), in senso inverso; se \(Q = K\), il sistema è all'equilibrio. Esempio numerico: l'equilibrio N₂O₄(g) ⇌ 2 NO₂(g) ha \(K_c = 0,25\) a una certa temperatura. In un recipiente da 1,0 L si introducono 0,10 mol di N₂O₄ e 0 mol di NO₂. Indichiamo con x la quantità dissociata: [N₂O₄] = 0,10 − x, [NO₂] = 2x. All'equilibrio: \(K_c = \dfrac{(2x)^2}{0,10 - x} = 0,25\). Da cui \( \dfrac{4x^2}{0,10 - x} = 0,25 \Rightarrow 4x^2 = 0,25(0,10 - x) \Rightarrow 4x^2 + 0,25x - 0,025 = 0\). La soluzione fisicamente accettabile fornisce \(x \approx 0,070\,\text{mol L}^{-1}\). Quindi [NO₂] ≈ 0,140 M e [N₂O₄] ≈ 0,030 M.
Secondo il principio di Le Chatelier, un sistema all'equilibrio reagisce a una perturbazione esterna (variazione di concentrazione, pressione, volume o temperatura) spostando la composizione in modo da controbilanciare la perturbazione stessa. In termini di quoziente di reazione, la perturbazione porta \(Q \neq K\); l'evoluzione del sistema prosegue fino a ripristinare la condizione \(Q = K\).
Per la reazione N₂(g) + 3 H₂(g) ⇌ 2 NH₃(g):
- aggiungere NH₃ aumenta il numeratore di \(Q\), portando \(Q > K\); il sistema reagisce consumando NH₃ e rigenerando N₂ e H₂ (spostamento verso sinistra);
- rimuovere NH₃ rende \(Q < K\); la reazione procede a destra per ricostituire il prodotto;
- un aumento di [H₂] o [N₂] diminuisce \(Q\); l'equilibrio si sposta verso destra formando più NH₃.
Influenza delle concentrazioni
A volume costante, immettere o sottrarre una specie modifica la sua concentrazione e perturba l'equilibrio (Figura 04.09-02). La regola operativa è:
- aggiungere una specie sposta l'equilibrio nel verso che la consuma;
- rimuovere una specie sposta l'equilibrio nel verso che la rigenera;
- l'analisi con \(Q\) consente di prevedere il verso dell'evoluzione: \(Q > K\) implica spostamento a sinistra, \(Q < K\) implica spostamento a destra.
Temperatura e calore: effetti sull'equilibrio
La temperatura modifica il valore di \(K\). Una trattazione termodinamica porta all'equazione di van ’t Hoff:
\[
\frac{d \ln K}{dT} = \frac{\Delta H^\circ}{R T^{2}}.
\]
Per reazioni esotermiche (\(\Delta H^\circ < 0\)), \(K\) diminuisce all'aumentare di T; per reazioni endotermiche (\(\Delta H^\circ > 0\)), \(K\) cresce con T.
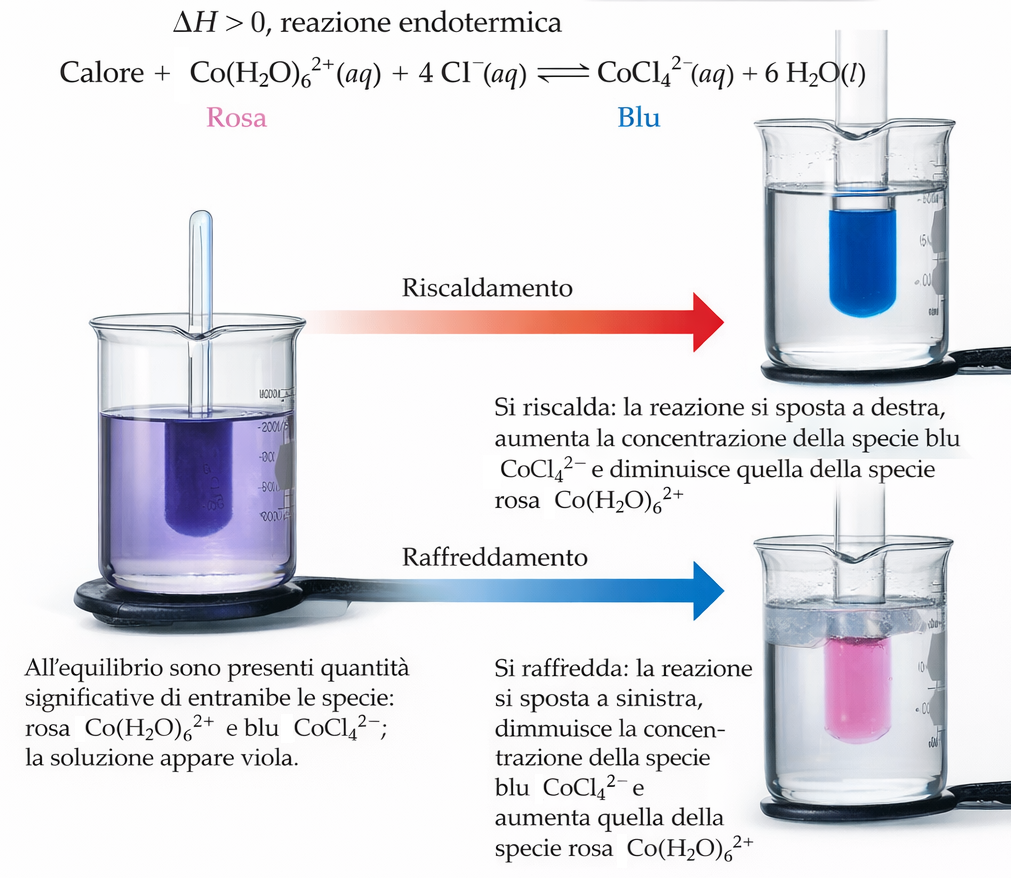
Un'interpretazione equivalente considera il calore come specie: per N₂(g) + 3 H₂(g) ⇌ 2 NH₃(g) + calore, un aumento di temperatura “aggiunge” prodotto, favorendo la direzione inversa (spostamento a sinistra) e riducendo \(K\).
L'abbassamento della temperatura favorisce la formazione di NH₃ e aumenta \(K\).
Per una reazione endotermica come N₂O₄(g) ⇌ 2 NO₂(g) (\(\Delta H^\circ > 0\) nel verso di dissociazione), un incremento di temperatura sposta l'equilibrio a destra, incrementando la frazione di NO₂, mentre una riduzione di temperatura sposta a sinistra.
La (Figura 04.09-03) illustra come la temperatura influenzi in modo marcato la posizione dell'equilibrio.
Pressione e volume: conseguenze sull'equilibrio
Variazioni di pressione o volume rilevano solo quando sono coinvolti gas, poiché solidi e liquidi sono praticamente incomprimibili. Per sistemi gassosi ideali, un aumento di pressione (o una diminuzione di volume) favorisce il verso che riduce il numero totale di moli gassose; viceversa, una diminuzione di pressione (o aumento di volume) favorisce il verso che aumenta il numero di moli gassose.
Nell'equilibrio N2(g) + 3 H2(g) ? 2 NH3(g), da 4 moli gassose a 2 moli: comprimere il sistema sposta la composizione verso destra, aumentando la resa di NH3. Espandere il volume ha l'effetto opposto, favorendo la dissociazione.
Per contro, nella decomposizione 2 HI(g) ? H2(g) + I2(g) il numero di moli gassose ? lo stesso in reagenti e prodotti; una variazione di pressione o volume non altera la posizione dell'equilibrio.
Ulteriori considerazioni utili:
- aggiunta di un gas inerte a volume costante non modifica le pressioni parziali delle specie reattive, quindi non sposta l'equilibrio;
- aggiunta di un gas inerte a pressione costante comporta un aumento del volume e una diminuzione delle pressioni parziali delle specie, con effetto analogo a un'espansione; l'equilibrio si sposta verso il lato con più moli gassose;
- per sistemi non ideali, occorre sostituire le pressioni parziali con le fugacità, mantenendo invariati i principi generali.
Ruolo dei catalizzatori
I catalizzatori non modificano la posizione dell'equilibrio nè il valore di \(K\), perché abbassano in egual misura le energie di attivazione delle reazioni diretta e inversa. L'effetto osservabile è la riduzione del tempo necessario a raggiungere l'equilibrio. Nella sintesi dell'ammoniaca, un catalizzatore eterogeneo a base di ferro promuove le velocità di entrambe le direzioni senza alterare la composizione di equilibrio.
La termodinamica stabilisce la relazione tra energia libera di Gibbs e composizione del sistema:
\[ \Delta G = \Delta G^\circ + RT \ln Q. \]
All'equilibrio, \(\Delta G = 0\) e \(Q = K\), per cui:
\[ \Delta G^\circ = -RT \ln K. \]
Questa identità connette la spontaneità standard di una reazione al corrispondente valore di \(K\) alla stessa temperatura: valori di \(K\) molto grandi corrispondono a \(\Delta G^\circ\) molto negativi; valori di \(K\) molto piccoli implicano \(\Delta G^\circ\) positivo. La (Tabella 04.09-01) riporta la corrispondenza quantitativa tra \(\Delta G^\circ\) e \(K\).
Nel contesto biochimico si usa spesso \(\Delta G^{\circ'}\), definita a pH 7,0, per tener conto dello stato standard fisiologico: le relazioni formali restano identiche, con \(K\) sostituito da \(K'\) calcolato nelle condizioni standard biochimiche. Il collegamento tra equilibrio e energia libera consente inoltre di comprendere la strategia della ?coppia? di reazioni: processi con \(\Delta G^\circ > 0\) possono procedere in avanti se accoppiati a trasformazioni fortemente esoergoniche (ad esempio l'idrolisi dell'ATP), ottenendo un \(\Delta G\) complessivo negativo.
Sotto il profilo applicativo, l'industria sfrutta la dipendenza di \(K\) dalla temperatura e il principio di Le Chatelier impostando condizioni di compromesso: per il processo Haber-Bosch si adottano alte pressioni per favorire la formazione di NH3, temperature intermedie per bilanciare resa ed efficienza cinetica, e catalizzatori efficienti per garantire velocità adeguate senza alterare l'equilibrio.
Energia libera standard e costante di equilibrio
| Keq | ln Keq | ΔG° | Considerazioni |
|---|---|---|---|
| > 1 | Positivo | Negativo | All’equilibrio sono favoriti i prodotti |
| = 1 | 0 | 0 | Reagenti e prodotti sono ugualmente favoriti |
| < 1 | Negativo | Positivo | All’equilibrio sono favoriti i reagenti |
| Molto > 1 | Grande | Molto negativo | Reazione praticamente completa, procede quasi interamente verso i prodotti |
| Molto < 1 | Molto negativo | Molto positivo | Reazione non spontanea, resta spostata fortemente verso i reagenti |
| Legame tra ΔG⁰ e Keq descritto dall’equazione ΔG⁰ = –RT ln Keq. | |||