Dosimetria
Definizione
Si fornisce una sintesi dei principali effetti delle radiazioni ionizzanti sui sistemi viventi, con attenzione agli aspetti fisici e biologici essenziali. Un utile punto di partenza è la stima dell’effetto puramente termico: se 1 gray viene depositato in 1 kg di acqua (che costituisce la quota prevalente dei tessuti biologici), l’incremento di temperatura è dato dal rapporto tra la dose assorbita e il calore specifico dell’acqua. Con il calore specifico dell’acqua pari a \(c_{\mathrm{H_2O}} \approx 4180\ \mathrm{J\,kg^{-1}\,K^{-1}}\), si ha:
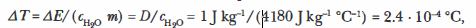
ovvero un innalzamento termico dell’ordine di \(2,4 \times 10^{-4}\ \mathrm{K}\), trascurabile ai fini di un effetto macroscopico. L’assenza di un segnale termico apprezzabile spiega perché l’esposizione non sia percepita dai sensi, pur potendo arrecare danni significativi: l’energia non è distribuita uniformemente, ma concentrata lungo le tracce ionizzanti, con trasferimenti locali sufficienti a rompere legami in molecole critiche.
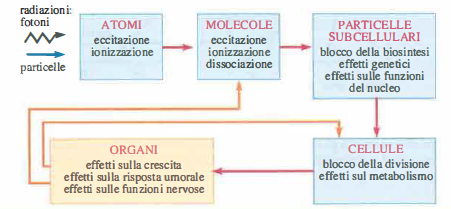
Quando fotoni, elettroni, neutroni o particelle α attraversano la materia, la ionizzazione e l’eccitazione atomico-molecolare dipendono dalla natura della radiazione e dalla sua energia, nonché dalla composizione del mezzo. Nei tessuti acquosi l’azione indiretta è preminente: l’radiolisi dell’acqua genera specie reattive dell’ossigeno (ROS) e radicali liberi con elettroni spaiati, come \(\mathrm{OH\cdot}\), \(\mathrm{O_2^{\cdot -}}\), \(\mathrm{H\cdot}\), altamente reattivi verso lipidi, proteine e acidi nucleici. Poiché l’acqua rappresenta oltre il 65% della massa dei tessuti, questi processi sono ubiqui. Gli eventi fisico-chimici iniziano entro tempi inferiori al nanosecondo; le alterazioni metaboliche e funzionali diventano rilevabili a livello cellulare su scale temporali di minuti-ore (Figura 07.27-01).
Il danno biologico può tradursi in disfunzioni cellulari e tissutali, con compromissione d’organo fino all’exitus, oppure in modificazioni ereditarie del materiale genetico (mutazioni) secondo lo schema a blocchi di (Figura 07.27-02). Si distinguono:
- danni stocastici, la cui probabilità aumenta con la dose senza soglia nota, e che includono effetti somatici (sull’individuo esposto) e genetici (sulla progenie), oggi ritenuti di minore entità rispetto al passato per le gonadi, come riflesso nella riduzione del corrispondente fattore di ponderazione tissutale \(w_T\) (Tabella 07.27-01);
- reazioni tissutali (danni deterministici), per le quali esiste una dose-soglia al di sopra della quale aumentano gravità e frequenza, con tempi di latenza tipicamente di giorni, settimane o mesi, in netto contrasto con la possibile latenza pluriennale dei danni stocastici.
La risposta biologica dipende dalla dose assorbita, dalla densità di ionizzazione della radiazione (LET), dal tasso di dose e dall’ossigenazione tissutale. Radiazioni ad alto LET (ad es. particelle α) inducono lesioni complesse (cluster di danni e rotture a doppio filamento del DNA) con elevata efficacia biologica relativa, mentre radiazioni a basso LET (fotoni X/γ, elettroni) agiscono prevalentemente per via indiretta attraverso ROS. L’ossigeno molecolare amplifica il danno fissando chimicamente le lesioni (effetto ossigeno), rendendo i tessuti ipossici più radioresistenti. Anche il ciclo cellulare influenza la radiosensibilità: cellule in fase G2/M risultano mediamente più sensibili.
La diversa suscettibilità di organi e tessuti è riassunta dai fattori di ponderazione tissutali \(w_T\) (Tabella 07.27-01), che concorrono alla definizione di dose efficace per la radioprotezione. In ambito protettivo i limiti di dose sono stabiliti proprio in funzione della radiosensibilità relativa (Tabella 07.27-02). Tra gli organi più radiosensibili si annoverano il midollo emopoietico, il colon, il polmone, lo stomaco e la mammella (Tabella 07.27-01). A parità di dose totale, il tasso di dose è cruciale: una somministrazione frazionata o a basso rateo consente una maggiore riparazione subletale e può ridurre le reazioni tissutali rispetto a un’esposizione acuta di breve durata.
Gli esseri viventi sono costantemente esposti a sorgenti naturali: radiazione cosmica, radionuclidi terrestri e isotopi incorporati nell’organismo. Ne derivano lesioni spontanee al DNA controbilanciate da sistemi di riparazione quali riparo per escissione di basi, riparo per escissione di nucleotidi, ricombinazione omologa e giunzione delle estremità non omologhe. L’esistenza di tali meccanismi è alla base del razionale radioterapico, in cui il frazionamento di dose sfrutta differenze di riparo tra cellule sane e neoplastiche. Le dosi efficaci per le principali componenti dell’esposizione naturale sono riportate in (Tabella 07.27-03).
| Organo / Tessuto | Fattore di ponderazione wT | Nota |
|---|---|---|
| Gonadi | 0.08 | Sensibilità ridotta rispetto a dati precedenti (aggiornamento post-2007). |
| Midollo osseo emopoietico rosso | 0.12 | Elevata radiosensibilità, rischio di leucemie e aplasie. |
| Colon | 0.12 | Rischio elevato di neoplasie radio-indotte. |
| Polmone, vie respiratorie toraciche | 0.12 | Alta radiosensibilità, frequenti complicanze in radioterapia toracica. |
| Stomaco | 0.12 | Tessuto radiosensibile per rischio di tumori secondari. |
| Vescica | 0.04 | Sensibilità moderata. |
| Mammella | 0.12 | Considerata ad alta radiosensibilità (importanza oncologica). |
| Fegato | 0.04 | Resistenza moderata, rischio secondario in esposizioni diffuse. |
| Esofago | 0.04 | Radiosensibilità intermedia. |
| Tiroide | 0.04 | Particolarmente rilevante nei soggetti pediatrici. |
| Pelle | 0.01 | Danno principale: radiodermiti. |
| Superficie ossea | 0.01 | Coinvolgimento limitato, ma rischio a lungo termine. |
| Cervello | 0.01 | Relativamente radioresistente. |
| Ghiandole salivari | 0.01 | Possibile xerostomia in radioterapia testa-collo. |
| Organi e tessuti rimanenti | 0.12 | Valore medio assegnato al “resto” dei tessuti. |
| Rene | 0.02 | Radiosensibilità bassa, ma rischio di nefropatia da radiazioni. |
| Intestino tenue | 0.08 | Moderata radiosensibilità, importante in radioterapia addominale. |
| Pancreas | 0.02 | Sensibilità relativamente bassa. |
| Ovaie / Testicoli (dettaglio) | 0.08 | Rischio di infertilità e mutazioni genetiche. |
Fattori di peso del tessuto (WT)
Coefficienti che esprimono la sensibilità relativa di organi e tessuti agli effetti delle radiazioni ionizzanti.
| Organo / Tessuto | Fattore di ponderazione wT | Nota |
|---|---|---|
| Gonadi | 0.08 | Sensibilità ridotta rispetto a dati precedenti (aggiornamento post-2007). |
| Midollo osseo emopoietico rosso | 0.12 | Elevata radiosensibilità, rischio di leucemie e aplasie. |
| Colon | 0.12 | Rischio elevato di neoplasie radio-indotte. |
| Polmone, vie respiratorie toraciche | 0.12 | Alta radiosensibilità, frequenti complicanze in radioterapia toracica. |
| Stomaco | 0.12 | Tessuto radiosensibile per rischio di tumori secondari. |
| Vescica | 0.04 | Sensibilità moderata. |
| Mammella | 0.12 | Considerata ad alta radiosensibilità (importanza oncologica). |
| Fegato | 0.04 | Resistenza moderata, rischio secondario in esposizioni diffuse. |
| Esofago | 0.04 | Radiosensibilità intermedia. |
| Tiroide | 0.04 | Particolarmente rilevante nei soggetti pediatrici. |
| Pelle | 0.01 | Danno principale: radiodermiti. |
| Superficie ossea | 0.01 | Coinvolgimento limitato, ma rischio a lungo termine. |
| Cervello | 0.01 | Relativamente radioresistente. |
| Ghiandole salivari | 0.01 | Possibile xerostomia in radioterapia testa-collo. |
| Organi e tessuti rimanenti | 0.12 | Valore medio assegnato al “resto” dei tessuti. |
| Rene | 0.02 | Radiosensibilità bassa, ma rischio di nefropatia da radiazioni. |
| Intestino tenue | 0.08 | Moderata radiosensibilità, importante in radioterapia addominale. |
| Pancreas | 0.02 | Sensibilità relativamente bassa. |
| Ovaie / Testicoli (dettaglio) | 0.08 | Rischio di infertilità e mutazioni genetiche. |
Fattori di peso del tessuto (WT)
Coefficienti che esprimono la sensibilità relativa di organi e tessuti agli effetti delle radiazioni ionizzanti.
| Categoria di soggetti | Dose efficace (mSv/anno) | Dose equivalente estremità (mSv/anno) | Dose equivalente pelle (mSv/anno) | Dose equivalente cristallino (mSv/anno) | Note |
|---|---|---|---|---|---|
| Lavoratori professionalmente esposti | 20 | 500 | 500 | 20 | Valori medi su base quinquennale; include medici nucleari, radiologi, tecnici di radiologia |
| Popolazione generale | 1 | — | 50 | 15 | Protezione della collettività; dose di riferimento ambientale |
| Nascituro (durante la gravidanza) | 1 (per tutta la gestazione) | — | — | — | Valore di protezione del feto; applicato alle lavoratrici esposte |
Limiti annuali di dose individuale
Valori massimi di esposizione a radiazioni ionizzanti stabiliti per garantire la protezione della salute.
| Organo / Tessuto | Fattore di ponderazione wT | Nota |
|---|---|---|
| Gonadi | 0.08 | Sensibilità ridotta rispetto a dati precedenti (aggiornamento post-2007). |
| Midollo osseo emopoietico rosso | 0.12 | Elevata radiosensibilità, rischio di leucemie e aplasie. |
| Colon | 0.12 | Rischio elevato di neoplasie radio-indotte. |
| Polmone, vie respiratorie toraciche | 0.12 | Alta radiosensibilità, frequenti complicanze in radioterapia toracica. |
| Stomaco | 0.12 | Tessuto radiosensibile per rischio di tumori secondari. |
| Vescica | 0.04 | Sensibilità moderata. |
| Mammella | 0.12 | Considerata ad alta radiosensibilità (importanza oncologica). |
| Fegato | 0.04 | Resistenza moderata, rischio secondario in esposizioni diffuse. |
| Esofago | 0.04 | Radiosensibilità intermedia. |
| Tiroide | 0.04 | Particolarmente rilevante nei soggetti pediatrici. |
| Pelle | 0.01 | Danno principale: radiodermiti. |
| Superficie ossea | 0.01 | Coinvolgimento limitato, ma rischio a lungo termine. |
| Cervello | 0.01 | Relativamente radioresistente. |
| Ghiandole salivari | 0.01 | Possibile xerostomia in radioterapia testa-collo. |
| Organi e tessuti rimanenti | 0.12 | Valore medio assegnato al “resto” dei tessuti. |
| Rene | 0.02 | Radiosensibilità bassa, ma rischio di nefropatia da radiazioni. |
| Intestino tenue | 0.08 | Moderata radiosensibilità, importante in radioterapia addominale. |
| Pancreas | 0.02 | Sensibilità relativamente bassa. |
| Ovaie / Testicoli (dettaglio) | 0.08 | Rischio di infertilità e mutazioni genetiche. |
Fattori di peso del tessuto (WT)
Coefficienti che esprimono la sensibilità relativa di organi e tessuti agli effetti delle radiazioni ionizzanti.
| Fonte di esposizione | Dose efficace media (mSv/anno) |
|---|---|
| Radiazione terrestre naturale | 0,6 |
| Radiazioni cosmiche | 0,4 |
| Ingestione di radionuclidi con alimenti | 0,3 |
| Ambienti interni (principalmente radon) | 2,0 |
Totale radiazione naturale | 3,3 |
| Esposizioni mediche (Italia, media) | 1,2 |
| Produzione di energia nucleare | 0,0002 |
| Test nucleari atmosferici storici | 0,005 |
| Incidente di Chernobyl (residuale) | 0,002 |
| Incidenti nucleari recenti (Fukushima) | trascurabile |
Totale generale | 4,5 |
| Viaggi aerei frequenti (piloti, assistenti) | 2–3 |
| Abitazioni in zone con elevato radon | 5–10 |
| Terapie mediche con radiazioni (oncologia) | fino a centinaia di mSv (localizzati) |
Dose efficace annua della popolazione italiana
Quantità media di radiazioni ionizzanti assorbita annualmente per effetto di sorgenti naturali e artificiali.
L’evoluzione temporale del danno a carico di organi e apparati segue le fasi descritte in (Figura 07.27-01) e si articola secondo lo schema causale di (Figura 07.27-02). Gli effetti clinicamente rilevanti dipendono dalla dose, dalla porzione corporea irradiata e dal tempo di esposizione. In caso di irradiazione acuta dell’intero organismo, la sequenza tipica comprende una fase prodromica, un intervallo di latenza e la fase a manifestazione conclamata, con quadri sindromici differenti a seconda del sistema prevalente interessato. Esempi di effetti osservabili in relazione alla dose acuta assorbita sull’intero corpo sono sintetizzati in (Tabella 07.27-04), mentre l’andamento nel tempo degli esiti sull’essere umano è illustrato in (Figura 07.27-03).
Alcune considerazioni di ordine pratico:
- le reazioni cutanee deterministiche compaiono tipicamente oltre soglie dell’ordine di alcuni gray, con gravità crescente se la dose è elevata o somministrata ad alto tasso di dose;
- l’irradiazione parziale può limitare la severità della sindrome sistemica ma causare danni locali marcati (cute, cristallino, midollo), in funzione del volume irradiato;
- la frazionazione della dose e gli intervalli temporali tra le esposizioni influenzano la riparazione subletale, la ripopolazione cellulare e la riossigenazione, modulando la risposta tissutale.
| Soggetto / tessuto | Dose efficace (Sv) | Effetto biologico osservato |
|---|---|---|
| Uomo | 0,25 | Nessuna manifestazione clinica rilevante |
| Uomo | 0,25 – 1 | Minime alterazioni ematologiche (formula leucocitaria), lieve incremento rischio leucemie |
| Uomo | 1 – 2 | Nausea, affaticamento, modifiche marcate della formula leucocitaria, emorragie lievi, rischio aumentato di leucemie e anomalie genetiche |
| Uomo | 2 – 3 | Emorragie significative, shock, prostratazione |
| Uomo | 4 – 5 | Mortalità in circa il 30% dei casi |
| Uomo | 6 – 7 | Mortalità in circa il 60% dei casi |
| Uomo | 8 – 10 | Mortalità pressoché totale (≈100%) |
| Rana | ~7 | Mortalità nel 50% dei soggetti |
| Insetti | ~600 | Mortalità nel 50% dei soggetti |
| Batteri | ~200 | Mortalità nel 50% dei soggetti |
| Cellule tumorali | ~4 | Mortalità nel 50% dei casi cellulari |
| Esposizione radiologia torace | 0,1 mSv | Nessun rischio clinico rilevante, dose diagnostica |
| Esposizione TC addome | ~10 mSv | Dose diagnostica moderata, incremento statistico del rischio oncologico a lungo termine |
| Limite esposizione lavoratori | 20 mSv/anno (media su 5 anni) | Livello massimo raccomandato per operatori esposti (radiologi, tecnici di radiologia, ecc.) |
Conseguenze dell’irraggiamento acuto
Reazioni biologiche precoci causate da un assorbimento rapido e massivo di radiazioni ionizzanti.
Dosi elevate di radiazioni ionizzanti, in particolare fotoni γ emessi da sorgenti come il cobalto-60, sono impiegate per la riduzione microbica (sanificazione) o per la sterilizzazione, nel rispetto degli standard tecnici di convalida (ad esempio livelli di assicurazione di sterilità, SAL, pari a \(10^{-6}\), e metodiche di dosimetria e mappatura di dose conformi alla normativa di settore). La scelta della dose dipende dal bioburden, dal materiale e dall’obiettivo del trattamento:
- basso intervallo dosimetrico, circa 5–15 kGy, indicato per ottenere sterilità in prodotti o materie prime a bassa carica microbica oppure per la sanificazione quando è richiesta la sola riduzione di muffe e lieviti, come per tappi per bevande o contenitori alimentari;
- intervallo medio, approssimativamente 20–30 kGy, comunemente adottato per dispositivi medici monouso (ad esempio set di dialisi, medicazioni, siringhe), nonché per imballaggi farmaceutici e alimentari;
- dosi molto elevate, dell’ordine di 100 kGy, utilizzate non a fini microbiologici ma per modificare la struttura dei polimeri (reticolazione o scissione di catena, con variazione di proprietà meccaniche e termiche).
In alternativa o in combinazione si impiegano fasci di elettroni (\(\beta^{-}\)) generati da acceleratori: essi consentono alti tassi di dose e cicli produttivi rapidi, ma presentano limitazioni nella profondità di penetrazione, risultando adatti a materiali a bassa densità e spessore contenuto. La scelta tra γ e fascio elettronico considera penetrazione, uniformità di dose, sensibilità del materiale (ad esempio alterazioni del colore o della resistenza) e requisiti regolatori. Per garantire l’efficacia del processo sono necessari la qualificazione dell’impianto, la definizione della “dose minima garantita” al punto più sfavorito del prodotto e il monitoraggio dosimetrico di routine.