Distribuzioni di cariche elettriche: dipolo elettrico
Definizione
Si chiama dipolo elettrico un sistema costituito da due cariche puntiformi, uguali in modulo e opposte in segno, poste a distanza finita e non sovrapposte. Quando si osservano punti dello spazio a distanza molto maggiore della separazione \(d\) tra le cariche, il potenziale generato dalla coppia può essere descritto in prima approssimazione da un’unica espressione compatta, detta potenziale di dipolo elettrico. In tale regime “lontano”, i contributi delle due cariche tendono in gran parte a compensarsi, cosicché il potenziale risulta piccolo rispetto a quello dovuto a una singola carica di ugual modulo.
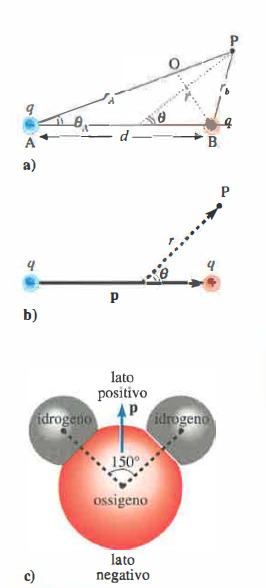
Per il calcolo esplicito del potenziale nel punto generico \(P\), si considerino due cariche \(+q\) e \(-q\) localizzate rispettivamente in \(B\) e in \(A\), come nello schema di riferimento (Figura 06.04-01). Sulla base della legge per il potenziale di una carica puntiforme (V(r) = \frac{Q}{4 \pi \varepsilon_0 \varepsilon_r} \frac{1}{r}), il potenziale totale in \(P\) si ottiene per sovrapposizione:
\[V(P) = \frac{q}{4\pi\varepsilon_o\varepsilon_r} \left(\frac{1}{r_B} - \frac{1}{r_A}\right) = \frac{q}{4\pi\varepsilon_o\varepsilon_r} \left(\frac{r_A - r_B}{r_A r_B}\right)\]
Nel limite asintotico \(r\gg d\), si impiegano le approssimazioni geometriche:
\[r_A - r_B \approx \overline{OA} = d \cos \theta_A \approx d \cos \theta\]
e inoltre:
\[r_A r_B \approx r^2.\]
Inserendole in (V(\text{P}) = \frac{q}{4 \pi \varepsilon_0 \varepsilon_r} \left( \frac{1}{r_B} - \frac{1}{r_A} \right) = \frac{q}{4 \pi \varepsilon_0 \varepsilon_r} \left( \frac{r_A - r_B}{r_A r_B} \right)) si ottiene:
\[V(P) = \frac{q d \cos\theta}{4\pi\varepsilon_o\varepsilon_r} \frac{1}{r^2} = \frac{1}{4\pi\varepsilon_o\varepsilon_r} \frac{1}{r^3} (\mathbf{p} \cdot \mathbf{r}),\]
Qui compare il prodotto scalare tra due vettori: \(\mathbf{p}\) e \(\mathbf{r}\). Il momento di dipolo elettrico \(\mathbf{p}\) ha modulo \(p=q\,d\), direzione lungo la congiungente delle due cariche e verso orientato dalla carica negativa a quella positiva. Il vettore \(\mathbf{r}\) è tracciato dal centro del dipolo (punto medio del segmento \(AB\)) verso il punto di osservazione \(P\). Poiché \(\mathbf{p}\!\cdot\!\mathbf{r}=p\,r\cos\theta\), il potenziale è proporzionale a \(\cos\theta\) e decresce come \(1/r^2\); il suo segno coincide con quello del prodotto scalare, risultando positivo quando \(P\) è “più vicino angolarmente” alla carica positiva e negativo nel semispazio prossimo alla carica negativa.
È utile sottolineare che, per distribuzioni globalmente neutre, il termine di dipolo rappresenta il primo contributo non nullo della espansione multipolare del potenziale a grande distanza: il termine monopolare (totale di carica) si annulla, il termine dipolare scala come \(1/r^2\), mentre il successivo contributo quadrupolare è più piccolo e scala tipicamente come \(1/r^3\). La validità dell’approssimazione dipolare richiede inoltre un mezzo omogeneo e isotropo con permettività relativa \(\varepsilon_r\) costante, nonché la condizione \(r\gg d\).
Molte strutture molecolari realizzano dipoli elettrici permanenti: la separazione tra i baricentri delle cariche elettroniche e nucleari produce un momento di dipolo statico (Tabella 06.04-01). Il caso dell’acqua è emblematico per le sue conseguenze fisico-chimiche e biologiche. L’unità del Sistema Internazionale per il momento di dipolo è il coulomb·metro (C·m); un’unità pratica assai diffusa in chimica fisica è il debye (Deb), pari a \(1\,\mathrm{Deb}\approx 3,336\cdot 10^{-30}\,\mathrm{C\cdot m}\).
Proprietà essenziali e note operative
- Legge di scala: il potenziale dipolare decresce come \(1/r^2\), più rapidamente del potenziale monopolare \(1/r\);
- Anisotropia angolare: la dipendenza \(\cos\theta\) implica massimi lungo la direzione di \(\mathbf{p}\) e annullamento sul piano equatoriale perpendicolare a \(\mathbf{p}\);
- Condizioni di applicabilità: l’approssimazione è affidabile per \(r\gg d\) in mezzi lineari e omogenei, con \(\varepsilon_r\) uniforme;
- Invarianza per traslazione di sistemi neutri: per una distribuzione a somma di carica nulla, \(\mathbf{p}=\sum_i q_i\,\mathbf{r}_i\) è, a meno di scarti d’ordine superiore, indipendente dall’origine scelta, purché si lavori nel regime di campo lontano;
- Unità di misura: \(p\) si esprime in C·m; conversione pratica con 1 Deb \(=3,336\cdot 10^{-30}\) C·m.
Esempio numerico distinto
Due cariche puntiformi \(+2,0\,\mathrm{nC}\) e \(-2,0\,\mathrm{nC}\) sono separate da \(d=1,0\,\mathrm{cm}\) in aria \((\varepsilon_r\simeq 1)\). Il momento di dipolo ha modulo \(p=q\,d=2,0\cdot 10^{-9}\,\mathrm{C}\times 1,0\cdot 10^{-2}\,\mathrm{m}=2,0\cdot 10^{-11}\,\mathrm{C\cdot m}\), pari a circa \(6,0\cdot 10^{18}\) Deb. A distanza \(r=1,0\,\mathrm{m}\) lungo la direzione di \(\mathbf{p}\) \((\theta=0)\), il potenziale vale \[ V\simeq \frac{1}{4\pi \varepsilon_0}\,\frac{p\cos\theta}{r^2}\approx 8,99\cdot 10^{9}\,\frac{\mathrm{V\,m}}{\mathrm{C}}\times \frac{2,0\cdot 10^{-11}\,\mathrm{C\cdot m}}{(1,0\,\mathrm{m})^2}\approx 0,18\,\mathrm{V}. \] L’ordine di grandezza conferma la riduzione del potenziale rispetto a quello di una singola carica dello stesso modulo alla medesima distanza.
| Molecola | Formula | Momento di dipolo (Coulomb·metro) | Momento di dipolo (debye) | Nota |
|---|---|---|---|---|
| Metano | CH₄ | zero | zero | Molecola apolare, gas naturale. |
| Cloroformio | CHCl₃ | 3.4 × 10⁻³⁰ | 1.02 | Solvente organico con lieve polarità. |
| Acqua | H₂O | 6.13 × 10⁻³⁰ | 1.84 | Molecola fortemente polare, fondamentale in tutti i processi biologici. |
| Metanolo | CH₃OH | 5.66 × 10⁻³⁰ | 1.70 | Solvente polare, utilizzato in laboratorio. |
| Etanolo | C₂H₅OH | 5.63 × 10⁻³⁰ | 1.69 | Molecola polare, impiegata in biologia e medicina come antisettico. |
| Nitrobenzene | C₆H₅NO₂ | 14.22 × 10⁻³⁰ | 4.27 | Molecola con elevata polarità, usata come riferimento sperimentale. |
| Ammoniaca | NH₃ | 4.90 × 10⁻³⁰ | 1.47 | Molecola polare, importante nei cicli metabolici. |
| Formaldeide | CH₂O | 7.36 × 10⁻³⁰ | 2.33 | Molecola polare, rilevante in biochimica come agente fissativo. |
| Acido acetico | CH₃COOH | 6.10 × 10⁻³⁰ | 1.83 | Molecola polare, presente nei processi metabolici (ciclo di Krebs). |
| Peptide (modello) | –NH–CO– | ~15 × 10⁻³⁰ | ~4.5 | I legami peptidici mostrano elevata polarità, cruciale nella struttura proteica. |
Momento di dipolo elettrico permanente di diverse molecole
Valori del dipolo elettrico intrinseco associato a varie molecole.