Determinazione sperimentale delle variazioni di energia nelle reazioni chimiche
Definizione
La determinazione del calore scambiato durante una trasformazione chimica è oggetto della calorimetria. Il principio operativo consiste nel rilevare la variazione di temperatura di una massa nota di acqua o di soluzione a contatto con il sistema reagente, posta in condizioni di isolamento termico. L’apparato impiegato è il calorimetro: esso non misura il calore direttamente, ma consente di ricavarlo dalla variazione di temperatura del mezzo circostante, nota la sua capacità termica. In prima approssimazione il calorimetro è trattato come un ambiente adiabatico: il sistema e il suo intorno scambiano calore tra loro, mentre gli scambi con l’esterno sono trascurabili.
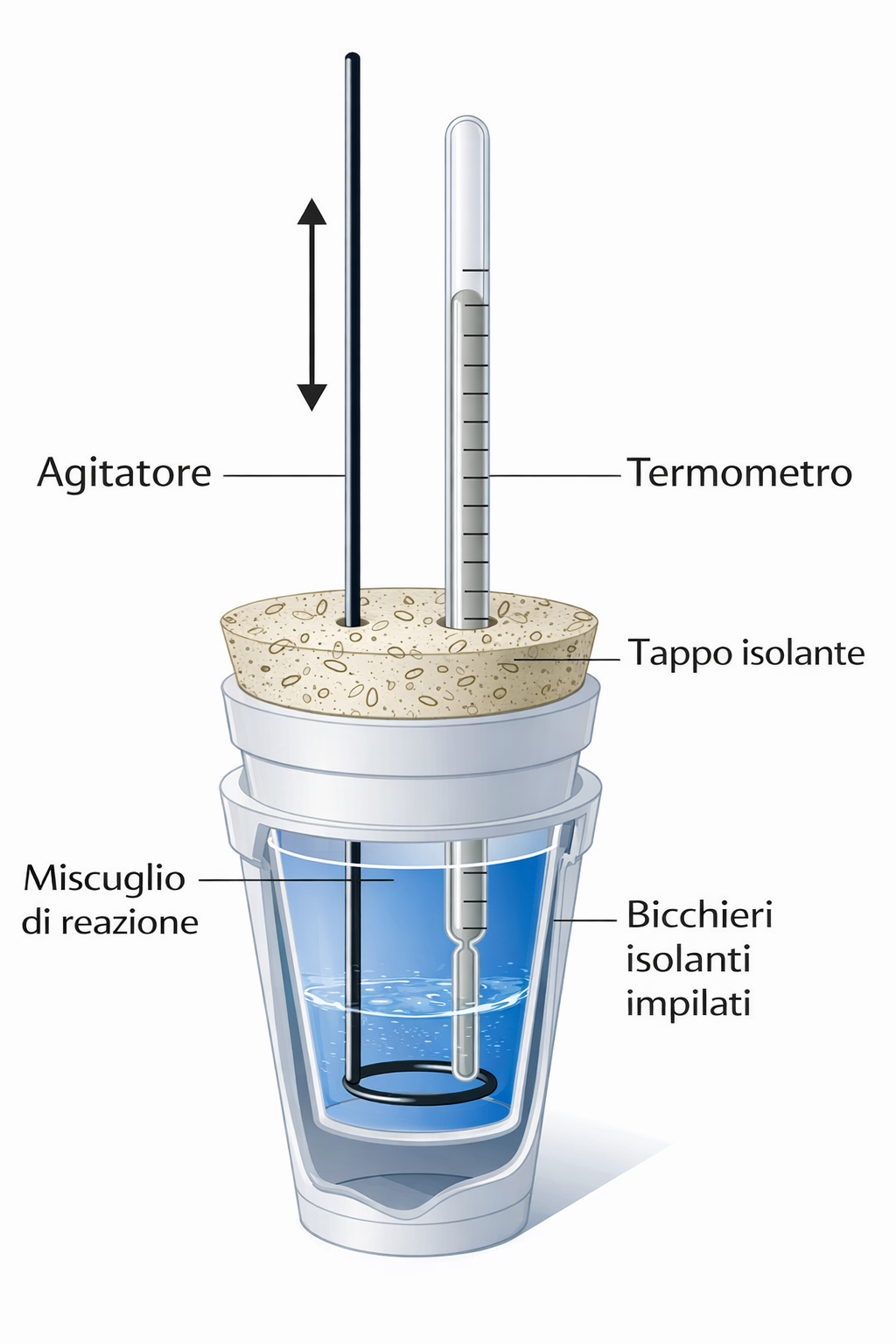
Un semplice ma efficace calorimetro da banco è una tazza in polistirolo espanso con coperchio e termometro (Figura 04.07-01). Il polistirolo riduce le perdite per conduzione e convezione; la misura del salto di temperatura della soluzione consente di stimare il calore liberato o assorbito dalla reazione. In condizioni di pressione atmosferica approssimativamente costante, il calore scambiato con la soluzione coincide con la variazione di entalpia del processo, \(q_p \approx \Delta H\), per reazioni in soluzione diluita.
Il calore specifico di una sostanza è la quantità di calore necessaria ad aumentare di 1 °C la temperatura di 1 g della sostanza. Per l’acqua, per definizione storica, \(c_{\text{H}_2\text{O}} \approx 1{,}00\ \text{cal}\ \text{g}^{-1}\ \text{°C}^{-1}\) (equivalente a \(4{,}184\ \text{J}\ \text{g}^{-1}\ \text{K}^{-1}\)). Se una massa \(m\) di soluzione con calore specifico medio \(c\) subisce una variazione di temperatura \(\Delta T = T_f - T_i\), il calore scambiato dall’ambiente (soluzione + recipiente) vale:
\[ q_{\text{sol}} = m\,c\,\Delta T. \]
Il segno del calore del sistema segue la convenzione termodinamica: per una reazione esotermica il sistema cede calore e \(q_{\text{reaz}} < 0\), mentre la soluzione si riscalda (\(\Delta T > 0\)); per una reazione endotermica il sistema assorbe calore e \(q_{\text{reaz}} > 0\), con corrispondente diminuzione della temperatura della soluzione.
In pratica, anche il contenitore e il termometro assorbono calore. Si introduce quindi la costante del calorimetro, \(C_{\text{cal}}\), tale che il calore assorbito dal dispositivo sia \(q_{\text{cal}} = C_{\text{cal}}\,\Delta T\). Il bilancio energetico diventa:
\[ \begin{aligned} q_{\text{reaz}} + q_{\text{sol}} + q_{\text{cal}} &= 0,\\ q_{\text{reaz}} &= -\big(m\,c\,\Delta T + C_{\text{cal}}\,\Delta T\big). \end{aligned} \]
La costante \(C_{\text{cal}}\) si determina per calibrazione, ad esempio mediante un riscaldatore elettrico di potenza nota o con una reazione a entalpia nota. Per soluzioni acquose diluite si assume spesso \(c \approx c_{\text{H}_2\text{O}}\) e densità \(1{,}00\ \text{g mL}^{-1}\), così da ricavare la massa dal volume:
- isolamento termico: minimizzare scambi di calore con l’ambiente esterno e correggere, se necessario, con \(C_{\text{cal}}\);
- miscele diluite: approssimare il calore specifico a quello dell’acqua e considerare trascurabile l’effetto di espansione;
- agitazione omogenea: garantire uniformità di temperatura nella soluzione;
- rilevazione accurata: registrare la temperatura iniziale e quella finale correggendo per eventuali derive strumentali.
Esempio numerico. In una tazza calorimetrica si mescolano 100,0 g di soluzione acquosa; la temperatura passa da 20,5 °C a 22,85 °C. Assumendo \(c = 4{,}184\ \text{J}\ \text{g}^{-1}\ \text{K}^{-1}\) e \(C_{\text{cal}} = 35,0\ \text{J}\ \text{K}^{-1}\), si ha \(\Delta T = 2,35\ \text{K}\). Allora: \[ q_{\text{sol}} = 100{,}0 \times 4{,}184 \times 2,35 = 983\ \text{J},\quad q_{\text{cal}} = 35,0 \times 2,35 = 82{,}3\ \text{J}. \] Il calore della reazione è \(q_{\text{reaz}} = -(983 + 82{,}3) = -1{,}07 \times 10^{3}\ \text{J} \approx -0{,}256\ \text{cal}\) per grammo di soluzione, se normalizzato alla massa impiegata; il segno negativo conferma l’esotermicità. Molte reazioni fortemente esotermiche sono combustioni. Per processi di combustione a volume costante si usa il calorimetro a bomba, che fornisce il calore a volume costante \(q_v \approx \Delta U\); la correzione a \(\Delta H\) si ottiene aggiungendo \( \Delta n_g RT\) quando varia il numero di moli gassose. Lo stesso principio è impiegato per stimare il valore energetico degli alimenti. In nutrizione, il potere calorico esprime l’energia rilasciata per grammo di alimento; l’unità comune è la caloria alimentare, 1 Cal = 1 kcal = 4,184 kJ. In media, carboidrati e proteine apportano circa 4 Cal g\(^{-1}\), i lipidi circa 9 Cal g\(^{-1}\), l’etanolo circa 7 Cal g\(^{-1}\). Nell’organismo l’energia chimica non utilizzata per lavoro meccanico o per mantenere la temperatura corporea viene immagazzinata prevalentemente nei legami dei lipidi, in particolare sotto forma di triacilgliceroli; un bilancio energetico positivo protratto nel tempo è associato all’aumento della massa adiposa. La tazza in polistirolo espanso da caffè americano illustrata in (Figura 04.07-01), opportunamente coperta e dotata di termometro e agitatore, rappresenta dunque un calorimetro didattico semplice, ma capace di fornire stime affidabili del calore di reazione quando si controllano le condizioni sperimentali e si eseguono le opportune correzioni strumentali.