Configurazione elettronica e tavola periodica
Definizione
La portata esplicativa del modello di Bohr si rivelò presto limitata. Gli spettri di emissione e assorbimento degli atomi polielettronici, a differenza dell’idrogeno, non risultavano descrivibili entro lo schema delle orbite circolari con energie fissate. Inoltre, l’evidenza sperimentale del carattere ondulatorio dell’elettrone (interferenza e diffrazione) entrava in conflitto con l’idea di traiettorie determinate e con raggi definiti; in tale contesto, la natura estesa delle onde e il principio di indeterminazione resero insostenibile l’ipotesi di posizioni esatte all’interno dell’atomo. L’intuizione centrale di Bohr — la quantizzazione delle energie — non venne però abbandonata: fu riformulata in un quadro più generale, coerente con la dualità onda-particella.
Erwin Schrödinger estese la quantizzazione introducendo una descrizione ondulatoria degli stati elettronici. Formalmente, gli elettroni in un campo coulombiano sono descritti dall’equazione agli autovalori \( \hat{H}\,\psi = E\,\psi \), in cui le soluzioni \(\psi\) (funzioni d’onda) determinano una densità di probabilità \( |\psi(\mathbf{r})|^2 \) per il ritrovamento della particella nello spazio. Gli autovalori di energia risultano discreti e sono organizzati in livelli caratterizzati dal numero quantico principale \( n = 1, 2, 3, \ldots \). Ogni livello si suddivide in sottolivelli identificati dal numero quantico del momento angolare \( l = 0, 1, 2, \ldots, n-1 \); ciascun sottolivello comprende più orbitali, distinti dal numero quantico magnetico \( m_l = -l, \ldots, +l \). Gli orbitali non rappresentano orbite classiche, ma regioni di spazio in cui la probabilità di localizzare l’elettrone è elevata, corrispondenti alle soluzioni spaziali della funzione d’onda. Questa impostazione quanto-meccanica, pur conservando la quantizzazione energetica, rende conto degli spettri complessi degli atomi con più elettroni e fornisce la base per prevedere la distribuzione elettronica negli atomi stabili.
Livelli energetici principali
Nel quadro della meccanica quantistica, gli elettroni di un atomo non occupano posizioni arbitrarie, ma stati quantizzati caratterizzati dal numero quantico principale \(n = 1, 2, 3, \ldots\). Ciascun valore di \(n\) identifica un livello energetico principale (o guscio) e correla, in media, con la distanza dell’elettrone dal nucleo: a \(n\) crescente corrispondono energia e raggio medio maggiori. Nei sistemi idrogenoidi (un solo elettrone) l’energia dipende unicamente da \(n\); negli atomi polielettronici, invece, gli effetti di schermaggio e di carica nucleare efficace (\(Z_{\text{eff}}\)) introducono scostamenti energetici tra sottolivelli all’interno dello stesso \(n\).
Il numero totale di orbitali disponibili in un dato livello \(n\) è pari a \(n^2\); poiché ogni orbitale può accogliere al massimo due elettroni, la capienza massima del livello risulta \(2n^2\). Ne seguono i valori classici:
- \(n = 1\): capienza \(2 \times 1^2 = 2\) elettroni;
- \(n = 2\): capienza \(2 \times 2^2 = 8\) elettroni;
- \(n = 3\): capienza \(2 \times 3^2 = 18\) elettroni.
Nei modelli idrogenoidi il raggio più probabile degli orbitali s scala approssimativamente con \(n^2\) (proporzionalità all’unità di Bohr), mentre nelle specie polielettroniche tale dipendenza è modulata dal parziale schermaggio degli elettroni interni.
Sottolivelli
Ogni livello principale si suddivide in sottolivelli identificati dal numero quantico angolare orbitale \(\ell\) con valori \(\ell = 0, 1, 2, 3, \ldots, n-1\). Convenzionalmente, \(\ell=0,1,2,3\) sono indicati con le lettere s, p, d, f. In un atomo a più elettroni, a parità di \(n\), l’energia tende ad aumentare lungo la sequenza s < p < d < f, a causa di penetrazione e schermaggio differenti; in un sistema idrogenoide, invece, tutti i sottolivelli di uno stesso \(n\) sono degeneri.
Per i primi livelli energetici principali valgono quindi le seguenti possibilità:
- Primo livello (\(n = 1\)): un solo sottolivello, 1s;
- Secondo livello (\(n = 2\)): due sottolivelli, 2s e 2p;
- Terzo livello (\(n = 3\)): tre sottolivelli, 3s, 3p e 3d.
La specificazione completa della “posizione” quantistica di un elettrone richiede almeno coppie come 1s, 2s, 2p, 3d, che combinano livello principale e sottolivello; la completa identificazione dello stato include anche i numeri quantici magnetico e di spin (si veda la sezione sugli orbitali e sulle regole di occupazione).
Orbitali
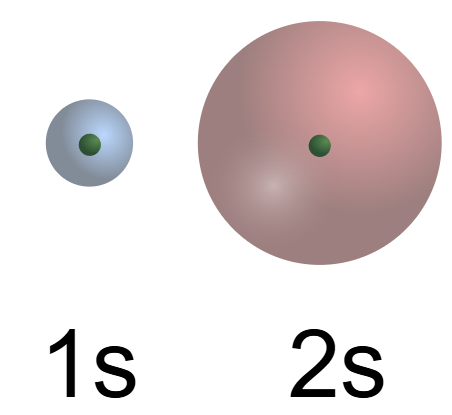
Un orbitale atomico è una funzione d’onda stazionaria che definisce una regione dello spazio in cui è elevata la probabilità di localizzare l’elettrone; ciascun orbitale può contenere al massimo due elettroni con spin opposti. La (Figura 01.10-01) illustra un orbitale s, isotropo e a simmetria sferica. Il suo “volume” rende l’idea della distribuzione spaziale della densità elettronica a data energia. La densità di probabilità \(|\psi|^2\) può essere finita anche a ridosso del nucleo per gli orbitali s, ma la probabilità radiale \(4\pi r^2|\psi|^2\) si annulla in \(r=0\); in chimica si interpreta l’orbitale come esterno al nucleo, che resta sede delle particelle nucleari.
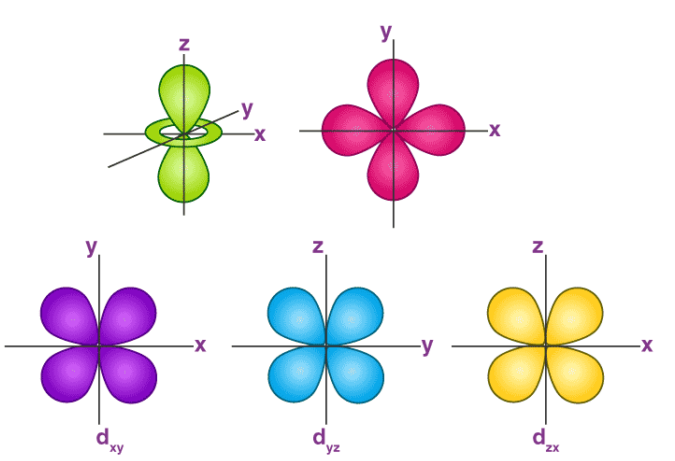
In ciascun livello \(n\) esiste un solo orbitale s (1s, 2s, 3s, …). Per i sottolivelli p, la (Figura 01.10-02) mostra i tre orbitali degeneri, identici per energia ma orientati diversamente nello spazio. Essi sono etichettati come \(p_x\), \(p_y\), \(p_z\) e i loro lobi si dispongono lungo gli assi cartesiani. La (Figura 01.10-03) rappresenta i cinque orbitali d degeneri: le loro forme, caratterizzate da nodi angolari più numerosi, risultano cruciali per le proprietà dei metalli di transizione e per la chimica di coordinazione. Esistono inoltre orbitali di ordine superiore (f, g, …), rilevanti soprattutto negli elementi delle ultime righe della tavola periodica.
Le superfici nodali (radiali e angolari) emergono dalle soluzioni dell’equazione di Schrödinger e crescono in numero con \(n\) e \(\ell\); ciò spiega l’aumentata complessità delle forme passando da s a p, d e oltre. Non tutti gli orbitali previsti sono necessariamente occupati in un dato atomo: le regioni evidenziate nelle figure rappresentano solo dove è più probabile trovare elettroni se presenti in quello stato.
Elettroni nei sottolivelli
La struttura fine della distribuzione elettronica è determinata dai numeri quantici \(\ell\) (angolare), \(m_\ell\) (magnetico, con \(m_\ell = -\ell, \ldots, 0, \ldots, +\ell\)) e \(m_s\) (spin, con \(m_s = \pm \tfrac{1}{2}\)). Da questi discendono il numero di orbitali e la capienza dei sottolivelli:
- Principio di esclusione di Pauli: in un atomo non possono esistere due elettroni con tutti e quattro i numeri quantici identici; per conseguenza, ogni orbitale accoglie al più due elettroni con spin antiparalleli;
- Numero di orbitali in un sottolivello \(\ell\): \(2\ell + 1\) (corrispondenti ai possibili valori di \(m_\ell\));
- Capienza massima del sottolivello \(\ell\).
\[ N_{\text{max}}(\ell) = 2 \times (2\ell + 1). \]
Esempi applicativi (con orbitali degeneri all’interno dello stesso sottolivello):
- Sottolivello s (\(\ell = 0\)): orbitali \(2\ell+1 = 1\) (solo s); capienza \(N_{\text{max}} = 2\);
- Sottolivello p (\(\ell = 1\)): orbitali \(2\ell+1 = 3\) (\(p_x, p_y, p_z\)); capienza \(N_{\text{max}} = 6\);
- Sottolivello d (\(\ell = 2\)): orbitali \(2\ell+1 = 5\) (cinque d); capienza \(N_{\text{max}} = 10\).
(Per completezza: per \(\ell = 3\), sottolivello f, si hanno 7 orbitali e \(N_{\text{max}} = 14\).) Sommando su tutti i valori di \(\ell\) ammessi per un dato \(n\) si ottiene \(\sum_{\ell=0}^{n-1}(2\ell+1) = n^2\), da cui la capienza \(2n^2\) del livello principale.
Quando più orbitali di uguale energia sono disponibili, la distribuzione degli elettroni segue anche il principio di massima molteplicità (regola di Hund): gli elettroni tendono a occupare prima orbitali distinti con spin paralleli, poi si appaiano. Ad esempio, in un 2p con tre elettroni, la configurazione più stabile è \(2p_x^1 2p_y^1 2p_z^1\) con spin allineati, anziché appaiare due elettroni nello stesso orbitale p.
Due elettroni che condividono un orbitale con spin opposti sono detti accoppiati. La presenza o assenza di elettroni spaiati determina il comportamento magnetico macroscopico: specie con tutti gli elettroni appaiati sono diamagnetiche, mentre la presenza di uno o più elettroni spaiati conferisce paramagnetismo, come illustrato schematicamente in (Figura 01.10-04).
La distribuzione degli elettroni negli orbitali di un atomo (configurazione elettronica) si ricava a partire dal numero atomico Z, che in un atomo neutro coincide con il numero totale di elettroni. La teoria degli orbitali quantistici impone alcuni vincoli generali: per ogni livello principale con numero quantico n sono ammessi esattamente n sottolivelli (con numeri quantici angolari l = 0, 1, …, n−1), e la capacità massima del livello è pari a \(2n^2\) elettroni. Ciascun orbitale può ospitare al più due elettroni con spin antiparallelo, e i sottolivelli presentano un numero fissato di orbitali: 1 per s, 3 per p, 5 per d, 7 per f. Il popolamento segue un ordine energetico determinato dai principi di Aufbau e di esclusione di Pauli e dalla regola di Hund, che guidano la costruzione della configurazione fondamentale.
Principio di Aufbau
Il principio di Aufbau stabilisce che gli elettroni occupano prima gli stati a energia più bassa disponibili, procedendo via via verso quelli più alti. Un utile promemoria dell’ordine teorico di riempimento è sintetizzato nella (Figura 01.10-05), spesso riassunto anche dalla regola di Madelung (n + l): a parità di n + l si riempie per primo il sottolivello con n minore. Questa convenzione, facile da ricordare, consente di prevedere correttamente sequenze come 1s → 2s → 2p → 3s → 3p → 4s → 3d, e funge da guida operativa per dedurre le configurazioni elettroniche degli elementi.
Principio di esclusione di Pauli (formulazione e implicazioni)
Il principio di esclusione, introdotto da Wolfgang Pauli nell’ambito della meccanica quantistica, impone che due elettroni di uno stesso atomo non possano condividere l’intero set di numeri quantici. Da ciò consegue l’enunciato pratico: ogni orbitale può contenere al massimo due elettroni con spin opposti, cioè con \(m_s = +\tfrac{1}{2}\) e \(m_s = -\tfrac{1}{2}\). La restrizione di Pauli determina la struttura fine dell’assetto elettronico e condiziona profondamente la periodicità delle proprietà chimiche.
Regola di Hund
Negli insiemi di orbitali degeneri (ad esempio i tre orbitali p o i cinque orbitali d di un medesimo sottolivello), la disposizione di minima energia è quella che massimizza il numero di elettroni spaiati con spin parallelo. In pratica, gli elettroni si collocano singolarmente in orbitali distinti prima di accoppiarsi, minimizzando la repulsione coulombiana e massimizzando la molteplicità di spin. Questo criterio è una conseguenza dell’interazione di scambio e si applica nella configurazione fondamentale a temperatura ordinaria.
- Individuare il numero di elettroni dell’atomo, pari al numero atomico riportato in tavola periodica;
- popolare gli orbitali procedendo dall’energia più bassa, a partire da 1s, seguendo l’ordine di Aufbau;
- ricordare che per ogni livello principale n sono presenti n sottolivelli con l = 0, 1, …, n−1;
- tenere conto che ogni sottolivello contiene un numero fissato di orbitali: 1 per s, 3 per p, 5 per d, 7 per f;
- non superare due elettroni per orbitale, con spin antiparalleli in accordo con Pauli;
- rispettare la capienza massima per livello principale, pari a \(2n^2\);
- utilizzare l’ordine di riempimento sintetizzato nella (Figura 01.10-05) come guida pratica.
Si considerino ora alcuni casi rappresentativi, che illustrano la costruzione passo dopo passo.
Idrogeno
Per Z = 1, l’unico elettrone occupa lo stato di minima energia, 1s. La notazione è 1s1, dove l’apice indica il numero di elettroni in quell’orbitale. Il corrispondente diagramma degli orbitali è:
 |
| Idrogeno – configurazione elettronica 1s¹ |
Elio
Per Z = 2, entrambi gli elettroni si collocano nel livello 1s, con spin opposti in virtù del principio di Pauli. La configurazione fondamentale è 1s2, e il diagramma corrispondente è:
 |
| Elio – configurazione elettronica 1s² |
Le due frecce in direzione opposta segnalano l’accoppiamento di spin, condizione necessaria quando due elettroni condividono lo stesso orbitale.
Litio
Con Z = 3, i primi due elettroni saturano 1s; il terzo occupa l’orbitale di energia più bassa disponibile nel secondo livello, 2s. Si ottiene 1s2 2s1. Il diagramma degli orbitali è:
 |
| Litio – configurazione elettronica 1s² 2s¹ |
Berillio
Per Z = 4, l’elettrone aggiuntivo rispetto al litio completa 2s, portando alla configurazione 1s2 2s2. Il diagramma conseguente è:
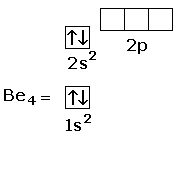 |
| Berillio – configurazione elettronica 1s² 2s² |
Boro
Per Z = 5, dopo aver saturato 2s, l’elettrone successivo entra nel sottolivello 2p, che ospita tre orbitali degeneri. La configurazione diventa 1s2 2s2 2p1, con diagramma:
 |
| Boro – configurazione elettronica 1s² 2s² 2p¹ |
Carbonio
Per Z = 6, in accordo con la regola di Hund, i due elettroni nel sottolivello 2p si dispongono in orbitali distinti con spin paralleli. La configurazione fondamentale è 1s2 2s2 2p2 e il relativo diagramma è:
 |
| Carbonio – configurazione elettronica 1s² 2s² 2p² |
In contesti chimici reattivi si può considerare una configurazione eccitata, ottenuta promuovendo un elettrone da 2s a un orbitale 2p (ad esempio 2pz): 1s2 2s1 2p3. Ciò risulta utile nell’interpretare la formazione di quattro legami equivalenti in molti composti del carbonio, come illustrato dal seguente schema:
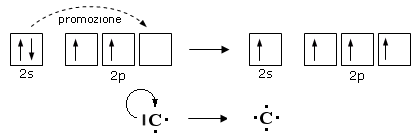 |
| Carbonio – promozione elettronica e formazione di quattro orbitali sp³ |
Azoto
Per Z = 7, il sottolivello 2p presenta tre elettroni spaiati con spin paralleli, in ossequio alla regola di Hund. La configurazione fondamentale è 1s2 2s2 2p3 e il diagramma associato è:
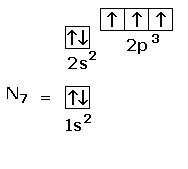 |
| Azoto – configurazione elettronica 1s² 2s² 2p³ |
Serie: ossigeno, fluoro e neon
Procedendo oltre, gli elettroni aggiunti si accoppiano gradualmente negli orbitali 2p già occupati, fino alla chiusura del secondo guscio:
ossigeno:
 |
| Ossigeno – configurazione elettronica 1s² 2s² 2p⁴ |
fluoro:
 |
| Fluoro – configurazione elettronica 1s² 2s² 2p⁵ |
neon:
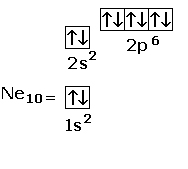 |
| Neon – configurazione elettronica 1s² 2s² 2p⁶ |
Dalla specie sodio fino ad argon
Gli elementi successivi conservano il nucleo elettronico del neon, [Ne] = 1s2 2s2 2p6, e iniziano a riempire il terzo livello: dapprima 3s (sodio e magnesio), poi 3p (da alluminio ad argon). L’illustrazione seguente mostra le relative energie orbitali:
| Livelli energetici degli orbitali atomici |
Gli orbitali 3p, in numero di tre, possono contenere complessivamente 6 elettroni; l’argon li completa insieme a 3s, conferendo un guscio chiuso (n = 3) e spiegando la sua elevata inerzia chimica.
Conoscendo la sequenza energetica degli orbitali, è possibile dedurre la configurazione di qualunque elemento. La (Figura 01.10-05) fornisce uno schema operativo molto pratico, mentre la (Figura 01.10-06) rappresenta i livelli energetici mediante un diagramma a scale, con gli stati di bassa energia in basso e quelli di alta energia in alto. Gli elementi dei gruppi 1, 2 e 13–18 (blocchi s e p) sono detti rappresentativi; per essi le regole di Aufbau, Pauli e Hund consentono previsioni affidabili. Negli elementi di transizione, soprattutto quando entrano in gioco i sottolivelli d e f, compaiono eccezioni dovute a sottili differenze energetiche, schermaggio e penetrazione orbitale: casi noti sono, ad esempio, Cr e Cu, per i quali configurazioni con sottolivelli d semipieni o pieni risultano particolarmente stabilizzate.
La costruzione della tavola periodica, inaugurata da Mendeleev su base empirica, è oggi giustificata dalla sequenza di riempimento degli orbitali. Gli elementi che appartengono alla stessa colonna condividono la configurazione del guscio esterno, che determina la chimica di valenza: per i metalli alcalini (gruppo 1) la forma è ns1, per i metalli alcalino-terrosi (gruppo 2) è ns2, mentre nei gruppi 13–18 si completano progressivamente gli orbitali p del livello n indicato dal numero di periodo. In tal modo la periodicità di proprietà come raggio atomico, energia di ionizzazione ed elettronegatività emerge direttamente dalle configurazioni.
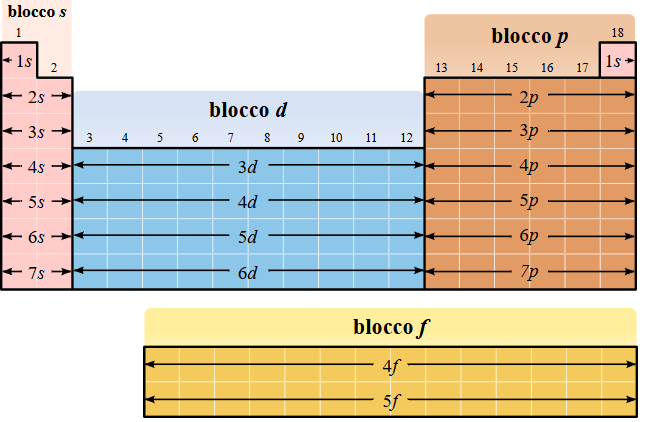
La corrispondenza tra disposizione elettronica e struttura della tavola è evidenziata nella (Figura 01.10-07): la particolare geometria a blocchi (s, p, d, f) riflette l’ordine di riempimento energetico e spiega l’affinità di comportamento tra elementi del medesimo gruppo. Le configurazioni con guscio completo o sottolivelli semipieni/pieni sono associate a stabilità marcata, come illustrato dai gas nobili e da specifiche eccezioni nei blocchi d e f.





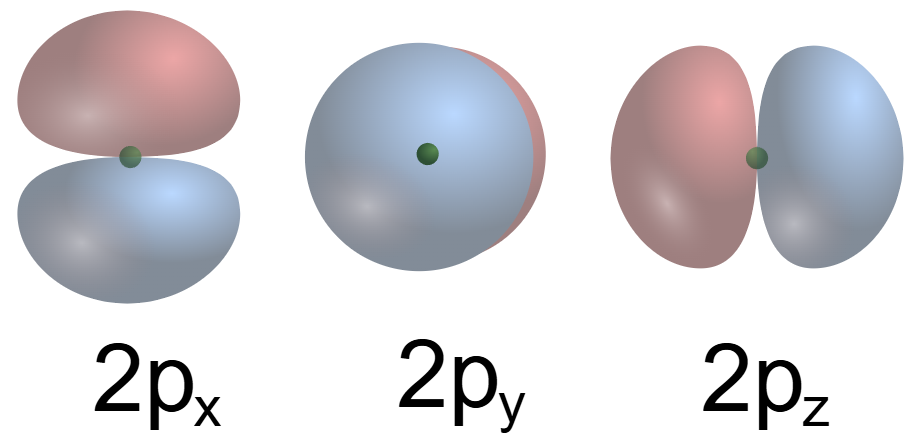

:max_bytes(150000):strip_icc()/800px-Orbital_representation_diagram.svg-589bd6285f9b58819cfd8460.png)