Comportamento acido-basico in aldeidi e chetoni
Definizione
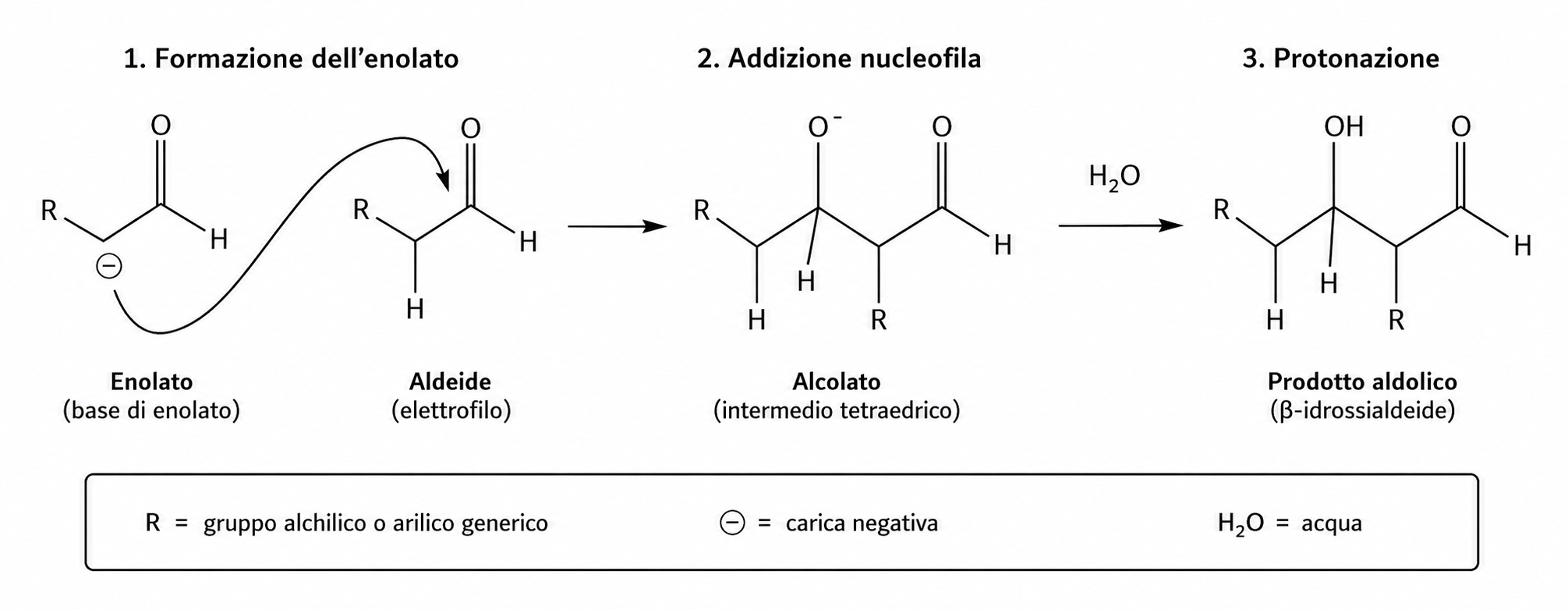
In presenza di basi sufficientemente forti, aldeidi e chetoni che possiedono almeno un idrogeno in posizione α rispetto al gruppo carbonilico possono essere deprotonati, agendo quindi come acidi di debolezza estrema. La rimozione di \( \mathrm{H}^+ \) dall’atomo di carbonio α genera l’enolato corrispondente (Figura 07.14-01) , (primo stadio), con costanti di dissociazione acida tipiche dell’ordine di \(K_a \approx 10^{-20}\) (ossia \(pK_a \sim 20\)). Sebbene ciò li collochi tra acidi molto deboli, la loro acidità è marcatamente superiore a quella di alcani e alcheni: per confronto, l’etene presenta \(pK_a \approx 44\) (quindi \(K_a \approx 10^{-44}\)).
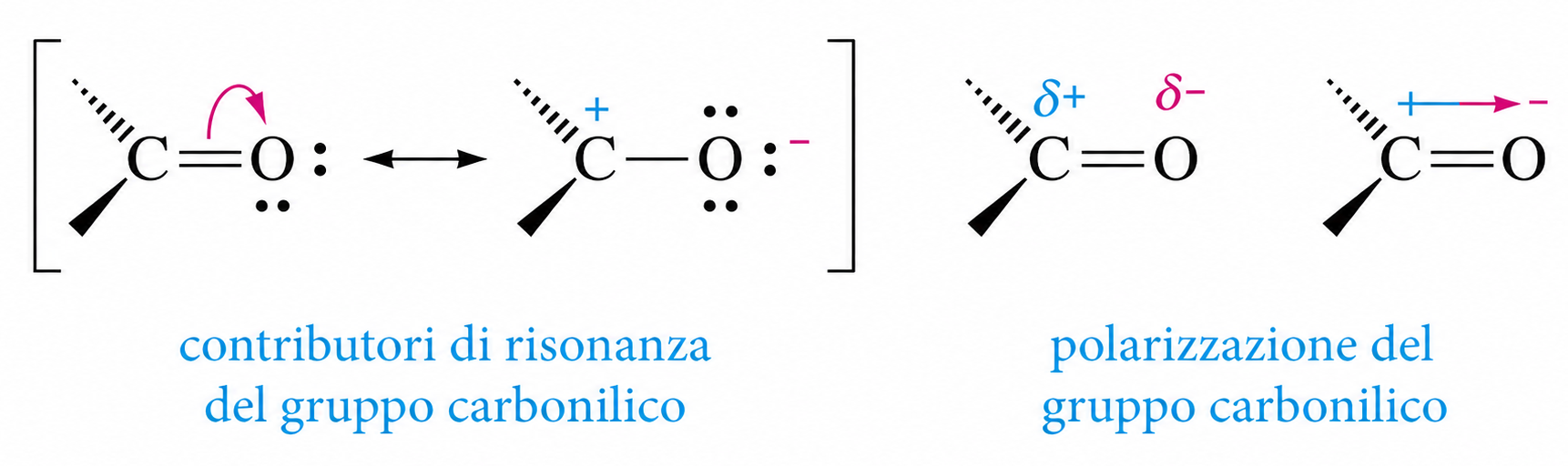
La maggiore acidità degli idrogeni α deriva da due contributi principali: (i) l’effetto induttivo elettron-attrattore del gruppo carbonilico e (ii) la stabilizzazione per risonanza dello ione enolato. L’elevata elettronegatività dell’ossigeno polarizza il legame C=O, rendendo il carbonio carbonilico più elettrofilo e il carbonio in α relativamente più povero di elettroni; di conseguenza, i legami C–H in α risultano più acidi rispetto a quelli in posizioni più lontane. Questo effetto di polarizzazione, illustrato in (Figura 07.14-02), si attenua rapidamente all’aumentare della distanza dal gruppo carbonilico, motivo per cui l’acidificazione è sostanzialmente confinata alla posizione α.
Il prodotto della deprotonazione, l’enolato, è stabilizzato dalla delocalizzazione della carica negativa tra ossigeno e carbonio α secondo forme limite di risonanza: \[ \ce{R-CO-CH^-R' <-> R-C(=O^-)=CHR'}. \] Questa delocalizzazione, assente negli idrocarburi saturi o negli alcheni non attivati, abbassa l’energia della base coniugata e accresce l’acidità dell’acido coniugato. In condizioni appropriate, l’equilibrio acido–base è in competizione con la tautomeria cheto–enolica, per la quale la forma chetonica/aldeidica e quella enolica sono interconvertibili: \[ \ce{R-CO-CHR' <=> R-CH=C(OH)R'}. \] In solventi protici e a temperatura ambiente, la forma chetonica/aldeidica è solitamente preponderante, ma la piccola quota di enolo risulta chimicamente significativa per molte trasformazioni.
L’acidità degli idrogeni α spiega anche la sequenza elementare che avvia la condensazione aldolica in ambiente basico acquoso. Il primo passaggio, catalizzato da basi quali \( \ce{NaOH} \) o alcossidi, è la deprotonazione in α con formazione dell’enolato (Figura 07.14-01) , (primo stadio): \[ \ce{R-CO-CH2-R' + B^- -> R-CO-CH^-R' + HB}. \] L’enolato così generato agisce da nucleofilo verso il carbonio carbonilico di una seconda molecola (attivato dalla polarizzazione C=O), formando un nuovo legame C–C e un intermedio alcossido in cui la carica negativa risiede sull’ossigeno (Figura 07.14-01) , (secondo e terzo stadio). L’alcossido, essendo la base coniugata di un alcol (acido molto debole), viene rapidamente protonato dal solvente, portando al β-idrossialdeide o β-idrossicheto corrispondente. In condizioni opportune, può seguire la disidratazione, con formazione dell’α,β-enone.
Oltre al mezzo acquoso, basi forti non nucleofile in solventi aprotici (ad esempio LDA in THF a bassa temperatura) consentono la generazione selettiva di enolati “cin-etici” o “termodinamici”, modulando la posizione della deprotonazione e quindi la regiocontrollo delle reazioni successive. Come regola orientativa, aldeidi sono generalmente più acide dei chetoni analoghi, ed entrambi diventano più acidi quando gruppi elettron-attrattori addizionali (per esempio carbonili, nitrili, nitro) sono in coniugazione con il centro deprotonabile:
- effetto induttivo: il gruppo C=O, fortemente elettron-attrattore, aumenta la polarità dei legami Cα–H, facilitandone la scissione eterolitica;
- risonanza: la delocalizzazione della carica nell’enolato tra O e Cα stabilizza la base coniugata, riducendo il \(pK_a\);
- sostituenti: ulteriori gruppi elettron-attrattori (per coniugazione o per induzione) incrementano l’acidità degli idrogeni in α;
- solvente e base: solventi protici favoriscono la protonazione rapida degli alcossidi, mentre solventi aprotici e basi ingombrate permettono il controllo sulla formazione dell’enolato e sulla sua reattività.
Nel complesso, la lieve ma significativa acidità degli idrogeni α in aldeidi e chetoni abilita la tautomeria cheto–enolica e rende possibili trasformazioni cardine della chimica organica, come la condensazione aldolica, attraverso la sequenza di stadi mostrata in (Figura 07.14-01) e la polarizzazione descritta in (Figura 07.14-02).