Calcoli stechiometrici basati sull’equazione chimica
Definizione
Con il termine stechiometria si indica il calcolo delle quantità relative di reagenti e prodotti sulla base di un’equazione chimica bilanciata. Tale approccio è cruciale sia nella sintesi industriale di farmaci e materiali ad alto valore, dove minimizzare sprechi e costi dipende da rapporti reagenti esatti, sia nei processi energetici: il rapporto combustibile/ossidante in caldaie e motori deve rispettare le proporzioni di reazione per massimizzare l’energia utile e ridurre emissioni indesiderate.
Nei calcoli stechiometrici si seguono alcune regole essenziali:
- Devono essere note e corrette le formule di tutti i reagenti e di tutti i prodotti;
- La base di ogni calcolo è un’equazione chimica bilanciata, in accordo con la legge di conservazione della massa; in assenza di bilanciamento i risultati non hanno significato fisico;
- I calcoli si svolgono in termini di moli; i coefficienti stechiometrici rappresentano i rapporti molari tra specie reagenti e prodotti;
- È necessario poter convertire in modo affidabile tra moli e massa (g o kg) tramite le masse molari, perché le misure di laboratorio e di impianto sono spesso in unità di massa.
In una reazione bilanciata, il numero totale di moli di specie molecolari nei reagenti può differire da quello nei prodotti, pur rimanendo costante il numero di atomi di ciascun elemento. Un esempio istruttivo è la formazione di acqua:
2 H2(g) + O2(g) → 2 H2O(g)
Qui 3 mol di reagenti danno 2 mol di prodotti, ma il conteggio atomico è invariato: 4 atomi di H e 2 atomi di O sia prima sia dopo. Se traduciamo in masse, otteniamo una corrispondenza coerente con le masse molari:
2 mol H2 (≈ 4,0 g) + 1 mol O2 (≈ 32,0 g) → 2 mol H2O (≈ 36,0 g).
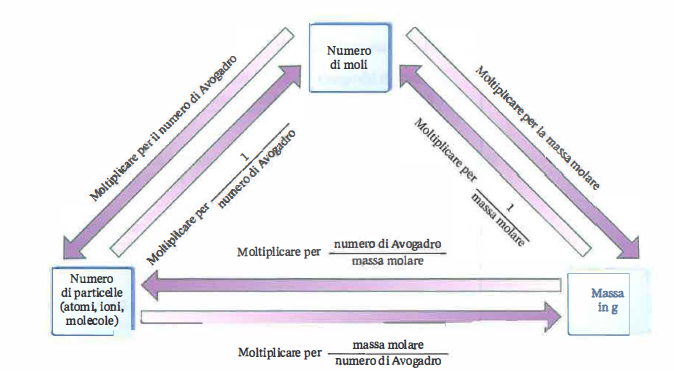
La mole resta quindi l’unità cardine del calcolo, ma la pratica richiede passaggi sistematici tra moli e grammi; a tal fine è utile lo schema riassuntivo di conversione riportato in (Figura 04.05-01).
Trasformare moli in grammi e viceversa
La conversione tra moli e massa sfrutta la massa molare M (g/mol) del composto o dell’elemento considerato. Le relazioni operative sono:
\( n = \dfrac{m}{M} \) e \( m = n \, M \),
dove n è la quantità di sostanza (mol) e m la massa (g). Questa identità consente di collegare misure sperimentali (masse) con i rapporti stechiometrici dettati dai coefficienti dell’equazione.
Dalle moli dei reagenti alle moli dei prodotti
I coefficienti dell’equazione bilanciata forniscono i rapporti molari esatti tra specie. Consideriamo, ad esempio, la combustione del metano:
CH4(g) + 2 O2(g) → CO2(g) + 2 H2O(g)
Da questa equazione risulta che 1 mol di CH4 corrisponde a:
- 2 mol di O2 consumate;
- 1 mol di CO2 formata;
- 2 mol di H2O formate.
Tali relazioni si impiegano come fattori di conversione (rapporti stechiometrici) in analisi dimensionale, ad esempio:
1 mol CH4 / 2 mol O2 → “1 mol di CH4 reagisce con 2 mol di O2”;
1 mol CH4 / 1 mol CO2 → “1 mol di CH4 genera 1 mol di CO2”;
1 mol CH4 / 2 mol H2O → “1 mol di CH4 produce 2 mol di H2O”.
In termini generali, per una reazione del tipo \( a\,A + b\,B \rightarrow c\,C + d\,D \), i rapporti molari consentiti sono, ad esempio, \( \frac{c\,\text{mol } C}{a\,\text{mol } A} \) o \( \frac{d\,\text{mol } D}{b\,\text{mol } B} \). Una procedura risolutiva sistematica per i problemi stechiometrici, basata su catene di fattori di conversione, è illustrata nella (Figura 04.05-02).
La resa teorica è la quantità massima di prodotto ottenibile quando tutti i passaggi procedono secondo i rapporti stechiometrici e senza perdite. Nella pratica, la resa reale è spesso inferiore per motivi quali conversione incompleta, reazioni collaterali, inefficienze di trasferimento e perdite meccaniche o termiche.
Per confrontare risultato sperimentale e previsione ideale si impiega la resa percentuale:
\[ \text{resa \%} = \frac{\text{resa reale}}{\text{resa teorica}} \times 100 \]
La resa reale può essere espressa in mol, g o altra unità coerente, purché identica a quella utilizzata per la resa teorica, così che il rapporto sia adimensionale e interpretabile come percentuale.
Situazione peculiare: il reagente limitante
I reagenti devono essere forniti nel rapporto indicato dai coefficienti della reazione bilanciata; quando ciò non accade, uno di essi si esaurisce per primo e determina la quantità massima di prodotto ottenibile: è il reagente limitante. Il calcolo corretto della resa teorica si fonda quindi sulla quantità di prodotto generabile a partire dal reagente in difetto.
Un’analogia quotidiana chiarisce il concetto. Supponiamo di voler preparare panini con formaggio e hamburger, utilizzando una unità di ciascun ingrediente per panino. Disponiamo di 14 panini, 11 fette di formaggio e 9 hamburger. L’ingrediente limitante è l’hamburger: possiamo assemblare solo 9 panini completi; avanzeranno 5 panini (14 − 9) e 2 fette di formaggio (11 − 9). L’elemento “in difetto” determina il numero massimo di porzioni complete.
La stessa logica si applica alle reazioni chimiche. Una strategia operativa utile è:
- bilanciare l’equazione di reazione;
- convertire le quantità disponibili di ciascun reagente in moli;
- per ogni reagente, calcolare quante moli di un prodotto prescelto si formerebbero se quel reagente reagisse completamente, usando i relativi rapporti stechiometrici;
- identificare il valore più piccolo: il reagente che lo genera è il limitante; la corrispondente quantità è la resa teorica del prodotto scelto;
- calcolare le quantità in eccesso dei reagenti non limitanti, sottraendo l’ammontare effettivamente consumato.
Ad esempio, per la reazione \( \text{N}_2 + 3\,\text{H}_2 \rightarrow 2\,\text{NH}_3 \), se si hanno 5,0 mol di N2 e 12,0 mol di H2, il massimo NH3 ottenibile è vincolato da H2: da N2 si potrebbero formare \(5,0 \times \frac{2}{1} = 10,0\) mol di NH3, mentre da H2 si ottengono \(12,0 \times \frac{2}{3} = 8,0\) mol; il reagente limitante è quindi H2 e la resa teorica è 8,0 mol di NH3.
L’insieme di questi strumenti — equazioni bilanciate, conversioni moli/massa (Figura 04.05-01), fattori di conversione tra specie e identificazione del reagente limitante — consente di affrontare in modo rigoroso e riproducibile i calcoli stechiometrici in ambito sia laboratoriale sia industriale (Figura 04.05-02).