Atomi
Definizione
Le leggi ponderali e volumetriche della chimica, sistematizzate tra la fine del Settecento e l’inizio dell’Ottocento, hanno corroborato l’ipotesi che la materia sia costituita da unità discrete, gli atomi. Un elemento chimico è una sostanza che non può essere scissa con mezzi chimici in componenti più semplici e dalla cui combinazione derivano i composti (molecole). L’atomo è la porzione minima di un elemento che ne conserva l’identità chimica.
Nel linguaggio contemporaneo si adotta la mole come quantità di riferimento: un campione contenente un numero di unità elementari pari alla costante di Avogadro, \(N_\mathrm{A} = 6{,}02214076 \times 10^{23}\ \mathrm{mol}^{-1}\) (definizione SI). In precedenza si usavano i termini «grammo-atomo» e «grammo-molecola». Il conteggio su scala macroscopica stabilisce il ponte tra quantità chimiche e numero di particelle.
Per illustrare gli ordini di grandezza molecolari, consideriamo l’etanolo, \( \mathrm{C_2H_5OH} \), con massa molare circa 46,07 g mol⁻¹ e densità \( \rho \approx 0{,}789\ \mathrm{g\ cm^{-3}} \) a 20 °C. Una mole occupa allora un volume \(V_m \approx 58{,}4\ \mathrm{cm^3}\). Se le molecole fossero idealmente accostate, il volume medio per molecola sarebbe \(V_m/N_\mathrm{A} \approx 9{,}7 \times 10^{-23}\ \mathrm{cm^3}\); la dimensione lineare caratteristica, pari alla radice cubica di tale volume, risulta dell’ordine di \(4{,}6 \times 10^{-8}\ \mathrm{cm}\), cioè circa 4,6 Å. Le dimensioni tipiche degli atomi e delle molecole piccole sono pertanto dell’ordine degli ångström, con valori medi che, a seconda del metodo di misura e del legame, ricadono in genere tra 0,5 Å e 3 Å.
Ogni atomo è costituito da un nucleo centrale, che contiene protoni (carica positiva) e neutroni (neutri), e da una nube elettronica di carica negativa distribuita nello spazio attorno al nucleo. Il raggio nucleare è dell’ordine di \(10^{-13}\ \mathrm{cm}\) (cioè \(10^{-15}\ \mathrm{m}\)), quindi circa \(10^5\) volte più piccolo del raggio atomico medio, come sintetizzato in (Tabella 07.11-01). La massa dell’elettrone è circa 1/1836 di quella del protone o del neutrone; ne segue che la quasi totalità della massa atomica è concentrata nel nucleo. Un atomo neutro contiene \(Z\) protoni e \(Z\) elettroni; l’acquisto o la perdita di uno o più elettroni genera, rispettivamente, anioni e cationi. Si definisce ionizzazione il processo di rimozione o acquisizione di elettroni da parte di atomi o molecole, con formazione di specie cariche.
Il numero atomico \(Z\) determina l’identità dell’elemento e ne colloca la posizione nella tavola periodica. Nuclei con lo stesso \(Z\) ma differente numero di neutroni \(N\) danno luogo a isotopi, caratterizzati da differente numero di massa \(A\), con \(A = Z + N\). Gli elementi presenti in natura sono tradizionalmente elencati dall’idrogeno (\(Z=1\)) all’uranio (\(Z=92\)); in termini moderni, tracce geochimiche mostrano che anche alcuni nuclei con \(Z > 92\) (es., nettunio e plutonio) possono ritrovarsi in quantità minime, ma sono comunque instabili su scale temporali geologiche. La massa atomica relativa è riferita per convenzione all’isotopo \(^{12}\mathrm{C}\), al quale è assegnato il valore esatto di 12 unità di massa atomica unificata (u, o dalton). Gli scarti rispetto ai numeri interi, riportati in (Tabella 07.11-02), riflettono la composizione isotopica naturale di ciascun elemento.
Le dimensioni atomiche non sono definibili con un’unica lunghezza «assoluta» sia per motivi teorici (natura quantistica della nube elettronica) sia per ragioni sperimentali (metodo dipendente: raggi X, scattering, potenziali efficaci). Per questa ragione si adottano raggi «medi» o «efficaci» che variano con il contesto chimico-fisico.
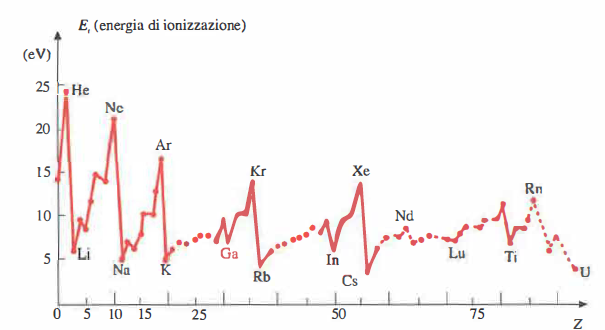
La coesione tra elettroni e nucleo è governata dall’interazione coulombiana; la gravità è trascurabile alla scala atomica in confronto alla forza elettromagnetica, come messo in evidenza in (Tabella 07.11-03). Le forze nucleari forti agiscono solo entro il nucleo e non determinano direttamente la struttura della nube elettronica. Per distaccare elettroni dal potenziale attrattivo del nucleo è necessario compiere un lavoro pari in modulo all’energia di legame elettronica (negativa). La scala energetica conveniente è l’elettronvolt: \(1\ \mathrm{eV} = e \times 1\ \mathrm{V} = 1{,}602176634 \times 10^{-19}\ \mathrm{J}\). Le energie di prima ionizzazione degli elementi sono tipicamente comprese tra pochi eV e alcune decine di eV, con valori rappresentativi nell’intervallo 1–25 eV (Figura 07.11-02); per esempio, l’elio richiede 24,6 eV, mentre un metallo alcalino richiede pochi eV.
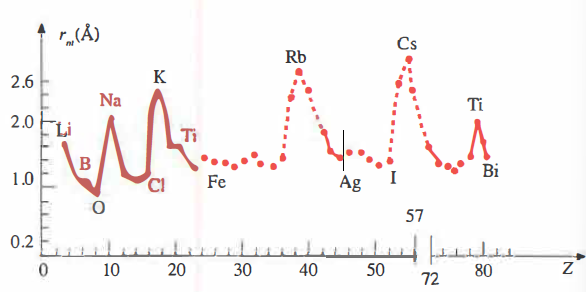
La periodicità delle proprietà chimiche dipende dall’assetto dell’involucro elettronico. In funzione di \(Z\), sia l’energia di ionizzazione sia il raggio atomico medio \(r_m\) mostrano andamenti oscillanti e regolari (Figura 07.11-01) e (Figura 07.11-02), in stretta analogia con l’ordinamento della tavola di Mendeleev. Tale comportamento è una manifestazione diretta della struttura a livelli e sottolivelli della nube elettronica, responsabile della quasi totalità delle caratteristiche fisiche e chimiche degli atomi:
- Numero atomico: \(Z\), uguale ai protoni nel nucleo e agli elettroni nell’atomo neutro;
- Numero di massa: \(A = Z + N\), totale dei nucleoni (protoni + neutroni);
- Isotopi: specie con stesso \(Z\) e differente \(N\), con masse atomiche relative che riflettono la miscela isotopica naturale (Tabella 07.11-02);
- Scala delle lunghezze: raggio nucleare \(\sim 10^{-13}\ \mathrm{cm}\), raggio atomico medio \(\sim 10^{-8}\ \mathrm{cm}\);
- Forze in gioco: interazione elettrostatica dominante, gravità trascurabile (Tabella 07.11-03), forza nucleare confinata al nucleo.
| Particella | Carica elettrica | Dimensione stimata | Massa (g) | Vita media (τ) | Note cliniche |
|---|---|---|---|---|---|
| Elettrone | −e | <10⁻²⁸ cm (limite sup.) | 9,11·10⁻²⁸ | stabile | Usato in radioterapia elettronica e imaging PET (come positrone e⁺) |
| Protone | +e | ≈10⁻¹³ cm | 1,67·10⁻²⁴ | stabile | Responsabile della carica positiva nucleare; impiegato in protonterapia oncologica |
| Neutrone | 0 | ≈10⁻¹³ cm | 1,67·10⁻²⁴ | ~17,3 minuti (libero) | Essenziale per la stabilità nucleare; in eccesso contribuisce alla radioattività β⁻ |
| Positrone (e⁺) | +e | <10⁻²⁸ cm | 9,11·10⁻²⁸ | ~10⁻¹⁰ s | Antiparticella dell’elettrone; impiegata in PET (Tomografia a Emissione di Positroni) |
| Neutrino | ~0 | <10⁻²⁰ cm | ~0 (quasi nullo) | estremamente lungo | Presente nei decadimenti nucleari; rilevante in biofisica e medicina nucleare |
Caratteristiche fondamentali delle particelle atomiche
Massa, carica e proprietà distintive di protoni, neutroni ed elettroni.
| Elemento | Isotopo | Z | A | N = A−Z | Abbondanza relativa (%) | Peso atomico medio | Note cliniche |
|---|---|---|---|---|---|---|---|
| Carbonio | ¹²C | 6 | 12 | 6 | 98,89 | 12,011 | Isotopo stabile, base della chimica organica |
| ¹³C | 6 | 13 | 7 | 1,11 | Stabile, usato in NMR e traccianti metabolici | ||
| ¹⁴C | 6 | 14 | 8 | tracce (radioattivo) | Datazioni radiocarboniche, studi biologici | ||
| Ossigeno | ¹⁶O | 8 | 16 | 8 | 99,759 | 15,9994 | Isotopo stabile, componente principale dell’aria |
| ¹⁷O | 8 | 17 | 9 | 0,037 | Stabile, usato in NMR | ||
| ¹⁸O | 8 | 18 | 10 | 0,204 | Traccianti in studi metabolici e idrologici | ||
| Potassio | ³⁹K | 19 | 39 | 20 | 93,188 | 39,0983 | Principale isotopo stabile |
| ⁴⁰K | 19 | 40 | 21 | 0,012 (radioattivo) | Usato in geocronologia, fonte naturale di radioattività | ||
| ⁴¹K | 19 | 41 | 22 | 6,8 | Stabile, importante in fisiologia cellulare | ||
| Piombo | ²⁰⁴Pb | 82 | 204 | 122 | 1,3 | 207,19 | Isotopo stabile |
| ²⁰⁶Pb | 82 | 206 | 124 | 26,0 | Stabile, prodotto di decadimento dell’uranio | ||
| ²⁰⁷Pb | 82 | 207 | 125 | 20,7 | Stabile, usato in studi geologici | ||
| ²⁰⁸Pb | 82 | 208 | 126 | 52,0 | Isotopo più abbondante, stabile |
Isotopi e relative abbondanze naturali
Elenco di isotopi stabili e radioattivi con le loro concentrazioni in natura.
| Forza | Intensità relativa | Raggio d’azione | Note |
|---|---|---|---|
| Gravitazionale | ≈ 10⁻³⁸ | Infinito | Responsabile dell’attrazione tra masse; irrilevante a livello subatomico ma dominante su scala astrofisica |
| Elettromagnetica | ≈ 10⁻² (1/137) | Infinito | Governa interazioni tra particelle cariche; fondamentale in biofisica e chimica molecolare |
| Nucleare debole | ≈ 10⁻¹⁴ | ~10⁻¹³ cm | Coinvolta nei decadimenti β, rilevante in medicina nucleare (es. radioisotopi) |
| Nucleare forte | 1 – 10 | ~10⁻¹³ cm | Mantiene uniti protoni e neutroni nel nucleo; forza a corto raggio |
Interazioni fondamentali della Natura
Sintesi delle quattro forze con relative intensità e proprietà principali.
| Elemento | Isotopo | Z | A | N = A−Z | Abbondanza relativa (%) | Peso atomico medio | Note cliniche |
|---|---|---|---|---|---|---|---|
| Carbonio | ¹²C | 6 | 12 | 6 | 98,89 | 12,011 | Isotopo stabile, base della chimica organica |
| ¹³C | 6 | 13 | 7 | 1,11 | Stabile, usato in NMR e traccianti metabolici | ||
| ¹⁴C | 6 | 14 | 8 | tracce (radioattivo) | Datazioni radiocarboniche, studi biologici | ||
| Ossigeno | ¹⁶O | 8 | 16 | 8 | 99,759 | 15,9994 | Isotopo stabile, componente principale dell’aria |
| ¹⁷O | 8 | 17 | 9 | 0,037 | Stabile, usato in NMR | ||
| ¹⁸O | 8 | 18 | 10 | 0,204 | Traccianti in studi metabolici e idrologici | ||
| Potassio | ³⁹K | 19 | 39 | 20 | 93,188 | 39,0983 | Principale isotopo stabile |
| ⁴⁰K | 19 | 40 | 21 | 0,012 (radioattivo) | Usato in geocronologia, fonte naturale di radioattività | ||
| ⁴¹K | 19 | 41 | 22 | 6,8 | Stabile, importante in fisiologia cellulare | ||
| Piombo | ²⁰⁴Pb | 82 | 204 | 122 | 1,3 | 207,19 | Isotopo stabile |
| ²⁰⁶Pb | 82 | 206 | 124 | 26,0 | Stabile, prodotto di decadimento dell’uranio | ||
| ²⁰⁷Pb | 82 | 207 | 125 | 20,7 | Stabile, usato in studi geologici | ||
| ²⁰⁸Pb | 82 | 208 | 126 | 52,0 | Isotopo più abbondante, stabile |
Isotopi e relative abbondanze naturali
Elenco di isotopi stabili e radioattivi con le loro concentrazioni in natura.
| Forza | Intensità relativa | Raggio d’azione | Note |
|---|---|---|---|
| Gravitazionale | ≈ 10⁻³⁸ | Infinito | Responsabile dell’attrazione tra masse; irrilevante a livello subatomico ma dominante su scala astrofisica |
| Elettromagnetica | ≈ 10⁻² (1/137) | Infinito | Governa interazioni tra particelle cariche; fondamentale in biofisica e chimica molecolare |
| Nucleare debole | ≈ 10⁻¹⁴ | ~10⁻¹³ cm | Coinvolta nei decadimenti β, rilevante in medicina nucleare (es. radioisotopi) |
| Nucleare forte | 1 – 10 | ~10⁻¹³ cm | Mantiene uniti protoni e neutroni nel nucleo; forza a corto raggio |
Interazioni fondamentali della Natura
Sintesi delle quattro forze con relative intensità e proprietà principali.