Assorbimento dei fotoni gamma
Definizione
In ambito medico le radiazioni ionizzanti trovano impiego nell’imaging con due principali approcci: (a) l’irradianza del paziente con raggi X per ottenere immagini per trasmissione, e (b) l’utilizzo di radionuclidi in Medicina nucleare per immagini di emissione. Queste tecniche, complementari tra loro, permettono di visualizzare struttura e funzione degli organi con finalità diagnostiche e di monitoraggio terapeutico.
Le dosi assorbite medie in diagnostica con raggi X sono riportate in (Tabella 07.28-01). Nella pratica clinica le dosi per singolo esame sono in genere contenute e non tali da determinare effetti deterministici, tuttavia l’esposizione cumulativa può crescere con il numero di indagini e va quindi limitata agli esami giustificati clinicamente. Le stime correnti indicano, per la popolazione dei Paesi industrializzati, una dose media annua dovuta a procedure radiologiche intorno a 1 mSv/persona, valore confrontabile con il limite per il pubblico non esposto professionalmente (Tabella 07.28-03). Poiché su scala mondiale il numero di esami radiologici è in incremento di circa il 10% annuo, è essenziale coniugare giustificazione e ottimizzazione secondo il principio ALARA, riducendo gli esami non necessari e investendo in tecnologie e protocolli a bassa dose.
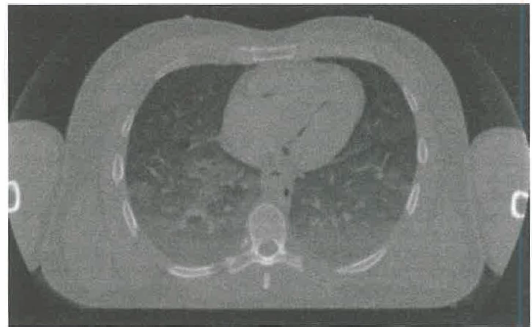
Particolare attenzione è richiesta in TC e radiologia interventistica, che comportano esposizioni più elevate e potenziali rischi cutanei e deterministici; per queste pratiche si applicano specifiche disposizioni di protezione del paziente previste dalla normativa nazionale (d.lgs. 101/2020) e dai livelli diagnostici di riferimento. Nella gestione della dose sono rilevanti indicatori tecnici quali:
- per radiografia e fluoroscopia: kerma in aria in ingresso e prodotto dose-area (PDA), utili per confrontare e ottimizzare i protocolli;
- per TC: CTDIvol e DLP, dai quali si può stimare la dose efficace con fattori conversione specifici per distretto;
- strategie di riduzione della dose: filtrazione spettrale, modulazione automatica della corrente tubo, algoritmi di ricostruzione iterativa e controllo del campo di vista;
- giustificazione clinica e aderenza ai livelli diagnostici di riferimento, con audit periodici e formazione del personale.
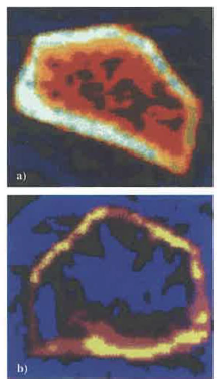
Quando un fascio di raggi X attraversa i tessuti, l’attenuazione dipende dalla composizione e dalla densità dei materiali biologici. Mediante opportuni algoritmi si ricava la distribuzione spaziale del coefficiente di attenuazione, distinguendo tra tessuti molli e strutture ossee. La densitometria ossea a raggi X, o MOC (Mineralometria Ossea Computerizzata), sfrutta queste proprietà per stimare la mineralizzazione ossea, fornendo indici quantitativi (ad esempio T-score e Z-score) utili per identificare osteopenia e osteoporosi e per valutarne la severità (Figura 07.28-01).
| Esame radiologico | Dose efficace (mSv) | Equivalente in RX torace |
|---|---|---|
| Radiografia arti | 0,01 – 0,05 | <1 |
| Colonna cervicale | 0,2 | 2 |
| Radiografia torace | 0,1 | 1 |
| Mammografia | 0,3 | 3 |
| Colonna lombare | 1,2 | 12 |
| Addome | 0,9 | 9 |
| Cintura pelvica | 0,7 | 7 |
| Colonna toracica | 0,6 | 6 |
| Tomografia cranio | 1,9 | 19 |
| TC seni paranasali | 2,5 | 25 |
| Urografia endovenosa | 2,9 | 29 |
| TC torace | 6,6 | 66 |
| Angiografia cardiaca | 7,7 | 77 |
| Studio baritato intestinale | 7,2 | 72 |
| Clistere baritato | 8,5 | 85 |
| Pasto baritato | 6,2 | 62 |
| TC colonna | 7,7 | 77 |
| TC pelvica | 7,3 | 73 |
| TC addome | 11,3 | 113 |
| TC tronco | 14,8 | 148 |
| Angioplastica coronarica | 15,2 | 152 |
| Radiografia panoramica dentale | 0,02 – 0,03 | <1 |
| Risonanza magnetica (RMN) | 0 | — |
| Ecografia diagnostica | 0 | — |
| PET-TC corpo intero | 25 | ≈250 |
| Fluoroscopia interventistica | 10 – 40 | 100 – 400 |
Valutazione delle dosi efficaci medie nei 20 principali Paesi europei
Stima delle dosi per tipologia di esame radiologico, calcolata sulla media complessiva dei Paesi.
| Categoria di soggetti | Dose efficace (mSv/anno) | Dose equivalente estremità (mSv/anno) | Dose equivalente pelle (mSv/anno) | Dose equivalente cristallino (mSv/anno) | Note |
|---|---|---|---|---|---|
| Lavoratori professionalmente esposti | 20 | 500 | 500 | 20 | Valori medi su base quinquennale; include medici nucleari, radiologi, tecnici di radiologia |
| Popolazione generale | 1 | — | 50 | 15 | Protezione della collettività; dose di riferimento ambientale |
| Nascituro (durante la gravidanza) | 1 (per tutta la gestazione) | — | — | — | Valore di protezione del feto; applicato alle lavoratrici esposte |
Limiti annuali di dose individuale
Valori massimi di esposizione a radiazioni ionizzanti stabiliti per garantire la protezione della salute.
Radiazioni corpuscolari e fotoni γ sono emessi nel decadimento di nuclei instabili presenti in natura o prodotti artificialmente (reattori, ciclotroni, acceleratori). La disponibilità di radionuclidi e di fasci dedicati ha favorito l’ampia diffusione delle applicazioni in Medicina e Biologia. In diagnostica i radioisotopi vengono impiegati come traccianti: legati a molecole biologicamente attive (radiofarmaci), mappano la distribuzione topografica e la cinetica di specifici processi fisiologici o patologici. La sensibilità è molto elevata: la rivelazione può avvenire a livello di minime concentrazioni, consentendo l’uso di attività relativamente ridotte.
Dal punto di vista della sensibilità spaziale, l’imaging per trasmissione con raggi X fornisce contrasto proporzionale a differenze di attenuazione integrate su volumi dell’ordine di circa 1 grammo di tessuto (circa 109 cellule), mentre in PET è sufficiente rivelare l’emissione di un numero di decadimenti dell’ordine di 104, corrispondenti a segnali generati da poche decine o centinaia di cellule: la capacità di rilevare fenomeni molecolari precoci è quindi notevole. Dopo la somministrazione, il radiofarmaco si distribuisce e viene metabolizzato secondo le leggi della diffusione e della cinetica biochimica; la maggiore o minore captazione in specifiche regioni costituisce un indicatore di funzionalità o di alterazione, su cui si fonda l’interpretazione diagnostica.
L’attività da somministrare è definita valutando la cinetica del carrier e del radionuclide, la vita media fisica e il potenziale di dose agli organi bersaglio e non bersaglio. In Medicina e Biologia Nucleare si distinguono due tipi di dimezzamento: il tempo di dimezzamento fisico \(t_{1/2\,F}\), che rappresenta la velocità con cui il radionuclide si trasforma per decadimento radioattivo, e il tempo di dimezzamento biologico \(t_{1/2\,B}\), legato all’eliminazione o al metabolismo del radionuclide da parte dell’organismo.
Poiché i due processi (fisico e biologico) agiscono simultaneamente e in modo indipendente, l’effetto combinato si esprime attraverso il tempo di dimezzamento effettivo \(t_{1/2\,\text{EFF}}\), definito dalla relazione:
\[
t_{1/2\,\text{EFF}} = \frac{t_{1/2\,F} \cdot t_{1/2\,B}}{t_{1/2\,F} + t_{1/2\,B}}
\]
Questa formula mostra che il tempo di dimezzamento effettivo è sempre minore di ciascuno dei due tempi parziali, poiché tiene conto sia del decadimento fisico sia dell’eliminazione biologica. In pratica, descrive la rapidità con cui l’attività complessiva del radionuclide si riduce all’interno del corpo umano.
Conoscere t1/2 EFF consente di stimare l’attività residua nel paziente in ogni istante post-somministrazione e di pianificare misure di radioprotezione per i conviventi e il personale (distanziamento, igiene di feci e urine come residui radioattivi).
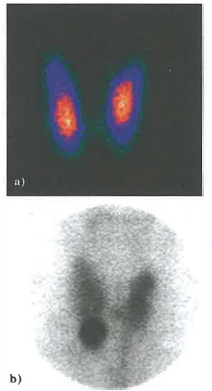
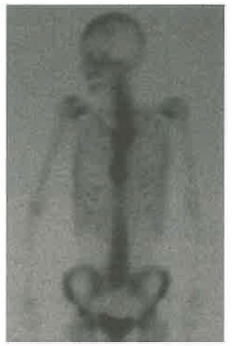
Lo studio della tiroide è tra le applicazioni storiche. La ghiandola utilizza iodio per sintetizzare ormoni tiroidei; in ipotiroidismo la captazione è ridotta, mentre in ipertiroidismo aumenta (Figura 07.28-02). A fini diagnostici si può somministrare una piccola attività di iodio radioattivo, per esempio pochi MBq di 123I o di 131I, in soluzione o capsula; dopo un intervallo prestabilito (ad esempio 24 ore per 131I) si misura l’emissione γ con un contatore o si acquisiscono immagini planari mediante gamma-camera. La misura può essere integrale (conteggi totali in un tempo definito) o spazialmente risolta, ottenendo una scintigrafia che rappresenta la distribuzione della captazione; esempi di scintigrafia ossea sono mostrati in (Figura 07.28-03). Per completezza, si ricorda la corrispondenza tra unità storiche e SI: 1 mCi = 37 MBq.
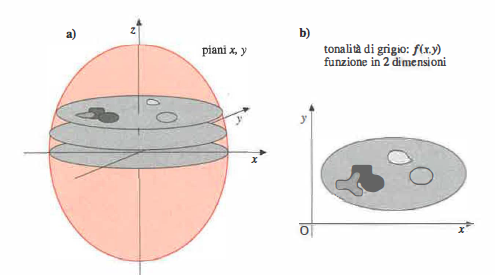
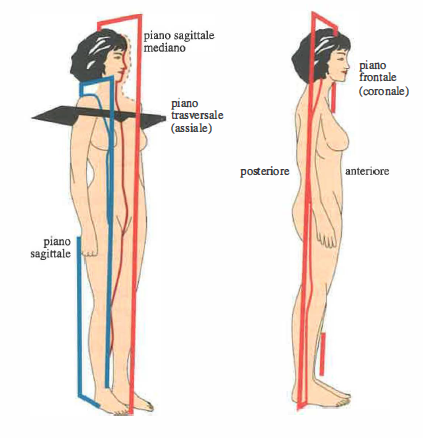
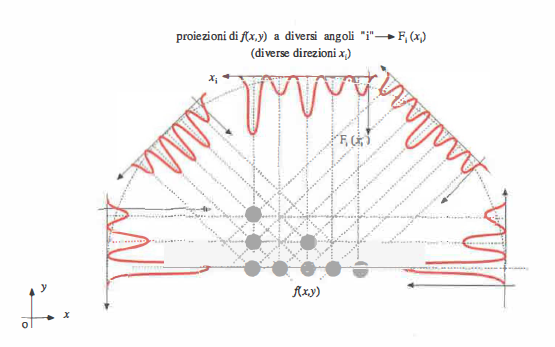
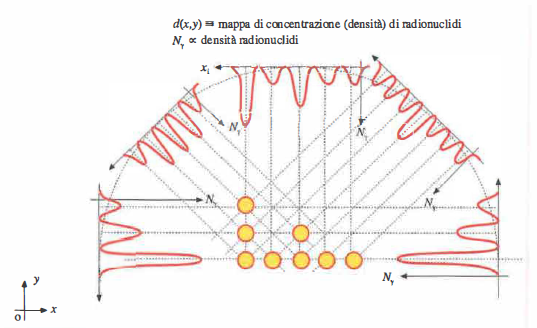
L’evoluzione dell’hardware di calcolo e delle interfacce ha reso possibile gestire grandi volumi di dati e flussi complessi, aprendo la strada a nuove metodiche d’imaging e a un’elaborazione avanzata delle immagini cliniche. Oltre a ecografia, microscopia digitale e digitalizzazione radiografica, un ruolo centrale è svolto dalle tecniche di tomografia, che ricostruiscono sezioni del corpo umano a partire da proiezioni acquisite da molteplici angolazioni. La ricostruzione tomografica mira a determinare la funzione f(x,y) che descrive le intensità (toni di grigio) in un piano specifico del soggetto (Figura 07.28-04). I piani di riferimento anatomici standard sono indicati in (Figura 07.28-05), con la possibilità di definire piani obliqui ove clinicamente necessario.
Il problema matematico può essere formulato in termini di proiezioni della scena su diverse direzioni angolari e della successiva inversione della trasformata di Radon, secondo il teorema della sezione centrale: la trasformata di Fourier di una proiezione a un angolo dato corrisponde a una sezione del trasformato bidimensionale dell’oggetto (Figura 07.28-06). Le principali famiglie di algoritmi includono:
- retroproiezione filtrata (FBP), che applica un filtro in dominio delle frequenze per compensare la sfocatura della retroproiezione semplice, con ricostruzione rapida e stabile;
- metodi iterativi (p.es. MLEM/OSEM), che modellano statistiche del rumore e geometria del sistema, migliorando il rapporto segnale-rumore e la qualità a bassa dose, a costo di maggior tempo computazionale;
- approcci ibridi e regolarizzati, che integrano vincoli di sparsità o prior per ridurre artefatti e sfruttare dati incompleti.
La natura fisica della funzione ricostruita dipende dalla modalità:
- TC: f(x,y) rappresenta il coefficiente di attenuazione dei raggi X lungo la direzione di proiezione x;
- SPECT e PET: f(x,y) esprime il tasso di emissione fotonica dovuto alla distribuzione del radionuclide nel tessuto;
- RM: il segnale a radiofrequenza è proporzionale alla densità protonica e modulato dai tempi di rilassamento T1 e T2, fornendo contrasti funzionali e tissutali.
La combinazione di acquisizione ottimizzata e ricostruzioni avanzate ha consentito di ridurre le dosi in TC e SPECT e di migliorare la risoluzione spaziale e temporale in PET e RM, ampliando gli scenari clinici e la capacità di evidenziare pattern patologici altrimenti non apprezzabili alla sola ispezione visiva.
Un sistema TC clinico moderno integra quattro sottosistemi fondamentali:
- una sorgente di raggi X ad alta potenza, con spettro il più possibile ristretto e stabilità di emissione elevata;
- rivelatori compatti a elevata efficienza quantica e grande stabilità, tipicamente basati su scintillatori accoppiati a fotodiodi o, nei sistemi più recenti, su rivelatori a conteggio di fotoni;
- un calcolatore ad alte prestazioni con ampia memoria per la ricostruzione numerica delle immagini;
- un sistema di visualizzazione e post-processing orientato all’uso clinico, in scala di grigi e con strumenti di misura dedicati.
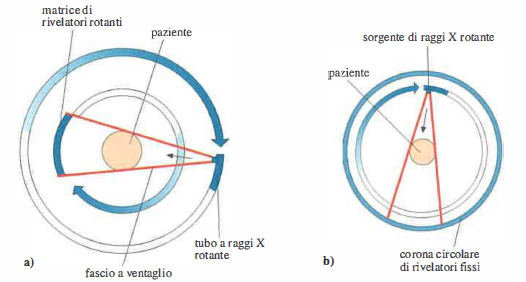
Negli anni ’70, la maturazione congiunta di questi elementi rese possibile lo sviluppo progressivo delle diverse generazioni di TC. In configurazione classica, il tubo radiogeno percorre una traiettoria circolare e irradia il centro di rotazione; il paziente è allineato con l’asse di rotazione, mentre i rivelatori ruotano solidalmente al tubo o sono disposti in posizioni fisse attorno al gantry, come schematizzato in (Figura 07.28-07). L’introduzione di contatti rotanti a collettore (slip-ring) ha poi consentito la rotazione continua e, con lo scorrimento rettilineo del lettino durante l’acquisizione, ha dato origine alla TC elicoidale (o spirale), nella quale i piani tomografici si raccordano permettendo ricostruzioni volumetriche coerenti. In ambito di ricerca sono stati proposti anche assetti con più sorgenti distribuite su un arco o su una corona, attivate in sequenza per ridurre parti in movimento e abbreviare i tempi di acquisizione.
Per incrementare la velocità e l’estensione di copertura lungo l’asse z, si è affermata la TC Multislice (MSCT), in cui array di rivelatori a più file acquisiscono simultaneamente più sezioni a ogni rotazione del gantry, come illustrato in (Figura 07.28-08). Tempi di rotazione inferiori a 0,5 s con 4 o 16 strati per giro sono storicamente divenuti standard, mentre configurazioni più estese (decine o centinaia di file) hanno ulteriormente migliorato la risoluzione assiale e la qualità delle ricostruzioni. La geometria a cono del fascio e tecniche come lo “z-flying focal spot” aumentano la densità di campionamento lungo z, riducendo aliasing e artefatti. Parallelamente, l’adozione di algoritmi iterativi e, più recentemente, di ricostruzioni basate su modelli fisici e su apprendimento statistico ha migliorato il rapporto segnale-rumore a parità di dose.
Un avanzamento rilevante è rappresentato dai sistemi a doppia energia. Le configurazioni più diffuse impiegano due tubi a raggi X indipendenti che operano a tensioni diverse oppure una singola sorgente con commutazione rapida della kVp o filtraggi spettrali dedicati. La combinazione pesata delle immagini a bassa e alta energia permette la caratterizzazione spettrale dei tessuti e dei materiali, distinguendo strutture a bassa e alta numerosità atomica, con miglioramento della visualizzazione di tessuti molli e strutture ossee. Tecniche di decomposizione materiale consentono, ad esempio, mappe di iodio, sottrazioni virtuali senza mezzo di contrasto e riduzione di artefatti da indurimento di fascio.
La ricostruzione della sezione di un oggetto si ottiene misurando l’attenuazione del fascio X a molte angolazioni attorno al soggetto, tipicamente su 180° con opportune simmetrie di dati. Il numero di proiezioni (Figura 07.28-06) e la loro distribuzione angolare determinano la qualità di ricostruzione; nel modello concettuale dei “pallini di piombo”, ciascun elemento ad alta densità produce una firma nelle diverse proiezioni, da cui l’immagine viene ricostruita combinando le misure acquisite nelle diverse direzioni. Accanto alla retroproiezione filtrata, ampiamente utilizzata per decenni, sono oggi diffuse ricostruzioni iterative penalizzate e metodi statistici che modellano la fisica dell’acquisizione e la risposta del rivelatore, con vantaggi in termini di riduzione del rumore e contenimento della dose.
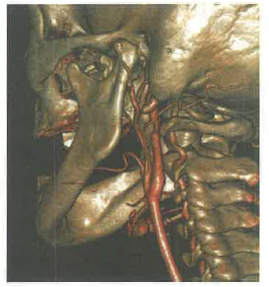
Gli artefatti possono compromettere la fedeltà diagnostica. I movimenti del paziente generano sfasamenti tra proiezioni con striature e aree ombreggiate nell’immagine ricostruita; contribuire possono anche indurimento di fascio, presenza di metalli, artefatti ad anello da rivelatori non perfettamente calibrati e errori di sincronizzazione. La stabilità operativa del tubo e dei rivelatori è quindi cruciale sia per l’ottimale ricostruzione sia per minimizzare gli artefatti di sistema. Un tipico apparato TC è mostrato in (Figura 07.28-09); esempi di immagini TC sono riportati in (Figura 07.28-10) e (Figura 07.28-11), dove, grazie all’acquisizione elicoidale e al raccordo dei piani, si ottiene la ricostruzione tridimensionale delle strutture anatomiche.
La valutazione dosimetrica merita un confronto con altri esami radiologici. Nella TC, l’immagine volumetrica è ottenuta da più sezioni contigue: la risoluzione lungo l’asse trasversale z (asse z) di (Figura 07.28-06) migliora al diminuire dello spessore di strato Δz, ma a costo di un incremento di dose. In prima approssimazione, per un dato livello di rumore, la dose richiesta cresce rapidamente al ridursi dello spessore, secondo una dipendenza che si può esprimere come \( D \propto \Delta z^{-3} \); ne consegue che dimezzare Δz comporta un aumento di dose di circa un fattore 8. Nel caso di una TC del capo, un compromesso clinicamente accettato corrisponde a una dose efficace dell’ordine di 2 mSv, equivalente a circa 100 radiografie del torace (Tabella 07.28-01). Per una TC addominale tipica (circa 11 mSv), il rischio stimato di morte per tumore attribuibile al singolo esame è dell’ordine di 6 casi ogni 10 000 pazienti, con variabilità legata a età, sesso e condizioni cliniche.
La pratica clinica adotta diverse strategie di ottimizzazione dose-immagine:
- modulazione automatica della corrente tubolare in funzione dell’attenuazione del paziente;
- scelta appropriata di kVp e filtrazione (inclusi filtri “bow-tie” e filtrazioni spettrali dedicate nella doppia energia);
- collimazione e pitch configurati per limitare la sovrapposizione delle spirali e gli sprechi di dose;
- ricostruzioni iterative e basate su modelli per ridurre il rumore a pari qualità diagnostica;
- tecniche spettrali per migliorare il contrasto senza incrementare la dose.
L’evoluzione congiunta di hardware (sorgenti, rivelatori, gantry) e software (ricostruzione, correzioni fisiche, algoritmi di riduzione artefatti) ha permesso di migliorare significativamente velocità, risoluzione e caratterizzazione tissutale, mantenendo sotto controllo la dose al paziente.
| Esame radiologico | Dose efficace (mSv) | Equivalente in RX torace |
|---|---|---|
| Radiografia arti | 0,01 – 0,05 | <1 |
| Colonna cervicale | 0,2 | 2 |
| Radiografia torace | 0,1 | 1 |
| Mammografia | 0,3 | 3 |
| Colonna lombare | 1,2 | 12 |
| Addome | 0,9 | 9 |
| Cintura pelvica | 0,7 | 7 |
| Colonna toracica | 0,6 | 6 |
| Tomografia cranio | 1,9 | 19 |
| TC seni paranasali | 2,5 | 25 |
| Urografia endovenosa | 2,9 | 29 |
| TC torace | 6,6 | 66 |
| Angiografia cardiaca | 7,7 | 77 |
| Studio baritato intestinale | 7,2 | 72 |
| Clistere baritato | 8,5 | 85 |
| Pasto baritato | 6,2 | 62 |
| TC colonna | 7,7 | 77 |
| TC pelvica | 7,3 | 73 |
| TC addome | 11,3 | 113 |
| TC tronco | 14,8 | 148 |
| Angioplastica coronarica | 15,2 | 152 |
| Radiografia panoramica dentale | 0,02 – 0,03 | <1 |
| Risonanza magnetica (RMN) | 0 | — |
| Ecografia diagnostica | 0 | — |
| PET-TC corpo intero | 25 | ≈250 |
| Fluoroscopia interventistica | 10 – 40 | 100 – 400 |
Valutazione delle dosi efficaci medie nei 20 principali Paesi europei
Stima delle dosi per tipologia di esame radiologico, calcolata sulla media complessiva dei Paesi.
La tomografia a emissione di fotone singolo (SPECT) e la tomografia a emissione di positroni (PET) sono metodiche di Medicina Nucleare non invasive, impiegate tanto nella pratica clinica quanto nella ricerca in fisiologia, biochimica tissutale e farmacologia. Entrambe sfruttano radionuclidi somministrati come traccianti e rilevano, in vivo, la radiazione emessa dai decadimenti: nella SPECT si registrano fotoni γ singoli, nella PET si sfruttano coppie di fotoni da annichilazione. La ricostruzione delle immagini adotta schemi matematici analoghi a quelli della TC, basati su proiezioni a più angoli e sulla trasformata di Radon (Figura 07.28-12), tipicamente con filtraggi e algoritmi iterativi (ad esempio OSEM) per migliorare risoluzione e contrasto.
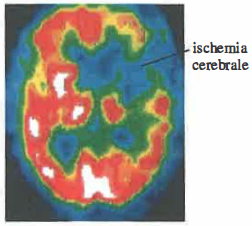
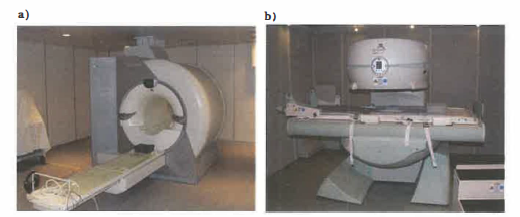
SPECT (Single Photon Emission Computed Tomography). L’obiettivo è ottenere una mappa della distribuzione di radionuclidi che emettono singoli fotoni γ. La disponibilità di radiofarmaci è ampia (ad esempio ⁹⁹ᵐTc, ¹²³I, ²⁰¹Tl), come noto in Medicina Nucleare, e rappresenta un vantaggio pratico rispetto alla PET, per la quale l’elenco di radionuclidi β⁺ impiegabili è più contenuto (Tabella 07.28-02). La strumentazione tipica impiega gamma‑camere con cristalli scintillatori (NaI(Tl) o rivelatori CZT), collimatori meccanici (fori paralleli, convergenti o pinhole) e rotazione attorno al paziente per acquisire proiezioni tomografiche (Figura 07.28-13). Le limitazioni principali sono legate alla necessità del collimatore, che riduce l’efficienza e impone un compromesso risoluzione‑sensibilità; la dose somministrabile, vincolata dai criteri di radioprotezione, condiziona ulteriormente la qualità d’immagine. L’uso di algoritmi iterativi, correzioni per attenuazione e diffusione, e l’integrazione con immagini morfologiche ad alta risoluzione (RM o TC) hanno consentito di ottenere risoluzioni spaziali dell’ordine di 6–8 mm e una più accurata localizzazione delle lesioni (Figura 07.28-14).
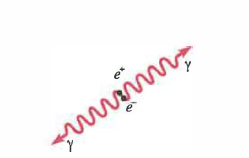
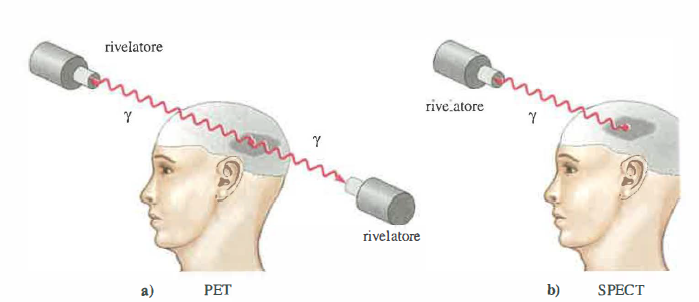
PET (Positron Emission Tomography). I radionuclidi β⁺ emettono positroni che, dopo aver percorso nel tessuto una distanza media di poco superiore al millimetro, si annichilano con elettroni atomici generando due fotoni γ di 511 keV emessi quasi in direzioni opposte (Figura 07.28-15). La rivelazione in coincidenza dei due fotoni definisce una linea di risposta lungo la quale si colloca l’evento. In (Figura 07.28-16) è confrontato il principio di rivelazione tra SPECT (collimazione meccanica) e PET (collimazione elettronica per coincidenza). I radioisotopi β⁺ più diffusi sono isotopi di elementi biologici (Tabella 07.28-02): ¹⁵O (t₁/₂ = 2,1 min), ¹³N (t₁/₂ = 10 min) e ¹¹C (t₁/₂ = 20,1 min). L’¹⁸F (t₁/₂ = 110 min) è un sostituto versatile per l’idrogeno in molte molecole; il ¹⁸F‑FDG (fluoro‑desossi‑glucosio) è il tracciante più impiegato per lo studio del metabolismo glucidico, con accumulo aumentato in tessuti a elevato consumo energetico, inclusi numerosi tumori. Sono disponibili anche traccianti per processi neurodegenerativi e sinaptici, recettori e metabolismo aminoacidico, espandendo il raggio d’azione diagnostico.
La rivelazione in coincidenza temporale avviene entro finestre dell’ordine di 10 ÷ 20 ns, riducendo gli eventi spurii e migliorando la specificità spaziale; l’impiego di cristalli a tempo di decadimento rapido (LSO, LYSO) e di rivelatori a silicio (SiPM) abilita anche la tecnologia time‑of‑flight (TOF), che stima il punto di annichilazione lungo la linea di risposta e incrementa il rapporto segnale/rumore, specialmente in pazienti di corporatura elevata. In (Figura 07.28-17) è raffigurato un tomografo PET ad anello.
I dati registrati a partire da molteplici proiezioni permettono di ricostruire la mappa di attività del radiofarmaco nelle sezioni esaminate. La risoluzione spaziale pratica dei sistemi PET clinici si colloca intorno a 2–3 mm, limitata dalla non perfetta collinearità dei fotoni di annichilazione e dalla distanza media percorsa dai positroni prima dell’annichilazione (circa 1,3 mm).
Un vantaggio peculiare della PET, rispetto alla SPECT, è la correzione accurata per l’attenuazione fotonica: i due fotoni emessi in coincidenza attraversano complessivamente lo spessore corporeo \(L\) lungo la linea di risposta, e la probabilità di trasmissione dipende unicamente dal coefficiente di attenuazione lineare \(\mu\) e dallo spessore totale attraversato.
Indicando con \(P_{\gamma 1}\) e \(P_{\gamma 2}\) le probabilità di trasmissione dei singoli fotoni, per la distribuzione \(I(x) = I_0 e^{-\mu x}\) si ottiene, lungo una direzione in cui il punto di annichilazione dista \(x\) da un rivelatore e \(L-x\) dall’opposto:
\[
P_{\gamma 1} \propto e^{-\mu x}
\quad \text{e} \quad
P_{\gamma 2} \propto e^{-\mu (L - x)}
\]
Questo modello consente di stimare la perdita di intensità dovuta all’assorbimento e di correggere i dati PET per ottenere un’immagine quantitativamente accurata dell’attività del radiofarmaco all’interno del corpo. Poiché i due fotoni γ sono emessi in direzioni opposte e devono essere rivelati in coincidenza, la probabilità complessiva di trasmissione della coppia è data dal prodotto delle singole probabilità:
\[
P_{\gamma 1 \gamma 2} = P_{\gamma 1} \, P_{\gamma 2} \propto e^{-\mu x} \, e^{-\mu (L - x)} = e^{-\mu L}
\]
Ne consegue che la probabilità di rilevazione in coincidenza dipende unicamente dallo spessore totale \(L\) attraversato dai fotoni e non dal punto preciso di annichilazione all’interno del corpo. Questo principio è alla base della correzione di attenuazione nei sistemi PET.
La dipendenza esclusiva da μ e L consente la correzione quantitativa dell’attenuazione una volta noto, lungo ogni direzione, lo spessore attraversato. A tal fine si acquisisce una TC rapida per generare la mappa di attenuazione che la PET utilizza nelle correzioni. Esempio: supponiamo che, lungo una specifica direzione, si siano verificate 12 annichilazioni (24 fotoni); se un rivelatore ne registra 9 e quello opposto 8, la coincidenza ne conta 8. Nota la coppia (μ, L) dalla TC e usando la P_{\gamma 1 \gamma 2} = P_{\gamma 1} P_{\gamma 2} \propto e^{\mu x} e^{\mu (L-x)} = e^{\mu L}, il sistema risale da 8 coincidenze ai 12 eventi effettivi. Tale passaggio è alla base della quantificazione (ad esempio mediante SUV) e della riproducibilità delle misure.
La qualità d’immagine è condizionata dal numero di fotoni collineari rivelati, ma la quantità di radionuclide somministrabile è limitata dalla radioprotezione; di conseguenza, solo una frazione ridotta degli eventi contribuisce all’immagine per diversi motivi:
- distribuzione sistemica del radiofarmaco con frazione d’accumulo limitata nel distretto bersaglio;
- angolo solido effettivo dei rivelatori, che intercettano solo una piccola parte delle coppie collineari emesse isotropicamente;
- attenuazione e diffusione dei fotoni nei tessuti con perdita di fotoni primari e introduzione di scatter;
- efficienza quantica finita, tempi morti del sistema e criteri di coincidenza che escludono eventi casuali o fuori finestra energetica.
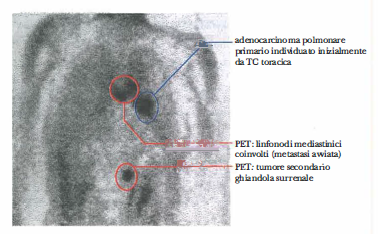
Le immagini PET hanno un ruolo cruciale nella pianificazione radioterapica e nella chirurgia oncologica, in quanto permettono la valutazione dell’estensione metabolica del tumore, l’individuazione di linfonodi sentinella e la rilevazione di metastasi spesso non evidenti con metodiche esclusivamente morfologiche (Figura 07.28-19). La fusione PET/TC e PET/RM è divenuta prassi clinica per coniugare informazione funzionale e anatomica.
| Elemento | Radionuclide | Tipo di emissione (energia in keV) | Tempo di dimezzamento (t½) |
|---|---|---|---|
| Iodio | ¹³¹I | β⁻ (608), γ (364) | 8 giorni |
| Fluoro | ¹⁸F | β⁺ (650), γ (511) | 110 minuti |
| Sodio | ²⁴Na | β⁻ (1389), γ (1369) | 15 ore |
| Carbonio | ¹¹C | β⁺ (980), γ (511) | 20,5 minuti |
| Potassio | ⁴⁰K | β⁻ (1320), γ (14,6) | 1,29·10⁹ anni |
| Idrogeno | ³H | β⁻ (18,6) | 12,26 anni |
| Ossigeno | ¹⁵O | β⁺ (1720), γ (511) | 2,5 minuti |
| Mercurio | ¹⁹⁷Hg | γ (77) | 65 ore |
| Fosforo | ³²P | β⁻ (1710) | 14,5 giorni |
| Cobalto | ⁶⁰Co | β⁻ (319), γ (1173, 1332) | 5,27 anni |
| Iodio | ¹²⁵I | γ (35) | 60 giorni |
| Xenon | ¹³³Xe | β⁻ (350), γ (81) | 5,3 giorni |
| Oro | ¹⁹⁸Au | β⁻ (960), γ (412) | 2,7 giorni |
| Carbonio | ¹⁴C | β⁻ (156) | 5640 anni |
| Tecnezio | ⁹⁹ᵐTc | γ (140) | 6 ore |
| Gallio | ⁶⁷Ga | γ (93, 185, 300) | 78 ore |
| Indio | ¹¹¹In | γ (171, 245) | 2,8 giorni |
Radionuclidi in ambito medico e biologico
Principali proprietà fisiche e usi diagnostici e terapeutici.
| Elemento | Radionuclide | Tipo di emissione (energia in keV) | Tempo di dimezzamento (t½) |
|---|---|---|---|
| Iodio | ¹³¹I | β⁻ (608), γ (364) | 8 giorni |
| Fluoro | ¹⁸F | β⁺ (650), γ (511) | 110 minuti |
| Sodio | ²⁴Na | β⁻ (1389), γ (1369) | 15 ore |
| Carbonio | ¹¹C | β⁺ (980), γ (511) | 20,5 minuti |
| Potassio | ⁴⁰K | β⁻ (1320), γ (14,6) | 1,29·10⁹ anni |
| Idrogeno | ³H | β⁻ (18,6) | 12,26 anni |
| Ossigeno | ¹⁵O | β⁺ (1720), γ (511) | 2,5 minuti |
| Mercurio | ¹⁹⁷Hg | γ (77) | 65 ore |
| Fosforo | ³²P | β⁻ (1710) | 14,5 giorni |
| Cobalto | ⁶⁰Co | β⁻ (319), γ (1173, 1332) | 5,27 anni |
| Iodio | ¹²⁵I | γ (35) | 60 giorni |
| Xenon | ¹³³Xe | β⁻ (350), γ (81) | 5,3 giorni |
| Oro | ¹⁹⁸Au | β⁻ (960), γ (412) | 2,7 giorni |
| Carbonio | ¹⁴C | β⁻ (156) | 5640 anni |
| Tecnezio | ⁹⁹ᵐTc | γ (140) | 6 ore |
| Gallio | ⁶⁷Ga | γ (93, 185, 300) | 78 ore |
| Indio | ¹¹¹In | γ (171, 245) | 2,8 giorni |
Radionuclidi in ambito medico e biologico
Principali proprietà fisiche e usi diagnostici e terapeutici.
La risonanza magnetica utilizza radiazione elettromagnetica a radiofrequenza, non ionizzante e priva di effetti stocastici documentati alle potenze impiegate in ambito clinico. Con la RM si ottengono immagini bi‑ e tridimensionali ad alto contrasto dei tessuti molli e, tramite spettroscopia, si possono indagare in situ composizione chimica e processi metabolici. L’informazione è spesso complementare a quella di TC, SPECT e PET.
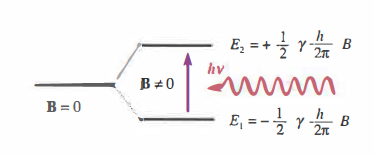
Dal punto di vista fisico, la RM è una spettroscopia in cui l’assorbimento e l’emissione di fotoni di energia \(h \nu\) avvengono tra livelli energetici quantizzati, separati dall’interazione tra momento magnetico nucleare e campo magnetico. Per i protoni (¹H), che dominano il segnale nei tessuti ricchi d’acqua, la frequenza di Larmor è \(\omega_0 = \gamma B_0\), con \(\gamma \approx 42{,}58\ \text{MHz/T}\); in campi clinici di 1,5–3,0 T corrispondono frequenze tipiche di 63,9–127,7 MHz, in accordo con l’intervallo 10 ÷ 100 MHz citato per sistemi a campi differenti. Il nucleo di idrogeno, dotato di spin e momento magnetico, in un campo B₀ si può trovare in due stati energetici (antiparallelo e parallelo a B₀), come schematizzato in (Figura 07.28-20).
L’irraggiamento del campione alla frequenza di risonanza induce transizioni tra i due livelli; cessato l’impulso a radiofrequenza, il sistema ritorna allo stato di equilibrio rilasciando energia sotto forma di segnale RM. Il segnale captato da bobine a radiofrequenza è proporzionale alla densità di protoni e modulato dai tempi di rilassamento T₁ (spin‑reticolo) e T₂ (spin‑spin), i quali riflettono l’ambiente molecolare locale e forniscono il contrasto tissutale.
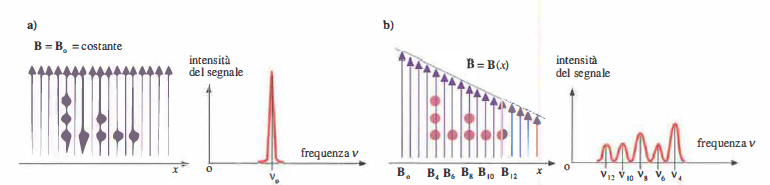
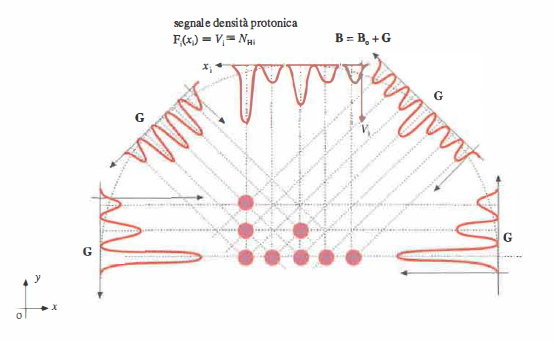
La codifica spaziale si ottiene applicando gradienti di campo magnetico, che rendono la frequenza di risonanza funzione della posizione. Variando nel tempo i gradienti lungo le tre direzioni (x, y, z), si selezionano fette e si attribuisce la codifica di fase e di frequenza ai segnali, discriminando i contributi dei diversi volumetti (Figura 07.28-21). L’insieme delle misure, interpretabile come una collezione di proiezioni della stessa grandezza fisica a più angoli e configurazioni (Figura 07.28-22), consente la ricostruzione della mappa di densità protonica e dei parametri di rilassamento. Poiché la sensibilità è principalmente verso i protoni, le immagini RM riflettono in larga misura la distribuzione dell’idrogeno, abbondante nelle molecole d’acqua e nei lipidi.
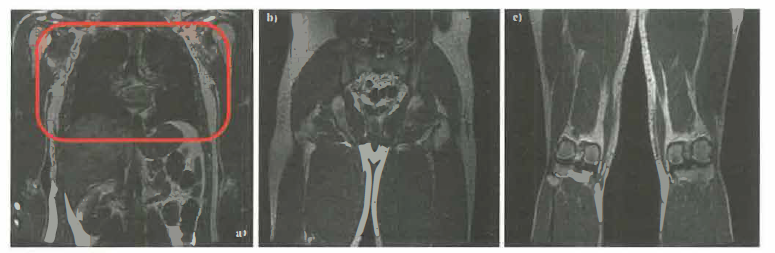
La flessibilità dei parametri di sequenza permette pesature differenti (T₁, T₂, densità protonica) e applicazioni avanzate: diffusione (DWI), perfusione, imaging funzionale BOLD, angiografia senza mezzo di contrasto, e spettroscopia ¹H‑MRS per metaboliti selezionati. Esempi di immagini cliniche sono illustrati in (Figura 07.28-23); un sistema RM a corpo intero è mostrato in (Figura 07.28-24).
Sicurezza e aspetti tecnici per il paziente. L’ambiente RM combina un forte campo magnetico statico (B₀), gradienti variabili e radiofrequenza. Questi elementi impongono misure di protezione specifiche:
- Dispositivi e impianti: i pazienti con pacemaker o defibrillatori devono segnalare il dispositivo; solo i modelli certificati “MR‑conditional” possono essere considerati secondo le specifiche del costruttore. Protesi e impianti metallici vanno valutati per composizione e ancoraggio; clip emostatiche ferromagnetiche (in particolare modelli storici) possono essere controindicate;
- Materiali e oggetti personali: rimozione di oggetti metallici ed elettronici (orologi, carte magnetiche, dispositivi indossabili) per evitare proiezione balistica, malfunzionamenti o artefatti d’immagine. Attenzione ai cavi e alle configurazioni ad anello a contatto con la pelle, che possono causare riscaldamento localizzato;
- Radiofrequenza e SAR: l’energia assorbita specifica (SAR) è controllata dal sistema secondo le normative per prevenire incrementi termici; la sorveglianza clinica è indicata in pazienti vulnerabili;
- Gradienti e comfort: la rapida commutazione dei gradienti può produrre stimolazione nervosa periferica e vibrazioni delle bobine, responsabili del elevato rumore acustico; è opportuno fornire protezione uditiva. La collaborazione del paziente e l’immobilità sono essenziali; nei soggetti claustrofobici o nei bambini può essere necessaria la sedazione con presenza di anestesista;
- Criogenia e atmosfera: i magneti superconduttori richiedono sistemi di raffreddamento a elio e azoto liquidi; in caso di rilascio di criogeni è necessaria la ventilazione e il monitoraggio dell’ossigeno ambientale per prevenire ipossia. Il controllo continuo dei sensori di O₂ nel locale RM è obbligatorio.
Queste cautele, unite ai protocolli di screening pre‑esame, consentono di sfruttare la RM in sicurezza, ottenendo un’elevata qualità d’immagine senza esposizione a radiazioni ionizzanti.