Andamenti nella tavola periodica
Definizione
Andamenti nella tavola periodica
Molte proprietà degli elementi riflettono direttamente la loro configurazione elettronica e, di conseguenza, la posizione nella tavola periodica. Poiché gli elettroni interagiscono tra loro e con il nucleo in modo non banale, le tendenze periodiche presentano eccezioni; ciononostante la tavola resta uno strumento predittivo molto efficace. La dimensione di un atomo può essere pensata come il raggio della regione in cui è più probabile trovare gli elettroni di valenza. In pratica si utilizzano raggi convenzionali (per esempio raggio covalente o metallico) per confrontare gli elementi.
Due fattori dominano l’andamento del raggio atomico lungo la tavola periodica:
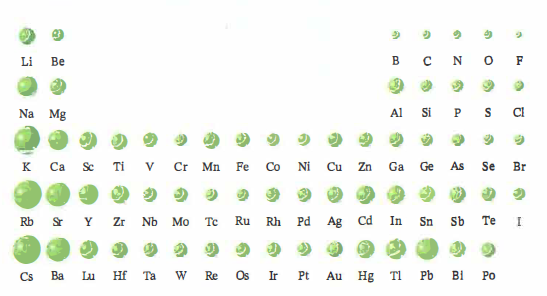
- Numero quantico principale del guscio di valenza: scendendo lungo un gruppo si occupano livelli con \(n\) crescente, la cui distanza media dal nucleo aumenta; di conseguenza il raggio atomico cresce dall’alto verso il basso (Figura 02.07-01);
- Carica nucleare efficace: lungo un periodo, da sinistra a destra, aumenta l’attrazione netta del nucleo sugli elettroni di valenza, cioè \(Z_{\mathrm{eff}}\), perché la schermatura non cresce quanto la carica nucleare; l’effetto è una contrazione del cloud elettronico e quindi un raggio minore. L’andamento non è perfettamente monotono a causa di differenze di schermatura e penetrazione tra sottolivelli \(s\), \(p\), \(d\) e \(f\), come si evince dalle irregolarità in (Figura 02.07-01).
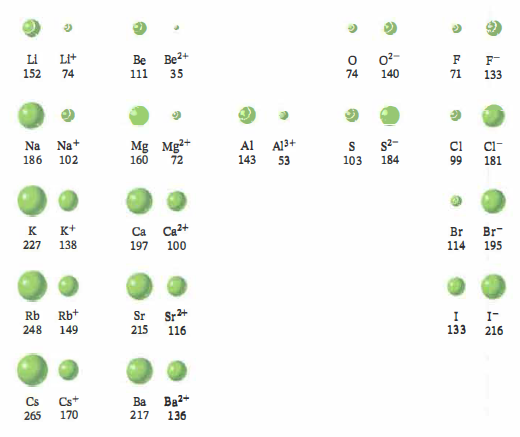
I cationi risultano più piccoli dell’atomo neutro corrispondente. La perdita di elettroni riduce le repulsioni elettrone–elettrone e, a parità di carica nucleare, aumenta \(Z_{\mathrm{eff}}\) percepita dagli elettroni rimasti; frequentemente si svuota l’intero guscio di valenza, producendo un restringimento marcato del raggio. Al contrario, gli anioni sono più grandi dell’atomo di partenza: l’acquisto di elettroni accresce le repulsioni tra elettroni e diminuisce l’attrazione netta per ciascun elettrone, espandendo il cloud elettronico.
La dipendenza dalla carica è regolare: a parità di elemento, ioni con carica positiva maggiore (per esempio \(\mathrm{Cu^{2+}}\)) sono più piccoli dei corrispondenti monovalenti (\(\mathrm{Cu^+}\)); viceversa, ioni con carica negativa multipla (come \(\mathrm{O^{2-}}\)) presentano raggi superiori rispetto agli anioni con minore carica. Un ulteriore confronto utile è nelle serie isoelettroniche (stesso numero di elettroni): lungo la serie il raggio diminuisce all’aumentare del numero atomico, poiché cresce l’attrazione nucleare a parità di schermatura. Le dimensioni relative di numerosi atomi e ioni sono riportate in (Figura 02.07-02).
L’energia di ionizzazione è l’energia necessaria per rimuovere un elettrone da un atomo isolato allo stato gassoso. Per la prima energia di ionizzazione del sodio vale, ad esempio, il processo:
\(\mathrm{Na(g)} \rightarrow \mathrm{Na^+(g)} + e^-\)
Questa grandezza misura l’intensità con cui il nucleo trattiene gli elettroni più esterni e risente sia della distanza dal nucleo sia della schermatura da parte degli elettroni interni. Nel Sistema Internazionale (SI) le energie sono espresse in \(\mathrm{kJ\,mol^{-1}}\) (talvolta in \(\mathrm{eV}\)):
- Lungo un gruppo, procedendo verso il basso, l’energia di ionizzazione diminuisce perché aumenta il raggio e la schermatura: l’elettrone di valenza è più lontano dal nucleo ed è trattenuto meno saldamente;
- Lungo un periodo, da sinistra a destra, l’energia di ionizzazione tende ad aumentare: cresce \(Z_{\mathrm{eff}}\) e il raggio si riduce, rendendo più difficile la rimozione dell’elettrone.
Queste tendenze specchiano quelle dei raggi atomici: il raggio, in generale, diminuisce dal basso verso l’alto in un gruppo e da sinistra a destra in un periodo, mentre l’energia di ionizzazione segue l’andamento opposto. Le energie di ionizzazione dei gas nobili sono tra le più elevate dell’intera tavola (Figura 02.07-03a), in accordo con la loro stabilità elettronica. Sono note alcune deviazioni sistematiche alle tendenze medie, spesso attribuibili all’inizio di nuovi sottolivelli (per esempio tra gruppi 2 e 13) o all’appaiamento elettronico nei \(p\) (per esempio tra gruppi 15 e 16).
Esercizio. Scrivere l’equazione simbolica per la prima energia di ionizzazione del sodio e indicare se il processo richiede o rilascia energia. Soluzione: il processo è \(\mathrm{Na(g)} \rightarrow \mathrm{Na^+(g)} + e^-\) ed è endotermico; l’energia richiesta è la prima energia di ionizzazione \(I_1\).
L’affinità elettronica è l’energia che si libera quando un atomo isolato allo stato gassoso acquista un elettrone formando un anione. In termini operativi, un valore elevato (grande quantità di energia rilasciata) indica che l’anione risultante è particolarmente stabilizzato. Le affinità sono espresse in \(\mathrm{kJ\,mol^{-1}}\) nel Sistema Internazionale (SI) e talvolta in \(\mathrm{eV}\). Consideriamo l’acquisto di un elettrone da parte del bromo:
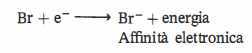
L’andamento periodico dell’affinità elettronica mostra regolarmente che:
- scendendo in un gruppo l’affinità elettronica tende a diminuire, per via della maggiore distanza del livello di valenza e della più efficace schermatura, che riducono il guadagno energetico all’aggiunta dell’elettrone;
- procedendo da sinistra a destra lungo un periodo l’affinità elettronica tende ad aumentare, in quanto cresce \(Z_{\mathrm{eff}}\) e l’aggiunta di un elettrone risulta complessivamente più stabilizzante.
Le irregolarità riportate nel grafico in (Figura 02.07-03b) mostrano che vi sono eccezioni legate a configurazioni particolarmente stabili (gusci o sottogusci semipieni o completi) e a effetti di repulsione quando l’elettrone in ingresso deve appaiarsi in un orbitale già occupato.
Esercizio. Rappresentare la formazione dello ione bromuro a partire dall’atomo di bromo allo stato gassoso e specificare la natura energetica del processo. Soluzione: \(\mathrm{Br(g) + e^- \rightarrow Br^-(g)}\) con rilascio di energia pari all’affinità elettronica del bromo.