Alcuni quadri ereditari rappresentano eccezioni alla teoria dell’ereditarietà mendeliana classica
Definizione
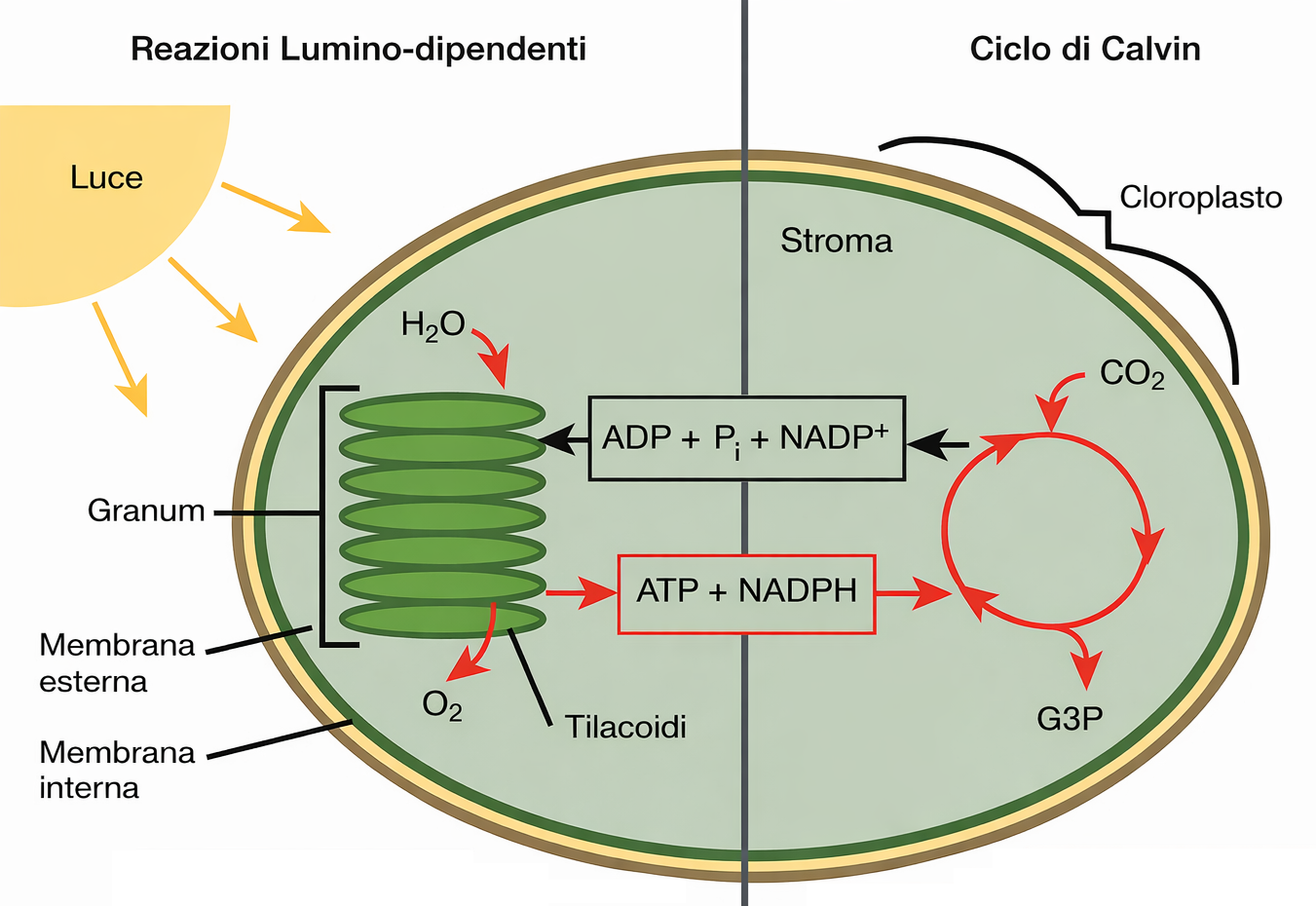
La quasi totalità del carbonio organico che sostiene gli ecosistemi contemporanei deriva dalla fotosintesi, un insieme coordinato di reazioni fotoindotte che trasformano il diossido di carbonio atmosferico (\(\mathrm{CO_2}\)) in composti ridotti. Piante, alghe e molti batteri fotosintetici evoluti, in particolare i cianobatteri, utilizzano come fonte di elettroni l’acqua e sfruttano l’energia luminosa per convertire il \(\mathrm{CO_2}\) in molecole organiche; la scissione dell’acqua libera ossigeno molecolare nell’atmosfera. L’ossigeno così prodotto alimenta la fosforilazione ossidativa non solo negli animali, ma anche nelle piante e in numerosi procarioti, e l’aumento della sua concentrazione atmosferica, innescato dall’attività dei primi fototrofi ossigenici, ha reso possibile l’evoluzione di forme di vita aerobichedipendenti dalla produzione di ATP tramite metabolismo ossidativo (Figura 05.14-01). Nelle piante superiori la fotosintesi si svolge prevalentemente nelle foglie, all’interno dei cloroplasti, organuli specializzati che catturano la radiazione solare e la convertono in equivalenti energetici e riducenti, principalmente ATP e NADPH. Questi trasportatori ad alta energia alimentano la fissazione del carbonio, mediante la quale il \(\mathrm{CO_2}\) è incorporato in scheletri carboniosi per generare zuccheri e, di conseguenza, un’ampia varietà di biomolecole.
I cloroplasti condividono principi architetturali con i mitocondri, pur differendo per dimensioni e per la presenza di un sistema di membrane aggiuntivo. L’involucro cloroplastico consta di una membrana esterna relativamente permeabile e di una membrana interna selettiva, separate da un ridotto spazio intermembrana. La membrana interna racchiude lo stroma, un compartimento ricco di enzimi del metabolismo intermedio e di componenti del corredo genetico cloroplastico, in analogia funzionale con la matrice mitocondriale. La caratteristica distintiva del cloroplasto è una terza membrana: quella tilacoidale. In essa risiedono i complessi di raccolta della luce, le catene fotosintetiche di trasporto elettronico e l’ATP sintasi responsabile della fotofosforilazione. La membrana tilacoidale è organizzata in dischi appiattiti, i tilacoidi, spesso impilati a costituire i grani; lo spazio interno ai tilacoidi è in continuità e forma il lume tilacoidale, un terzo compartimento distinto dallo stroma (Figura 05.14-02):
- involucro a doppia membrana che isola lo stroma, sede di vie biosintetiche e della fissazione del carbonio;
- membrana tilacoidale che ospita fotosistemi, citocromi e ATP sintasi e che separa il lume dallo stroma;
- orientamento funzionale dei complessi: la riduzione di \(\mathrm{NADP^+}\) e la sintesi di ATP avvengono sul lato stromale, dove i prodotti sono immediatamente disponibili per la fissazione del carbonio.
Questa organizzazione topologica consente la generazione e l’utilizzo spazialmente coordinati della forza proton-motrice e degli equivalenti riducenti. Ad esempio, in condizioni di luce intensa, il lume tilacoidale può acidificarsi fino a pH 5,5 mentre lo stroma si alcalinizza a pH 8,0, instaurando un \(\Delta pH \approx 2,5\) che alimenta l’ATP sintasi.
Il risultato netto può essere espresso in forma semplificata come:
\[\text{luce} + \mathrm{CO_2} + \mathrm{H_2O} \rightarrow \text{zuccheri} + \mathrm{O_2} + \text{calore}\]
Questa rappresentazione, sebbene utile, non esplicita i vettori energetici coinvolti. La fotosintesi procede infatti mediante due insiemi integrati di reazioni: nella prima fase la luce viene convertita in potenziale chimico sotto forma di ATP e NADPH; nella seconda, tali risorse sono consumate per ridurre il carbonio inorganico a composti organici (Figura 05.14-03).
Fase 1: reazioni fotochimiche e fotofosforilazione. Una catena di trasporto elettronico localizzata nella membrana tilacoidale sfrutta l’energia di fotoni assorbiti dai fotosistemi per estrarre elettroni dall’acqua, generando \(\mathrm{O_2}\) e protoni nel lume. Gli elettroni fluiscono attraverso una serie di trasmettitori, contribuendo alla formazione di un gradiente protonico trans-tilacoidale che guida l’ATP sintasi. Diversamente dalla fosforilazione ossidativa mitocondriale, il flusso elettronico lineare termina con la riduzione di \(\mathrm{NADP^+}\) a NADPH sul lato stromale, non con la riduzione dell’ossigeno. L’insieme dei processi accoppiati di trasporto elettronico e pompaggio protonico costituisce la fotofosforilazione. La catena fotosintetica presenta due particolarità di rilievo:
- la sorgente degli elettroni è l’acqua, la cui ossidazione a livello del fotosistema II porta alla produzione di \(\mathrm{O_2}\);
- l’orientamento dei complessi fa sì che sia l’ATP che il NADPH si accumulino nello stroma, dove vengono immediatamente impiegati dalla fissazione del carbonio.
Oltre al flusso lineare, le piante possono attivare un flusso ciclico degli elettroni intorno al fotosistema I, che incrementa la produzione di ATP senza generare NADPH, modulando così il rapporto ATP/NADPH in funzione delle richieste metaboliche.
Fase 2: fissazione del carbonio e sintesi degli zuccheri. L’ATP e il NADPH prodotti nella fase luminosa alimentano nello stroma un ciclo di reazioni enzimatiche che incorporano il \(\mathrm{CO_2}\) in accettori organici. Il prodotto netto esportabile è una trioso-fosfato, la gliceraldeide 3-fosfato, che può essere inviata al citosol per la sintesi di saccarosio o trattenuta nello stroma per la deposizione di amido. La stechiometria globale per la formazione di una trioso-fosfato può essere approssimata come:
\[3\,\mathrm{CO_2} + 9\,\mathrm{ATP} + 6\,\mathrm{NADPH} \rightarrow \mathrm{G3P} + 9\,\mathrm{ADP} + 8\,\mathrm{P_i} + 6\,\mathrm{NADP^+} + 3\,\mathrm{H_2O}\]
Queste reazioni, pur potendo procedere in assenza diretta di luce, sono strettamente dipendenti dall’attivazione indotta dalla fase luminosa. La denominazione “reazioni al buio” è pertanto fuorviante, poiché molte delle loro componenti enzimatiche vengono regolate dallo stato redox e dal gradiente ionico generati alla luce.
Le due fasi sono saldamente interconnesse da meccanismi di controllo che coordinano la produzione e l’utilizzo di potere energetico e riducente. Numerosi enzimi della fissazione del carbonio risultano inattivi in condizioni di buio e vengono attivati alla luce grazie a segnali generati dalla catena di trasporto elettronico tilacoidale. Tra i principali meccanismi regolativi si annoverano:
- alcalinizzazione dello stroma e rilascio di \(\mathrm{Mg^{2+}}\) dal lume, che modulano l’attività enzimatica e favoriscono la carbossilazione;
- il sistema ferredossina–tioredossina, che riduce ponti disolfuro su enzimi chiave, portandoli in forma attiva;
- la modulazione del rapporto ATP/NADPH tramite flusso elettronico ciclico, che adatta l’offerta energetica alle richieste della fissazione del carbonio;
- il trasporto antiporto trioso-fosfato/fosfato in membrana interna, che coordina l’esportazione dei prodotti e il riciclo del \(\mathrm{P_i}\) necessario alla fotofosforilazione.
In sintesi, la formazione di ATP e NADPH nella fase fotochimica e la successiva assimilazione del \(\mathrm{CO_2}\) in carboidrati sono processi distinti ma integrati: la loro interdipendenza assicura che la sintesi degli zuccheri avvenga in condizioni energeticamente favorevoli e in stretta risposta alle variazioni dell’ambiente luminoso (Figura 05.14-03).
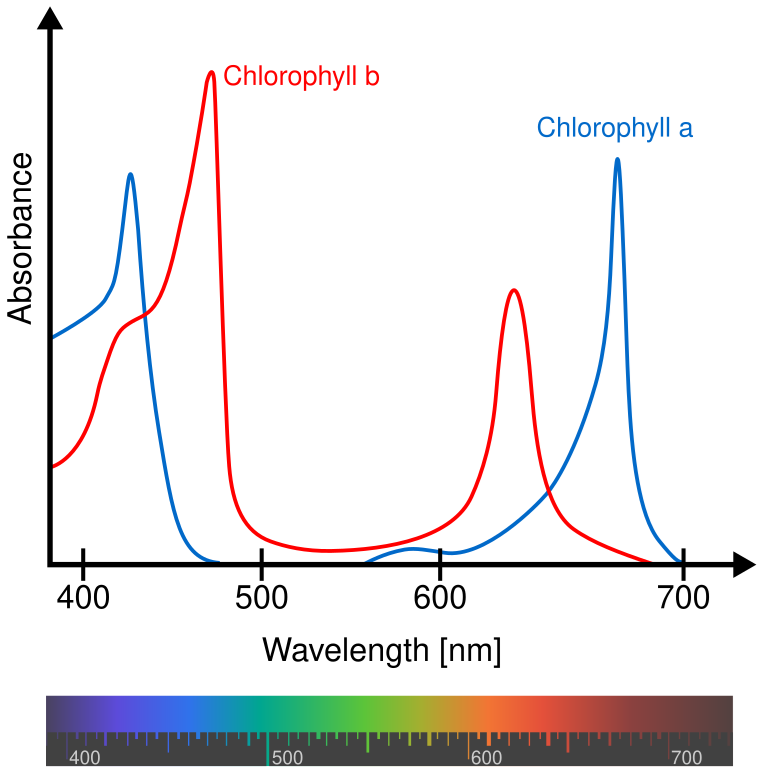
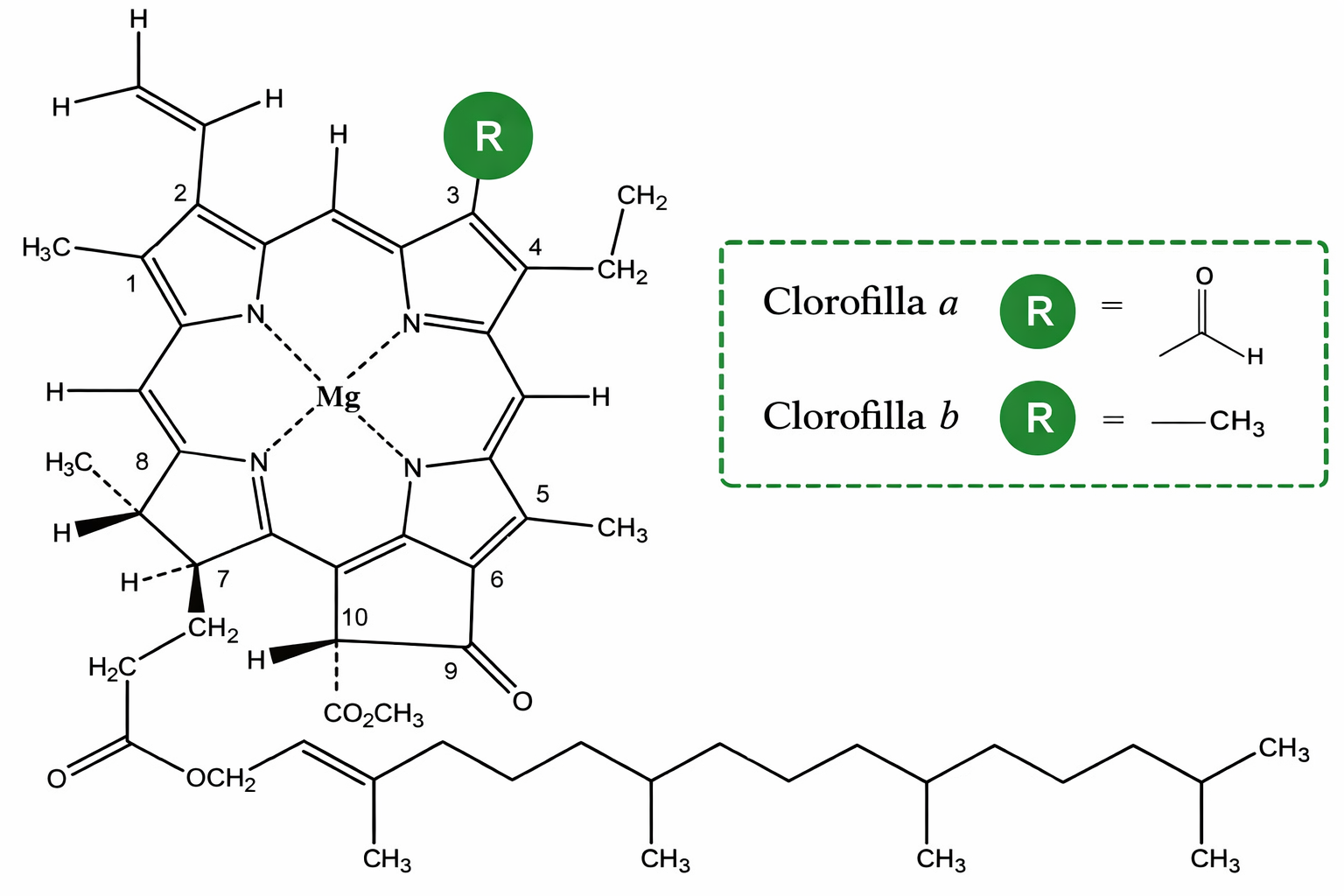
Lo spettro della radiazione visibile, porzione della radiazione elettromagnetica, si estende approssimativamente tra 400 e 700 nm, dal violetto al rosso. I pigmenti clorofilliani mostrano massimi di assorbimento nelle regioni blu e rossa, mentre risultano poco efficienti nel catturare la luce verde, che perciò viene principalmente riflessa, conferendo alle piante il tipico colore verde (Figura 05.14-04). In particolare, la clorofilla a assorbe con picchi attorno a ~430 nm e ~662 nm, mentre la clorofilla b mostra massimi nell’intorno di ~453 nm e ~642 nm, contribuendo ad ampliare la finestra di assorbimento complessiva del fotosistema. La capacità della clorofilla di attivarsi con la luce dipende dalla sua architettura elettronica. Il cromoforo principale è un anello porfirinico policiclico, ai cui doppi legami coniugati è associata una distribuzione di elettroni π delocalizzati; un catione Mg2+ centrale stabilizza la struttura, mentre una lunga coda fitolica idrofoba ancora la molecola alla membrana tilacoidale. Questo sistema π-coniugato costituisce il sito di assorbimento della luce (Figura 05.14-05). Quando un fotone di opportuna lunghezza d’onda viene assorbito, un elettrone passa a uno stato eccitato di energia superiore, alterando la densità elettronica della porfirina. Lo stato eccitato è transiente e tende a decadere verso lo stato fondamentale, liberando energia. Isolata in soluzione, la clorofilla dissipa l’energia assorbita per fluorescenza o come calore, senza compiere lavoro chimico utile. Nel contesto del cloroplasto, invece, l’interazione con specifiche proteine di membrana organizza le clorofille in complessi che ne dirigono l’energia verso trasformazioni biochimiche di interesse cellulare. Il legame tra la luce e il salto energetico elettronico è descritto dalla relazione \(E = \frac{hc}{\lambda}\), dove h è la costante di Planck e c la velocità della luce. Ad esempio, un fotone a 680 nm (regione rossa) possiede energia pari a circa 1,82 eV, sufficiente ad avviare le reazioni fotochimiche nei centri di reazione dei fotosistemi.
Nelle membrane tilacoidali delle piante e in quelle dei procarioti fotosintetici, le clorofille sono organizzate in grandi complessi proteici, i fotosistemi. Ciascun fotosistema comprende: (i) complessi antenna, che catturano e trasferiscono l’energia dei fotoni; (ii) un centro di reazione, sede della conversione dell’energia luminosa in energia chimica trasferibile. Nei complessi antenna, centinaia di clorofille e carotenoidi sono disposti con distanze e orientamenti tali da favorire il trasferimento risonante di energia tra cromofori vicini, un processo riconducibile alla Förster Resonance Energy Transfer (FRET). L’energia “migra” stocasticamente da molecola a molecola fino a raggiungere una coppia speciale di clorofille con stato eccitato leggermente a energia inferiore rispetto alle altre. Questa “trappola energetica” immagazzina l’energia con elevata efficienza, minimizzando le perdite per emissione o dissipazione termica. La coppia speciale non risiede nell’antenna ma nel centro di reazione, un complesso transmembrana di pigmenti e proteine di antichissima origine evolutiva. A contatto ravvicinato con accettori primari di elettroni, la coppia speciale, una volta eccitata, cede un elettrone ad alta energia a un trasportatore immediatamente adiacente. Questo evento di separazione di carica costituisce l’atto fotochimico primario della fotosintesi. L’elettrone, ora su un accettore, è instradato lungo una catena di trasporto elettronico; la clorofilla ossidata della coppia speciale, divenuta temporaneamente a potenziale ossidante elevato, verrà rifornita di un nuovo elettrone a valle del processo. L’allontanamento rapido dell’elettrone eccitato, attraverso una serie di trasportatori con potenziali di riduzione decrescenti, stabilizza la separazione di carica e impedisce la ricombinazione, trasformando l’energia luminosa in una forma chimica immagazzinata in elettroni ad alto potenziale di riduzione:
- nei fotosistemi delle piante superiori, la coppia speciale del fotosistema II (PSII) è denominata convenzionalmente P680, mentre quella del fotosistema I (PSI) P700;
- gli accettori primari includono, a seconda del fotosistema, molecole come feofitina e chinoni (PSII) o clorofille/feofitine specializzate e centri ferro-zolfo (PSI);
- la catena di trasporto garantisce il flusso direzionale dell’elettrone e la sua progressiva caduta di energia libera, accoppiata a funzioni utili come il pompaggio protonico.
La fissazione del carbonio a partire da CO2 richiede ingenti quantità di energia sotto forma di ATP e di potere riducente come NADPH. Negli organismi fotosintetici, questi due “combustibili” sono generati coordinando l’attività di due fotosistemi strutturalmente affini ma funzionalmente complementari. Nel fotosistema II, l’assorbimento di luce porta al trasferimento dell’elettrone eccitato a un trasportatore chinonico mobile, la plastochinone (PQ), che veicola elettroni ad alta energia verso il complesso citocromo b6f. Quest’ultimo funziona da pompa protonica tramite un meccanismo di “Q-cycle”, sfruttando l’energia del flusso elettronico per accumulare protoni nel lume tilacoidale e creare un gradiente elettrochimico. Il gradiente protonico alimenta l’ATP sintasi tilacoidale, che converte l’energia del flusso di ioni H+ in legami fosforici di alta energia, sintetizzando ATP (Figura 05.14-06). Una caratteristica cruciale del PSII è la sua capacità ossidante: la coppia speciale ossidata estrae elettroni dall’acqua mediante il complesso evolvente ossigeno (OEC), contenente un cluster Mn4CaO5. L’ossidazione dell’H2O fornisce elettroni per rigenerare la coppia speciale, libera O2 e contribuisce al gradiente protonico rilasciando H+ nel lume. Gli elettroni provenienti dal complesso b6f passano quindi alla plastocianina (PC), un trasportatore rameico solubile nel lume, che li consegna al fotosistema I. Nel PSI, l’assorbimento di fotoni eccita la coppia P700; l’elettrone ad alta energia è trasferito a una serie di accettori fino alla ferredossina (Fd), che, a sua volta, lo conferisce alla ferredossina-NADP+ reduttasi (FNR). Questo enzima riduce NADP+ a NADPH utilizzando due elettroni e un protone dello stroma (Figura 05.14-07). L’azione concertata di PSII e PSI produce, pertanto, ATP e NADPH, impiegati nella fase di assimilazione del carbonio (Figura 05.14-03):
- flusso lineare degli elettroni: PSII → PQ → citocromo b6f → PC → PSI → Fd → FNR → NADPH;
- generazione del gradiente di protoni: pompaggio attraverso b6f e rilascio di H+ da scissione dell’acqua nel lume;
- fosforilazione fotochimica: l’ATP sintasi tilacoidale (CF0CF1) utilizza il gradiente protonico per la sintesi di ATP;
- flusso ciclico degli elettroni (variabile): in condizioni di squilibrio tra fabbisogno di ATP e NADPH, il PSI può deviare elettroni verso il b6f senza produzione di NADPH, aumentando la sola resa di ATP.
Esempio numerico indicativo: per il trasferimento di 4 elettroni (equivalenti all’ossidazione di 2 H2O e alla liberazione di 1 O2) il ciclo di b6f può contribuire con ~8 H+ nel lume; l’OEC rilascia ulteriori ~4 H+. Il totale di ~12 H+ può generare un numero di molecole di ATP che dipende dalla stechiometria dell’ATP sintasi; assumendo un rapporto di 4,5–5,0 H+/ATP, si ottengono approssimativamente 2,4–2,7 ATP per O2. Valori effettivi variano in base alla composizione dell’ATP sintasi e alle condizioni fisiologiche. La cooperazione dei due fotosistemi, spesso rappresentata nello “schema a Z” dei potenziali redox, garantisce una caduta energetica sufficiente a: (i) estrarre elettroni dall’acqua, il donatore più abbondante ma chimicamente inerte; (ii) ridurre NADP+ a NADPH; (iii) accumulare un gradiente protonico utile alla sintesi di ATP. ATP e NADPH sono quindi veicolati alla fase di conversione del carbonio, dove saranno utilizzati per ridurre il CO2 a carboidrati nell’ambiente stroma del cloroplasto (Figura 05.14-03).
Lo schema fotochimico di base presenta un apparente paradosso: ogni volta che un trasportatore mobile strappa un elettrone al centro di reazione, la coppia speciale di clorofille resta nello stato ossidato, generando una carica positiva che deve essere compensata per evitare l’arresto del flusso elettronico. Nel fotosistema II (PSII) tale “debito elettronico” è ripagato da un apparato enzimatico dedicato, capace di estrarre elettroni dall’acqua. Questo complesso, localizzato sul lato luminale del tilacoide e convenzionalmente indicato come complesso evolvente ossigeno o water-splitting complex, ospita un nucleo inorganico Mn₄CaO₅ coordinato a residui proteici e molecole d’acqua. Il trasferimento elettronico avviene in modo scalare: gli elettroni sono rimossi uno per volta da due molecole di H₂O e convogliati verso la coppia speciale del PSII (P680) tramite un residuo tirosinico redox-attivo (TyrZ) della subunità D1. Una volta accumulate quattro ossidazioni equivalenti sul cluster, il ciclo si chiude con la liberazione concertata di ossigeno molecolare e protoni nel lume tilacoidale:
\[ 2\,\mathrm{H_2O} \;\rightarrow\; \mathrm{O_2} + 4\,\mathrm{H^+_{lume}} + 4\,\mathrm{e^-} \]
Il meccanismo opera per stati discreti di ossidazione (stati S del ciclo di Kok: S0→S4), svolgendo una rigorosa “contabilità a quattro elettroni” che impedisce il rilascio di specie parzialmente ossidate dell’acqua, potenzialmente dannose. Solo al compimento del quarto evento fotochimico viene emesso O₂, ossigeno che nel tempo geologico ha alimentato la composizione ossigenata dell’atmosfera terrestre. Una logica analoga di sicurezza redox, ma nella direzione inversa, governa la citocromo c ossidasi mitocondriale, la quale riceve sequenzialmente quattro elettroni per ridurre in modo coordinato l’O₂ a H₂O durante la fosforilazione ossidativa. In entrambi i casi, la gestione a pacchetti di quattro elettroni evita intermedi reattivi pericolosi.
Il fotosistema I (PSI) non ossida direttamente l’acqua: per ripristinare la sua coppia speciale (P700) dopo l’eccitazione, riceve elettroni forniti dal PSII tramite la catena di trasporto interposta. Il tracciato complessivo del flusso elettronico, segue uno schema a Z: l’energia luminosa assorbita in due stadi successivi consente di sollevare gli elettroni da un potenziale molto positivo a uno fortemente riducente. Nel dettaglio, gli elettroni estratti dall’acqua dal PSII sono trasferiti al plastochinone e, in forma ridotta (PQH₂), raggiungono il complesso del citocromo b₆-f. Quest’ultimo agisce come pompa protonica mediante un ciclo Q, rilasciando protoni nel lume e riciclando elettroni verso la plastochinone pool. Dalla b₆-f, gli elettroni passano alla plastocianina, un piccolo cuproproteide solubile nel lume, che li consegna a P700 del PSI. Una nuova eccitazione fotochimica eleva l’elettrone lungo la catena accettrice del PSI (A₀, A₁, centri ferro-zolfo) fino alla ferredossina, che a sua volta riduce NADP⁺ a NADPH per azione della ferredossina–NADP⁺ reduttasi (FNR). Grazie a questa cooperazione, l’elettrone è spostato termodinamicamente dall’acqua, che trattiene i propri elettroni con un potenziale redox di circa \(E^\circ' \approx +820\ \mathrm{mV}\), al NADPH, che li porta a un potenziale di circa \(E^\circ' \approx -320\ \mathrm{mV}\). La differenza di energia immagazzinata è sufficiente non solo per la riduzione di NADP⁺, ma anche per generare una forza proton-motrice attraverso la membrana tilacoidale. Quest’ultima risulta dalla somma di:
- rilascio di protoni nel lume durante l’ossidazione dell’acqua al PSII;
- pompaggio protonico del complesso citocromo b₆-f durante il ciclo Q;
- consumo di protoni nello stroma per la riduzione di NADP⁺ a NADPH.
La conseguente differenza di pH (tipicamente ΔpH ≈ 3,0) alimenta l’ATP sintasi cloroplastica (CF0CF1), che converte l’energia del gradiente in ATP. Una resa stechiometrica di riferimento per le reazioni fotochimiche lineari è approssimativamente:
\[ 2\,\mathrm{H_2O} + 2\,\mathrm{NADP^+} + 3\,\mathrm{ADP} + 3\,\mathrm{P_i} + \text{luce} \;\rightarrow\; \mathrm{O_2} + 2\,\mathrm{NADPH} + 3\,\mathrm{ATP}. \]
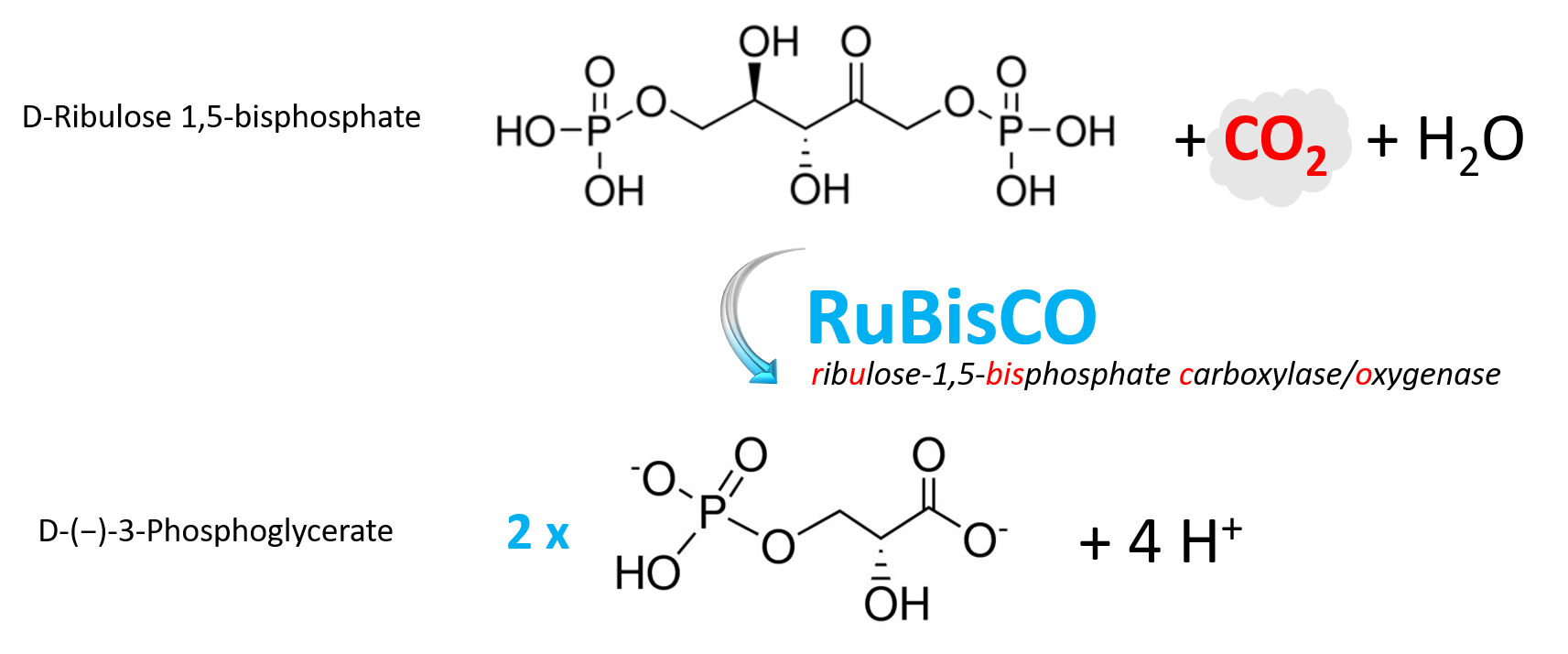
Gli eventi fotochimici producono ATP e NADPH nello stroma. Poiché la membrana interna del cloroplasto è sostanzialmente impermeabile a questi nucleotidi, il loro “valore energetico” è trasferito al metabolismo cellulare mediante la sintesi di zuccheri esportabili. Tale processo, che costituisce la fase chimica o oscura della fotosintesi, è la fissazione del carbonio. La reazione cardine è la carbossilazione del ribulosio 1,5-bisfosfato (RuBP) operata dalla ribulosio-1,5-bisfosfato carbossilasi/ossigenasi (Rubisco), un enzima stromatico di grandi dimensioni e tra i più abbondanti in natura. L’equazione complessiva della carbossilazione è:
\[ \mathrm{RuBP} + \mathrm{CO_2} + \mathrm{H_2O} \;\xrightarrow{\text{Rubisco}}\; 2\,\mathrm{3\text{-}fosfoglicerato}. \]
Nonostante la bassa velocità catalitica specifica (circa poche molecole di substrato al secondo), l’elevata concentrazione di Rubisco compensa il limite cinetico, assicurando una notevole capacità di fissazione. La Rubisco richiede attivazione carbamilativa e cofattori metallici; la luce favorisce l’attività attraverso aumenti di pH stromatico e di Mg²⁺, nonché mediante regolazione redox via tioredossina (Figura 05.14-08). Le reazioni della fissazione costituiscono il ciclo di Calvin-Benson (Figura 05.14-09), che può essere organizzato in tre fasi funzionali:
- carbossilazione: il CO₂ viene incorporato nel RuBP generando 3-fosfoglicerato;
- riduzione: il 3-fosfoglicerato è fosforilato e ridotto a triose fosfato, principalmente gliceraldeide 3-fosfato (G3P), consumando ATP e NADPH;
- rigenerazione: una parte del G3P è riorganizzata per ricostituire il RuBP, richiedendo ulteriore ATP.
Per ogni tre molecole di CO₂ che entrano nel ciclo si ottiene una molecola netta di G3P, al costo di nove ATP e sei NADPH. Il G3P costituisce il precursore per zuccheri superiori, amido, saccarosio, acidi grassi e numerosi metaboliti secondari. Sul piano energetico, la carbossilazione del RuBP è favorita, mentre il mantenimento del ciclo dipende dall’apporto continuo di energia e potere riducente dalle reazioni alla luce. È utile ricordare che la Rubisco possiede anche attività ossigenasica, che porta alla fotorespirazione con costi energetici; ciononostante, in condizioni di elevata disponibilità di CO₂ e adeguata regolazione stromatica, la via carbossilasica domina. Poiché ATP e NADPH non possono attraversare la membrana interna, l’energia della luce è “imballata” nel G3P, che viene scambiato con fosfato inorganico attraverso trasportatori specifici della membrana interna, permettendo l’integrazione con il metabolismo citosolico.
Il G3P generato nello stroma può seguire strade metaboliche alternative a seconda dello stato fisiologico della foglia. Durante periodi di intensa illuminazione, una quota significativa è trattenuta nello stroma e convertita in amido tramite l’attivazione dell’ADP-glucosio pirofosforilasi e delle sintasi dell’amido. L’amido, un polimero del glucosio paragonabile al glicogeno animale, si accumula in granuli stromatici e rappresenta una riserva transitoria e modulabile che alimenta la pianta quando l’illuminazione cala. Un’altra frazione dei triosi fosfato è destinata alla biosintesi lipidica nel plastidio, con produzione di acidi grassi e triacilgliceroli che si accumulano in goccioline lipidiche come riserva energetica e strutturale (Figura 05.14-10). Durante la notte, amido e lipidi vengono mobilizzati: l’amido è degradato a maltosio e glucosio, esportati nel citosol e convertiti in saccarosio o catabolizzati; i lipidi rilasciano acidi grassi che, dopo attivazione, possono contribuire al metabolismo ossidativo. Gli zuccheri esportati alimentano la glicolisi citosolica, con formazione di piruvato. Il piruvato, insieme ad acidi grassi, entra nei mitocondri dove sostiene il ciclo dell’acido citrico e la catena respiratoria, generando ATP per fosforilazione ossidativa (Figura 05.14-11). L’ATP mitocondriale sostiene i processi energetici del tessuto vegetale in condizioni non fotosintetiche e integra il fabbisogno della cellula in diverse condizioni ambientali. Il G3P esportato dai cloroplasti alimenta anche la sintesi di disaccaridi, in particolare il saccarosio, prodotto nel citosol attraverso la via del saccarosio-fosfato. Il saccarosio costituisce la principale forma di trasporto dei carboidrati nel floema: muovendosi dai tessuti fonte (foglie) ai tessuti sink (radici, semi, frutti), svolge un ruolo analogo a quello del glucosio nel sangue animale, assicurando una distribuzione capillare del carbonio ridotto a tutto l’organismo vegetale.