Alcheni in natura
Definizione
L’etene (etilene) rappresenta l’alchene più semplice e, in ambito biologico, agisce come fitormone chiave nella regolazione di numerosi processi vegetali. La sua biosintesi avviene a partire dalla metionina tramite S-adenosilmetionina (SAM) e 1-aminociclopropano-1-carbossilato (ACC), con l’intervento sequenziale di ACC-sintasi e ACC-ossidasi. I tessuti con elevata attività meristematica e le fasi fenologiche come maturazione dei frutti, senescenza dei fiori e abscissione fogliare mostrano un’elevata produzione di etilene; la sintesi aumenta inoltre in condizioni di stress abiotico e biotico, quali sbalzi termici, squilibri idrici o infezioni. Come regolatore gassoso, l’etene modula l’espressione genica e le vie metaboliche implicate nella colorazione, nell’ammorbidimento della polpa, nella risposta difensiva e nella modulazione della crescita.
In natura è estremamente diffusa anche la classe dei polieni, alcheni contenenti molteplici doppi legami coniugati o isolati. Una porzione significativa di tali composti appartiene alla famiglia degli isoprenoidi (o terpenoidi), derivati dall’assemblaggio di unità di isoprene, formalmente riconducibili alla formula \( \mathrm{C_5H_8} \) secondo la cosiddetta “regola dell’isoprene”, con composizione generale \( (C_5H_8)_n \) (Figura 06.09-01). L’unità biosintetica attiva non è l’isoprene libero, bensì i suoi precursori pirofosforilati, isopentenil pirofosfato (IPP) e dimetilallil pirofosfato (DMAPP), prodotti in due vie distinte e complementari: la via del mevalonato (citosolica) e la via MEP/DOXP (plastidiale).
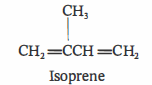 |
| Struttura dell’isoprene. |
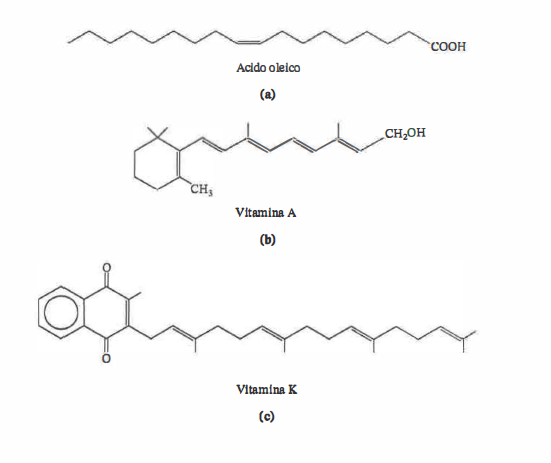
Gli isoprenoidi comprendono categorie funzionalmente e strutturalmente eterogenee, tra cui steroidi, pigmenti fotosintetici (clorofille e carotenoidi) e vitamine liposolubili A, D, E e K (Figura 06.09-02). In termini di numero di unità isopreniche si distinguono:
- monoterpeni (C10), formati da due unità isopreniche, spesso volatili e aromatici;
- sesquiterpeni (C15), frequenti negli oli essenziali e con marcata diversità strutturale;
- diterpeni (C20), tra cui fitolo e molte molecole bioattive di origine vegetale;
- triterpeni (C30), precursori degli steroidi e di numerosi saponosidi;
- tetraterpeni (C40), come i carotenoidi, fondamentali per fotoprotezione e trasferimento di energia.
Le vitamine A, D, E e K illustrano bene la versatilità biochimica del gruppo: il retinoide (vitamina A) è cruciale per la visione e il differenziamento cellulare; la vitamina D modula l’omeostasi del calcio e la fisiologia scheletrica; la vitamina E svolge principalmente funzioni antiossidanti nella membrana; la vitamina K è cofattore essenziale nella carbossilazione di residui glutammici in proteine coinvolte nella coagulazione.
Nell’ambito dei monoterpeni, diversi composti sono responsabili degli aromi tipici di piante e fiori. Il geraniolo, un alcol monoterpenico presente in molte essenze floreali, deriva dall’unione di due unità isopreniche e costituisce un componente caratteristico degli oli di geranio e di altre specie aromatiche. Oltre all’impiego in profumeria, è incluso in formulazioni repellenti a base vegetale, dove contribuisce a una protezione temporanea contro insetti ematofagi; la durata dell’effetto dipende dalla concentrazione, dalla matrice formulativa e dalle condizioni ambientali.
Il D-limonene è il principale costituente degli oli essenziali ottenuti dalle scorze degli agrumi ed è impiegato come aroma alimentare e, soprattutto, come solvente “a base bio” in grado di sostituire, in varie applicazioni, frazioni petrolifere e solventi alogenati, con vantaggi in termini di odore, profilo di sicurezza e biodegradabilità. La chiralità del limonene è didatticamente rilevante: l’enantiomero destrogiro (D) è associato a note olfattive agrumate, mentre l’enantiomero levogiro (L) richiama sentori resinati, simili alla trementina. Tali differenze olfattive discendono dall’interazione enantioselettiva con i recettori olfattivi.
Il mircene, un altro monoterpene, si riscontra, tra l’altro, nelle foglie d’alloro e nel luppolo; trova impiego in profumeria come modulatore delle note verdi ed erbacee ed è talora presente in tracce in bevande aromatizzate come parte del profilo sensoriale complessivo. Per la sua reattività, il mircene è anche un utile intermedio nella sintesi di altri terpeni di interesse industriale.
Il jasmone, naturalmente presente in gelsomino, fiori d’agrumi e altre specie ornamentali, è ampiamente adottato in ambito cosmetico e profumistico per conferire sfumature floreali complesse. In alcuni prodotti per la cura della pelle è proposto come coadiuvante cosmetico; sono stati ipotizzati effetti di supporto alla funzionalità della matrice extracellulare attraverso la modulazione di vie cellulari coinvolte nel rinnovamento epidermico, sebbene l’evidenza debba essere valutata caso per caso sulla base di studi controllati e della concentrazione impiegata.
Tra i diterpenoidi e i composti correlati merita menzione il retinal, forma aldeidica della vitamina A (Figura 06.09-02). Nella fisiologia visiva, l’11-cis-retinal è il cromoforo della rodopsina; in ambito dermocosmetico, retinoidi affini (per esempio retinaldeide e retinolo) sono noti per la capacità di influenzare il turnover cellulare e la sintesi di componenti dermiche come collagene ed elastina, con conseguenti benefici sull’aspetto e sulla consistenza della pelle, in relazione al dosaggio e alla veicolazione.