Alcani
Definizione
Nella descrizione delle molecole organiche si impiegano rappresentazioni con diverso livello di dettaglio, ciascuna utile per rispondere a domande specifiche sulla composizione e sulla connettività. In particolare, si distinguono: formula molecolare, formula di struttura, formula condensata e formula prospettica. La formula molecolare enuncia soltanto il tipo e il numero di atomi presenti, senza specificare come essi siano collegati tra loro. Per esempio, per gli alcani più semplici (metano, etano, propano e butano) la formula molecolare consente di stabilire la composizione; tuttavia, mentre per metano, etano e propano la connettività è univoca, per C4H10 sono possibili due diverse strutture. Per identificare la corretta disposizione dei legami è indispensabile ricorrere alla formula di struttura, che esplicita le connessioni tra gli atomi.
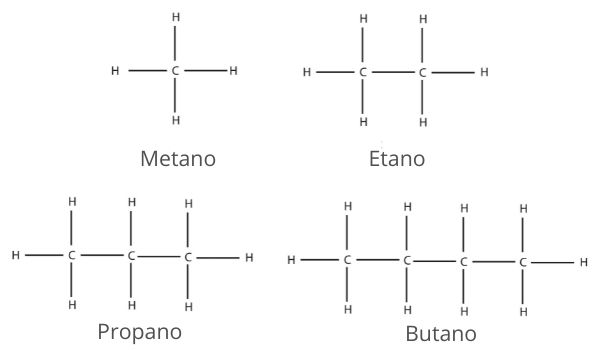 |
| Serie omologa degli alcani. |
La formula di struttura visualizza in modo completo la topologia della molecola, ma può risultare ingombrante per composti di grandi dimensioni. Una soluzione intermedia è la formula condensata, che elenca tutti gli atomi seguendo l’ordine di legame, offrendo compattezza senza rinunciare alla connettività essenziale. Nella (Tabella 06.02-01) sono riportati nomi, formule e alcune proprietà fisiche dei primi dieci alcani a catena lineare (n-alcani), utili per cogliere l’andamento regolare delle grandezze fisiche lungo la serie omologa.
Un’ulteriore rappresentazione, estremamente pratica nelle strutture organiche, è la formula a segmenti (o “line-angle”): ogni estremità o vertice di segmento sottintende un atomo di carbonio e gli atomi di idrogeno legati al carbonio sono omessi, assumendo che ciascun carbonio raggiunga valenza quattro. La figura seguente illustra le formule di struttura e a segmenti del butano e del metilpropano, mettendo a confronto la catena lineare e la catena ramificata:
 |
| Isomeria strutturale del butano. |
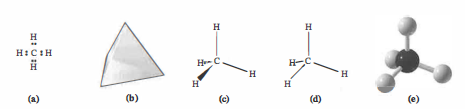
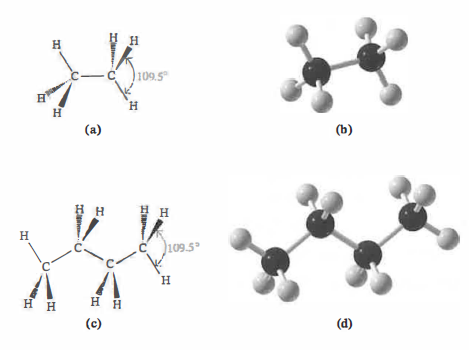
Il carbonio è tetravalente: forma quattro legami covalenti (singoli o multipli) condividendo quattro coppie di elettroni; l’idrogeno, avendo un solo elettrone, è monovalente. La struttura di Lewis del metano evidenzia quattro coppie condivise (Figura 06.02-01). Quando un carbonio forma quattro legami singoli, questi sono legami \(\sigma\) e l’atomo adotta un’ibridazione \(\mathrm{sp^3}\) con angoli di legame ideali pari a \(109,5^\circ\). Tale previsione si ottiene anche mediante il modello VSEPR (Valence-Shell Electron-Pair Repulsion), che minimizza le repulsioni tra coppie elettroniche nel guscio di valenza. Ne risulta la geometria tetraedrica tipica degli alcani; il solido regolare corrispondente è illustrato in (Figura 06.02-01). La proiezione tridimensionale si rende spesso con codici grafici convenzionali: legami su piano (linee), verso l’osservatore (cunei pieni) e dietro il piano (cunei tratteggiati), come in (Figura 06.02-01); rappresentazioni equivalenti, ma più stilizzate, sono mostrate in (Figura 06.02-01). Il modello a sfere e bastoncini (Figura 06.02-01) enfatizza distanza e angoli di legame; proiezioni 3D di due alcani elementari sono riportate in (Figura 06.02-02).
Per completezza, si richiamano le principali notazioni, con la loro funzione didattica:
- formula molecolare: riporta soltanto conteggio e specie atomiche, ad esempio la legge generale degli alcani \(C_nH_{2n+2}\);
- formula di struttura: esplicita tutte le connessioni tra gli atomi, utile per distinguere isomeri di costituzione;
- formula condensata: conserva l’informazione sulla connettività in modo compatto, in sequenza lineare;
- formula prospettica: rende la tridimensionalità tramite convenzioni grafiche (linee, cunei, tratteggi), o modelli molecolari, per ragionare su geometria e stereochimica.
Le proprietà fisiche degli idrocarburi alifatici riflettono la loro bassa polarizzabilità direzionale e l’assenza di momenti dipolari permanenti: sono generalmente apolari, insolubili in acqua e ben solubili in solventi organici apolari; presentano punti di fusione ed ebollizione relativamente bassi e densità inferiori a quella dell’acqua. L’incremento della lunghezza della catena carboniosa (quindi della massa molecolare e dell’area superficiale efficace) produce un aumento regolare dei punti di fusione e ebollizione e, in minor misura, della densità, come evidenziato dalla (Tabella 06.02-01). L’origine microscopica di tali andamenti risiede nel rafforzamento delle interazioni di dispersione di London al crescere dell’area di contatto tra molecole.
| Nome | Formula molecolare | Formula condensata | T. di fusione (°C) | T. di ebollizione (°C) | Osservazioni cliniche / Applicazioni |
|---|---|---|---|---|---|
| Metano | CH₄ | CH₄ | −182.5 | −162.2 | Gas semplice, usato come fonte energetica; in elevate concentrazioni può indurre ipossia. |
| Etano | C₂H₆ | CH₃–CH₃ | −183.9 | −88.6 | Idrocarburo volatile; inalazioni elevate possono causare narcosi. |
| Propano | C₃H₈ | CH₃–CH₂–CH₃ | −187.6 | −42.1 | Componente di gas combustibili; esposizione acuta può deprimere il sistema nervoso centrale. |
| Butano | C₄H₁₀ | CH₃–(CH₂)₂–CH₃ | −137.2 | −0.5 | Utilizzato come propellente; inalazioni non controllate associate a rischio aritmico. |
| Pentano | C₅H₁₂ | CH₃–(CH₂)₃–CH₃ | −129.8 | 36.1 | Solvente organico; esposizione non controllata può avere effetti neurotossici. |
| Esano | C₆H₁₄ | CH₃–(CH₂)₄–CH₃ | −95.2 | 68.8 | Impiegato in estrazioni industriali; esposizioni croniche correlate a neuropatie periferiche. |
| Eptano | C₇H₁₆ | CH₃–(CH₂)₅–CH₃ | −90.6 | 98.4 | Standard in studi di combustione; può indurre irritazione delle mucose. |
| Ottano | C₈H₁₈ | CH₃–(CH₂)₆–CH₃ | −56.9 | 125.6 | Riferimento per indice di ottano; rilevante in tossicologia ambientale. |
| Nonano | C₉H₂₀ | CH₃–(CH₂)₇–CH₃ | −53.6 | 150.7 | Liquido idrofobico, utilizzato in solventi e rivestimenti. |
| Decano | C₁₀H₂₂ | CH₃–(CH₂)₈–CH₃ | −29.8 | 174.0 | Studiato come modello di lipidi idrofobici nelle ricerche farmacologiche. |
| Dodecano | C₁₂H₂₆ | CH₃–(CH₂)₁₀–CH₃ | −9.6 | 216.0 | Componente di membrane artificiali usate in studi di biologia cellulare. |
| Tetradecano | C₁₄H₃₀ | CH₃–(CH₂)₁₂–CH₃ | 5.9 | 253.0 | Standard cromatografico; presente nei lipidi naturali. |
| Esadecano | C₁₆H₃₄ | CH₃–(CH₂)₁₄–CH₃ | 18.0 | 287.0 | Riferimento sperimentale per la fluidità delle membrane biologiche. |
Alcani lineari: primi dieci composti
I primi dieci alcani a catena continua, con i rispettivi nomi e formule chimiche.
| Nome | Formula molecolare | Formula condensata | T. di fusione (°C) | T. di ebollizione (°C) | Osservazioni cliniche / Applicazioni |
|---|---|---|---|---|---|
| Metano | CH₄ | CH₄ | −182.5 | −162.2 | Gas semplice, usato come fonte energetica; in elevate concentrazioni può indurre ipossia. |
| Etano | C₂H₆ | CH₃–CH₃ | −183.9 | −88.6 | Idrocarburo volatile; inalazioni elevate possono causare narcosi. |
| Propano | C₃H₈ | CH₃–CH₂–CH₃ | −187.6 | −42.1 | Componente di gas combustibili; esposizione acuta può deprimere il sistema nervoso centrale. |
| Butano | C₄H₁₀ | CH₃–(CH₂)₂–CH₃ | −137.2 | −0.5 | Utilizzato come propellente; inalazioni non controllate associate a rischio aritmico. |
| Pentano | C₅H₁₂ | CH₃–(CH₂)₃–CH₃ | −129.8 | 36.1 | Solvente organico; esposizione non controllata può avere effetti neurotossici. |
| Esano | C₆H₁₄ | CH₃–(CH₂)₄–CH₃ | −95.2 | 68.8 | Impiegato in estrazioni industriali; esposizioni croniche correlate a neuropatie periferiche. |
| Eptano | C₇H₁₆ | CH₃–(CH₂)₅–CH₃ | −90.6 | 98.4 | Standard in studi di combustione; può indurre irritazione delle mucose. |
| Ottano | C₈H₁₈ | CH₃–(CH₂)₆–CH₃ | −56.9 | 125.6 | Riferimento per indice di ottano; rilevante in tossicologia ambientale. |
| Nonano | C₉H₂₀ | CH₃–(CH₂)₇–CH₃ | −53.6 | 150.7 | Liquido idrofobico, utilizzato in solventi e rivestimenti. |
| Decano | C₁₀H₂₂ | CH₃–(CH₂)₈–CH₃ | −29.8 | 174.0 | Studiato come modello di lipidi idrofobici nelle ricerche farmacologiche. |
| Dodecano | C₁₂H₂₆ | CH₃–(CH₂)₁₀–CH₃ | −9.6 | 216.0 | Componente di membrane artificiali usate in studi di biologia cellulare. |
| Tetradecano | C₁₄H₃₀ | CH₃–(CH₂)₁₂–CH₃ | 5.9 | 253.0 | Standard cromatografico; presente nei lipidi naturali. |
| Esadecano | C₁₆H₃₄ | CH₃–(CH₂)₁₄–CH₃ | 18.0 | 287.0 | Riferimento sperimentale per la fluidità delle membrane biologiche. |
Alcani lineari: primi dieci composti
I primi dieci alcani a catena continua, con i rispettivi nomi e formule chimiche.
Si definiscono isomeri di struttura (o isomeri costituzionali) specie molecolari aventi la stessa formula molecolare ma diversa connettività tra gli atomi. Differendo la struttura, variano anche proprietà fisiche e reattività chimica. I dati riportati nella (Tabella 06.02-03) e (Tabella 06.02-04) mostrano che, per il sistema C6H14, gli isomeri ramificati hanno, in media, temperature di fusione ed ebollizione inferiori rispetto all’isomero lineare, l’n-esano. La ragione è geometrica: la ramificazione riduce l’area superficiale accessibile e diminuisce l’efficacia delle interazioni di van der Waals tra catene adiacenti.
L’isomero lineare di C6H14, n-esano, possiede una catena continua di sei atomi di carbonio; gli altri quattro isomeri presentano uno o più centri di ramificazione, come illustrato di seguito:
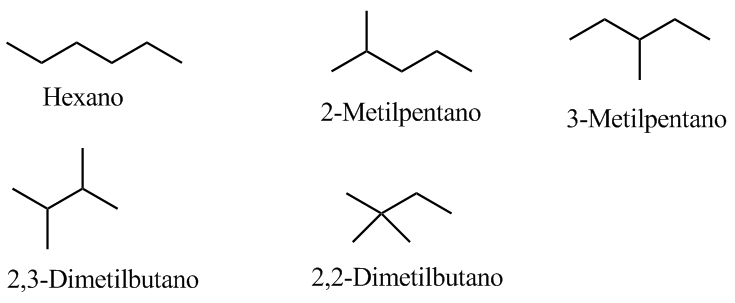 |
| Isomeri strutturali dell’esano. |
Le differenze di forma molecolare influenzano il modo in cui le particelle si avvicinano e interagiscono nello stato liquido e solido. Catene lineari, potendo “impacchettarsi” con maggiore efficienza e massimizzando l’area di contatto, manifestano interazioni di dispersione più intense e dunque punti di ebollizione più elevati. Al contrario, le molecole ramificate sono più compatte e offrono minore superficie per le interazioni intermolecolari, con conseguente abbassamento del punto di ebollizione. Per i punti di fusione, oltre all’intensità delle forze di coesione, gioca un ruolo importante la simmetria cristallografica: strutture più simmetriche possono talvolta impaccarsi meglio nel reticolo, risultando in punti di fusione non perfettamente monotoni con il grado di ramificazione.
In sintesi, a parità di formula molecolare, il confronto lineare/ramificato segue tendenze generali:
- area superficiale: maggiore nelle catene lineari, minore nelle molecole ramificate;
- forze di dispersione (van der Waals): più marcate per le catene estese, attenuate per strutture compatte;
- punto di ebollizione: tende a crescere con la linearità e a diminuire con la ramificazione;
- punto di fusione: dipende sia dalla forza delle interazioni sia dall’efficienza di impaccamento; la simmetria può innalzarlo anche in isomeri relativamente compatti.
I valori sperimentali dei punti di fusione ed ebollizione dei cinque isomeri di C6H14 sono riportati nella (Tabella 06.02-02). Considerazioni analoghe si applicano ad altri insiemi isomerici, come C5H12, in cui l’aumento della ramificazione diminuisce progressivamente il punto di ebollizione pur mantenendo identica la formula molecolare.
| Gruppo alchilico | Denominazione | Descrizione |
|---|---|---|
| —CH₃ | Metile | Unità monocarboniosa semplice, coinvolta nei processi di metilazione del DNA, con impatto diretto sull’espressione genica ed epigenetica. |
| —CH₂–CH₃ | Etilico | Catena a due atomi di carbonio, frequente in molecole farmacologiche; la sostituzione etilica può modificare lipofilia e biodisponibilità. |
| —CH₂–CH₂–CH₃ | Propilico | Presente in derivati organici usati come solventi e intermedi; influenza la permeabilità delle membrane cellulari. |
| —CH₂–CH₂–CH₂–CH₃ | Butilico | Sostituente di quattro atomi di carbonio, utilizzato in farmaci per aumentare la solubilità lipidica e la distribuzione tissutale. |
| —CH₂–CH₂–CH₂–CH₂–CH₃ | Pentilico | Catena a cinque atomi di carbonio; caratterizza composti volatili e modula la farmacocinetica delle molecole bioattive. |
| —(CH₂)₅–CH₃ | Esilico | Gruppo lipofilo allungato, sfruttato nella progettazione di molecole con maggiore affinità per le membrane lipidiche. |
| —(CH₂)₆–CH₃ | Eptilico | Più raro nei farmaci, ma rilevante nello studio delle code idrofobiche presenti nei lipidi naturali. |
| —(CH₂)₇–CH₃ | Ottilico | Catena estesa che incrementa in modo significativo la liposolubilità; utile in sistemi di rilascio controllato dei farmaci. |
Sostituenti alchilici lineari
Nomi e formule dei primi gruppi alchilici a catena continua.
| Formula di struttura | Classificazione | Denominazione d’uso (comune) | Nome IUPAC | Descrizione |
|---|---|---|---|---|
| CH₃–CH–CH₃ | Secondario (2°) | Isopropile | 1-metiletilico | Gruppo frequentemente presente in disinfettanti e solventi clinici (es. alcol isopropilico), noto per le proprietà antisettiche e sgrassanti. |
| CH₃–CH(CH₃)– | Primario (1°) | Isobutile | 2-metilpropile | Catena ramificata utilizzata in derivati farmacologici e intermedi chimici, con influenza sulla liposolubilità. |
| CH₃–CH₂–CH(CH₃)– | Secondario (2°) | sec-Butile | 1-metilpropile | Struttura ramificata che compare in solventi organici; la configurazione secondaria può modificare la reattività metabolica. |
| (CH₃)₃C– | Terziario (3°) | t-Butile o tert-Butile | 1,1-dimetiletilico | Gruppo voluminoso che riduce la reattività della molecola; usato come sostituente protettivo in sintesi organiche, con implicazioni in chimica farmaceutica. |
Sostituenti alchilici ramificati
Struttura e denominazione di alcuni gruppi alchilici a catena ramificata.
| Nome | Formula condensata | T. di ebollizione (°C) | T. di fusione (°C) | Osservazioni cliniche / Applicazioni |
|---|---|---|---|---|
| n-Esano | CH₃–CH₂–CH₂–CH₂–CH₂–CH₃ | 68.8 | −95.2 | Impiegato come solvente; esposizione cronica associata a neuropatie periferiche. |
| 2-Metilpentano | CH₃–CH(CH₃)–CH₂–CH₂–CH₃ | 60.9 | −153.2 | Isomero ramificato, volatile; potenziale irritante respiratorio. |
| 3-Metilpentano | CH₃–CH₂–CH(CH₃)–CH₂–CH₃ | 63.3 | −118 | Utilizzato come solvente; esposizione acuta può indurre narcosi leggera. |
| 2,3-Dimetilbutano | CH₃–CH(CH₃)–CH(CH₃)–CH₃ | 58.1 | −130.2 | Liquido volatile; raramente impiegato in ambito clinico, più diffuso in applicazioni industriali. |
| 2,2-Dimetilbutano | CH₃–C(CH₃)₂–CH₂–CH₃ | 49.8 | −100.2 | Maggiore ramificazione, minore punto di ebollizione; solvente organico in laboratorio. |
| 3,3-Dimetilbutano | CH₂(CH₃)₂–C(CH₃)₂ | 57.9 | −105 | Isomero ulteriore dell’esano, poco diffuso ma rilevante come modello in studi di stabilità molecolare. |
| Cicloesano | C₆H₁₂ (anello saturo) | 80.7 | 6.5 | Analogo ciclico, usato come modello sperimentale di conformazioni molecolari. |
Punti di fusione ed ebollizione degli isomeri dell’esano (C₆H₁₄)
Sintesi delle temperature di fusione e di ebollizione dei cinque isomeri costituzionali di formula C₆H₁₄.
Con il termine gruppo alchilico, indicato convenzionalmente con la lettera R, si intende il frammento che si ottiene da un alcano per rimozione di un atomo di idrogeno. Per gli alcani aciclici vale la relazione generale \( \mathrm{C_nH_{2n+2}} \); di conseguenza, i corrispondenti gruppi alchilici hanno formula \( \mathrm{C_nH_{2n+1}-} \), dove il trattino rappresenta il punto di attacco al resto della molecola. La denominazione deriva da quella dell’alcano con pari numero di atomi di carbonio sostituendo il suffisso -ano con -ile: il frammento −CH3 è detto metile, mentre −CH2CH3 è un etile. La linea terminale nelle strutture di questi gruppi indica la valenza libera disponibile per legare un altro atomo o gruppo. I primi cinque gruppi alchilici lineari ottenibili dai corrispondenti n-alcani sono riportati nella (Tabella 06.02-03).
Negli idrocarburi saturi si adotta una classificazione degli atomi di carbonio in base al numero di vicini carboniosi: un carbonio primario (1°) è connesso a un solo atomo di carbonio, un secondario (2°) a due, un terziario (3°) a tre e un quaternario (4°) a quattro. In modo analogo, si definisce il tipo di un gruppo alchilico considerando il grado del carbonio che realizza il legame di unione con il resto della molecola. Tutti i gruppi alchilici a catena non ramificata sono primari (Tabella 06.02-03). Esempi di gruppi ramificati sono elencati nella (Tabella 06.02-04): fra questi, i gruppi isopropilico e sec-butilico sono secondari, l’isobutilico è primario, mentre il t-butilico (tert-butile) è terziario. Nella nomenclatura IUPAC sistematica, sono correnti le forme propan-2-il per isopropile, butan-2-il per sec-butile, 2-metilpropil per isobutile e 1,1-dimetiletil per tert-butile, impiegate in alternativa alle denominazioni tradizionali quando richiesto da contesti formali.
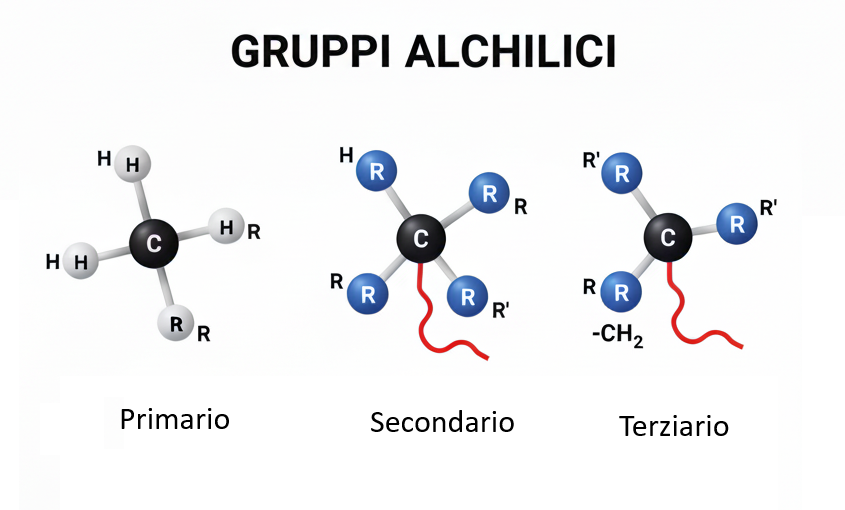 |
| Gruppi alchilici. |
Oltre agli alchilici, sono frequenti gruppi cicloalchilici, ottenuti da cicloalcani per rimozione di un idrogeno, come cicloesil e ciclopropil; anch’essi seguono le medesime regole di classificazione primaria/secondaria/terziaria in funzione del carbonio di collegamento. Nella pratica, si utilizzano R, R′, R″ per indicare genericamente gruppi alchilici non specificati, e Ar per gruppi arilici, evitando l’equivoco con i “radicali” intesi come specie a elettrone spaiato: in questo contesto, radicale va inteso nel senso storico di sostituente.
| Gruppo alchilico | Denominazione | Descrizione |
|---|---|---|
| —CH₃ | Metile | Unità monocarboniosa semplice, coinvolta nei processi di metilazione del DNA, con impatto diretto sull’espressione genica ed epigenetica. |
| —CH₂–CH₃ | Etilico | Catena a due atomi di carbonio, frequente in molecole farmacologiche; la sostituzione etilica può modificare lipofilia e biodisponibilità. |
| —CH₂–CH₂–CH₃ | Propilico | Presente in derivati organici usati come solventi e intermedi; influenza la permeabilità delle membrane cellulari. |
| —CH₂–CH₂–CH₂–CH₃ | Butilico | Sostituente di quattro atomi di carbonio, utilizzato in farmaci per aumentare la solubilità lipidica e la distribuzione tissutale. |
| —CH₂–CH₂–CH₂–CH₂–CH₃ | Pentilico | Catena a cinque atomi di carbonio; caratterizza composti volatili e modula la farmacocinetica delle molecole bioattive. |
| —(CH₂)₅–CH₃ | Esilico | Gruppo lipofilo allungato, sfruttato nella progettazione di molecole con maggiore affinità per le membrane lipidiche. |
| —(CH₂)₆–CH₃ | Eptilico | Più raro nei farmaci, ma rilevante nello studio delle code idrofobiche presenti nei lipidi naturali. |
| —(CH₂)₇–CH₃ | Ottilico | Catena estesa che incrementa in modo significativo la liposolubilità; utile in sistemi di rilascio controllato dei farmaci. |
Sostituenti alchilici lineari
Nomi e formule dei primi gruppi alchilici a catena continua.
| Gruppo alchilico | Denominazione | Descrizione |
|---|---|---|
| —CH₃ | Metile | Unità monocarboniosa semplice, coinvolta nei processi di metilazione del DNA, con impatto diretto sull’espressione genica ed epigenetica. |
| —CH₂–CH₃ | Etilico | Catena a due atomi di carbonio, frequente in molecole farmacologiche; la sostituzione etilica può modificare lipofilia e biodisponibilità. |
| —CH₂–CH₂–CH₃ | Propilico | Presente in derivati organici usati come solventi e intermedi; influenza la permeabilità delle membrane cellulari. |
| —CH₂–CH₂–CH₂–CH₃ | Butilico | Sostituente di quattro atomi di carbonio, utilizzato in farmaci per aumentare la solubilità lipidica e la distribuzione tissutale. |
| —CH₂–CH₂–CH₂–CH₂–CH₃ | Pentilico | Catena a cinque atomi di carbonio; caratterizza composti volatili e modula la farmacocinetica delle molecole bioattive. |
| —(CH₂)₅–CH₃ | Esilico | Gruppo lipofilo allungato, sfruttato nella progettazione di molecole con maggiore affinità per le membrane lipidiche. |
| —(CH₂)₆–CH₃ | Eptilico | Più raro nei farmaci, ma rilevante nello studio delle code idrofobiche presenti nei lipidi naturali. |
| —(CH₂)₇–CH₃ | Ottilico | Catena estesa che incrementa in modo significativo la liposolubilità; utile in sistemi di rilascio controllato dei farmaci. |
Sostituenti alchilici lineari
Nomi e formule dei primi gruppi alchilici a catena continua.
| Formula di struttura | Classificazione | Denominazione d’uso (comune) | Nome IUPAC | Descrizione |
|---|---|---|---|---|
| CH₃–CH–CH₃ | Secondario (2°) | Isopropile | 1-metiletilico | Gruppo frequentemente presente in disinfettanti e solventi clinici (es. alcol isopropilico), noto per le proprietà antisettiche e sgrassanti. |
| CH₃–CH(CH₃)– | Primario (1°) | Isobutile | 2-metilpropile | Catena ramificata utilizzata in derivati farmacologici e intermedi chimici, con influenza sulla liposolubilità. |
| CH₃–CH₂–CH(CH₃)– | Secondario (2°) | sec-Butile | 1-metilpropile | Struttura ramificata che compare in solventi organici; la configurazione secondaria può modificare la reattività metabolica. |
| (CH₃)₃C– | Terziario (3°) | t-Butile o tert-Butile | 1,1-dimetiletilico | Gruppo voluminoso che riduce la reattività della molecola; usato come sostituente protettivo in sintesi organiche, con implicazioni in chimica farmaceutica. |
Sostituenti alchilici ramificati
Struttura e denominazione di alcuni gruppi alchilici a catena ramificata.
Si definisce carbocatione alchilico la specie cationica che si ottiene per sottrazione di un idruro, \( \mathrm{H^-} \), da un alcano: il carbonio che perde l’idrogeno assume carica positiva. A seconda che il centro cationico sia 1°, 2° o 3°, si distinguono carbocationi primari, secondari e terziari:
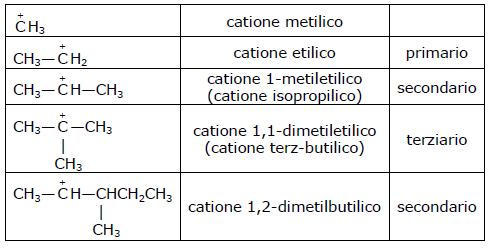 |
| Classificazione dei cationi alchilici. |
I carbocationi sono altamente reattivi e, in condizioni ordinarie, hanno concentrazioni stazionarie molto basse; ciononostante, rivestono un ruolo centrale come intermedi in numerosi meccanismi, tra cui sostituzioni nucleofile unimolecolari (SN1), eliminazioni unimolecolari (E1) e addizioni elettrofile ad alcheni. L’ordine di stabilità per i carbocationi alchilici è:
\( 3^\circ \;>\; 2^\circ \;>\; 1^\circ \;>\; \mathrm{^{+}CH_3} \).
Questa gerarchia si interpreta considerando due contributi cooperativi: effetto induttivo elettron-donatore dei sostituenti alchilici e iperconiugazione. I gruppi −R saturi tendono a spingere densità elettronica verso il carbonio carente di elettroni, attenuando la carica positiva per via induttiva, mentre i legami C−H sui carboni β possono delocalizzare la carica mediante sovrapposizione del loro orbitale σ con l’orbitale p vuoto del centro cationico (iperconiugazione). In termini generali, quanto maggiore è il numero di legami C−H disponibili per l’iperconiugazione e di sostituenti alchilici in grado di fornire stabilizzazione induttiva, tanto più dispersa risulta la carica e più basso è il contenuto energetico della specie. Per completezza, carbocationi allilici e benzylici sono ulteriormente stabilizzati per risonanza rispetto ai terziari puramente alchilici.
La generazione di un carbocatione comporta un cambiamento di ibridazione del carbonio coinvolto: l’atomo cationico è ibridizzato sp2, ha geometria planare trigonal con angoli prossimi a 120° e possiede un orbitale p vuoto perpendicolare al piano molecolare, sede della delocalizzazione per iperconiugazione e risonanza. La tendenza verso stati più stabili spiega anche i frequenti riarrangiamenti 1,2− (migrazione di idruro o di un gruppo alchilico) che trasformano carbocationi meno sostituiti in specie più sostituite e quindi più stabilizzate.
Molti composti organici furono in origine battezzati con nomi d’uso comune o storici, spesso legati alla fonte naturale o a caratteristiche macroscopiche: si pensi, per esempio, a urea, vanillina o adrenalina. Queste denominazioni di fantasia sono pratiche nell’uso quotidiano, ma non forniscono informazioni strutturali univoche. Per questo la International Union of Pure and Applied Chemistry (IUPAC) ha codificato un sistema sistematico di nomenclatura, descritto nelle raccomandazioni ufficiali (IUPAC “Blue Book”), in grado di associare a ogni struttura un solo nome e, viceversa, di ricostruire la struttura a partire dal nome.
Per gli alcani, le regole fondamentali secondo la normativa IUPAC sono le seguenti:
- Individuare la catena continua più lunga di atomi di carbonio e attribuirle il nome dell’alcano lineare corrispondente servendosi della (Tabella 06.02-01), (Tabella 06.02-05) e (Tabella 06.02-06); il nome base è formato da un prefisso che dipende dal numero di carboni e dal suffisso -ano, caratteristico degli alcani;
- Numerare la catena principale in modo da ottenere l’insieme di locanti più basso per i sostituenti (regola del “primo punto di differenza”); in caso di due catene di pari lunghezza, si sceglie quella che porta il maggior numero di sostituenti, e in ulteriore parità quella con la sequenza di locanti più bassa;
- Assegnare a ciascun sostituente il suo locante e il suo nome: tra i sostituenti sono comuni alogeni [fluoro (F), cloro (Cl), bromo (Br), iodio (I)] e gruppi alchilici, elencati nella (Tabella 06.02-05) e (Tabella 06.02-06); per sostituenti ramificati complessi si ricorre a nomi sistematici, racchiudendo eventualmente il nome del sostituente tra parentesi e numerandolo internamente;
- Quando compaiono più sostituenti identici, ripetere i locanti separati da virgole e anteporre i prefissi moltiplicativi di-, tri-, tetra-, penta- ecc.; per sostituenti complessi è ammesso l’uso di bis-, tris-, tetrakis- per evitare ambiguità;
- Disporre i nomi dei sostituenti in ordine alfabetico, ignorando i prefissi di-, tri-, tetra-, bis-, tris-; i prefissi sec- e tert- non si considerano per l’ordine alfabetico, mentre iso- e neo sono tradizionalmente contati, anche se la nomenclatura sistematica preferisce propan-2-il, 2-metilpropil, 1,1-dimetiletil, ecc;
- Separare i numeri tra loro con virgole e i numeri dai nomi con trattini, senza spazi superflui; il nome della catena principale si colloca per ultimo e determina la classe del composto.
Esempi didattici: 4-etil-3-metilnonano indica una catena di nove carboni con gruppi etile e metile rispettivamente ai carboni 4 e 3; 3,3-dimetilpentano descrive due metili legati al terzo carbonio della catena a cinque atomi; 2-bromo-4-metileptano include un alogeno e un gruppo alchilico; 3-(1-metiletil)esano è la forma sistematica per il composto recante un sostituente isopropilico al carbonio 3.
Il procedimento inverso, dalla denominazione alla struttura, segue lo schema: si traccia e si numera la catena principale indicata dal nome base, si collocano i sostituenti alle posizioni specificate dai locanti e si completa ogni carbonio con il numero appropriato di atomi di idrogeno per rispettare la valenza del carbonio pari a quattro.
| Isomeri del pentano e punti di ebollizione. |
| Nome | Formula molecolare | Formula condensata | T. di fusione (°C) | T. di ebollizione (°C) | Osservazioni cliniche / Applicazioni |
|---|---|---|---|---|---|
| Metano | CH₄ | CH₄ | −182.5 | −162.2 | Gas semplice, usato come fonte energetica; in elevate concentrazioni può indurre ipossia. |
| Etano | C₂H₆ | CH₃–CH₃ | −183.9 | −88.6 | Idrocarburo volatile; inalazioni elevate possono causare narcosi. |
| Propano | C₃H₈ | CH₃–CH₂–CH₃ | −187.6 | −42.1 | Componente di gas combustibili; esposizione acuta può deprimere il sistema nervoso centrale. |
| Butano | C₄H₁₀ | CH₃–(CH₂)₂–CH₃ | −137.2 | −0.5 | Utilizzato come propellente; inalazioni non controllate associate a rischio aritmico. |
| Pentano | C₅H₁₂ | CH₃–(CH₂)₃–CH₃ | −129.8 | 36.1 | Solvente organico; esposizione non controllata può avere effetti neurotossici. |
| Esano | C₆H₁₄ | CH₃–(CH₂)₄–CH₃ | −95.2 | 68.8 | Impiegato in estrazioni industriali; esposizioni croniche correlate a neuropatie periferiche. |
| Eptano | C₇H₁₆ | CH₃–(CH₂)₅–CH₃ | −90.6 | 98.4 | Standard in studi di combustione; può indurre irritazione delle mucose. |
| Ottano | C₈H₁₈ | CH₃–(CH₂)₆–CH₃ | −56.9 | 125.6 | Riferimento per indice di ottano; rilevante in tossicologia ambientale. |
| Nonano | C₉H₂₀ | CH₃–(CH₂)₇–CH₃ | −53.6 | 150.7 | Liquido idrofobico, utilizzato in solventi e rivestimenti. |
| Decano | C₁₀H₂₂ | CH₃–(CH₂)₈–CH₃ | −29.8 | 174.0 | Studiato come modello di lipidi idrofobici nelle ricerche farmacologiche. |
| Dodecano | C₁₂H₂₆ | CH₃–(CH₂)₁₀–CH₃ | −9.6 | 216.0 | Componente di membrane artificiali usate in studi di biologia cellulare. |
| Tetradecano | C₁₄H₃₀ | CH₃–(CH₂)₁₂–CH₃ | 5.9 | 253.0 | Standard cromatografico; presente nei lipidi naturali. |
| Esadecano | C₁₆H₃₄ | CH₃–(CH₂)₁₄–CH₃ | 18.0 | 287.0 | Riferimento sperimentale per la fluidità delle membrane biologiche. |
Alcani lineari: primi dieci composti
I primi dieci alcani a catena continua, con i rispettivi nomi e formule chimiche.
| Lunghezza catena carboniosa | Prefisso | Nome dell’alcano | Nota |
|---|---|---|---|
| 1 | Met- | Metano | Gas semplice, di interesse ambientale e industriale; in alte concentrazioni può provocare ipossia per sostituzione dell’ossigeno. |
| 2 | Et- | Etano | Idrocarburo volatile, impiegato come componente di miscele gassose; inalato ad alte dosi può causare depressione del SNC. |
| 3 | Prop- | Propano | Utilizzato come combustibile e propellente; l’esposizione acuta può determinare effetti narcotici lievi. |
| 4 | But- | Butano | Gas presente in spray e accendini; inalazioni non controllate associate a rischio aritmico. |
| 5 | Pent- | Pentano | Solvente organico, usato in laboratorio; richiede ventilazione per evitare neurotossicità. |
| 6 | Es- | Esano | Impiegato nell’industria estrattiva; esposizioni croniche correlate a neuropatia periferica. |
| 7 | Ept- | Eptano | Standard in studi di combustione; noto per effetti irritativi sulle vie respiratorie. |
| 8 | Ott- | Ottano | Parametro di riferimento nell’indice di ottano; non usato in clinica ma rilevante in tossicologia ambientale. |
| 9 | Non- | Nonano | Catena lineare lipofila, con usi limitati in ambito medico diretto ma presente in solventi industriali. |
| 10 | Dec- | Decano | Liquido idrofobico studiato come modello sperimentale nella ricerca sui lipidi biologici. |
Prefissi IUPAC della catena carboniosa
Indicazione della lunghezza della catena e relativi prefissi secondo la nomenclatura IUPAC.
| Numero di atomi di carbonio | Nome IUPAC | Nota |
|---|---|---|
| 11 | Undecano | Composto idrofobico; poco usato clinicamente, ma rilevante come modello in studi di membrane biologiche. |
| 12 | Dodecano | Componente in detergenti e membrane artificiali; utilizzato in studi di biologia cellulare. |
| 13 | Tridecano | Idrocarburo lineare raro in applicazioni dirette, ma studiato come riferimento in cromatografia. |
| 14 | Tetradecano | Presente nei lipidi naturali (acido miristico); importante nei processi di ancoraggio proteico. |
| 15 | Pentadecano | Acido grasso saturo secondario, riscontrabile in piccole quantità nei tessuti; può influenzare la fluidità di membrana. |
| 16 | Esadecano | Analogo dell’acido palmitico, costituente principale dei lipidi biologici; centrale in metabolismo lipidico. |
| 17 | Eptadecano | Idrocarburo lungo, meno comune nei lipidi umani, ma utilizzato in ricerche tossicologiche. |
| 18 | Ottadecano | Correlato all’acido stearico; parte integrante delle membrane cellulari e della riserva energetica. |
| 19 | Nonadecano | Catena lunga idrofobica, utilizzata come standard in analisi cromatografiche. |
Alcani lineari con oltre dieci atomi di carbonio
Denominazione secondo la nomenclatura IUPAC per le catene lineari superiori a C₁₀.
| Lunghezza catena carboniosa | Prefisso | Nome dell’alcano | Nota |
|---|---|---|---|
| 1 | Met- | Metano | Gas semplice, di interesse ambientale e industriale; in alte concentrazioni può provocare ipossia per sostituzione dell’ossigeno. |
| 2 | Et- | Etano | Idrocarburo volatile, impiegato come componente di miscele gassose; inalato ad alte dosi può causare depressione del SNC. |
| 3 | Prop- | Propano | Utilizzato come combustibile e propellente; l’esposizione acuta può determinare effetti narcotici lievi. |
| 4 | But- | Butano | Gas presente in spray e accendini; inalazioni non controllate associate a rischio aritmico. |
| 5 | Pent- | Pentano | Solvente organico, usato in laboratorio; richiede ventilazione per evitare neurotossicità. |
| 6 | Es- | Esano | Impiegato nell’industria estrattiva; esposizioni croniche correlate a neuropatia periferica. |
| 7 | Ept- | Eptano | Standard in studi di combustione; noto per effetti irritativi sulle vie respiratorie. |
| 8 | Ott- | Ottano | Parametro di riferimento nell’indice di ottano; non usato in clinica ma rilevante in tossicologia ambientale. |
| 9 | Non- | Nonano | Catena lineare lipofila, con usi limitati in ambito medico diretto ma presente in solventi industriali. |
| 10 | Dec- | Decano | Liquido idrofobico studiato come modello sperimentale nella ricerca sui lipidi biologici. |
Prefissi IUPAC della catena carboniosa
Indicazione della lunghezza della catena e relativi prefissi secondo la nomenclatura IUPAC.
| Numero di atomi di carbonio | Nome IUPAC | Nota |
|---|---|---|
| 11 | Undecano | Composto idrofobico; poco usato clinicamente, ma rilevante come modello in studi di membrane biologiche. |
| 12 | Dodecano | Componente in detergenti e membrane artificiali; utilizzato in studi di biologia cellulare. |
| 13 | Tridecano | Idrocarburo lineare raro in applicazioni dirette, ma studiato come riferimento in cromatografia. |
| 14 | Tetradecano | Presente nei lipidi naturali (acido miristico); importante nei processi di ancoraggio proteico. |
| 15 | Pentadecano | Acido grasso saturo secondario, riscontrabile in piccole quantità nei tessuti; può influenzare la fluidità di membrana. |
| 16 | Esadecano | Analogo dell’acido palmitico, costituente principale dei lipidi biologici; centrale in metabolismo lipidico. |
| 17 | Eptadecano | Idrocarburo lungo, meno comune nei lipidi umani, ma utilizzato in ricerche tossicologiche. |
| 18 | Ottadecano | Correlato all’acido stearico; parte integrante delle membrane cellulari e della riserva energetica. |
| 19 | Nonadecano | Catena lunga idrofobica, utilizzata come standard in analisi cromatografiche. |
Alcani lineari con oltre dieci atomi di carbonio
Denominazione secondo la nomenclatura IUPAC per le catene lineari superiori a C₁₀.