Acidi e basi
Definizione
La formulazione di Arrhenius rappresenta una delle prime formalizzazioni del comportamento acido-base in soluzione acquosa. In tale quadro, un acido è una sostanza che, disciolta in acqua, genera ioni idrogeno, mentre una base dà luogo a ioni idrossido. In acqua il protone non esiste libero: esso si coordina alle molecole di solvente formando specie idratate, il più delle volte rappresentate come ione idrossonio, \( \mathrm{H_3O^+} \). Per esempio, l’acido cloridrico si comporta come acido di Arrhenius perché produce ioni idrogeno in soluzione:
\[ \mathrm{HCl(aq) \rightarrow H^+(aq) + Cl^-(aq)} \qquad \text{equivalentemente} \qquad \mathrm{HCl(aq) + H_2O(l) \rightarrow H_3O^+(aq) + Cl^-(aq)}. \]
Analogamente, un idrossido alcalino come l’idrossido di sodio rientra nella definizione di base di Arrhenius poiché fornisce ioni idrossido in acqua:
\[ \mathrm{NaOH(aq) \rightarrow Na^+(aq) + OH^-(aq)}. \]
La definizione di Arrhenius è utile e predittiva per molti sistemi acquosi, ma è intrinsecamente legata alla presenza esplicita di \( \mathrm{H^+} \) o \( \mathrm{OH^-} \). Questa restrizione rende difficile classificare composti come l’ammoniaca, \( \mathrm{NH_3} \), che manifestano marcate proprietà basiche pur non contenendo gruppi idrossido. Una trattazione più generale è fornita dalla teoria di Brønsted–Lowry, che interpreta le reazioni acido-base come processi di trasferimento di protoni, indipendentemente dall’esistenza preventiva di \( \mathrm{H^+} \) o \( \mathrm{OH^-} \) nel reagente (Figura 05.01-01).
Nel modello di Brønsted–Lowry, un acido è un donatore di protoni e una base è un accettore di protoni. Ogni interazione acido-base genera una coppia coniugata: all’acido \( \mathrm{HA} \) corrisponde la sua base coniugata \( \mathrm{A^-} \), e alla base \( \mathrm{B} \) corrisponde l’acido coniugato \( \mathrm{BH^+} \):
\[ \mathrm{HA + B \rightleftharpoons A^- + BH^+}. \]
In acqua, il trasferimento di protone dall’acido cloridrico alla molecola di solvente illustra con chiarezza la definizione:
\[ \mathrm{HCl(aq) + H_2O(l) \rightarrow H_3O^+(aq) + Cl^-(aq)}. \]
La basicità dell’ammoniaca è spiegata in modo naturale: \( \mathrm{NH_3} \) accetta un protone dall’acqua, formando il suo acido coniugato \( \mathrm{NH_4^+} \) e liberando ioni idrossido:
\[ \mathrm{NH_3(aq) + H_2O(l) \rightleftharpoons NH_4^+(aq) + OH^-(aq)}. \]
Questa visione sottolinea che il solvente partecipa attivamente alla protolisi e che acidi e basi si riconoscono per il loro ruolo nel trasferimento del protone, non per la sola composizione chimica iniziale. La nozione di coppie coniugate consente inoltre di inquadrare la direzione di equilibrio: quanto più forte è un acido, tanto più debole sarà la sua base coniugata, e viceversa.
L’acqua è anfiprotica: può comportarsi sia come base, accettando un protone, sia come acido, donandolo. Nei due esempi sopra, l’acqua accetta un protone da \( \mathrm{HCl} \) (funzione basica) e dona un protone a \( \mathrm{NH_3} \) (funzione acida). Questa duplice natura si riflette anche nella sua autoionizzazione, un equilibrio debolmente spostato verso i reagenti:
\[ \mathrm{2\,H_2O(l) \rightleftharpoons H_3O^+(aq) + OH^-(aq)}. \]
Il prodotto ionico dell’acqua, \( K_w \), è definito da \( K_w = [\mathrm{H_3O^+}][\mathrm{OH^-}] \), e a 25 °C vale circa \( 1{,}0 \times 10^{-14} \). Questo parametro lega in modo termodinamico l’acidità e la basicità in ambiente acquoso e giustifica l’effetto di livellamento: in acqua tutti gli acidi “più forti” di \( \mathrm{H_3O^+} \) risultano equivalenti in forza effettiva, poiché protonano completamente il solvente, mentre tutte le basi “più forti” di \( \mathrm{OH^-} \) vengono completamente protonate, apparendo egualmente forti.
Le interazioni soluto–solvente, inclusi solvatazione e stabilizzazione coulombiana degli ioni, favoriscono la dissociazione di molte specie acide e basiche e determinano, insieme alla temperatura, i valori di equilibrio osservati in soluzione.
È cruciale distinguere fra forza e concentrazione. La forza descrive il grado di dissociazione in soluzione: un acido o una base sono detti forti se reagiscono con l’acqua in modo pressoché completo, deboli se l’equilibrio resta largamente spostato verso la forma indissociata. La concentrazione, invece, indica semplicemente quanto soluto è presente per unità di volume, indipendentemente dal suo stato di dissociazione.
Per un acido monoprotico generico \( \mathrm{HA} \) vale: \[ K_a = \frac{[\mathrm{H_3O^+}][\mathrm{A^-}]}{[\mathrm{HA}]}, \] mentre per una base \( \mathrm{B} \): \[ K_b = \frac{[\mathrm{BH^+}][\mathrm{OH^-}]}{[\mathrm{B}]}. \] Valori elevati di \( K_a \) o \( K_b \) indicano acidi o basi più forti; valori piccoli, specie deboli. In prima approssimazione, per acidi o basi deboli diluiti, il grado di dissociazione \( \alpha \) cresce all’aumentare della diluizione.
Tra gli acidi forti comunemente incontrati in acqua rientrano le specie che protonano quasi completamente il solvente. Esempi tipici sono:
- acido cloridrico: \( \mathrm{HCl + H_2O \rightarrow H_3O^+ + Cl^-} \);
- acido nitrico: \( \mathrm{HNO_3 + H_2O \rightarrow H_3O^+ + NO_3^-} \);
- acido solforico, prima dissociazione: \( \mathrm{H_2SO_4 + H_2O \rightarrow H_3O^+ + HSO_4^-} \).
Per gli acidi forti si usa spesso una singola freccia per sottolineare l’assenza pratica della reazione inversa in condizioni standard, a differenza degli acidi deboli, per i quali si rappresenta l’equilibrio con la doppia freccia. Altri acidi forti in acqua includono \( \mathrm{HBr} \), \( \mathrm{HI} \) e \( \mathrm{HClO_4} \).
Le basi forti più comuni, in ambiente acquoso, sono gli idrossidi dei metalli alcalini, completamente dissociati all’atto della solubilizzazione:
- idrossido di sodio: \( \mathrm{NaOH \rightarrow Na^+ + OH^-} \);
- idrossido di potassio: \( \mathrm{KOH \rightarrow K^+ + OH^-} \).
Idrossidi di metalli alcalino-terrosi come \( \mathrm{Ca(OH)_2} \) e \( \mathrm{Ba(OH)_2} \) generano soluzioni fortemente basiche nella frazione disciolta, pur avendo solubilità limitata per alcuni di essi.
Acidi e basi deboli rimangono prevalentemente non dissociati; solo una frazione delle molecole partecipa alla formazione degli ioni. Tra gli acidi deboli di interesse generale si possono citare:
- acido acetico (etanoico): \( \mathrm{CH_3COOH + H_2O \rightleftharpoons H_3O^+ + CH_3COO^-} \);
- acido carbonico: \( \mathrm{H_2CO_3 + H_2O \rightleftharpoons H_3O^+ + HCO_3^-} \).
Tra le basi deboli, oltre all’ammoniaca già discussa, si annoverano ammine e basi eterocicliche:
- metilammina: \( \mathrm{CH_3NH_2 + H_2O \rightleftharpoons CH_3NH_3^+ + OH^-} \);
- piridina: \( \mathrm{C_5H_5N + H_2O \rightleftharpoons C_5H_5NH^+ + OH^-} \);
- anilina: \( \mathrm{C_6H_5NH_2 + H_2O \rightleftharpoons C_6H_5NH_3^+ + OH^-} \).
La distinzione chimica tra specie forti e deboli si coglie confrontando le concentrazioni all’equilibrio: un acido forte come \( \mathrm{HCl} \) risulta, a parità di condizioni, completamente convertito nei suoi ioni idrossonio e cloruro, mentre un acido debole come l’acido acetico stabilisce un equilibrio dinamico con la sua base coniugata. Ne consegue che una soluzione molto diluita di un acido forte può avere una concentrazione di \( \mathrm{H_3O^+} \) inferiore rispetto a una soluzione più concentrata di un acido debole; la valutazione del pH richiede pertanto di considerare congiuntamente forza intrinseca e concentrazione analitica.
La formulazione di Brønsted–Lowry interpreta le trasformazioni acido–base come scambi di protoni tra specie chimiche. In tale prospettiva, molte reazioni coinvolgono direttamente il solvente: l’acqua, in particolare, è anfiprotica perché può donare o accettare H⁺. Un aspetto cruciale è la reversibilità: il trasferimento di protone genera in genere un equilibrio dinamico, la cui posizione dipende dalle energie relative delle specie coinvolte e dalla natura del solvente. Una rappresentazione generale è:
\[ \mathrm{HA\;(acido) + B\;(base)\;\rightleftharpoons\;BH^+ + A^-} \]
Nella direzione diretta, HA cede H⁺ a B formando l’acido coniugato BH⁺ e la base coniugata A⁻. Nel verso opposto, BH⁺ agisce da acido restituendo il protone ad A⁻, che a sua volta si comporta da base:
- si definisce acido coniugato la specie che risulta quando una base acquisisce un protone;
- si definisce base coniugata la specie che risulta quando un acido cede un protone.
Le specie che differiscono per un singolo protone e si trovano su lati opposti dell’equazione formano una coppia acido–base coniugata. In riferimento allo schema di cui sopra:
- BH⁺ è l’acido coniugato della base B;
- A⁻ è la base coniugata dell’acido HA;
- B e BH⁺ costituiscono una coppia acido–base coniugata;
- HA e A⁻ costituiscono una coppia acido–base coniugata.
È spesso utile annotare esplicitamente i ruoli:
\[ \underset{\text{(Acido)}}{\mathrm{HA}} + \underset{\text{(Base)}}{\mathrm{B}} \;\rightleftharpoons\; \underset{\text{(Acido)}}{\mathrm{BH^+}} + \underset{\text{(Base)}}{\mathrm{A^-}} \]
\[ \text{Coppia coniugata: HA / A^-} \qquad \text{Coppia coniugata: B / BH^+} \]
La doppia freccia indica reversibilità ma non equivalenza tra i due sensi: nella pratica, uno dei due processi risulta prevalentemente favorito. Si consideri, ad esempio, l’interazione tra acido nitrico e acqua:
\[ \underset{\text{(Acido)}}{\mathrm{HNO_3}(aq)} + \underset{\text{(Base)}}{\mathrm{H_2O}(l)} \;\rightleftharpoons\; \underset{\text{(Acido)}}{\mathrm{H_3O^+}(aq)} + \underset{\text{(Base)}}{\mathrm{NO_3^-}(aq)} \]
HNO₃ è un donatore di protoni più efficace di H₃O⁺, per cui l’equilibrio è fortemente spostato verso destra: la reazione inversa è trascurabile e l’acido nitrico è classificato come acido forte. In tali casi la costante di equilibrio ha un valore molto elevato e, nel trattamento operativo, si scrive spesso una singola freccia verso destra per indicare una dissociazione pressoché completa in acqua.
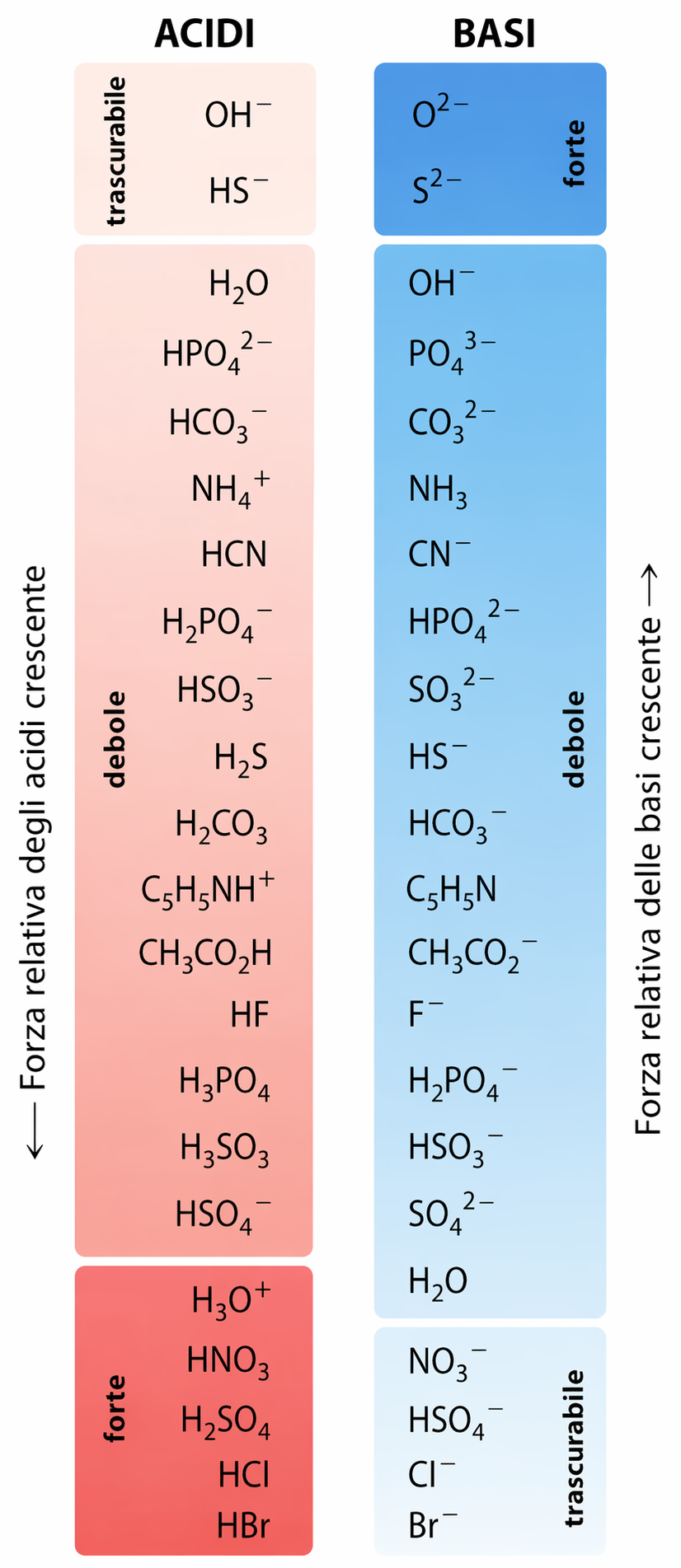
La propensione di un acido a cedere H⁺ o di una base ad accettarlo determina la loro forza relativa e condiziona profondamente il comportamento in soluzione. Un acido tanto più forte quanto più facilmente dona il protone e, di conseguenza, ha una base coniugata tanto più debole; specularmente, una base forte ha un acido coniugato debole. Questa correlazione è riassunta in modo grafico nella (Figura 05.01-02), utile per confrontare e prevedere la forza relativa di acidi e basi.
Dal punto di vista della sicurezza, la pericolosità in laboratorio dipende sia dalla forza sia dalla concentrazione: soluzioni concentrate di specie forti generano elevate quantità di H₃O⁺ o di OH⁻. A titolo di confronto didattico, il succo di limone (ricco in acido citrico, acido debole) è tollerato dall’organismo, mentre una soluzione concentrata di acido nitrico è corrosiva e causa gravi lesioni. In generale:
- gli acidi forti e concentrati reagiscono rapidamente e in modo esotermico con l’acqua presente nei tessuti, provocando ustioni chimiche;
- le basi forti attaccano le proteine e i lipidi della pelle e degli occhi, con azione caustica e saponificante.
Le soluzioni acquose di acidi e basi sono elettrolitiche perché la dissociazione fornisce ioni mobili che trasportano carica. La conducibilità dipende principalmente dalla natura e dalla concentrazione del soluto: acidi e basi forti sono elettroliti forti, mentre le specie deboli sono elettroliti deboli.
Anche l’acqua pura è coinvolta in un limitato trasferimento di protoni tra molecole identiche, con formazione simultanea di ioni idrossonio e idrossido:
\[ \mathrm{H_2O}(l) + \mathrm{H_2O}(l) \;\rightleftharpoons\; \mathrm{H_3O^+}(aq) + \mathrm{OH^-}(aq) \]
Questo processo, detto autoionizzazione o autoprotolisi, mette in evidenza la duplice natura dell’acqua, capace di comportarsi sia da acido sia da base. A 25 °C, in acqua pura, le concentrazioni all’equilibrio sono uguali per ragioni stechiometriche:
[H₃O⁺] = 1,0 × 10⁻⁷ M
[OH⁻] = 1,0 × 10⁻⁷ M
Il prodotto delle concentrazioni di ioni idrossonio e idrossido è la costante di autoionizzazione dell’acqua, o prodotto ionico dell’acqua, indicato con \(K_w\). Poiché la frazione di molecole ionizzate è estremamente piccola, la concentrazione dell’acqua liquida resta pressoché costante e non compare nell’espressione della costante di equilibrio:
\[ \begin{aligned} K_w &= [\mathrm{H_3O^+}][\mathrm{OH^-}] \\ &= (1,0 \times 10^{-7})(1,0 \times 10^{-7}) \\ &= 1,0 \times 10^{-14}. \end{aligned} \]
Il valore di \(K_w\) è funzione della temperatura, come ogni costante di equilibrio. A temperatura fissata, la presenza di soluti può modificare le concentrazioni di H₃O⁺ e OH⁻, ma il loro prodotto rimane costante: a 25 °C, \([\mathrm{H_3O^+}]\cdot[\mathrm{OH^-}] = 1,0 \times 10^{-14}\). Questa relazione sostiene la definizione operativa della scala del pH, impiegata per quantificare acidità e basicità delle soluzioni.
La connessione tra forze coniugate si riflette anche nelle costanti di equilibrio: per una coppia acido–base coniugata vale \[ K_a \cdot K_b = K_w \quad (25\,^\circ\mathrm{C}), \] a ulteriore conferma che un acido forte è associato a una base coniugata debole, e viceversa.